虫草补肾胶囊对糖尿病性骨质疏松患者骨转化标志物的影响
2021-07-03段俊红梁贵廷
段俊红,梁贵廷
(石家庄市中医院,河北 石家庄 050000)
糖尿病是一种常见的代谢性疾病,主要特征是以胰岛素作用障碍或胰岛素分泌缺陷所导致的高血糖[1]。糖尿病可诱发各大系统并发症,如神经系统、循环系统等,同时对骨代谢也有一定程度影响,引起骨质疏松[2]。糖尿病和骨质疏松多发于老年群体,且两种疾病常同时存在,骨折概率大于单一糖尿病或单一骨质疏松,影响中老年人身体健康[3]。研究显示[4],合并骨质疏松的糖尿病患者在病情进展中可造成患者骨微结构破坏、骨形成减少。临床治疗该疾病多采用降糖药物联合补钙治疗,但其补钙效果不佳,仍有患者发生初次骨折或再次骨折。中医理论及临床症状研究表明[5],肾主骨生髓,为人生长发育之本,当患者出现肾虚则百病由生。虫草补肾胶囊由石家庄市中医院著名中医专家孟凡道主任集数年临床验研制而成,其主要功效为温肾补精,益气养血,补肝益肾,强筋壮骨。有研究报道[6],虫草补肾胶囊辅助治疗2 型糖尿病患者具有较佳疗效,但其治疗糖尿病性骨质疏松患者的研究仍未见报道。本研究选取本院107 例糖尿病性骨质疏松患者作为研究对象,旨在分析虫草补肾胶囊对糖尿病性骨质疏松患者骨转化标志物的影响,现报道如下。
1 资料与方法
1.1 一般资料
选择2016 年12 月~2019 年11 月本院收治的107 例糖尿病性骨质疏松患者作为研究对象,行随机数表法分为对照组(n=54)和观察组(n=53)。对照组男性21 例,女性33 例,年龄48~73 岁,平均年龄(64.95±6.24)岁,平均病程(5.47±1.37)年。观察组男性22 例,女性31 例,年龄46~72 岁,平均年龄(65.34±6.60)岁,平均病程(5.62±1.20)年。两组一般资料比较,差异无统计学意义(P>0.05),具有可对比性。本研究经本院医学伦理委员会批准。
1.2 诊断标准
(1)糖尿病:参照《中国2 型糖尿病防治指南(2017 年版)》[7]诊断标准:有“三多一少”的典型症状,空腹血糖≥7.0 mmol/L 或餐后2 h 血糖≥11.1 mmol/L;无典型症状,仅空腹血糖≥7.0 mmol/L或餐后2 h 血糖≥11.1 mmol/L;(2)骨质疏松:西医诊断标准:符合2019 年中国老年保健医学研究会制定的《老年骨质疏松症评估技术应用专家共识》[8];中医诊断标准:符合《中药新药治疗骨痿(骨质疏松)临床研究指导原则》[9]中证型:肝肾阴虚证型;主症:腰膝酸软、腰背疼痛;次症:下肢萎弱、倦怠乏力、步履艰辛、目眩头晕;舌脉:舌淡或红,苔少或无,脉沉细。若主症或次症符合2 项或以上,结合舌脉,均可确诊。
1.3 入选标准
(1)纳入标准:①符合上述中两种疾病的中西医诊断标准;②近1 年内无影响骨代谢治疗史,如钙制剂、VD、类固醇激素等;③患者或其家属知情且签字。(2)排除标准:①确诊为Ⅰ型糖尿病;②有影响骨代谢合并症,如类风湿、原发性甲旁亢等;③骨质疏松晚期,无劳动力者;④合并重要疾病如重要器官心肝肾等功能障碍、全身感染性疾病、自身免疫性疾病;⑤精神病患者或家族有精神病遗传史者。
1.4 方法
1.4.1 基础治疗 两组均进行糖尿病及骨质疏松疾病知识教育,同时给予科学饮食以及运动指导。接受门冬胰岛素(Novo Nordisk A/S,批准文号J20140140,规格:100 单位/1 mL)每日3 次皮下注射治疗,已达到控制血糖的作用。
1.4.2 对照组 给予牡蛎碳酸钙片(按钙计:25 mg克),2 片/次,2 次/d,早晚饭后咀嚼咽下。治疗3个月。
1.4.3 观察组 行虫草补肾胶囊采用口服方式用药,6 粒/次,3 次/d,三餐后口服。治疗3 个月。
1.5 评价指标
(1)临床疗效。根据患者临床症状以及体征的改善情况评价临床疗效。采用三级评分,显效、有效以及无效。显效:经治疗后,无腰膝酸软、下肢萎弱、倦怠无力、步履艰难以及目眩头晕等症状;有效:经治疗后,行走超过1 km 后,偶感下肢发酸、腰膝酸软等症状,偶有目眩症状,对生活无影响;无效:临床症状无改善情况,站立行走300 m 内,可感受到腰膝以及下肢酸软等症状,且经常出现目眩头晕等症状,对日常生活严重造成影响。(2)中医证候积分。对患者的中医主症、次症的严重程度进行赋值,0~3 分,分别代表无症状~重症症状。统计患者治疗前以及经3 个月治疗后的中医证候积分改善情况。(3)骨转化标志物。收集患者清晨8 点空腹静脉血5 mL,经3 000 r/min 离心10 min 后,分离血清,并保存于−20℃待测,使用ROCHE Cobas 品牌的型号为e411 的化学发光分析仪检测骨钙素、1 型前胶原氨基端前肽(total procollagen type amino termi‐nal peptide,tP1NP)、甲状旁腺素(parathyroid hor‐mone,PTH)、25‐羟基维生素D、β‐异构化的c 端肽(β‐C‐end peptide beta isomerization,β‐CTx)的水平。(4)骨密度。于患者治疗前和治疗3 个月后,使用自购于法国双能X 线骨密度仪检测患者股骨颈骨密度。
1.6 统计学处理
2 结果
2.1 临床疗效
观察组治疗总有效率高于对照组,差异有统计学意义(P<0.05)。见表1。

表1 两组临床疗效对比[n (%)]Tab 1 Comparison of clinical efficacy between the two groups[n (%)]
2.2 中医证候积分
两组治疗前中医证候积分腰膝酸软、腰背疼痛、下肢萎弱、倦怠乏力、步履艰辛以及目眩头晕的评分比较,差异无统计学意义(P>0.05);治疗后中医证候积分腰膝酸软、腰背疼痛、下肢萎弱、倦怠乏力、步履艰辛以及目眩头晕的评分比治疗前低,且观察组各症候积分比对照组低,差异有统计学意义(P<0.05)。见表2。
表2 两组中医证候积分对比(分,±s)Tab 2 Comparison of TCM syndrome points between the two groups(score,±s)
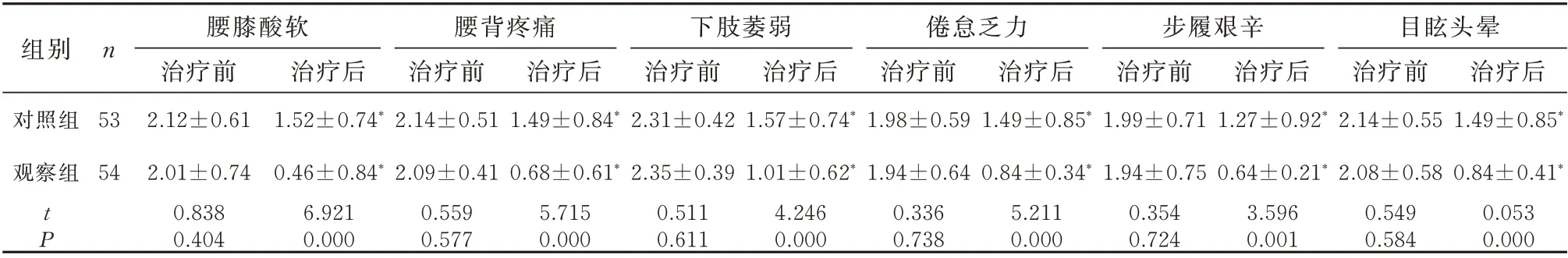
表2 两组中医证候积分对比(分,±s)Tab 2 Comparison of TCM syndrome points between the two groups(score,±s)
注:与本组治疗前比较,*P<0.05。
组别n 腰膝酸软治疗前2.12±0.61 2.01±0.74 0.838 0.404治疗后1.49±0.85*0.84±0.41*0.053 0.000治疗后1.49±0.84*0.68±0.61*5.715 0.000腰背疼痛治疗前2.14±0.51 2.09±0.41 0.559 0.577治疗后1.57±0.74*1.01±0.62*4.246 0.000下肢萎弱治疗前2.31±0.42 2.35±0.39 0.511 0.611倦怠乏力治疗前1.98±0.59 1.94±0.64 0.336 0.738治疗后1.49±0.85*0.84±0.34*5.211 0.000治疗后1.27±0.92*0.64±0.21*3.596 0.001步履艰辛治疗前1.99±0.71 1.94±0.75 0.354 0.724目眩头晕治疗前2.14±0.55 2.08±0.58 0.549 0.584 53 54对照组观察组tP治疗后1.52±0.74*0.46±0.84*6.921 0.000
2.3 骨转化标志物
两组治疗前骨钙素、25‐羟基维生素D、PTH、tP1NP、β‐CTx 水平比较,差异无统计学意义(P>0.05);治疗后骨钙素、PTH、tP1NP、β‐CTx 水平比治疗前低,且观察组低于对照组,差异有统计学意义(P<0.05);治疗后的血清25‐羟基维生素D 较治疗前高,且观察组水平较对照组高,差异有统计学意义(P<0.05)。见表3。
表3 两组骨转化标志物对比(±s)Tab 3 Comparison of bone turnover markers between the two groups(±s)
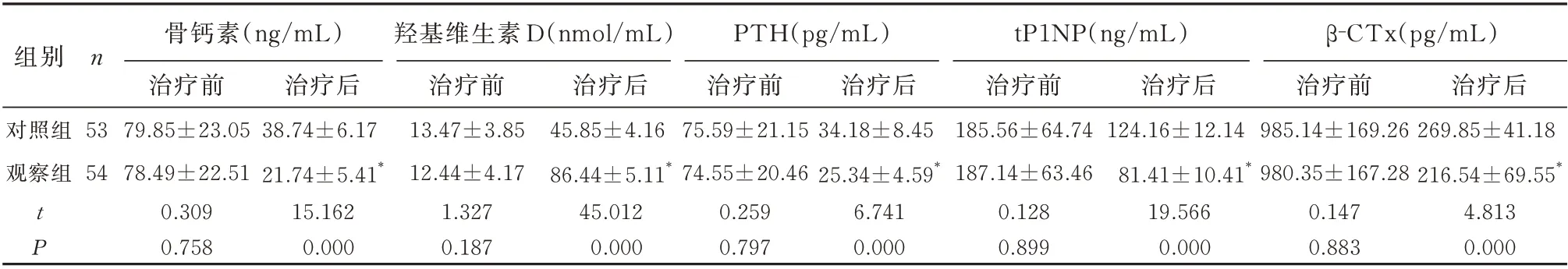
表3 两组骨转化标志物对比(±s)Tab 3 Comparison of bone turnover markers between the two groups(±s)
注:与本组治疗前比较,*P<0.05。
组别n 骨钙素(ng/mL)治疗前79.85±23.05 78.49±22.51 0.309 0.758治疗后269.85±41.18 216.54±69.55*4.813 0.000治疗后45.85±4.16 86.44±5.11*45.012 0.000羟基维生素D(nmol/mL)治疗前13.47±3.85 12.44±4.17 1.327 0.187治疗后34.18±8.45 25.34±4.59*6.741 0.000 PTH(pg/mL)治疗前75.59±21.15 74.55±20.46 0.259 0.797 tP1NP(ng/mL)治疗前185.56±64.74 187.14±63.46 0.128 0.899治疗后124.16±12.14 81.41±10.41*19.566 0.000对照组观察组53 54 tP治疗后38.74±6.17 21.74±5.41*15.162 0.000 β‐CTx(pg/mL)治疗前985.14±169.26 980.35±167.28 0.147 0.883
2.4 骨密度
两组治疗前骨密度比较,差异均无统计学意义(P>0.05)。两组治疗后骨密度比治疗前高,且观察组较高于对照组,差异有统计学意义(P<0.05)。见表4。
表4 两组骨密度对比(g/cm2,±s)Tab 4 Comparison of bone mineral density between the two groups(g/cm2,±s)

表4 两组骨密度对比(g/cm2,±s)Tab 4 Comparison of bone mineral density between the two groups(g/cm2,±s)
注:与本组治疗前比较,*P<0.05。
组别对照组观察组n 男性骨密度治疗前0.62±0.06 0.61±0.05 0.937 0.351治疗后0.61±0.41*0.71±0.52*2.207 0.030 53 54 tP治疗后0.74±0.04*0.82±0.07*7.240 0.000女性骨密度治疗前0.53±0.04 0.54±0.05 1.141 0.256
3 讨论
糖尿病合并骨质疏松症指的是机体在糖尿病病理生理过程中,骨骼系统发生慢性病变[10]。目前糖尿病合并骨质疏松症的发病机制尚未确定,但是有部分研究学者的研究结果证实,糖尿病可通过多种方式影响骨质量以及骨量,如胰岛素缺乏或功能障碍、性激素失调或者糖尿病相关慢性并发症[11,12]。因此,该疾病患者应在控制血糖的同时,采取有效措施治疗骨质疏松症。
中医认为,糖尿病合并骨质疏松症归属于“消渴合并骨痿”范围,肾为水,当肾水不足,则引起阴虚火旺,灼伤肾精;而肾主要生理功能为藏精,肾主骨,精生髓,骨需髓滋养,髓于骨中央,当肾精不足,则骨髓生化障碍,骨骼无法得到滋养,因此骨骼有萎软无力症状;而当肾精充足,则骨髓可化生,骨骼可得到充分滋养,骨骼因此坚固有力[13,14]。而肾精仍需肾气固摄,方可使得肾精存于体内。因此骨骼的正常发育需肾气以及肾精共同作用,故糖尿病合并骨质疏松症的病机在于肾气和肾精同时虚衰[15]。因此,治疗该疾病应以补肾益精为治疗原则。本研究结果显示,观察组总有效率高于对照组,中医证候积分低于对照组,骨转化标志物指标骨钙素、PTH、tP1NP、β‐CTx 水平均低于对照组,25‐羟基维生素D 水平及骨密度高于对照组,表明虫草补肾胶囊治疗糖尿病合并骨质疏松症,疗效更好,可改善患者临床症状,提高骨密度,改善骨转化标志物。分析其原因在于,虫草补肾胶囊是一种中药复方制剂,是由冬虫夏草、熟地黄、紫河车、枸杞子、生地黄、麦冬、酒山茱萸、柏子仁、山药、天冬、麸炒泽泻、茯苓、炙甘草等组成[16]。其配药原则遵循君臣佐使原则,其中冬虫夏草、熟地黄以及紫河车是君药,入肾经,主要作用是阴阳双补、滋肾填精;山茱萸、枸杞、山药、茯苓为臣药,其中山茱萸、枸杞,入肝经,有滋养肝肾和秘藏精气的作用,山药、茯苓入脾经,有健脾益气,有补后天不足之功效;麦冬、柏子仁、天冬以及泽泻则有养阴润肺之功效,可预防五心烦热、滋腻碍脾,均为佐药,甘草则调和以上药性,为使药。诸药合用,滋而不腻、健脾化湿、标本兼顾,可达到滋补肝肾以及涩精壮骨之功效[17]。且现代药理学表明,冬虫夏草中虫草多糖以及虫草素有减少胰岛素代谢、刺激胰岛素分泌作用,且对类固醇有有调节作用,类固醇有降低血清骨钙素作用,因此冬虫夏草不仅有降低血糖效果,也可改善骨质疏松患者血清中骨钙素[18];山茱萸水提液则可改善小鼠模型的骨细胞数量以及骨小梁面积,因此山茱萸有增加骨细胞以及增厚骨皮质的作用,故本研究中观察组患者的骨密度高于对照组;麦冬中提取物麦冬皂苷D 则有抗氧化的作用,大量的活性氧可加快骨质疏松的发生和发展,而麦冬则可通过降低活性氧生成,从而达到缓解骨质疏松发生作用[19]。以上药物现代药理学均可表明,虫草补肾胶囊在降糖的同时,对骨质疏松也有一定治疗作用,故观察组治疗有效率更高。
综上所述,糖尿病合并骨质疏松症患者经虫草补肾胶囊治疗,可改善临床症状,提高骨密度,改善骨转化标志物指标水平,疗效确切。
