格拉司琼贴剂在巴马香猪中的相对生物利用度
2021-07-03胡冰莹韦阳孙莹莹陈姗姗杭州医学院药学院浙江省神经精神疾病药物研究重点实验室杭州310013
胡冰莹,韦阳,孙莹莹,陈姗姗(杭州医学院药学院,浙江省神经精神疾病药物研究重点实验室,杭州 310013)
格拉司琼(granisetron)是一种强效高选择性外周和中枢神经系统5-羟色胺3受体拮抗剂,可拮抗上端小肠腹部向心神经纤维和孤束核或呕吐化学感受区上的5-羟色胺3受体,从而预防和治疗化疗及放疗等引起的恶心和呕吐[1]。与其他止吐药相比,格拉司琼具有效应高、选择性高且毒性低等特点,是临床止吐首选药之一[2]。
临床上,格拉司琼制剂以片剂和注射剂为主[3]。口服格拉司琼因首过效应明显,绝对生物利用度仅为60%,且个体间药代动力学差异很大,消除半衰期和总的血浆清除率有10倍以上的差异[4]。而注射剂的剂型特点限制了其使用。
贴剂为透皮给药系统,能避免肝脏的首过效应和药物在胃肠道的降解,药物吸收过程中的个体差异较口服给药小,且患者依从性好,能突破格拉司琼口服制剂和注射剂的多种局限[5-7]。美国食品药品监督管理局于2008年批准了首个用于控制化疗患者恶心与呕吐的格拉司琼透皮贴剂(SANCUSO)且已有该药的药代动力学研究报道[8-10]。国产格拉司琼透皮贴剂的相关研究较少,仅有少量三天制剂[11-12]和六天制剂[13]的药代动力学数据,七天制剂的药代动力学研究尚未见报道。
巴马香猪是中国特有的一种实验用小型猪,其皮肤的解剖学结构及生理学特性都与人类的皮肤极为相似,适宜于在皮肤相关研究中作为动物模型使用[14]。本研究以巴马香猪为动物模型,以SANCUSO为参比制剂,测定国产盐酸格拉司琼七天透皮给药贴剂的药代动力学特性,评价其相对生物利用度。
1 材料
1.1 仪器
液质联用系统(安捷伦1100双泵、安捷伦1100脱气仪、安捷伦1100自动进样器;AB SCIEX API3000质谱仪,Analyst 1.4工作站)。Allegra X-15R离心机(贝克曼);AE100电子分析天平(梅特勒);多管涡旋器(Cole-Parmer 4721-00);超低温冰箱(海尔);移液器(Eppendorf)。
1.2 试药
格拉司琼对照品(含量:99.8%,批号:100558-200602)和盐酸雷莫司琼对照品(含量:99.5%,批号:100662-201202)(中国食品药品检定研究院);甲醇、乙腈、甲基叔丁基醚和醋酸铵均为色谱纯(美国TEDIA公司);超纯水由Millipore超纯水仪制备。格拉司琼七天透皮给药贴剂(受试制剂,河南羚锐制药股份有限公司研制,规格为每52 cm2含药34.3 mg,批号:20130809);格拉司琼透皮贴剂(SANCUSO,参比制剂,ProStrakan公司,七天制剂,规格为每52 cm2含药34.3 mg,批号:40282)。
1.3 实验动物
巴马香猪[江苏泰州泰和生物科技有限公司,生产许可证号为SCXK(苏)2011-0002]。
2 方法与结果
2.1 色谱条件
色谱柱为Agilent Zorbax SB-C18(5 μm,150 mm×4.6 mm);流动相为有机相(30%甲醇-70%乙腈)∶水相(pH为4.1的12.5 mmol·L-1醋酸铵缓冲液)=75∶25(V/V);流速0.5 mL·min-1;进样量25 μL;柱温45℃。
2.2 质谱条件
离子源:Turbo Ionspray源;扫描方式:多反应监测(MRM);正离子模式;源温度:400℃;离子喷雾电压:5000 V;格拉司琼的定量离子对为m/z313.1→m/z138.1,去簇电压为85 V,碰撞能量为40 eV;内标(IS)雷莫司琼的定量离子对为m/z280.1→m/z121.0,去簇电压为65 V,碰撞能量为30 eV。
2.3 溶液配制
精密称取格拉司琼对照品两份,用甲醇溶解并制成1.0 mg·mL-1的格拉司琼对照品储备液和质控储备液。用甲醇梯度稀释对照品储备液得0.15、0.5、2.5、10、50、100、200 ng·mL-1的格拉司琼标准工作溶液;用甲醇梯度稀释质控储备液得0.15、0.25、25、150 ng·mL-1的格拉司琼质控工作溶液。
精密称取盐酸雷莫司琼对照品溶解于适量甲醇中,制成1.0 mg·mL-1的储备液,并用甲醇稀释制备25 ng·mL-1的内标工作溶液。
配制的溶液均于4℃保存。
2.4 样品处理
血浆室温下融化,涡旋10 s后,3000 r·min-1离心5 min,取0.5 mL上清液至已加入10 μL内标工作溶液的离心管中,加入100 μL 2 mol·L-1的NaOH,涡旋30 s混匀,加入5 mL甲基叔丁基醚,涡旋2 min,3000 r·min-1离心5 min。将离心管置于-80℃冷冻下层水相后约10 min,将上层有机相转移至干净离心管中,40℃条件下氮气吹干,加入100 μL流动相涡旋1 min,即得样品溶液。
2.5 方法学考察
2.5.1 专属性考察 取6份不同批次的空白血浆、定量限(LOQ,0.003 ng·mL-1)样品和巴马香猪使用受试制剂24 h后样品(1.42 ng·mL-1),按“2.4”项下方法处理后进样。典型色谱图见图1,可见空白血浆中的内源性物质不干扰格拉司琼和内标雷莫司琼的测定,方法专属性良好。

图1 格拉司琼和内标的典型色谱图Fig 1 Representative chromatogram of granisetron and IS
2.5.2 标准曲线 精密移取格拉司琼标准工作溶液10 μL和490 μL空白血浆,混匀,制成质量浓度分别为0.003、0.01、0.05、0.2、1、2、4 ng·mL-1的格拉司琼标准血浆样品,按“2.4”项下方法处理后进样。以血浆中格拉司琼和内标的质量浓度比为横坐标,以格拉司琼和内标的峰面积比为纵坐标,采用加权(1/χ)最小二乘法进行线性回归,得回归方程为y=1.41x+0.0115(r=0.9999),线性范围为0.003~4 ng·mL-1。
2.5.3 精密度和准确度 精密移取格拉司琼质控工作溶液10 μL和490 μL空白血浆,混匀,制备4个质量浓度水平的质控样品,分别为定量限浓度质控(LOQ,0.003 ng·mL-1)、低浓度质控(LQC,0.005 ng·mL-1)、中浓度质控(MQC,0.5 ng·mL-1)和高浓度质控(HQC,3 ng·mL-1)。质控样品按“2.4”项下方法处理后进样,考察方法的日内及日间精密度(RSD)和准确度。结果见表1,表明该方法的精密度和准确度良好。
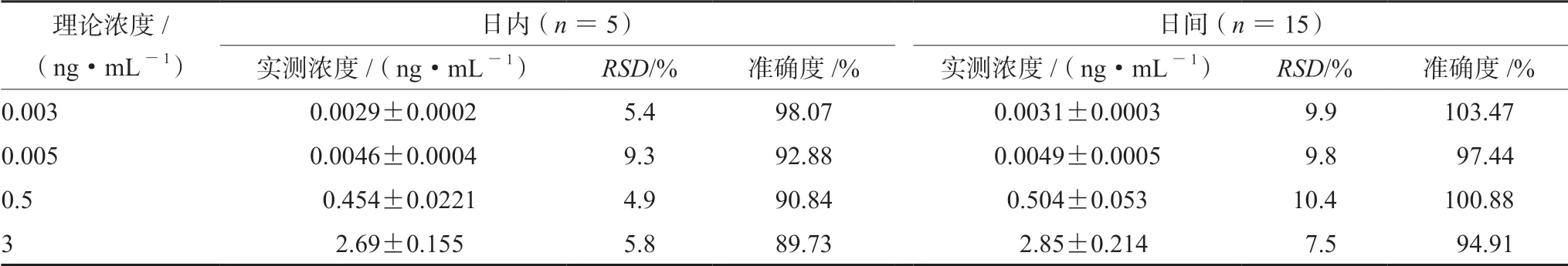
表1 格拉司琼分析方法的精密度和准确度Tab 1 Precision and accuracy of analytical method for granisetron
2.5.4 基质效应 取6个不同批次的空白血浆,按“2.4”项下方法进行萃取,将有机相转移至已分别加入10 μL 3个质量浓度水平的格拉司琼质控工作溶液和10 μL内标工作溶液的离心管中,40℃条件下氮气吹干,加入100 μL流动相涡旋1 min,进样25 μL。峰面积记为B。另取490 μL水代替490 μL空白血浆,重复以上操作,每个质量浓度平行做6份,峰面积记为A。B/A的值即为基质因子,并用内标的基质因子对格拉司琼的基质因子进行归一化。结果表明,在LQC、MQC和HQC 3个质量浓度的质控样品中,格拉司琼的内标归一化基质因子分别为97.50%、125.20%和122.99%,且6个不同批次血浆间LQC、MQC、HQC 3个质量浓度的质控样品中内标归一化基质因子的RSD分别为13.0%、6.0%和5.6%。
2.5.5 提取回收率 取LQC、MQC和HQC 3个质量浓度的质控样品,按“2.4”项下方法处理后进样,每个质量浓度平行做5份,峰面积记为C。与“2.5.4”中用同一批空白血浆制备的样品峰面积B计算比值C/B,即为提取回收率。结果表明,在LQC、MQC和HQC 3个质量浓度质控样品中格拉司琼的提取回收率平均值分别为81.75%、89.76%、93.21%,RSD分别为12.6%、5.0%、5.9%,内标的提取回收率平均值为86.53%,RSD为12.0%。
2.5.6 稳定性考察 取LQC、MQC和HQC 3个质量浓度质控样品,在室温下放置3 h、冻融3次和-80℃放置60 d后,按“2.4”项下方法处理后进样。结果见表2,表明格拉司琼在以上条件下均有良好的稳定性。取LQC、MQC和HQC 3个质量浓度质控样品,按“2.4”项下方法萃取,在自动进样器中放置12 h后分析测定。结果见表2,表明格拉司琼在该条件下稳定性良好。
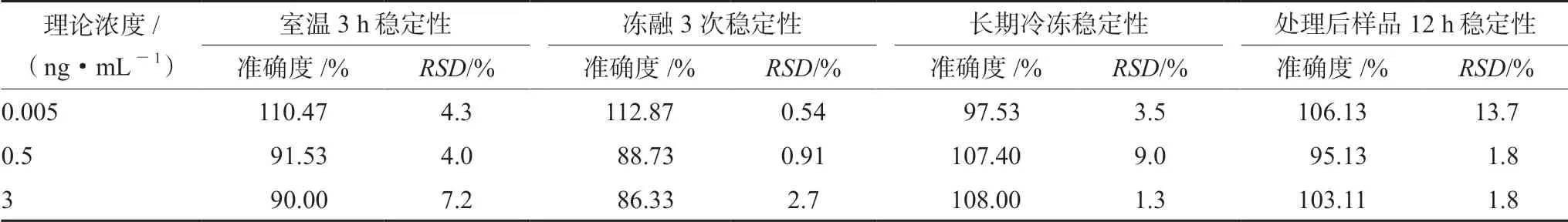
表2 格拉司琼的短期稳定性、冻融稳定性、长期稳定性和处理后样品稳定性(n=3)Tab 2 Matrix stability and processed sample stability of granisetron (n=3)
2.5.7 稀释可靠性 配制6 ng·mL-1格拉司琼血浆样品,吸取100 μL该溶液到离心管中,再加入400 μL空白血浆,混匀,按“2.4”项下方法处理后进样,样品平行做6份。结果表明,样品经稀释5倍后测定结果的准确度为102.08%,RSD为5.4%。
2.6 药代动力学及生物利用度
2.6.1 给药方案 6月龄的健康巴马香猪10只,雌雄各半,体质量(15.20±1.98)kg,实验期间正常饮食。在给予贴剂前一日,将上腹部毛发剃干净,给药前再剃一次,应保证皮肤不被创伤。
采用区组随机、两周期、自身交叉、单次给药的实验设计方法,将10只巴马香猪分为两组,每组5只。第一组先给予格拉司琼透皮贴剂受试制剂,后给予参比制剂,第二组给药顺序相反。每次给药时间为7 d,两次给药时间间隔为17 d。给药剂量均为0.626 mg·kg-1,即0.9552 cm2·kg-1。
2.6.2 血浆样品采集测定 在给药前及给药后6 h、12 h、24 h、d2、d3、d4、d5、d6、d7(移去贴剂前及移去贴剂后4 h、8 h和12 h)、d8、d9、d10和d11于猪前腔静脉丛取血3 mL。血样置于肝素抗凝管中并混匀,3000 r·min-1离心5 min,分离血浆,分成两份(每份不少于0.5 mL),-80℃冷冻待测。待测样品按“2.4”项下方法处理后测定。计算平均血药浓度,并绘制平均血药浓度-时间曲线,见图2。

图2 10只巴马香猪使用受试制剂和参比制剂的平均血药浓度-时间曲线图Fig 2 Mean plasma concentration-time curves of 10 bama miniature pigs after the administration of test preparation(rhombus)and reference preparation(square)
2.6.3 贴剂药物残留量测定 格拉司琼贴剂在巴马香猪使用7 d后,取下贴剂由河南羚锐制药完成贴剂药物残留量测定,经测定残留药物占给药量的1.68%~66.01%。
2.6.4 药代动力学参数计算 使用DAS 2.1.1软件计算药代动力学参数,其计算原理如下:取可检测到药物的最后3~5个时间点质量浓度的自然对数,对相应时间t进行线性回归,求得末端相消除速率常数λ;半衰期t1/2=0.693/λ;tmax和Cmax取实测值;用梯形法求算药-时曲线下面积AUC0~t值;AUC0~∞=AUC0~t+Ct/λ(Ct为末次可测样本的血药浓度)。结果见表3。

表3 巴马香猪使用受试制剂及参比制剂的主要药代动力学参数Tab 3 Main pharmacokinetic parameters of bama miniature pigs after the administration of test preparation and reference preparation
2.6.5 统计分析及生物利用度计算Cmax、AUC0~t和AUC0~∞运用多因素方差分析,tmax运用非参数检验进行分析。相对生物利用度F(%)=(AUC0~∞受试/AUC0~∞参比)×100%。
交叉给予受试制剂和参比制剂格拉司琼透皮贴剂后,巴马香猪体内的tmax、Cmax、AUC0~t和AUC0~∞等药代动力学参数差异无统计学意义(P>0.05)。受试制剂相对参比制剂的F为102.3%。表明两种制剂的吸收消除过程相似。
3 讨论
巴马香猪分别交叉给予受试制剂和参比制剂格拉司琼透皮贴剂后,药物经皮吸收较好。血药浓度在给药12 h后达到峰值,随后开始下降,但在给药2 d内均可维持在一个较高的浓度水平。给药7 d后撤药,撤药后血药浓度逐步降低,撤药4 d后(即给药11 d)血药浓度已低于检测方法的LOQ(0.003 ng·mL-1),这一现象在受试制剂和参比制剂之间并无明显差异,推测不会对药代动力学参数和生物利用度结果产生显著影响。
使用两种制剂后的t1/2、tmax、Cmax、AUC0~t和AUC0~∞等药代动力学参数均无显著差异,表明两种制剂的一致性较高,但给药后个体间的代谢特征差异较大。受试制剂Cmax均值为1.658 ng·mL-1(变异系数CV为72.5%),AUC0~∞均值为2.962 ng·d·mL-1(CV为58.0%);参比制剂Cmax均值为1.693 ng·mL-1(CV为87.2%),AUC0~∞均值为2.918 ng·d·mL-1(CV为47.1%);而根据参比制剂的产品说明书,其临床试验Cmax的均值为5.0 ng·mL-1(CV为170%),AUC0~168h均值为 527 ng·h·mL-1(CV为173%),同样表现出个体差异较大的特征。此外,药物残留量也表现出较大差异(1.68%~66.01%),但同一给药个体使用两种制剂后的药物残留量具有较好的一致性,且AUC0~∞和药物残留量也表现出一定相关性,药物残留量较少的个体相对具有较大的AUC0~∞。
