生理盐水导引腔内心电图技术在新生儿脐静脉置管定位中的应用
2021-07-03汪丽平鲁琦张海玲倪雨琴
汪丽平,鲁琦,张海玲,倪雨琴
脐静脉置管术(Umbilical Vein Catheterization,UVC)是利用新生儿脐静脉及静脉导管尚未关闭,将一次性硅胶导管插入脐静脉,经静脉导管置入下腔静脉的一种中心静脉置管术。临床行脐静脉置管时一般采用体质量计算或体表测量长度,通过预测长度盲穿,置入预测长度后固定再判断导管尖端位置,置管异位率高达21.46%~61.20%[1-2]。导管尖端异位会导致肝损伤、坏死性小肠结肠炎、气腹、心脏压塞等严重并发症[3]。美国静脉输液协会(INS)《输液护理操作指南(第8版)》[4]推荐脐静脉导管尖端应放置在下腔静脉与右心房连接处。目前对新生儿脐静脉置管尖端位置定位最可靠的方法是行胸腹部X线定位法,该法为中心静脉导管尖端定位的金标准[5],但X线胸片定位法逐步显现其滞后性[6],特别是对孕妇、新生儿等特殊人群,存在辐射伤害较大等弊端。腔内心电图(Intracavitary Electrocardiograghy,IC-ECG)技术辅助脐静脉置管是送管时通过观察Ⅱ导联P波及QRS波群振幅变化判断导管是否进入下腔静脉[7]。已有较多文献报道腔内心电图辅助新生儿PICC导管尖端定位方法可靠安全[8-11]。生理盐水导引IC-ECG技术在成人中已证实有效[12-13],但在新生儿中未见相关报道。为了进一步探讨应用IC-ECG引导脐静脉置管术导管尖端定位的可行性和精准性,我院新生儿科采用生理盐水导引IC-ECG技术辅助脐静脉置管术导管尖端定位,取得满意效果,报告如下。
1 资料与方法
1.1一般资料 选择2018年7月至2020年3月在我院采用生理盐水柱法IC-ECG引导技术辅助脐静脉置管术导管尖端定位的新生儿42例为干预组。2017年7月至2018年6月采用传统体质量计算法行导管尖端定位的42例新生儿为对照组。纳入标准:本院产科出生的危重新生儿,经评估需要进行静脉输液超过1周,患儿家属同意,签署脐静脉置管同意书;置管前基础ECG记录显示P波正常。排除标准:脐部感染、脐膨出、腹裂、腹膜炎及新生儿坏死性小肠结肠炎等疾病。两组一般资料比较,差异无统计学意义(均P>0.05),见表1。本研究经过院内护理质量与安全管理委员会批准,患儿家属均签署知情同意书。
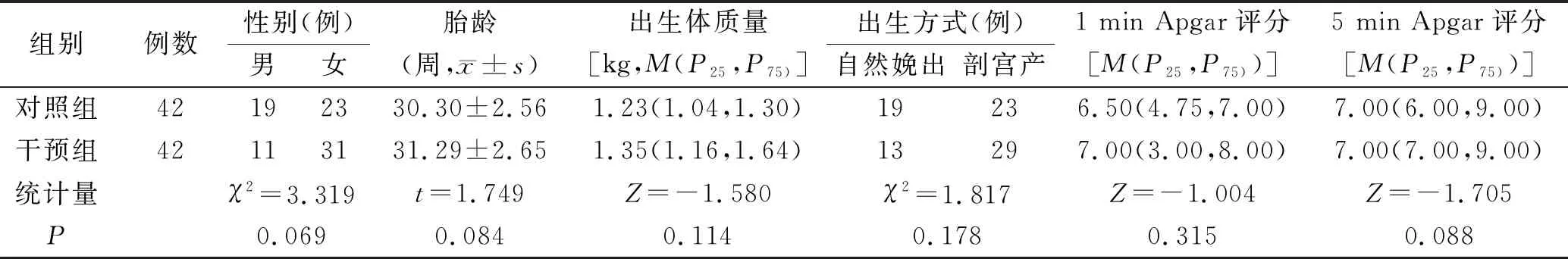
表1 两 组 一 般 资 料 比 较
1.2方法
1.2.1成立科室脐静脉置管小组 主要操作者为接受过脐静脉置管相关培训的新生儿专科护士,在研究实施前组织脐静脉置管小组4名成员进行相关知识学习、技能培训。
1.2.2脐静脉置管材料 3.5F脐血管导管、静脉切开包、心血管专用监护仪、无菌心电导联线、无菌鳄鱼夹、生理盐水100 mL、10 mL注射器、12号针头等。
1.2.3置管方法
1.2.3.1对照组 采用传统体质量计算法(脐带残端(cm)+[(体质量(kg)×3+9]/2)计算插入长度,脐血管导管插入预测长度后固定,行床旁胸腹部X线摄片确定导管尖端位置,导管尖端在T8~T10为精准。
1.2.3.2干预组 ①计算导管插入深度,同对照组。②患儿置于远红外辐射台上,仰卧位,固定四肢,监测血氧饱和度,于患儿左下腹、右下腹和右上锁骨第2肋粘贴电极片,将心血管专用监护仪无菌心电导联的绿色电极置于右下腹,红色电极置于左下腹,白色电极置于右上锁骨第2肋,蓝色电极放置一旁。③消毒脐周围,穿隔离衣,戴无菌手套,铺无菌巾及洞巾,暴露脐部区域,脐带根部系上1根无菌棉线,用无菌剪刀剪除脐带的多余部分,保留残端1~2 cm,用止血钳夹住脐带切面边缘,将充满生理盐水的脐血管导管插入。④用10 mL生理盐水注射器连接12号针头插入导管尾端肝素帽内,针头外露1/2,接预充满生理盐水的导管作为导电电极与血液介质将心电信号导出;将无菌鳄鱼夹夹住针头,无菌鳄鱼夹另一端连接监护仪的蓝色电极,在脐静脉插管过程中,导管插入预置入长度时,缓慢推注0.9%氯化钠注射液1 mL,观察心电图Ⅱ导联P波及QRS波群振幅变化,在进入下腔静脉时QRS波群振幅会逐渐增大,继续置入导管至看到倒置的P波或双向P波后再往外调整导管置入深度,调整至腔内心电图显示正常的QRS波和圆顿的P波且正向增高。⑤固定导管,记录。⑥行床旁胸腹部X线摄片确定导管尖端位置,导管尖端在T8~T10为精准。
1.2.4评价方法 ①特征性P波改变,指成功引导出腔内心电图,识别到特征性P波改变。特征性P波判断标准:当导管尖端未进入下腔静脉时,呈体表心电图;当导管尖端进入近下腔静脉,P波无变化或略增高;当进入到下腔静脉与右心房连接处,P波圆顿且正向增高;当导管尖端进入右心房下部,P波倒置;当导管尖端进入右心房中部,P波双向。②导管尖端位置,以胸腹部X线摄片为标准,观察导管尖端位置,尖端位置在T8~T10为精准,尖端位置在T11及以下为过浅,尖端位置超过T7及以上为过深,尖端在肝脏内判断为异位。③置管相关并发症,包括导管相关血流感染、腹胀(置管前未有腹胀症状,置管后渐次出现,拔管后相关症状减轻或消失, 可判断为UVC相关腹胀)、肝损伤、导管堵塞。观察期为置管后至拔出导管48 h内。
1.2.5统计学方法 采用SPSS19.0软件进行数据处理,行t检验、秩和检验及χ2检验,检验水准α=0.05。
2 结果
2.1干预组特征性P波改变百分比 干预组新生儿置管过程中出现特征性P波改变36例占85.7%;有6例经过3~5次调整仍未出现特征性P波及QRS波,胸腹部X线摄片证实尖端异位至门静脉。
2.2两组导管尖端分布情况比较 见表2。

表2 两组导管尖端分布情况比较 例(%)
2.3两组新生儿置管相关并发症 对照组观察期内出现UVC相关腹胀3例及导管堵塞1例;干预组出现导管堵塞和不明病原体感染各1例。
3 讨论
3.1生理盐水导引IC-ECG定位技术提高了导管定位精准率 本研究采用生理盐水导引IC-ECG定位技术,干预组导管尖端位于下腔静脉接近右心房连接处最佳位置的精准率76.2%,6例异位在门静脉,异位发生率14.3%。对照组导管尖端位置精准率38.1%,7例异位在门静脉,异位发生率16.7%。两组比较差异有统计学意义(P<0.01),说明生理盐水导引IC-ECG可以引导导管尖端定位更精准。本研究对照组中导管尖端过深到右心房18例(42.8%),显著高于干预组4例(9.5%),主要原因在于操作者在盲穿过程中担心过浅,而过深时适当退出后仍可使用。有研究表明,操作者只能通过积累经验和充分认识过深的危害才能按照预定深度置管[14],减少可能发生的并发症。本研究干预组有6例新生儿经过3~5次调整仍未出现特征性P波及QRS波的变化,胸腹部X线摄片证实尖端异位至门静脉;对照组有7例异位至门静脉,因为脐静脉与门静脉、静脉导管及下腔静脉的解剖结构存在个体差异,并非所有脐静脉导管均能成功经过静脉导管插入下腔静脉。
3.2生理盐水导引IC-ECG定位技术的安全性 生理盐水导引IC-ECG定位技术通过特征性P波和QRS波群振幅的变化,精准调节导管置入深度,避免留置位置不当引发的相关并发症。本研究发现,对照组在观察期内出现腹胀3例,原因是由于导管尖端未达到最佳位置(过深),通过X线检查估算,外拔调整,在使用过程中导管尖端异位,拔管后腹胀消失。干预组观察期内出现不明病原体感染1例,可能与导管留置时间长有关。两组均出现导管堵塞1例,与脐静脉置管后护理操作不当有关,需加强护理人员脐静脉置管护理相关知识的培训与考核。任何一种导管定位不当的并发症都可能危及生命,评估导管尖端位置是新生儿重症监护的一项重要技能[15]。IC-ECG定位技术操作简单,精准率高,使患儿及医护人员免受或减少X线辐射,目前没有研究报道在实施IC-ECG定位技术时发生与技术相关的并发症,如心律失常、电流损伤等,本研究在实施过程中也未发生任何与技术相关的并发症,此技术是安全的。
3.3生理盐水导引IC-ECG定位技术的临床应用价值 本研究结果显示,生理盐水IC-ECG技术应用于新生儿脐静脉置管导管尖端定位是可行的。因脐静脉导管无导丝,生理盐水柱技术是利用生理盐水的导电性,并以此作为探测电极,检测心房内心电图P波变化。且本研究采用的监护仪是心血管专用监护仪,抗干扰,对IC-ECG进行优化,波形清晰,85.7%的病例识别出特征性P波。孙红等[16]研究证实对于心电图有P波的患者,P波变化可用来指导置管操作和预测导管尖端位置,心电图定位可作为一种替代性方法。且国内外有较多研究报道,IC-ECG能清晰、可靠地反映PICC导管尖端的位置情况[12,17],有良好的可行性、安全性和准确性。美国静脉输液协会(INS)《输液护理操作指南(第8版)》[4]也指出,如果用替代性技术确认导管尖端已正确放置,则没必要在术后进行放射性成像。
4 小结
IC-ECG技术在危重新生儿中心静脉导管尖端在上腔静脉定位中的应用日益广泛,但在下腔静脉定位中的研究报道不多。导管尖端在下腔静脉定位依据不仅要观察特征性P波,还需要观察QRS波群振幅的变化。但由于本研究的样本量较小,在今后的研究中,建议扩大样本量,探索IC-ECG技术在新生儿脐静脉置管中的有效性和优越性。
