抗冻蛋白与冰-水界面层相互作用的理论机制研究进展
2021-07-01吴金鸿杨丹璐蔡茜茜杨傅佳汪少芸许璟珅
吴金鸿,杨丹璐,周 密,陈 旭,蔡茜茜,施 依,杨傅佳,汪少芸,,许璟珅,张 恒
(1.上海交通大学农业与生物学院,上海 200240;2.福州大学生物科学与工程学院,福建 福州 350108;3.安徽国肽生物科技有限公司,安徽 合肥 242199)
抗冻蛋白(antifreeze proteins,AFPs),又称冰结构蛋白或冰结合蛋白,是一类能控制冰晶生长和抑制冰晶重结晶作用的蛋白质,可在结冰或亚结冰条件下保护生物体不受伤害[1]。AFPs抗冻活性主要表现在其可以在不改变溶液熔点的前提下非依数性地降低溶液冰点[2],并且可以通过与冰晶结合抑制冰晶的生长或重结晶,减轻冰晶对细胞的机械损伤,从而保护生物体和生物大分子在低温下生物活性与结构完整性[3]。AFPs特殊抗冻作用使得其在冷冻食品品质调控、细菌低温保护、植物霜冻保护、生物矿化、医学器官移植等领域具有广泛的应用价值[4]。至今人们在鱼、昆虫、植物和细菌等生物体中已发现多种结构的AFPs[4],它们具有不同的结构特性与抗冻活性,没有共同的演化规律,并且其作用机制也存在显著差异[5]。因此,本文结合近年来国内外关于AFPs抗冻活性及作用机制的研究进展,针对AFPs如何调控冰-水界面层结构的理论问题,分析和探讨了几种典型的AFPs理论作用机制模型,揭示了AFPs通过调控冰-水界面层结构产生与冰晶结合或相互作用原理及其驱动力作用特点,从而为深入理解AFPs抗冻活性机制提供理论参考。
1 AFPs的抗冻活性概述
AFPs具有两种特殊的功能活性——热滞活性和重结晶抑制活性[6]。AFPs所具有的热滞活性主要表现在具有非依数性降低冰点的作用。一般当溶液温度达到水的凝固点0 ℃时,溶液中冰晶并不生长,当温度继续降低到一定程度时冰晶开始生长,溶液冻结,开始冻结的温度被称为凝固点,也就是溶液中的冰晶生长点温度。当溶液温度升高到冰晶生长点温度时,冰晶并不熔化,直到温度升高到接近0 ℃时,冰晶才开始熔化,这一温度是冰晶熔点[7]。AFPs对溶液体系冰结晶过程影响显著,但对熔化过程没有影响,因此含有AFPs的溶液体系凝固点显著降低,与熔点产生了热滞后现象,两者之间的差值就是热滞值[8]。AFPs热滞活性是冰晶形态调控的一种重要作用机制[7]。如图1所示,温度数轴左侧不含AFPs的水溶液中凝固点与熔点相同,在高于或低于此平衡温度时冰晶会收缩或生长为扁平圆盘状;温度数轴右侧含有AFPs的溶液中,AFPs通过吸附到冰晶表面而使冰晶形成多面晶体形状,使凝固点降低并且熔点基本不变,同时在高浓度AFPs存在下冰晶主要沿其六角对称结构中的c轴生长[9],显示了AFPs修饰冰晶形态的功能。Grandum等[10]研究也揭示了在一般水溶液中冰晶通常呈扁圆状,而在AFPs作用下冰晶形态变为六棱锥状,随着AFPs浓度升高逐渐转变成针状。因此,AFPs具有热滞活性的主要原因是其吸附在冰晶表面造成表层弯曲,修饰和改变了冰晶形态,阻止体系中的水与已存在的冰晶结合,导致局部凝固点下降,使整个体系的凝固点降低,因此冰晶必须在更低的温度下才能继续生长[11]。
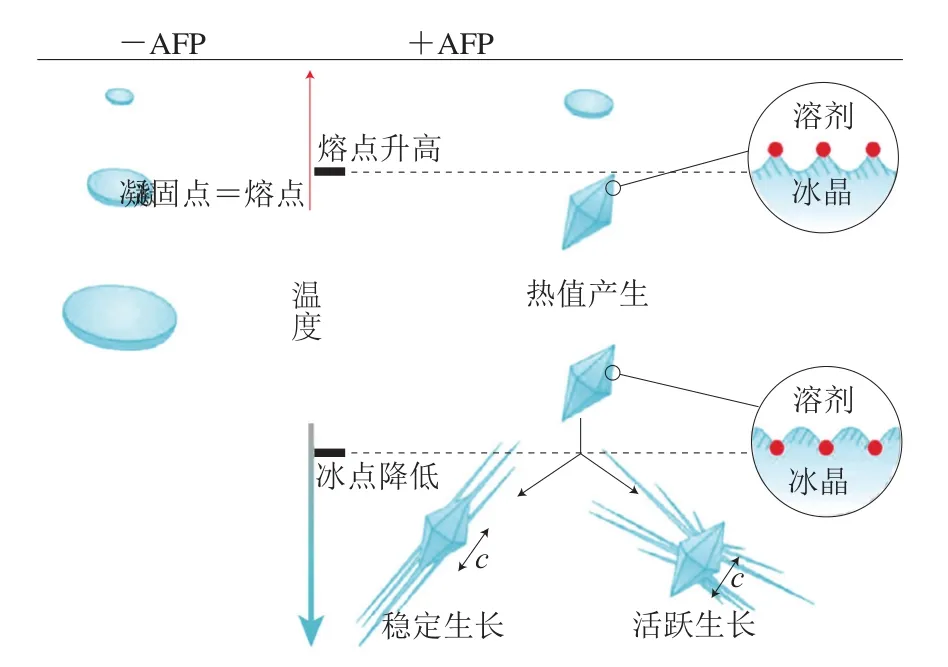
图1 抗冻蛋白热滞活性示意图[7]Fig.1 Schematic diagram of thermal hysteresis activity of AFPs[7]
重结晶抑制活性是AFPs另一个重要抗冻特性。重结晶是指在奥氏熟化作用下冰晶在已经形成的晶体颗粒之间进行生长重分配,小冰晶相互结合,较大冰晶继续长大,最终导致冰晶颗粒增大,连为一体[12]。重结晶一般在温度波动时相互接触的冰晶之间发生聚集,同时伴随冰晶颗粒在界面向不同方向位移,晶体颗粒之间的生长被重新分布。通过氢键、疏水相互作用和范德华力等分子之间作用力,AFPs吸附在液体冰晶表面,阻碍了冰晶在固-液界面位移及与水分子的结合[13]。AFPs通过对冰-水界面体系的作用,显著减缓小冰晶相互结合速率,使溶液体系形成的冰晶体积细小且均匀,从而减缓或阻止了冰水体系中重结晶过程[14]。大冰晶的形成一般对生物体细胞组织造成机械损伤,破坏细胞膜或细胞组织,对生物体产生致命的破坏。因此生物体内AFPs重结晶抑制活性相比于热滞活性更为重要。
2 AFPs调控冰-水界面层结构作用的理论模型
不同来源AFPs在结构或抗冻活性方面虽然存在着明显差异,抗冻机理也不完全相同[15],但研究发现其作用机制具有共同相似之处,即AFPs都能通过一定作用方式结合在冰-水体系交界面,与不同的冰晶面或水相界面互作,调控冰晶的形状与大小,抑制冰晶生长从而发挥其抗冻活性[16]。虽然在实验体系很难得到一个清楚的AFPs与冰晶在冰-水界面层的作用结果图,但随着计算机化学中分子模拟技术、物理分析方法体系及新型生物光谱分析手段的应用,关于AFPs调控冰-水界面层结构的理论机制模型被不断完善与更新。结合国内外相关研究报道,发现至今为止共有吸附-抑制模型、偶极子-偶极子模型、晶格匹配与占有模型、刚体能量模型、包合物锚定模型、亲和相互作用偶联团聚模型等理论模型被提出并广泛应用于对AFPs抗冻活性作用机制的理论解释。
2.1 吸附-抑制模型
吸附-抑制模型是最早也是目前被认可用于解释AFPs热滞活性机制的一种理论模型。在低温条件下,AFPs具有选择吸附性,与冰晶混合后吸附在冰晶生长的表面,冰晶在AFPs分子之间与水结合,在溶液中被AFPs分子覆盖的冰晶表面停止生长[17],而未被覆盖的区域则沿着平面继续向前推进形成一个圆形的表面,使其表面曲率增加[18]。
该模型最早是依据Raymond等[19]对4 种AFPs与冰晶相互作用的研究结果得出。该研究发现当将含有少量氯化钠的AFPs溶液在-2 ℃下冷冻时,AFPs不会在液相中浓缩,而是优先与冰相互作用,有很大一部分AFPs残留在冰中;同时观察冰晶形态发现,4 种AFPs质量浓度为10 mg/mL时,其中3 种AFPs都使冰晶形态变为针状结构。水溶液中形成的冰晶通常在垂直于c轴的方向上生长最快,而含有AFPs的溶液可以抑制冰晶在该方向生长,说明AFPs在平行于c轴的晶面优先进行吸附。此外,该研究还通过溶液中AFPs分子的浓度得到吸附结合到冰晶表面AFPs分子的分布情况,并计算由冰晶表面结合的AFPs分子引起的冰晶表面曲率变化,最后由Kelvin效应推演得到由于AFPs表面效应而降低的溶液平衡冻结温度(热滞活性,ΔT/℃)(公式(1))。

式中:α是分配系数;ρ是AFPs的质量浓度/(mg/cm3);MW是AFPs的相对分子质量。针对所研究的4 种AFPs,根据公式(1)绘制热滞活性与AFPs质量浓度的关系曲线,曲线的形状和计算得到的热滞活性均与实际通过冻结曲线测量得到热滞活性非常接近。
基于上述实验结果,Raymond等[19]认为AFPs通过自身吸附到冰晶表面并通过Kelvin效应抑制冰晶生长。Kelvin效应是指一般情况下冰晶生长垂直于晶体表面,假如杂质分子吸附于冰晶生长的表面,那么需要附加驱动力(凝固点温度下降),促使冰晶在杂质间生长[20]。由于表面曲率增大,因表面张力的影响,增加表面积将使体系的平衡状态发生改变,从而使凝固点下降。因此,Raymond等提出的模型为解释AFPs的热滞活性提供了一个重要的理论机制模型。
此后,有大量研究围绕吸附-抑制模型,针对AFPs与冰晶吸附-抑制作用的模型进行拓展和完善。de Vries等[21]提出了沿着冰晶生长主要方向的基面a轴方向上AFPs与冰晶作用的吸附-抑制模型,并提出了吸附-抑制模型非凝集性降低水凝固点的作用机制(图2):吸附在基面上的AFPs分子会干扰台阶在基面上的扩散,导致台阶高度弯曲。由于AFPs分子直径大约是台阶高度的两倍,因此AFPs分子在基面台阶上的吸附阻止了AFPs覆盖的台阶区域的生长,因此冰晶无法在其上传播,仅在吸附的分子之间可能进一步生长,因此呈现弯曲的前沿。这些高度不规则的前沿导致冰晶表面积与体积的大幅增加,从而导致其凝固点下降,并且下降幅度取决于表面积相对于体积的变化率。

图2 吸附-抑制模型降低水凝固点的作用机制[21]Fig.2 Mechanism of adsorption-inhibition model for lowering freezing point of water[21]
Sönnichsen等[22]进一步揭示了在吸附-抑制作用模型中AFPs与冰吸附结合过程其分子结构域表面结构特征,其用多维核磁共振确定了III型AFPs分子结构(AFP III),发现AFP III具有两个非常平坦的正交表面,可以同时与两个正交的冰表面结合,同时位于AFP III分子C-端的冰结合位点是平面且非极性的,具有低溶剂可及性和特定的冰结合残基(Gln9、Asn14、Thr15、Thr18和Gln44)极性侧链原子的特定空间排列特点。侧链的取向和可及性仅允许每个极性基团形成一个氢键(Gln9除外),这限制了氢键长度和角度。由于AFP III分子具有较大疏水核心,且非极性成分占比达到73%,这说明AFPs分子中非极性基团可能比极性残基更易接近冰结合位点,导致冰结合位点产生疏水性。该研究指出在吸附-抑制作用模型中,AFPs分子除了氢键作用外,也可以通过分子间疏水作用吸附结合到冰晶表面。
Kristiansen等[23]根据吸附-抑制模型,改进了定量计算热滞活性的理论模型。该模型假设结合到冰晶表面的AFPs分子覆盖度反比于其溶解度,并由此计算结合在冰晶表面的AFPs分子之间的空间尺度,最终理论推导得到公式(2)。

式中:ΔT是热滞活性/℃;σ是界面张力(32 ergs/cm2);Tm是熔点/K;θ是吸附的AFPs之间的冰-水临界凸面与平面夹角/(°);K是与AFPs种类相关的常数;[AFP]是溶液中AFPs浓度/(mmol/L);ΔH是水的溶解热(3.3×109ergs/cm3)。
公式(2)理论模型重新估算了冰晶表面曲率的变化,并由此得到了I型和III型鱼类AFPs(AFP I、AFP III)的热滞活性。该理论推导结果与通过冻结曲线或差示扫描量热实验测定得到的AFPs热滞活性基本吻合,从而证实了吸附-抑制作用理论模型的合理性。
吸附-抑制模型是目前最被接受的AFPs作用机制模型[24]。综上分析,该模型主要机理为AFPs通过氢键或疏水作用吸附到冰晶表面,通过Kelvin效应增加表面张力、改变冰晶表面曲率来抑制冰晶的生长速率和降低凝固点,从而使AFPs具有热滞活性。但这种模型只能解释冰晶生长速度的降低而不能解释冰晶的生长停止,同时AFPs与冰晶两者之间的具体相互作用方式难以用简单的吸附-抑制模型来解释。因此,以吸附-抑制模型为基础,研究者们又提出了偶极子-偶极子模型、晶体占位-晶格匹配模型、刚体能量模型、氢原子结合模型等,进一步解释AFPs与冰晶的结合方式以及其抗冻机制。
2.2 偶极子-偶极子模型
偶极子-偶极子模型是主要从冰的晶体结构出发,着眼于AFPs如何阻止冰晶a轴向生长而提出的一种作用机制模型。该模型认为AFPs可以基于AFPs分子中的α-螺旋极性与水分子极性的相互作用来阻止冰晶在基面(垂直于c轴)方向(a轴)上的生长。蛋白质中多肽链形成α-螺旋对亲水、疏水氨基酸残基的排列顺序有一定要求。通常情况下α-螺旋因这种排列而同时具有亲水性和疏水性,并可简化为一个偶极子。对于最常见的冰的晶系——六方晶系(图2)而言,其某个生长方向的外层水分子也可以看作是一个偶极子[25]。因此,在偶极子-偶极子相互作用力下AFPs将被吸引到冰晶的生长a轴上,其α-螺旋上的亲水氨基酸残基,尤其是Thr会与冰晶的水分子形成氢键,从而阻碍冰晶进一步生长[26]。
偶极子-偶极子模型最早由Yang等[27]基于对一种冬季比目鱼体内的一类甲胎蛋白(I型AFPs,RCSB ID:1J5B)的抗冻作用机制研究结果所证实,其研究指出,冬季比目鱼来源的这种AFPs富含Ala,且它们二级结构上仅有一个α-螺旋(图3),在α-螺旋与水分子的偶极相互作用驱动下AFPs贴近冰晶与游离水的界面层,与冰晶、游离水同时形成氢键后通过Kelvin效应抑制了冰晶的进一步生长。后续研究发现[26],若将冬季比目鱼AFPs中几个Thr突变为Ser,则其作用活性将显著降低,但此种突变并不会显著改变蛋白质的二级结构及偶极性。该模型将冬季比目鱼AFPs与冰的结合稳定性解释为二者之间氢键的形成,即AFP与冰之间若能形成更多氢键则二者的结合就更牢固。Graham等[28]最近以一种跳虫体内的AFPs为研究对象,分析了其中几种同源AFPs结构,结果表明这几种AFPs均以α-螺旋上特定氨基酸残基(Ala、Val、Pro等)与冰面形成氢键。分析结果在一定程度上证实了偶极子-偶极子模型理论,并显示α-螺旋结构对AFPs抗冻活性具有关键作用。

图3 冬季比目鱼I类AFPs结构[27]Fig.3 Structure of AFP I in winter flounder[27]
偶极子-偶极子理论模型对在I型AFPs干扰下冰晶外形角度参数发生变化这一现象作出了合理的解释,即轴向抑制结晶与另两个轴冰晶的生长相对独立。但该模型也存在一些问题,比如对于以β-片层为主要二级结构的AFPs,该模型就不能很好地解释将蛋白推向冰-水界面层的驱动力。该模型主要考虑整个AFPs分子与冰晶层的整体相互作用而忽略了不同的氨基酸残基与冰晶具体作用方式。例如将该AFPs活性区域的Thr突变为Ser后活性下降,如果仅从偶极子作用角度出发并不能解释为什么同为亲水残基,Thr有更强活性。
2.3 晶体占位-晶格匹配模型
晶体占位模型认为AFPs部分亲水残基与冰晶表层形成氢键,而这些氢键占据了晶体表面后晶胞(晶体中最小单元)中氧原子的位置,因而在AFPs吸附的生长a轴向上冰晶体生长受阻。在作用过程中,AFPs会使冰晶体各个棱向生长速度不同而致使晶体截面发生变化,趋向于变为六边形(图4)。
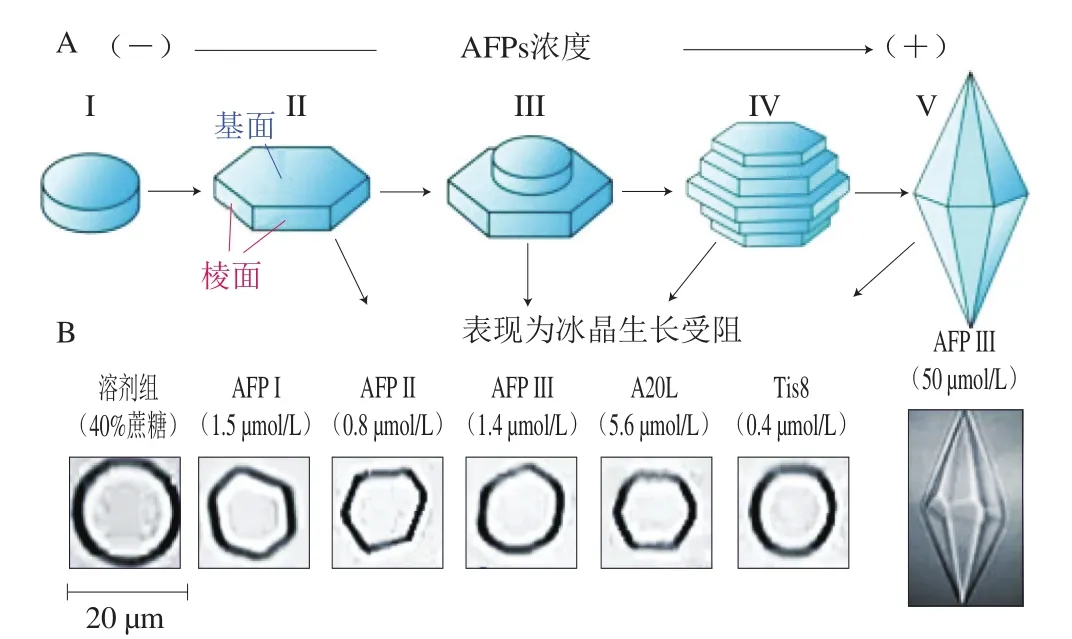
图4 AFPs对冰晶生长作用示意图[29]Fig.4 Schematic diagram of the effect of AFPs on ice crystal growth[29]
Knight等[29]基于对大西洋鱼(Dissostichus mawsoni)血液中两种抗冻糖蛋白(antifreeze glycopeptide,AFGP)的研究结果证实了晶体占位模型。这两种蛋白分子结构中有4~5 个重复单元且均富含Ala,同时在每个重复单元(Ala-Ala-Thr)中苏氨酸残基上以糖苷键与一个二糖结合。重复单元与冰结合位点呈平行轴向排列,每两个结合位点距离为9.31 Å,而冰晶生长轴上重复距离则为4.519 Å,近似为蛋白结合位点距离的一半(图5)。图5结构模型中上方的AFGP与冰晶层在一个平面上的若干水分子以氢键结合,此结合恰好代替了冰晶层中最外面一层晶胞,形成牢固而不可逆的结合。此外,该模型研究还提出Raymond的过冷水模型[30]中的双锥面并不是严格意义上具有合理参数的晶体学平面结构,而是AFPs吸附聚集形成的平面,这也解释了共聚冰晶在融化时表面蚀面形成,即在共聚冰晶融化过程中由于水分子与AFPs脱离共聚晶体的速度不同,表面有蚀面形成的现象。

图5 抗冻糖蛋白与冰晶结合结构模型示意图[29]Fig.5 Schematic diagram of antifreeze glycoprotein and ice crystal binding structure model[29]
Marks等[31]研究指出AFPs疏水性残基在其与冰面结合时起到重要作用。该研究基于分子动力学模拟研究结果,发现一种细菌AFPs(MpAFP)在与冰晶作用时整体结构中水分子具有高度有序的结构,在蛋白的疏水基团周围形成网格状的外壳,并且与其亲水基团形成氢键。这一结果支持晶体占位模型,并且指出了疏水性残基除了疏水外对整体结合也有一定贡献。
晶体占位理论模型作为偶极子-偶极子模型的补充和延伸,从分子层面很好地解释了AFPs为何能牢固地结合到冰晶体上,也补充解释了AFPs干扰下冰晶体生长为双锥的原因。这种模型不仅适用于I型鱼AFPs,也适用于很多其他的AFPs,尤其是具有重复性α-螺旋和β-片层结构的AFPs。但这种模型对于那些三级结构复杂和有多种二级结构包括螺旋、环、自由尾的AFPs抗冻机理并不能很好地进行解释,因为环等二级结构在起抗冻作用时有更复杂的行为。此外,此模型尚不能完美解释AFPs移动到冰-水界面层的驱动力。
晶格匹配模型是晶体占位模型先导,其理论机制基本一致,并由de Vries等[21]于1984年提出。Knight等[32]在2009年作出了补充说明,他将AFPs限制冰晶整体生长的作用归结为“台阶固定”(图4A)和“表面固定”(即蛋白尽可能铺满冰晶表面),并认为冰晶在生长中会形成新的表面,而冰晶伴随着新表面的形成会不可逆吸附更多AFPs,直到冰晶体被完全不能生长的表面包围。这解释了AFPs不可逆吸附于冰晶的过程中为何效果会随时间和浓度发生改变,因为两种固定模式可以认为是分步进行,即AFPs一般先选择性吸附到特定冰晶结合面形成台阶固定,然后随着AFPs吸附浓度的增加,又进一步形成了表面固定,最终使冰晶生长完全停止。
Berger等[33]研究了几种AFPs活跃亚型对不活跃亚型的协同作用,其研究结果显示,不同的AFPs在与冰晶结合的过程中会选择性地优先与冰晶的棱面或锥面结合。这一结果一定程度上支持Knight等[32]的“台阶固定”的观点,即单类AFPs在起作用时,其对冰晶结合面的选择性将导致台阶的形成。
2.4 刚体能量模型
刚体能量模型提出在冰水体系中AFPs在冰-水界面层具有较低的势能,即认为熵能是AFPs运动至冰层表面的驱动力;而AFPs到达冰-水界面层后的作用机制则由晶格匹配等理论解释,即到达冰-水界面层后与冰中的水分子发生不可逆结合而锚定在晶体表面。
这种模型是Knight[34]引用Asthana等[35]的观点而提出,此研究讨论了小颗粒在有固体表面的液体中是否能被固体表面黏附。该模型指出,AFPs在整个体系中可以看作小颗粒,因此可将AFPs在体系中的热力学行为描述为颗粒与晶体生长的相互作用。这种作用具体表现依据黏附自由能的正负性来判断,当黏附自由能Δσ(公式(3))数值为负时,AFPs颗粒就会自发被冰晶体所“吞噬”。图6即表现了这种过程,当颗粒黏附自由能为负值时,颗粒就会有被晶体界面黏附进而“吞噬”的热力学趋势[35]。
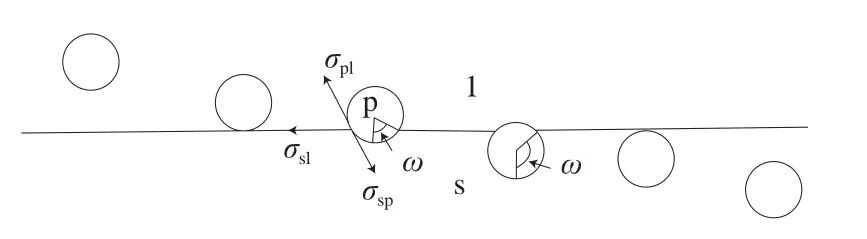
图6 刚体能量模型示意图[35]Fig.6 Schematic diagram of rigid body energy model[35]

式中:σsp、σpl、σsl分别表示晶体与颗粒界面、颗粒与液体界面、晶体与液体界面的界面能/(J/m2)。
刚体能量模型较好地解释了使AFPs运动至冰-水界面层的驱动力,但是并不能解释AFPs的全部作用机理。Knight[34]曾指出即使AFPs与冰晶和与水的作用力相当,界面能降低的趋势也会使AFPs聚集在冰晶表面。换言之,只要是Δσ<0的小颗粒都会有这种性质。Knight这种理论观点可作为吸附-抑制理论的一个补充说明,但也说明需要额外的模型来解释为何冰晶在“吞噬”AFPs后无法继续生长。
Knight等[32]在晶格匹配模型中对抗冻作用与AFPs浓度关系问题的解释可认为是对晶体占位模型和此模型的后续补充。后续有更多研究不断通过应用分子动力学模拟手段来模拟这个过程中体系的变化来进一步验证。例如,Liu Kai等[36]在2016年使用分子动力学方法模拟了AFPs在即将结冰的水层中的行为,如图7所示,模拟之前体系分为冰层和水层两层,AFP在水层上部,模拟之后AFP在体系中的位置下移,周围及后方水分子呈无序状态,表明AFP移动到与冰-水界面层后起到了抗冻作用,在宏观上证实了AFPs有向界面层移动的趋势。对于接触界面层后,更深入的分析则与其他几种模型,如晶体占位模型等契合。
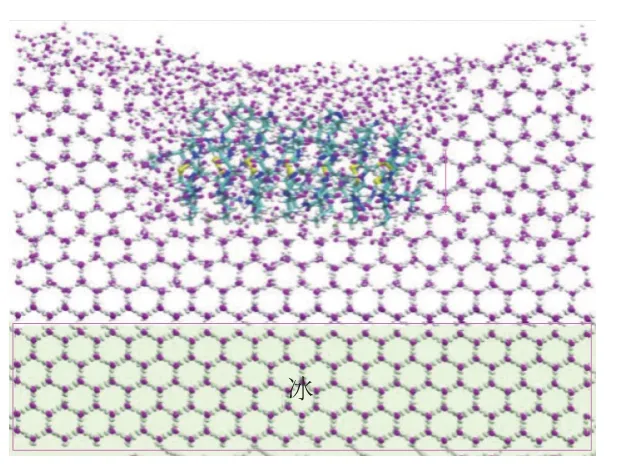
图7 AFPs对冰层的影响[36]Fig.7 Effect of AFPs on ice layer[36]
2.5 包合物锚定模型
近年来,在AFPs与冰-水界面层相互作用研究中,不少研究者提出了包合物锚定模型。该模型主要对冰晶结合域水合作用特征进行分析[37-38]。包合物锚定模型认为,AFPs通过疏水作用使水分子按晶格方式排列,并通过氢键锚定水分子晶格[39-40]。锚定的水分子晶格又通过匹配特定的冰晶表面使AFPs 与冰晶结合[41]。
Garnham等[42]在研究来源于南极细菌(Marinomonas primoryensis,MP)的一种Ca2+-依赖性AFPs抗冻作用机制时提出并证实了包合物锚定模型。该研究指出,这种AFPs中与抗冻活性相关分子结构区域具有一个由Ca2+结合序列中的Thr-Gly-Asx基元形成的长而平坦的冰结合区(ice-binding site,IBS),且沿Ca2+结合侧的长度延伸。该IBS具有疏水性,通过疏水效应将水分子排列成一个冰状晶格,并使晶格通过氢键锚定在AFPs上(图8)。这些锚定的水分子允许AFPs通过匹配一个或多个特定的冰平面来固定冰。研究发现高度活跃(即具有较高热滞活性或重结晶抑制活性)的AFPs能够使水分子吸附到多个冰平面,其中一个冰平面是基面;而适度活跃的AFPs能够使水分子吸附到多个冰平面,但不能被吸附到基面。因此,从实验和分子水平上揭示了疏水作用和氢键在AFPs结合冰晶过程中共同的重要作用,由此提出并说明了包合物锚定模型。

图8 MP-AFP的冰结合区及其包合物锚定模型结构[42]Fig.8 Marinomonas primoryensis (MP)-AFP ice-binding site and its inclusion anchoring model structure[42]
此后,先后有不少研究者进一步解释和拓展了包合物锚定理论模型。Chakraborty等[43]在研究云杉蚜虫sbwAFP与冰-水界面层相互作用机制中,通过分子模拟研究发现,由苏氨酸残基排列形成甲基侧链(THR阶梯),同时苏氨酸羟基与少量接近THR阶梯的那些高度有序的水分子形成强氢键,使sbwAFP围绕IBS通过氢键作用锚定包合水并实现在冰晶基面上固定(图9)。
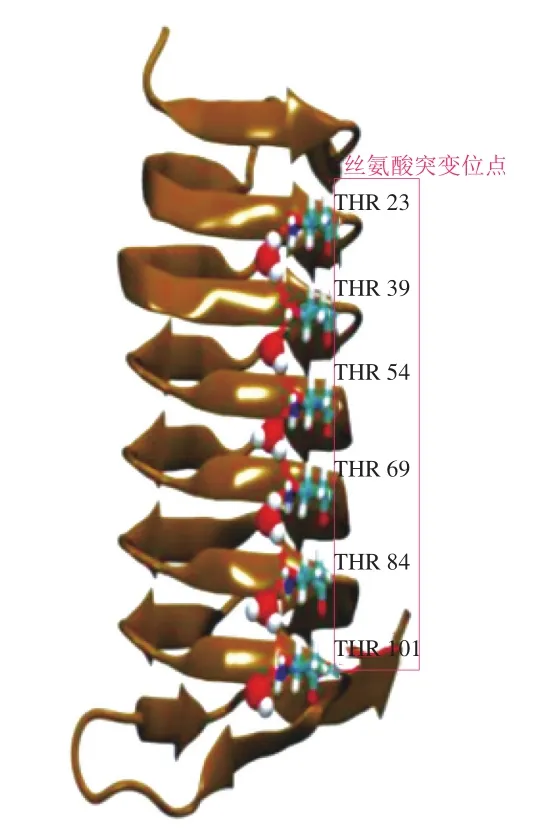
图9 sbwAFP分子中THR阶梯侧链结构及其包合物锚定模型结构[43]Fig.9 sbwAFP THR ladder side chain structure and its inclusion complex anchor model structure[43]
吸附的sbwAFP-冰复合物在特定热滞值范围内经历动态交换形成氢键结合的复合物。Chakraborty等[44]通过自由能计算分析进一步发现sbwAFP对不同冰面的结合亲和力顺序为基面>棱柱面>棱锥面,而且平面特异性主要与包合水的数量及其瞬时波动密切相关,且包合水与sbwAFP的IBS和冰表面形成双氢键,从而将AFP锚定在冰表面。在基面上,由于冰表面氧原子重复距离和IBS处苏氨酸重复距离的周期性是精确匹配的,因此锚定包合物-水的排列非常稳定。在棱镜平面吸附的情况下,IBS处苏氨酸重复距离与氧原子重复距离之间的匹配度较低,而在锥体平面吸附的情况下该匹配最低,因此锚定包合物-水阵列的稳定性随棱镜和锥平面吸附而逐渐降低。进一步分析发现,苏氨酸残基的甲基侧链在稳定被固定的包合水中起主要作用。其周围的水合作用在低温下变得非常显著,从而稳定了锚定的包合物-水阵列,而包合水与sbwAFP的IBS和冰表面形成的双氢键是这种稳定性的结果。
此外,Hudait等[45]使用分子模拟技术也发现高活性昆虫AFPs,如TmAFP、CfAFP和RiAFP具有TxT(T表示苏氨酸;x表示非保守氨基酸)重复结构特点的冰结合基序。该结合序列可使AFPs将水分子锚定在冰结合面上,从而使AFPs与冰晶结合。Sun Tianjun等[46]研究发现一种富含丙氨酸的四螺旋束二聚体的AFPs分子晶体结构核心保留了大约400 个水分子,其冰结合残基指向分子内部,并将内部水分子协调成两个相交的多角形网络,使螺旋束之间接触减少,并通过AFPs分子内部的主链羰基锚定到半包合水单分子膜上而稳定。有序的水分子向外延伸到蛋白质表面,与冰晶结合面进行结合,从而形成AFPs吸附到冰上的包合物锚定模型。Cheng Jing等[47]利用分子动力学模拟技术研究了牙鲆AFPs及其两个突变体在气相、溶剂化和水溶液等条件下吸附在冰晶基面上的作用模型。研究结果发现这些AFPs中的Asp、Asn和Thr残基在冰的结合中起重要作用;突变体氢键的数量越多,其抗冻活性就越大;同时范德华相互作用和疏水效应在冰结合中也起重要作用,且冰的表面有一个有利于疏水基团分配到冰表面的包合结构。
上述这些包合物锚定理论模型较好地揭示了冰-水界面层中的AFPs与其周围的水分子形成的水合作用在AFPs与冰晶结合过程中起到重要作用,并说明AFPs可通过氢键与疏水效应作用形成包合物,同时得到的水合结构的间隔能很好地将AFPs结合于冰晶棱面和基面上[41]。
2.6 亲和相互作用偶联团聚模型
相关研究显示,AFPs与冰晶相互作用过程中AFPs不仅与冰晶作用,而且可与冰晶界面层处其他组分发生亲和作用,影响或改变AFPs-冰晶复合体的分子结构[48]。研究指出,当AFPs-冰晶复合体与其他分子的亲和相互作用达到一定程度时,AFPs-冰晶复合体就会团聚起来,从而使冰核变大,表面自由能降低,冰晶生长被促进,AFPs呈破坏作用;反之,若亲和相互作用小,AFPs-冰晶复合体不团聚,AFPs仅起到抑制重结晶的作用,并有利于超低温保存。另外冷冻保护剂的组成和浓度、降温和复温速度、AFPs类型和浓度、最初冰晶数目,以及被冻细胞表面特征等,都可能影响亲和相互作用的强烈程度[1]。这种作用模式就是亲和相互作用偶联团聚模型。
亲和相互作用偶联团聚模型很好地解释了AFPs在超低温保存中具有双重作用。例如,一方面,AFPs在结合冰晶后所暴露的疏水面能够与细胞膜磷脂双分子层发生相互作用,对细胞起低温保护作用[1];另一方面,研究表明,II型AFPs是从C型动物凝集素(一类含有钙离子依赖糖识别域的蛋白质)中的碳水化合物识别区演化而来,因此II型AFPs可结合细胞膜上的糖蛋白[49]。体外实验证明,AFPs活性可通过一系列低分子化合物来增强或减弱。一种含有碳水化合物的细菌AFPs,既具有抗冻活性,又具有冰核活性(促进冰晶生长活性);去除碳水化合物部分,冰核活性也随之消失[50]。
亲和相互作用偶联团聚模型进一步揭示了其他组分对于AFPs与冰-水界面层相互作用过程的影响。这种影响是产生冰核效应还是抑制冰晶生长效应,还有待进一步研究。
3 结 语
AFPs所具有的独特抗冻活性一直以来广泛引起人们关注,因其不仅对低温生物体(如细胞结构)有着至关重要的生理作用,而且在食品工业、医药领域、生物材料保存、抗冻性相关转基因植物选育及抗冻材料开发等方面有着巨大的应用价值。然而,至今由于其种类和结构的复杂性,关于其在冷冻环境下到底如何调控冰-水界面层结构,以什么样方式与冰晶结合或互作从而实现其抑制冰晶生长,产生热滞活性和重结晶抑制活性一直以来未得到清晰而系统的解析。本文基于对以上问题的探讨,对国内外相关研究进行了综述,从几种典型的理论模型分析中,揭示了AFPs通过调控冰-水界面层结构产生结合或相互作用驱动力作用特点,解析了AFPs产生热滞活性和重结晶抑制活性的主要作用模式及其机理。其中吸附-抑制模型主要机理为AFPs通过氢键或疏水作用吸附到冰晶表面,通过Kelvin效应增加表面张力与改变冰晶表面曲率的变化抑制冰晶的生长速率和降低凝固点,从而使AFPs具有热滞活性;偶极子-偶极子模型认为AFPs可以基于AFPs分子中的α-螺旋极性与水分子极性的相互作用来阻止冰晶在基面(垂直于c轴)方向(a轴)上的生长;晶体占位-晶格匹配模型提出了AFPs与冰晶表层形成氢键或疏水作用,以及AFPs选择性吸附到特定冰晶结合面形成台阶固定及表面固定,从而使AFPs吸附到冰晶体上并阻止其生长;刚体能量模型较好地解释了黏附自由能是使AFPs运动至冰-水界面层的主要驱动力;包合物锚定理论模型较好地揭示了冰-水界面层中的AFPs与其周围的水分子形成的水合作用促进AFPs在冰晶棱面和基面上结合;亲和相互作用偶联团聚模型揭示了其他组分对于AFPs与冰-水界面层相互作用过程的影响,其作用既可以产生冰核效应也会产生抑制冰晶生长效应。
当然,每种理论模型都还有其不完善和不足之处,今后还需要应用更多的理论化学、物理化学、食品工程科学、计算机模拟技术以及原位分析的先进光谱成像技术(如冷冻电镜)来探究AFPs在复杂体系中对冰-水界面层结构调控机制,为开发更多具有应用价值的AFPs种类及促进其在食品、医药等工业领域中应用提供理论参考。
