安罗替尼治疗晚期非小细胞肺癌的疗效及安全性评价
2021-07-01陈丽娟叶永青李殿明
陈丽娟,叶永青,李殿明
肺癌是严重危害人类健康的疾病之一。肺癌主要分为小细胞肺癌(SCLC)和非小细胞肺癌(NSCLC),其中NSCLC进展较SCLC缓慢,是最常见的组织学类型,在肺癌病例中的比例超80%[1],但其侵袭性高,早期发现率低,我国68%的肺癌病人确诊时已是晚期,失去手术治疗机会。对于晚期NSCLC病人,药物治疗是重要的方法,对于一线、二线治疗失败的中晚期NSCLC病人,现有的三线治疗手段缺乏。研究[2]证实,新生血管的生成,对肿瘤的生长、转移发挥着重要的作用,抗血管生成药物可以改变肿瘤生长的环境,抑制肿瘤血管的生成,从而起到抗肿瘤作用。目前在我国批准用于晚期NSCLC治疗的抗血管生成药物有血管内皮生长因子抑制剂贝伐珠单抗、重组人血管内皮抑制素和小分子多靶点酪氨酸激酶抑制剂安罗替尼[3]。安罗替尼在2018年5月被中国食品监督管理局批准为难治性晚期NSCLC的第三线治疗方案[4],是至少接受过2种系统化疗后出现进展或复发的局部晚期或转移性NSCLC病人可选择的方案,也是中国第一批批准作为NSCLC病人三线治疗方案的药物。本研究选取NSCLC病人资料进行回顾性分析,对安罗替尼治疗晚期NSCLC病人的疗效及安全性进行评价。现作报道。
1 资料与方法
1.1 一般资料 2018-2019年期间入住六安市人民医院行安罗替尼治疗的病人50例,其中有45例病人接受安罗替尼三线治疗,5例病人接受四线治疗;3例因不良反应停药,47例病人纳入本研究;男38例,女9例;年龄46~86岁,平均年龄(66.89±9.83)岁;吸烟22例,不吸烟25例;ECOG评分为0~1分22例,2~3分25例;病理类型:腺癌21例,鳞癌26例;分期:ⅢB期6例,Ⅳ期41例;基因检测(EGFR突变或ALK重排):阳性4例,阴性21例,不详22例,阳性病人已接受相应靶向药物治疗且出现耐药;接受过贝伐珠单抗治疗病人9例,未接受病人38例。
1.2 纳入标准 经细胞学或组织学确诊的晚期非小细胞肺癌;病人年龄≥18岁;ECOG评分为0~2 分;预计生存时间≥3 个月;至少接受过2种系统化疗后出现进展或复发的局部晚期或转移性NSCLC;至少有一个可测量病灶作为靶病灶(根据 RECIST v1.1标准);纳入的脑转移病人必须是接受治疗后病情稳定的,无明显颅脑压迫症状;纳入的病人相关实验室检查指标及心肺功能基本正常;签署知情同意书。
1.3 排除标准 同时接受除安罗替尼以外其他抗肿瘤治疗;化疗期间方案调整;无可测量病灶作为靶病灶;2个周期化疗后未行疗效评价的病人;肝肾功能、血常规、心电图等检查异常。
1.4 治疗方法 本研究符合《世界医学协会赫尔辛基宣言》相关要求。所有病人均接受口服安罗替尼(正大天晴药业集团股份有限公司,生产批号:180809132、190318232、190606183)治疗,起始剂量根据病人具体情况指导为12 mg或10 mg或8 mg,连续服用2周,停药1周,3周为一个周期。治疗持续到疾病进展或病人不能耐受。如果病人不能耐受12 mg/d,可将剂量减至10 mg/d或8 mg/d,如仍不能耐受,则停止治疗。
1.5 临床评价 病人每2个周期评估一次疗效,本研究的主要研究终点是总生存时间(OS),次要终点是疾病控制率(DCR)、无进展生存时间(PFS)及安全性。根据不良事件的发生对治疗的安全性进行评价,并按照国家癌症研究所不良事件通用术语标准4.03版对不良事件进行分级。
根据实体瘤评价标准(RECIST1.1)[5]:完全缓解(CR),所有靶病灶消失,任何病理性淋巴结(无论是否为目标病灶)的短轴值必须<10 mm;部分缓解(PR),以基线状态总直径为参照,所有目标病灶直径的总和至少减少30%;病情进展(PD),以最小病灶直径综合为参考(包括基线下病灶直径总和,假如其为最小值),所有目标病灶直径总和至少增加20%,其总和的绝对值必须增加至少5 mm;病情稳定(SD),以研究过程中最小病灶直径总和为参照,病灶缩小既不符合PR,病灶增加也不符合PD。
PFS:从服用安罗替尼的第一天到记录进展或因任何原因死亡的时间。OS:从使用安罗替尼治疗的第一天到死亡或最后随访的时间。
1.6 统计方法 采用Kaplan-Meier方法及Log-rank检验。
2 结果
2.1 临床疗效 47例病人中,PR 2例,SD 24例,PD 21例。客观缓解率(ORR)及DCR分别为4.26%(2/47)和55.32%(26/47)。中位OS(mOS)及中位PFS(mPFS)分别是8.6个月(95%CI5.853~11.347)和4.8个月(95%CI2.904~6.696)。PFS及OS在不同年龄、不同性别等临床特征之间差异均无统计学意义(见表1~2)。
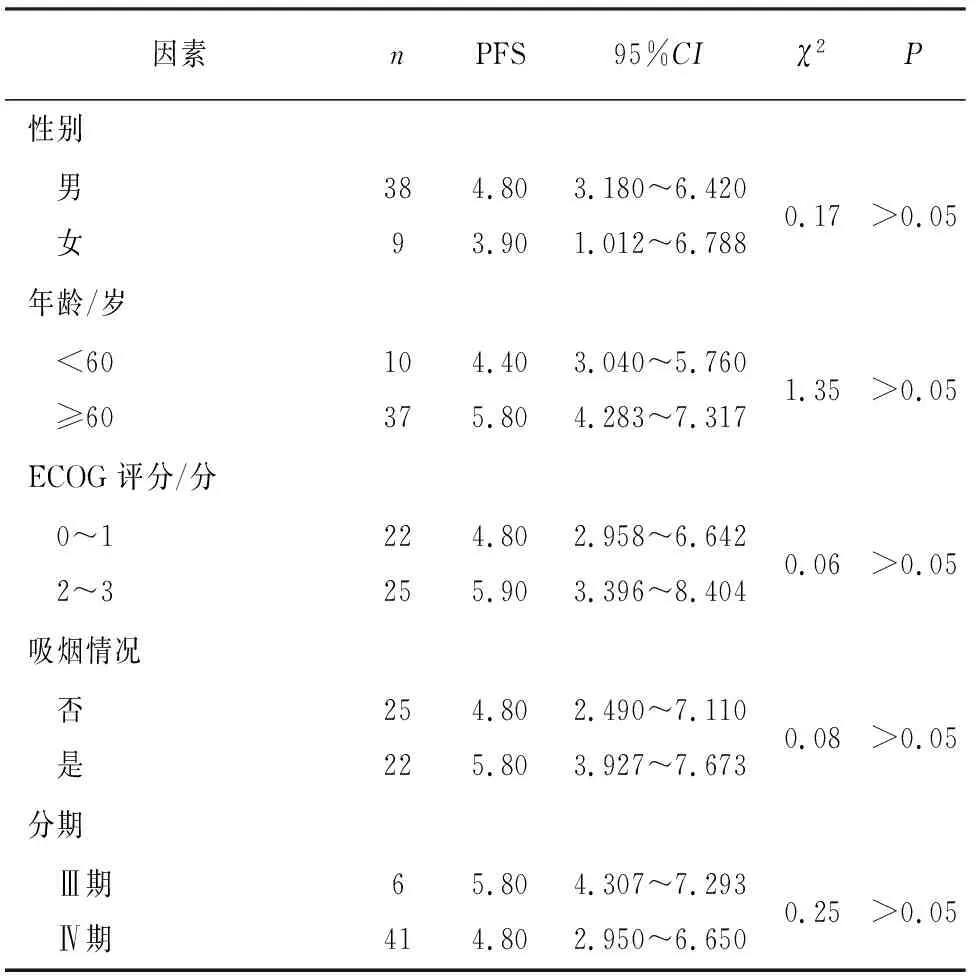
表1 病人PFS单变量分析
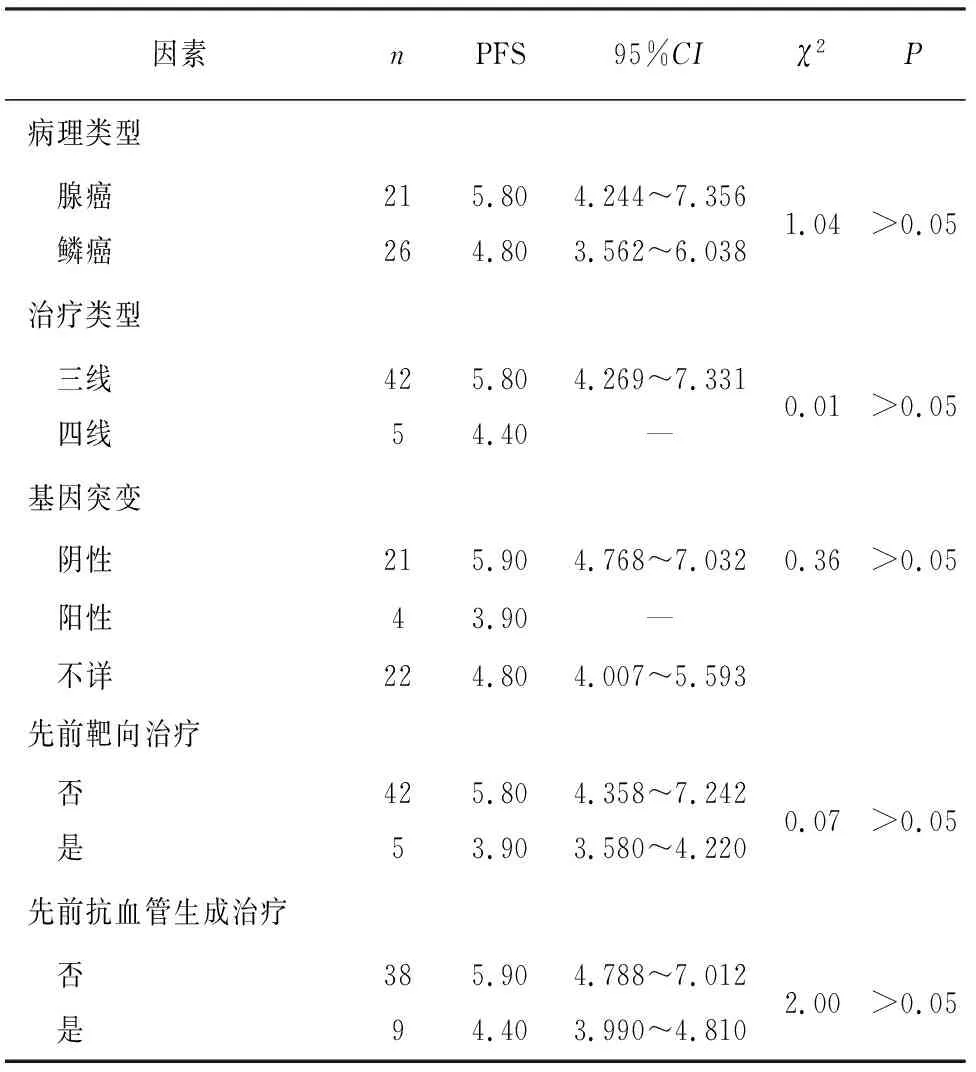
续表1
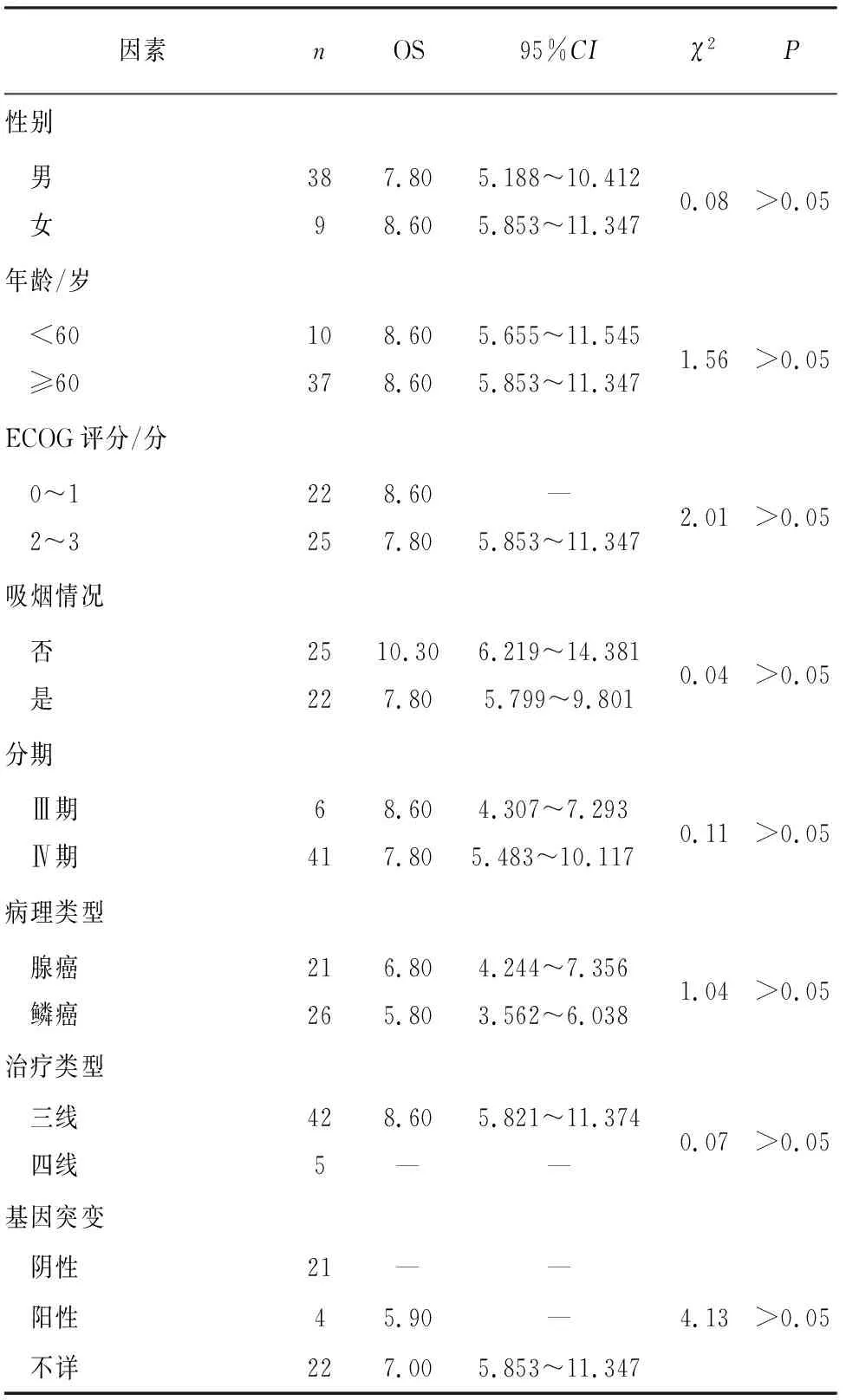
表2 病人OS单变量分析
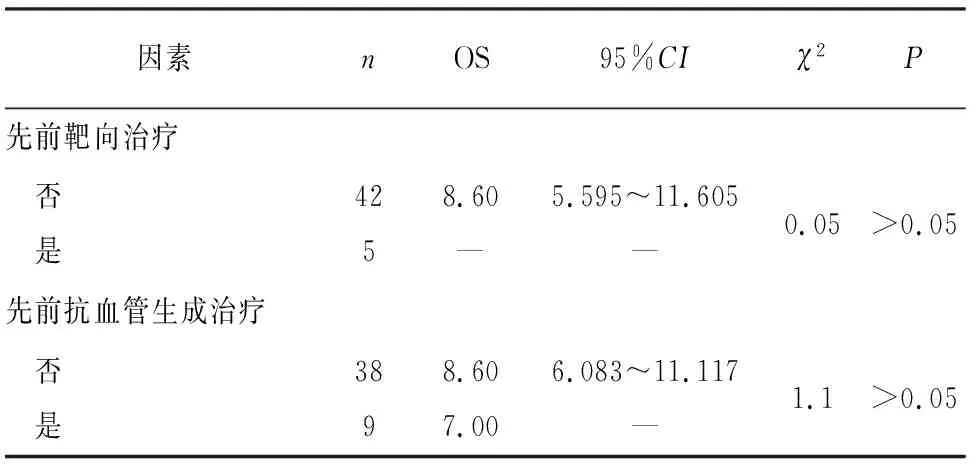
续表2
2.2 不良反应 随访过程中对所有病人的不良反应进行评估。本研究中病人常见的不良反应分别有厌食(12.0%)、咯血(12.0%)、肝功能异常(8.0%)、手足综合征(8.0%)、高血压(4.0%)等。有3例病人因腹泻、手足综合征及血尿而停药(见表3)。
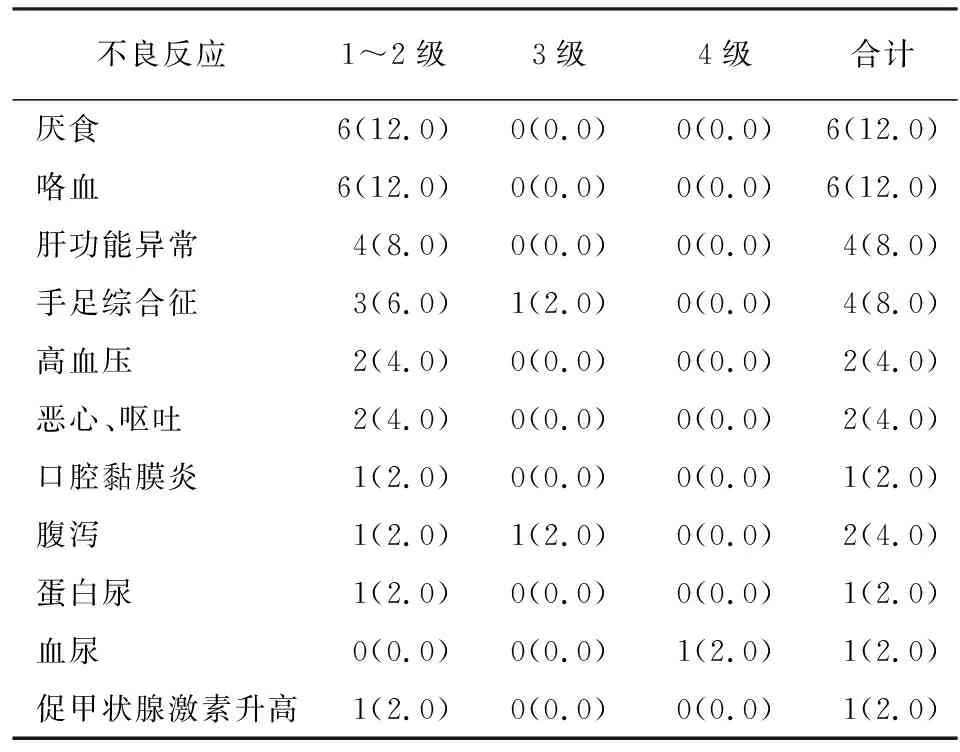
表3 安罗替尼治疗后病人发生的主要不良事件[n;百分率(%)]
3 讨论
本研究是关于安罗替尼治疗晚期NSCLC的有效性和安全性的研究,数据收集截至2020年2月,研究结果提示安罗替尼用于晚期NSCLC三线治疗是有效的,且耐受良好。
根据2015年中国癌症最新统计数据,肺癌的发病率和致死率均居首位[6]。对于晚期NSCLC病人,靶向治疗、免疫治疗和化疗可延长生存时间,并被推荐为晚期NSCLC的标准治疗[7-9],但无论哪种治疗方式,病人对既往使用药物均会出现耐药反应,需调整药物。目前,对于二线耐药后的方案选择仍缺乏。安罗替尼作为一种抗血管生成药物,已经被推荐用于晚期肺癌三线及以上的治疗。
受体酪氨酸激酶的异常激活或构成性激活与多种肿瘤细胞的增殖、存活和转移有关[10]。血管内皮生长因子及受体在血管生成中起到重要作用,对肿瘤诱导的新生血管形成非常重要[11]。安罗替尼作为一种多靶点受体酪氨酸激酶抑制剂,主用于抑制血管内皮生长因子受体、血小板衍生生长因子受体、干细胞因子受体和成纤维细胞生长因子受体,该药对肿瘤血管生成和生长有广泛的抑制作用[12],可用于晚期NSCLC三线及以上的治疗[13-16]。研究[17]显示,安罗替尼PFS优于安慰剂,明显延长了PFS。同样在关于安罗替尼的Ⅲ期实验(ALTER 0303)中显示安罗替尼组病人的 OS 为9.63个月,PFS 5.37个月,DCR 80.95%,ORR 9.18%,证明安罗替尼用于晚期NSCLC三线治疗有良好的耐受性,可以显著延长OS和PFS,是治疗晚期NSCLC的可行方案[18]。本研究中,mOS及mPFS分别是8.6个月和4.8个月,与这些研究结果相近。本研究老年病人(年龄≥60岁)居多,结果显示老年组的mOS及mPFS分别为8.6个月、5.8个月,老年病人对于安罗替尼的治疗同样获益。本研究的DCR及ORR分别是55.3%和4.3%,与同类研究相比较低,考虑可能与样本量少,病人年龄大、依从性较差等因素有关。
应用安罗替尼发生的主要不良反应是高血压、疲劳、促甲状腺激素升高、厌食、手足综合征等,本研究中主要发生的不良反应是厌食和咯血,但总体发生率低。在关于安罗替尼Ⅲ期实验不良反应的文章中较少提及血尿[19],但本研究中有3例病人因不良反应停药,分别是腹泻、手足综合征及血尿,其中发生血尿病人为4级不良反应。
本研究的不足之处首先研究为回顾性分析,其次,在随访过程中会因病人主观性原因造成偏差,且研究的样本量较少。总之,安罗替尼作为推荐的晚期NSCLC三线及以上治疗,有效且可耐受,老年病人对于安罗替尼的治疗同样获益。在治疗过程中需全程管理,严密监测不良反应。
