碱式硫酸镁晶须的可控制备及不同离子的影响机制
2021-06-30张少博方莉高雪焘程文婷
张少博,方莉,高雪焘,程文婷
(1山西大学化学化工学院,山西太原030006;2山西大学资源与环境工程研究所,山西太原030006)
引 言
无机盐晶须作为一种新型的纤维材料,由于其优异的耐高温、耐腐蚀性能以及良好的机械强度等,近年来被广泛用于高分子复合材料的增强增韧补强剂,可显著提高基底材料的拉伸强度、抗弯曲强度和抗冲击强度[1-3]。相较于其他无机盐晶须,镁盐晶须如氢氧化镁[4]、碱式硫酸镁[5]、硼酸镁[6]以及碳酸镁等[7],具有长径比高(50~200)、密度小、弹性模量和热分解温度高等优点,不仅可改善高分子材料的力学性能,还具有优异的阻燃性能[8-9]。特别是碱式硫酸镁晶须(magnesium hydroxide sulfate hydrate whisker,MHSH),由于具有更宽的热分解温度区间(260~1150℃),阻燃性能更好[10]。
碱式硫酸镁晶须的化学式为xMg(OH)2·yMgSO4·zH2O,通常用MHSH-xyz表示,如MHSH-512[11]和MHSH-513[12]等,制备方法主要有水热法、微波法和热回流法。其中,微波法制备的晶须长径比小(10~20)[13],热回流法制备的晶须长径比为40~200,但均一性较差,且反应时间过长(约30 h)[14],而水热法制备的晶须不仅纯度高、长径比大,而且反应条件易控制。因此,目前一般采用水热法制备MHSH晶须。而MHSH晶须的性能和微观形貌不仅与原料来源及配比、水热反应条件(如温度、时间)等有关,还可能受到杂质离子的影响。Tang等[15]以Mg(OH)2和MgSO4为原料,直接在160℃下水热反应10 h制备了长径比大于100的MHSH-513晶须,但是其原料中MgSO4需大量过量[MgSO4与Mg(OH)2的摩尔比高达7∶3],原子经济性差。高传慧等[16]在以MgSO4和NH3·H2O为原料制备MHSH-512晶须时发现,温度低于170℃时无法为晶须成核提供足够的能量,其水热产物为晶须和Mg(OH)2的混合物。岳涛等[17]以MgSO4和NaOH为原料在160℃下水热制备了MHSH-512晶须,研究表明反应时间超过24 h后会导致晶须团聚。Xiang等[18]以MgSO4和NaOH为原料先制备Mg(OH)2·MgSO4前驱物,然后在200℃下水热反应4 h,得到了长径比为20~100的MHSH-513晶须,并发现当前驱物活性较高时,晶须形貌更加规整。Li等[19]以过量的MgSO4和NaOH为原料先制得Mg(OH)2前驱物和MgSO4的混合物,然后于200℃下水热反应制备了长径比为80~100的MHSH-513晶须。研究表明,乙二胺四乙酸可与Mg2+络合,提高前驱物Mg(OH)2的活性。Yan等[20]以MgSO4和MgCl2为混合镁源,NH3·H2O为沉淀剂,在150℃下水热反应38 h合成了MHSH-512晶须。研究发现,当c(Mg2+)/c(SO2-4)(摩尔浓度)为1.6~2.5时可得到长径比为 150~200的MHSH-512一维扇形晶须,且扇形晶须的团聚端为未生长完全的Mg(OH)2,但是未考虑Cl-对水热产物的影响。Gao等[21]以卤水、NH3·H2O和MgSO4为原料,于190℃下水热反应4 h得到了长径比为50~200的MHSH-512晶须,并推断卤水中的K+、Cl-和Li+等离子的存在对晶核的形成可能有影响,但没有进一步验证和分析其影响机制。
到目前为止,关于不同离子浓度以及杂质离子等对MHSH晶须的生长及形貌影响尚未见系统的研究报道。此外,乌志明[22]发现MHSH-513与MHSH-512晶体结构相似,仅多出一个极不稳定的沸石水,加热到100℃时就会失去而转变为更加稳定的MHSH-512[23-24]。由于聚合物材料的加工温度一般为150~300℃[25],掺杂MHSH-513晶须可能会因加工过程中脱去沸石水而产生气泡,影响材料的加工性能和力学性能。因此,MHSH-512晶须更适合用作高分子材料的阻燃剂。鉴于此,本文以MgCl2、NaOH和MgSO4为原料,采用溶胶-凝胶-水热法,在高压反应釜中制备了MHSH-512晶须,系统研究了前驱物Mg(OH)2、Mg2+和SO2-4的浓度和杂质离子Cl-对MHSH-512晶须的生长机制和微观形貌的影响,提出了杂质离子存在时MHSH-512晶须的生长机制。所制备的MHSH-512晶须为一维结构,且表面光滑、长径比高,易于实现工业化生产,为青海盐湖镁资源的高值化利用提供了一条有效途径和技术支撑。
1 实验部分
1.1 实验试剂
六水氯化镁(MgCl2·6H2O,AR)、硫酸镁(MgSO4·7H2O,AR)购自国药集团化学试剂有限公司,氢氧化镁[Mg(OH)2,AR]、氢氧化钠(NaOH,AR)购自上海麦克林生化有限公司。
1.2 MHSH-512晶须的制备
(1)溶胶-凝胶法制备前驱物Mg(OH)2溶胶:在500 ml的三口烧瓶中加入150 ml浓度为1 mol/L的MgCl2溶液,升温至60℃后,搅拌下缓慢滴加150 ml浓度为2 mol/L的NaOH溶液,恒温反应2 h后得到前驱物Mg(OH)2溶胶[记作MH(gel)]。
(2)水热法制备MHSH-512晶须:将得到的MH(gel)转移至1 L的高压反应釜中,加入300 ml浓度为0.1~2 mol/L的MgSO4溶液后,升温至150~210℃进行水热反应;冷却至室温后将水热产物过滤分离,并用蒸馏水和乙醇交替洗涤3次,在80℃下真空干燥6 h,得到MHSH-512晶须。
1.3 MHSH-512晶须的表征
产物的物相结构采用D8-ADVANCE型X射线衍射仪(XRD,德国Bruker公司)进行表征,扫描速率为2(°)/min,扫描范围10°~70°;产物的形貌在JSMIT500HR型扫描电镜显微镜(SEM,日本JEOL公司)上进行观察,扫描电压5 kV,放大倍数50~3000;前驱物的Zeta电位和电导率在Nano Zs90型Zeta电位仪(英国马尔文仪器有限公司)上进行测试。
2 实验结果与讨论
2.1 前驱物氢氧化镁的活性和分散性对MHSH-512晶须形貌的影响
为了探讨前驱物Mg(OH)2的活性和分散性对MHSH-512晶须形貌的影响,分别以新制备的MH(gel)和购买的沉淀Mg(OH)2[简写为MH(d)]为前驱物,按照Mg2+和SO2-4浓度比为3投料,在190℃下水热反应10 h得到MHSH-512晶须,并进行XRD和SEM表征,结果如图1和图2所示。
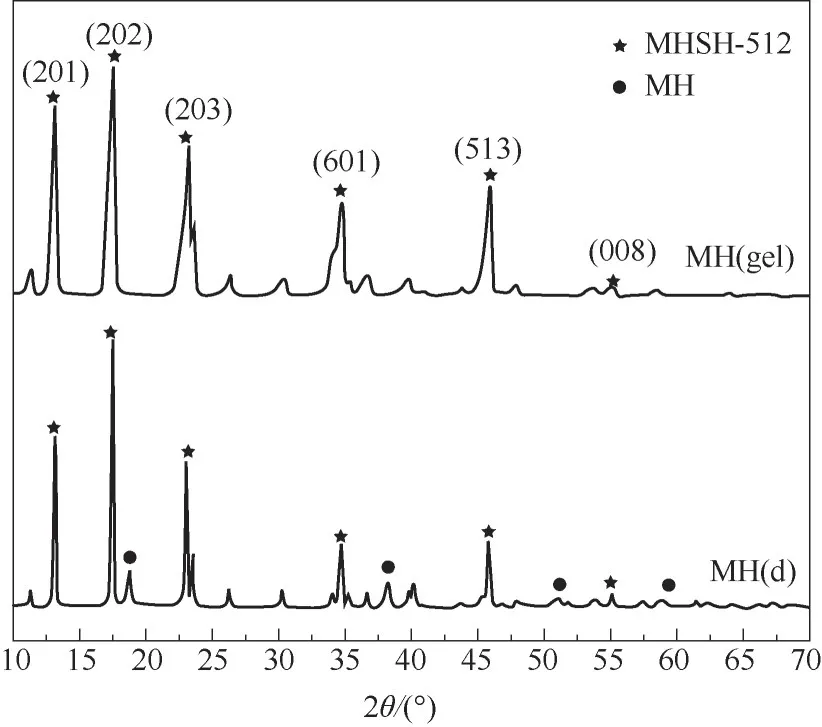
图1 不同MH前驱物合成的MHSH-512晶须的XRD谱图[c(Mg2+)/c(SO42-)=3,190℃,10 h]Fig.1 XRDpatternsof MHSH-512 whiskers synthesized with different MH precursors
从图1中看出,以MH(gel)为前驱物制备的水热产物在12.94°、17.32°、22.86°、34.48°、45.62°和54.9°出现了MHSH-512晶须的特征衍射峰,与标准卡片JCPDSNo.86-1322相一致,可分别归属于(201)、(202)、(203)、(601)、(513)和(008)晶面,且没有其他杂峰,说明产物的结晶度和纯度非常高[17]。同时,在与之对应的SEM图[图2(a)、(b)]中可看到长径比为150~200、表面光滑的MHSH-512晶须。相比较而言,以MH(d)为前驱物时得到的产物虽然也出现了MHSH-512晶须衍射峰,但在18.58°、37.96°、51.06°和58.56°处仍有明显的MH特征峰,且在图2(c)、(d)中可观察到大量的颗粒状物质,进一步证实了产物中残余大量未反应的MH(d)[26],这一结果与MH前驱物的活性和分散性有极大的关系。如图3(a)所示,新制备的MH(gel)在放置24 h后仍然保持稳定的胶体分散状态,其电导率和Zeta电位分别为68.45 mS/cm和24.0 mV,说明MH粒子高度分散、反应活性高,在水热过程中易发生溶解再结晶反应,形成结晶度高、长径比大、表面光滑的MHSH-512晶须[18]。而市售沉淀MH(d)的结晶度高、结构稳定,在水中搅拌分散后静置0.5 h就全部沉淀[图3(b)],静置24 h后的电导率和Zeta电位仅为1.07 mS/cm和1.45 mV,说明其分散性差、反应活性低,因此在水热过程中不易解离为Mg2+和OH-,阻碍MHSH-512晶核形成,导致MH(d)反应不完全。

图2 不同MH前驱物合成的MHSH-512晶须的SEM图[c(Mg2+)/c(SO24-)=3,190℃,10 h]Fig.2 SEM images of MHSH-512 whiskers synthesized with different MH precursors

图3 氢氧化镁前驱物静置24 h后的分散状态Fig.3 Dispersion states of different precursors after 24 h standing
2.2 不同硫酸根离子浓度下MHSH-512晶须的形成和生长机制
作为反应物之一的SO2-4,其浓度直接影响MHSH-512晶须的形成和生长[19]。图4、图5是不同原料浓度比[c(Mg2+)/c(SO2-4)]时得到的水热产物的XRD谱图和SEM图。
当c(Mg2+)/c(SO2-4)为6,即按照计量比投料时,其水热产物的XRD谱图中主要是MH的特征衍射峰,而MHSH的特征峰极其微弱,说明此时没有形成晶须。从图5中对应的SEM图也可以证实,水热产物的微观形貌仅为片状MH,没有晶须出现。但是,当c(Mg2+)/c(SO2-4)为4.3时,MHSH-512晶须的特征峰急剧增强,而MH晶体的衍射峰几乎完全消失,且直到浓度比变为2.6时,晶须的特征峰也没有明显变化(图4)。然而从SEM图发现,当c(Mg2+)/c(SO2-4)为4.3时,晶须表面仍然可看到少量颗粒状物质,可归属于未反应完全的MH颗粒;当c(Mg2+)/c(SO2-4)为3.5~2.6时,MHSH-512晶须的直径为2~3μm,长径比高达150~200,且表面光滑、分散性好。

图4 不同c(Mg2+)/c(SO24-)时合成的水热产物的XRD谱图(190℃,10 h)Fig.4 XRDpatterns of hydrothermal products synthesized with different c(Mg2+)/c(SO24-)ratios

图5 不同c(Mg2+)/c(SO24-)时水热产物的SEM图(190℃,10 h)Fig.5 SEMimages of hydrothermal products prepared with different c(Mg2+)/c(SO24-)ratios
当c(Mg2+)/c(SO2-4)减小至2.2~2时,虽然在XRD谱图上没有出现新的衍射峰,但是MHSH-512晶须的(202)、(203)和(008)晶面衍射峰却明显增强,同时伴随着(201)、(601)和(513)晶面特征峰的急剧减弱。从SEM图也可以看到,晶须尺寸明显增大,分散性变差,且表面重新出现了一些颗粒状物质。继续减小c(Mg2+)/c(SO2-4)至1.5时,MHSH-512晶须的特征峰全部消失,取而代之的是在26.68°、27.65°、34.1°处出现了新的衍射峰,可归属于一种无水碱式硫酸镁[Mg(OH)2·2MgSO4],与标准卡片79-1189相一致[27]。与之对应的SEM图中,水热产物呈现出团球状微观形貌,进一步证实了XRD结果。
在水热反应条件下,MHSH晶须的形成需经历MH固体的溶解和再结晶过程[28],即MH固体颗粒在溶液中解离成Mg2+和OH-,先形成游离的六配位八面体结构单元[Mg(OH)6]4-[29],然后这些结构单元之间以Mg-O-Mg键相互连接,同时与SO2-4形成Mg-O-S键相连接,形成MHSH晶核。晶核之间再通过氢键彼此结合,以b轴为主轴不断生长为一维结构的MHSH-512晶须[20,30]。根据上述表征结果,推测了不同SO2-4离子浓度对MHSH-512晶须形成和生长的影响机制。
当c(Mg2+)/c(SO2-4)为6时,按计量比理论上可形成MHSH-512晶体,但是由于溶液中SO2-4浓度较低,且S-O键比Mg-O键的键能略小,导致[Mg(OH)6]4-结构单元难以与SO2-4形成Mg-O-S键,只能进一步通过氢键相结合生长为MH晶核[30],最终生成MH片状晶体。当c(Mg2+)/c(SO2-4)减小至4.3时,SO2-4离子的浓度按照计量比增大了1.5倍,[Mg(OH)6]4-容易与SO2-4通过Mg-O-S键相连形成晶核,进而生长为MHSH-512晶须。但是,由于SO2-4浓度过量不够多,仍然有部分[Mg(OH)6]4-未能与SO2-4之间形成Mg-O-S键,导致MH反应不全,晶须收率较低(59%)。当SO2-4过量2~3倍,即c(Mg2+)/c(SO2-4)为3.5、3和2.6时,[Mg(OH)6]4-与大量的SO2-4通过Mg-O-Mg键和Mg-O-S键形成稳定的MHSH晶核,并以b轴为主轴不断生长,形成结晶度高、长径比大、表面光滑且分散性好的一维晶须,其收率分别为77%、80%和79%。考虑到原料经济性,确定最佳的离子浓度比为3。
当c(Mg2+)/c(SO2-4)为2.2~2,即SO2-4过量4~5倍时,[Mg(OH)6]4-更容易与SO2-4成键,导致MHSH晶核数量急剧增加而发生堆积,形成尺寸过大、分散性较差的扇形晶须。此外,过剩的SO2-4包裹在[Mg(OH)6]4-表面,阻碍了Mg-O-Mg键的形成,导致这些结构单元表面主要以Mg-O-S键为主,形成Mg(OH)2·2MgSO4晶体。而继续减小c(Mg2+)/c(SO2-4)至1.5,即SO2-4过量10倍时,[Mg(OH)6]4-结构单元的表面几乎全部被SO2-4包覆,生成的水热产物全部为Mg(OH)2·2MgSO4。
2.3 氯离子对MHSH-512晶须形成和生长的影响机制
为了探讨Cl–对MHSH-512晶须形成和生长的影响机制,将溶胶-凝胶法得到的MH(gel)通过反复洗涤、离心分离后得到纯MH(gel)前驱物,然后在c(Mg2+)/c(SO2-4)为3,190℃的条件下进行水热反应。图6、图7分别为Cl–去除前、后不同反应时间得到的水热产物的XRD和SEM图。
从图6(b)所示除去Cl–后制得水热产物的XRD谱图看出,反应2 h就出现了微弱的MHSH特征峰,但由于生成的晶体量太少,且结晶度低,因此在相应的SEM图(图7)中看不到晶须;至3 h时,MH特征峰急剧减弱,MHSH-512晶须的特征峰显著增强,同时其微观形貌为表面覆盖了大量MH颗粒的粗糙晶须;反应至4 h时,MH的特征峰完全消失,但相应的SEM图中晶须表面仍然有少量的颗粒状物质,且晶须的分散性较差;反应至8~10 h,MHSH-512晶须的特征峰强度达到最高,说明晶须的纯度和结晶度高,且相应的微观形貌呈长径比大(150~200)、表面光滑、分散性好的晶须。继续反应至12 h,虽然其XRD谱图没有明显变化,但是从微观形貌看有重新团聚的趋势。
相比较而言,当有Cl–存在时,MHSH-512晶须的形成和生长的速度明显降低[图6(a)]。水热反应3 h后出现了微弱的MHSH特征衍射峰,且在其相应的SEM图(图7)中只有极少量表面粗糙的晶须,主要以块状物和颗粒状物质为主;反应4 h时,MHSH-512晶须的特征峰明显增强,但MH的特征峰仍占主导,其SEM图中的晶须表面粗糙、分散性差,且有大量未反应的MH颗粒。反应至6~8 h时,虽然MH特征峰几乎完全消失,但是从SEM图看到,水热反应8 h后还有一些颗粒状物质覆盖于晶须表面,直到反应10~12 h,才呈现出表面光滑、分散性好的MHSH晶须。由此可知,Cl–的存在明显阻碍了MHSH-512晶须的形成和生长。
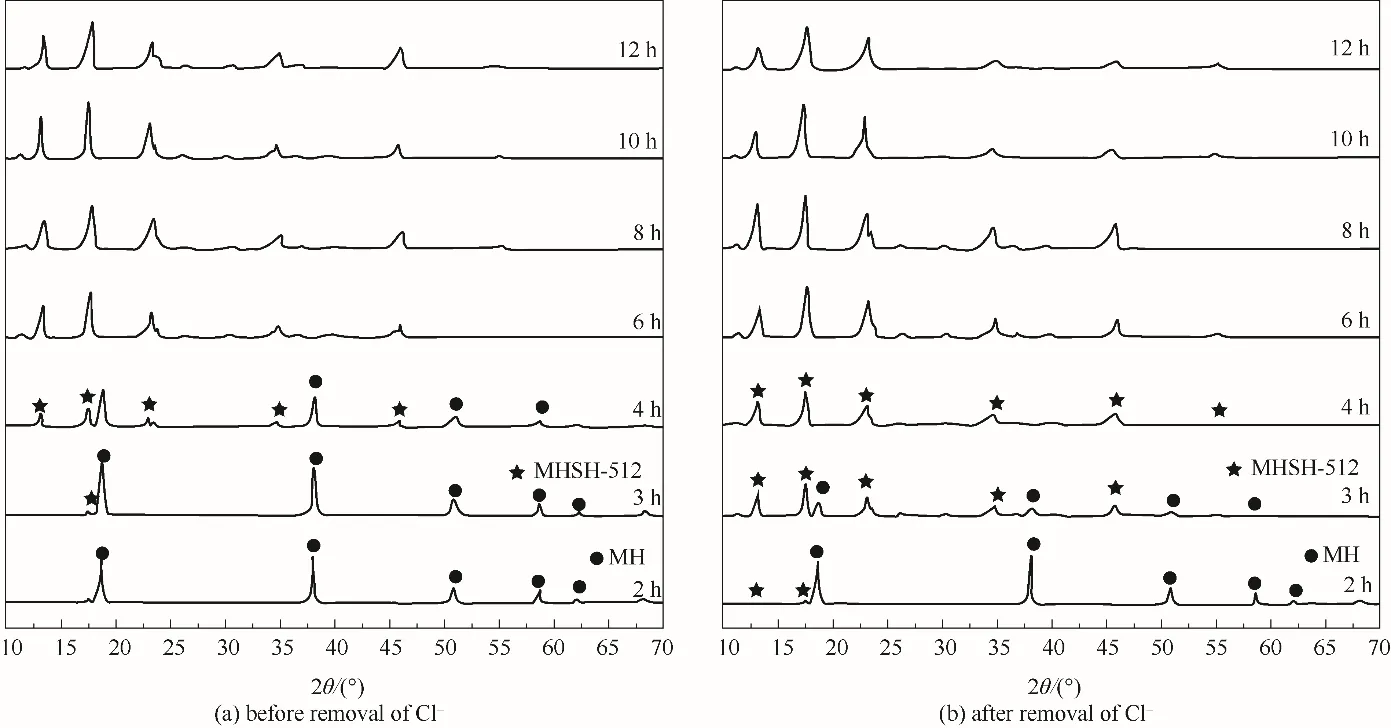
图6 去除Cl-前、后合成的MHSH-512晶须的XRD谱图[c(Mg2+)/c(SO24-)=3,190℃]Fig.6 XRDpatterns of MHSH-512 whiskerssynthesized before and after removal of Cl-

图7 不同水热时间去除Cl-前、后合成的MHSH-512晶须的SEM图[c(Mg2+)/c(SO24-)=3,190℃]Fig.7 SEMimages of MHSH-512 whiskers synthesized before and after removal of Cl–with different hydrothermal treatment time
图8为去除Cl-前后MHSH-512晶须的形成与生长机理示意图。去除Cl–后,溶液中只有MgSO4和MH(gel),在溶解再结晶过程中没有Cl-的干扰,Mg2+与OH–之间易形成[Mg(OH)6]4-,并进一步与SO2-4通过Mg-O-S键形成MHSH晶核,从而生长为MHSH-512晶须。而未除去Cl–时,溶液中除了MgSO4之外,还含大量Cl-和Na+,离子强度高,静电作用力大,导致Mg2+和OH-的活度因子减小、活度降低,促进MH(gel)在水热过程中的溶解平衡向解离方向移动[31]。但是,Cl-又可通过静电引力在Mg2+周围形成离子氛,阻碍OH-与Mg2+之间相互作用,延缓结构单元[Mg(OH)6]4-的形成。此外,大量存在的Cl–还可能与SO2-4发生竞争吸附,使结构单元[Mg(OH)6]4-表面的SO2-4数量减少,导致MHSH-512晶须的形成和生长滞后。
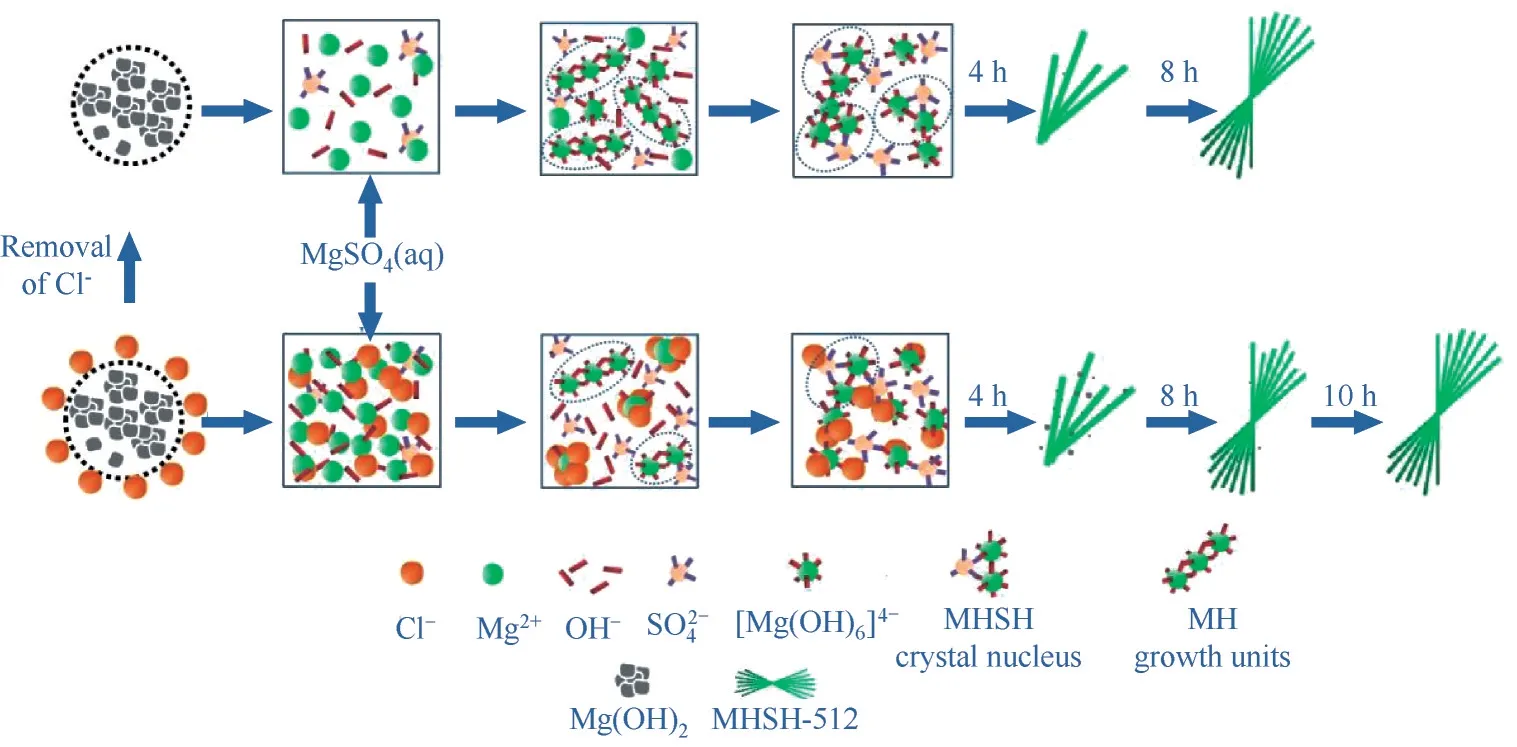
图8 去除Cl–前、后MHSH-512晶须的形成与生长机理示意图Fig.8 A schematic diagramof the formation and growth mechanisms of MHSH-512 whiskers before and after removal of Cl–
综上所述,去除Cl-后,生成结晶度高、长径比大、表面光滑且分散性好的MHSH-512晶须的水热反应时间为8 h,而有Cl–存在时则需要10 h,但是Cl-对MHSH-512晶须的最终形貌和分散性并没有明显的影响。此外,由于工业化生产过程中,前驱物MH(gel)的洗涤、分离等工序所需的人力、物力和能耗与延长2 h的反应时间相比要高得多,且流程更复杂,因此在实际生产中没有必要去除Cl–。
2.4 水热反应温度对MHSH-512晶须形成和生长的影响
不同温度下水热产物的XRD和SEM表征如图9和图10所示。150℃时,XRD谱图中只有MH晶体的特征峰,相应的SEM图中呈现的也是MH片状晶体团聚物,说明水热过低时,MH(gel)溶解缓慢,不利于MHSH晶须的形成[16,32]。当温度升至160℃时,XRD谱图中仍然以MH晶体的特征峰为主,只有微弱的MHSH特征峰,且其微观形貌主要呈颗粒状,仅能看到极少量的晶须。170℃时,出现了明显的MHSH-512晶须特征峰,同时MH晶体的特征峰几乎完全消失,但其微观形貌为分散性差的扇形晶须,且表面可观察到大量MH颗粒状物质。随着温度升高至180、190℃时,MHSH-512晶须衍射峰逐渐增强,峰型由宽变窄,说明结晶度增大;从对应的SEM图中也看出,180℃时,晶须的分散性有所提高,但表面光滑度较差;而到190℃时,扇形晶须显著减少,且形成的晶须长径比达150~200、表面光滑、分散性好。但是,当温度继续升高至200~210℃时,晶须特征峰强度减弱,峰型变宽,从微观形貌也可看出,晶须发生团聚而形成尺寸急剧增大、分散性差的扇形晶须,这可能是因为温度过高时,晶须成核速率过快,导致晶核堆积、生长过快,易发生团聚。因此,最适宜的水热反应温度为190℃。
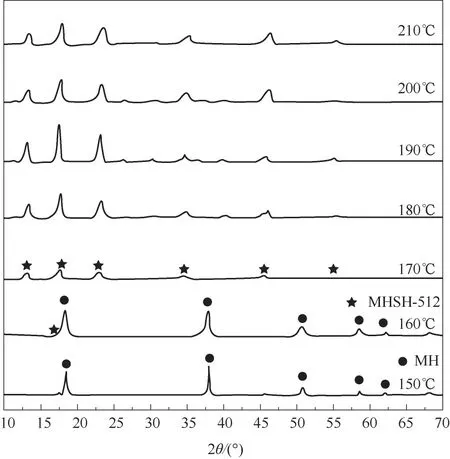
图9 不同水热温度下合成产物的XRD谱图[c(Mg2+)/c(SO24-)=3,10 h]Fig.9 XRDpatterns of the hydrothermal products synthesized at different temperatures

图10 不同水热温度下合成产物的SEM图[c(Mg2+)/c(SO24-)=3,10 h]Fig.10 SEM imagesof the hydrothermal products synthesized at different temperatures
3 结 论
通过研究溶胶-凝胶-水热法制备MHSH-512晶须过程中反应物离子浓度、水热条件和杂质离子对晶须生长机制的影响,得到以下主要结论。
(1)溶胶-凝胶法得到的前驱物MH(gel)分散性好、反应活性高,在后续水热条件下的溶解再结晶过程中易形成结构单元[Mg(OH)6]4-。
(2)适当过量的SO2-4对MHSH-512晶须形成和生长具有重要作用,当c(Mg2+)/c(SO2-4)为3.5~2.6时(SO2-4过量2~3倍),几乎全部的[Mg(OH)6]4-可与SO2-4之间形成MHSH晶核,并以b轴为主轴生长成一维MHSH-512晶须,而当SO2-4过量10倍时,水热产物转变为Mg(OH)2·2MgSO4团球状晶体。
(3)Cl–的存在可能阻碍OH-与Mg2+之间相互作用,延缓结构单元[Mg(OH)6]4-的形成,同时可能与SO2-4在[Mg(OH)6]4-表面发生竞争吸附,导致晶须生长滞后,但对MHSH-512晶须的最终形貌和分散性并没有明显的影响。
(4)所制备的MHSH-512晶须结晶度高、长径比大(150~200)、表面光滑、分散性好,易于实现工业化生产,为青海盐湖镁资源的高值化利用提供了一条有效途径。
