反相微乳液法制备单片层LDHs及其吸附性能
2021-06-24杨修洁吴鲁楠胡若娜王伟港殷长龙
杨修洁, 吴鲁楠, 胡若娜, 王伟港, 殷长龙, 刘 东
(中国石油大学(华东)化学工程学院,山东青岛 266580)
0 引 言
在诸多有机水体污染物中,染料是最难降解处理的一类,为此研究人员一直在寻找高效环保的废水处理方案[1]。现在最普遍的方式是吸附,传统的吸附材料如活性炭[2-3]、黏土[4]、离子树脂[5]等都存在对阴离子型染料去除效率较低的问题。相比之下,层状双金属氢氧化物(Layered Double Hydroxides,LDHs)由于其独特的二维层状结构和阴离子可交换性、热稳定性等理化性质,可有效吸附阴离子型染料,展示出很好的应用前景[6]。LDHs常规的合成方法是共沉淀法[7-8],但是制得的LDHs往往多片层堆叠,无法与染料分子进行充分接触,从而影响了LDHs的吸附性能。研究人员发现利用反相微乳液法制备LDHs可以很好地解决这一问题。反相微乳液[9-10]是一种水相以纳米级液滴分布在油相中所形成的两相分散体系。通过反相微乳液法制备纳米粒子,可以利用分布在油相中的纳米水相液滴形成微反应器,从而限制水相中纳米粒子的团聚,且纳米粒子的成核、生长、团聚等过程集中于水相纳米液滴中也可以有效限制纳米粒子的尺寸和层数,制备出单片层纳米尺寸LDHs[11]。
本文以反相微乳液法和共沉淀法两种方法合成CoAl-LDH,探讨不同制备方法对材料吸附性能的影响。本实验以问题为导向,引导学生利用所学知识解决实验过程中遇到的问题,融合了材料、界面化学、仪器分析等多种学科理论知识,结合当代科学研究前沿,适合作为综合性实验或开放性实验面向高年级本科生开设,有利于高校创新人才培养[12-13]。
1 实验部分
1.1 实验仪器与试剂
试剂:六水合氯化钴(CoCl2·6H2O),六水合氯化铝(AlCl3·6H2O),氢氧化钠(NaOH),25%氨水(NH3·H2O),二氯甲烷(CH2Cl2),乙醇(C2H5OH),十二烷基硫酸钠(SDS),正丁醇,异辛烷,尿素,甲基橙,均为分析纯。
仪器:电子天平,恒温磁力搅拌器,真空干燥箱,X-射线粉末衍射仪(Bruker D8,Cu Kα激发源),红外光谱仪,紫外-可见吸收光谱仪,离心机。
1.2 单片层CoAl-LDH的制备
1.2.1 无表面活性剂反相微乳液法CoAl-LDH的制备
首先,将0.381 g CoCl2·6H2O和0.193 g AlCl3·6H2O溶于5 mL超纯水中,超声5 min,得到含CoCl2·6H2O和AlCl3·6H2O且Co∶Al=2∶1的水溶液,然后加入28.5 mL二氯甲烷和16.5 mL乙醇,记为溶液A;将28.5 mL二氯甲烷、16.5 mL乙醇、和5 mL 1.6 mol·L-1NaOH溶液混合,搅拌5 min,记为溶液B。将溶液B在溶液A缓慢搅拌中逐渐滴入,然后在油浴中磁力搅拌下回流加热,在30℃下反应10 h至凝胶状态。通过6 000 r/min离心15 min收集产品,得到固体E-CoAl-LDH,用乙醇-水离心洗涤3次,60℃下干燥过夜,得到产品记为E-CoAl-LDH。
1.2.2 共沉淀法CoAl-LDH的制备
首先,将CoCl2·6H2O和AlCl3·6H2O溶于超纯水中,超声5 min,得到含CoCl2·6H2O和AlCl3·6H2O且Co∶Al=2∶1的水溶液,然后加入二氯甲烷和乙醇,记为溶液A;将二氯甲烷、乙醇和共沉淀剂溶液混合,搅拌5 min,记为溶液B。将溶液B在溶液A缓慢搅拌中逐渐滴入,然后在油浴中磁力搅拌下回流加热,在30℃下反应10 h至凝胶状态。通过6 000 r/min离心15 min收集产品,用乙醇-水离心洗涤3次,60℃下干燥过夜,得到产品记为C-CoAl-LDH。
1.3 染料吸附实验
1.3.1 标准曲线的绘制
配制一系列浓度范围为0~30 mg/L的甲基橙溶液。利用紫外-可见分光光度计测定不同浓度甲基橙溶液最大吸收波长处的吸光度。以最大吸收波长处的吸光度为纵坐标,染料浓度为横坐标作图,绘制吸光度-浓度标准曲线,如图1所示。

图1 甲基橙溶液的标准曲线
拟合得到的MO标准曲线方程为:A=0.072 45c-0.029 66,相关系数R2为0.998 8。其中:A为吸光度值;c为MO的浓度(mg·L-1)。
1.3.2 染料吸附实验
取一定质量的吸附剂加入一定体积不同浓度的甲基橙溶液中,在黑暗条件下搅拌吸附。在给定的时间间隔取样,离心后取上层清液,用紫外-可见分光光度计检测最大吸收波长处的吸光度,根据标准曲线计算得到对应的染料浓度。通过下列公式计算吸附剂的吸附量,即
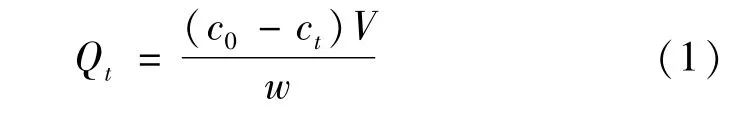
式中:Qt为吸附剂的染料吸附量(mg/g);c0为染料的初始浓度(mg/L);ct吸附后的染料浓度(mg/L);V为染料溶液体积(L);w为吸附剂的质量(g)。
2 结果与讨论
2.1 XRD表征
从图2可知,两者的特征峰位置基本一致,11.62°、23.37°、34.35°和61.54°的衍射峰分别对应层状双金属氢氧化物典型的(003),(006),(012)和(110)晶面,表明C-CoAl-LDH和E-CoAl-LDH均具有典型的类水滑石结构,并且C-CoAl-LDH峰高于ECoAl-LDH,证明C-CoAl-LDH结晶度高,表明E-CoAl-LDH较C-CoAl-LDH有更小的粒径。
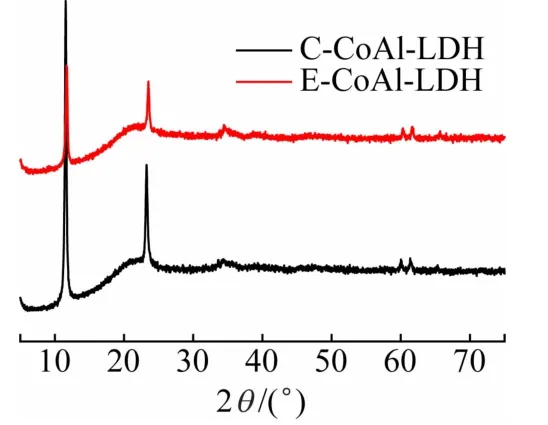
图2 C-CoAl-LDH和E-CoAl-LDH的XRD图
2.2 FTIR表征
由图3可知,两者的吸收峰位置基本一致,3 500 cm-1附近的吸收峰为H2O中O—H的伸缩振动峰,在1 630 cm-1附近的吸收峰为水分子以及层板中羟基的伸缩振动峰,1 300~1 400 cm-1附近的吸收峰为层间阴离子中碳酸根的伸缩振动峰。这是由于水中溶解二氧化碳形成了碳酸根离子,590 cm-1附近的峰为层板中Co、Al与氧形成的金属-氧键(M-O)、金属-氧-金属键(M-O-M)、金属-羟基键(M-OH)的晶格振动峰。

图3 C-CoAl-LDH和E-CoAl-LDH的FTIR谱图
2.3 p H对LDHs吸附性能的影响
溶液pH对LDHs的吸附性能有显著影响。不同pH下E-CoAl-LDH对甲基橙吸附性能如图4所示,E-CoAl-LDH在pH=4时吸附甲基橙的效果最佳。当pH进一步增加时,溶液的OH-增多,竞争吸附位点,导致甲基橙吸附量下降;pH过低时,E-CoAl-LDH的结构可能被强酸破坏导致吸附能力下降。
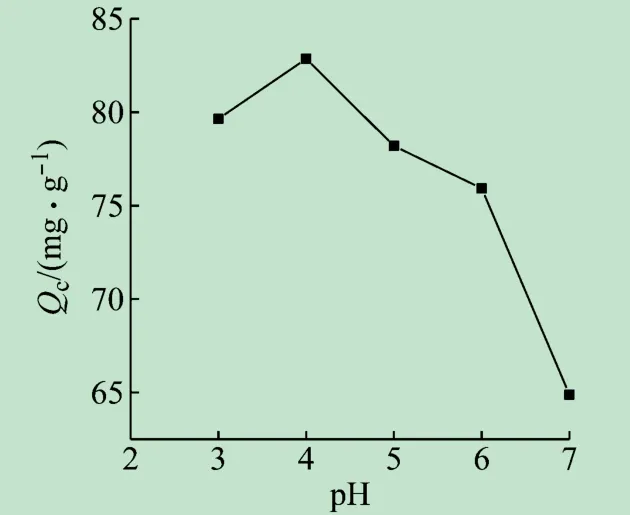
图4 E-CoAl-LDH对MO的吸附量随pH变化的关系曲线
2.4 不同制备方法制得的LDHs吸附性能比较
以甲基橙为探针分子,考察C-CoAl-LDH和E-CoAl-LDH的染料吸附性能,染料去除率随时间的关系曲线如图5所示。由图5可以看出,两种方法制备的LDHs其吸附性能有显著差异,其中E-CoAl-LDH 150 min的MO去除率达到71.5%,明显高于C-CoAl-LDH的吸附率。这可能是反相微乳液法制备的LDHs因在微乳液中反应从而具备较小粒径,进而拥有更大的比表面积和更多的吸附活性位点,从而拥有更强的吸附性能。

图5 不同制备方法制得的LDHs对MO吸附去除率与时间关系曲线
2.5 吸附时间对LDHs吸附性能的影响
由图6可知,各甲基橙浓度下E-CoAl-LDH吸附甲基橙在最初的10 min内快速增长,随后反应速度迅速下降,到120 min后才会达到平衡。吸附速率变化的原因是前10 min内E-CoAl-LDH上具有足够的吸附位点吸附甲基橙分子,随后固液界面存在的阻力阻碍甲基橙分子进一步扩散到E-CoAl-LDH表面利用剩余空吸附位点,导致速率的急速下降。

图6 E-CoAl-LDH吸附甲基橙的吸附量与时间的关系曲线
为进一步分析其吸附过程,分别采用拟一级动力学模型、拟二级动力学模型进行E-CoAl-LDH吸附甲基橙的动力学拟合:

式中:Qe为平衡吸附量(mg·g-1);Qt为对应时间下的吸附量(mg·g-1);k1为拟一级速率方程的反应常数;k2为拟二级速率方程的反应常数。
E-CoAl-LDH对甲基橙染料的吸附动力学拟合结果如图7所示,动力学参数如表1所示。拟二级动力学模型计算的理论平衡吸附量与实际平衡吸附量接近且相关系数较高,表明E-CoAl-LDH吸附甲基橙染料的吸附动力学符合拟二级动力学模型,说明E-CoAl-LDH对甲基橙染料的吸附过程主要为化学吸附。

图7 E-CoAl-LDH吸附甲基橙染料的动力学曲线
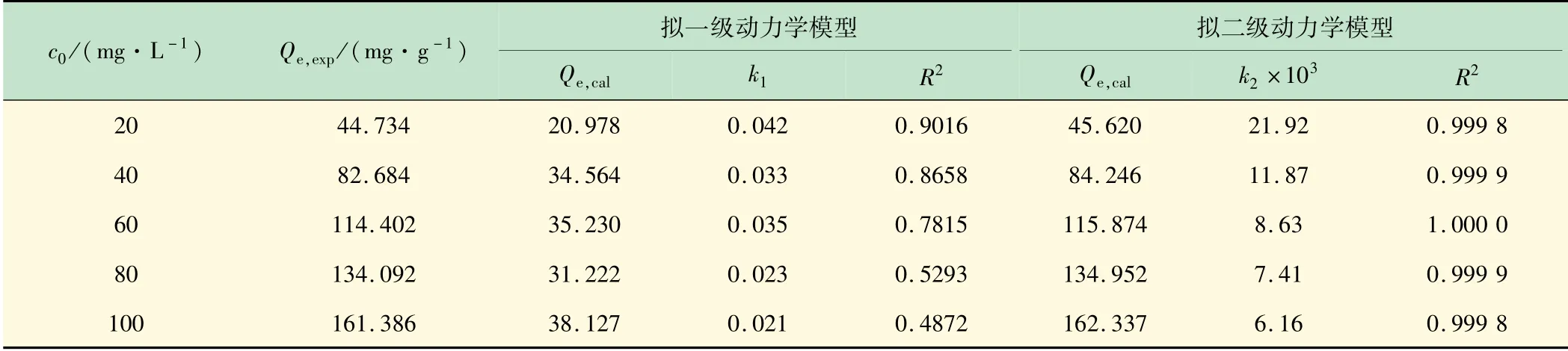
表1 E-CoAl-LDH吸附甲基橙染料的动力学参数
2.6 染料起始浓度对LDHs吸附性能的影响
由图8可知,随着染料起始浓度的增大,E-CoAl-LDH吸附甲基橙的平衡吸附量也不断增加。这可归结于甲基橙浓度的上升为甲基橙分子由液相扩散至固体表面被吸附提供了足够大的驱动力。

图8 E-CoAl-LDH吸附甲基橙的平衡吸附量与染料起始浓度的关系曲线
为进一步分析甲基橙在液相与固相间的分布规律,分别采用Langmuir模型和Freundlich模型进行数据拟合,即:
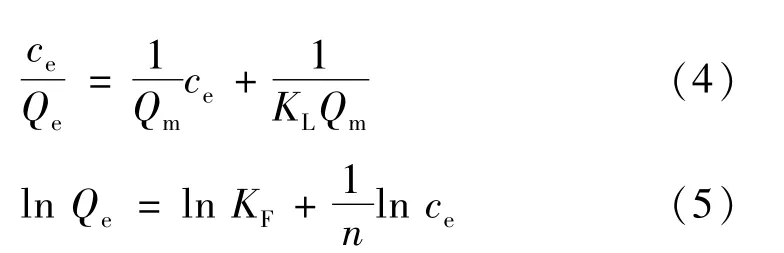
式中:Qm为饱和吸附量(mg·g-1);ce为吸附平衡时的溶质浓度(mg·L-1);KL为Langmuir模型的吸附平衡常数;KF和1/n为Freundlich模型的吸附平衡常数。
拟合得到各参数如表2所示,Langmuir和Freundlich等温吸附曲线如图9所示。结果表明,Langmuir模型的相关系数0.998 3明显大于Freundlich模型的相关系数0.9545。所以,E-CoAl-LDH对甲基橙的吸附符合Langmuir等温吸附模型,表明甲基橙在E-CoAl-LDH上的吸附主要是单层吸附。饱和吸附量随着染料浓度的增加而增大直至达到完全饱和吸附。通过Langmuir模型计算得出E-CoAl-LDH对甲基橙的理论饱和吸附量为178.89 mg/g。

表2 等温吸附模型参数
2.7 吸附机理
由图10可以看出,在吸附过程中甲基橙与E-CoAl-LDH的层间阴离子发生了离子交换。另外,结合甲基橙吸附动力学拟合的结果,E-CoAl-LDH吸附甲基橙的作用机理为外表面吸附与离子交换的协同作用。
3 结 语
本实验针对传统共沉淀法合成LDHs多片层堆叠导致吸附性能不佳的问题展开实验探索,采用反相微乳液法制备单片层LDHs,利用X-射线衍射、红外光谱等大型仪器对所制备材料进行表征,以甲基橙为探针研究LDHs的吸附性能,比较反相微乳液和共沉淀两种方法所制备LDHs材料的吸附性能差异及优劣性,同时探究了pH及甲基橙起始浓度对LDHs吸附性能的影响,并对其吸附机理进行分析,实验报告以论文的形式呈现,锻炼学生的科技论文撰写能力。
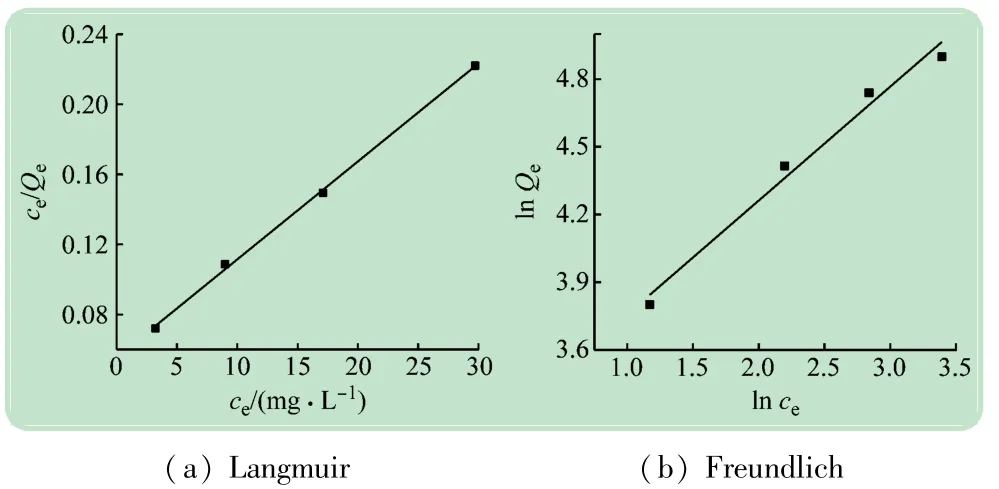
图9 E-CoAl-LDH吸附甲基橙染料的动力学曲线
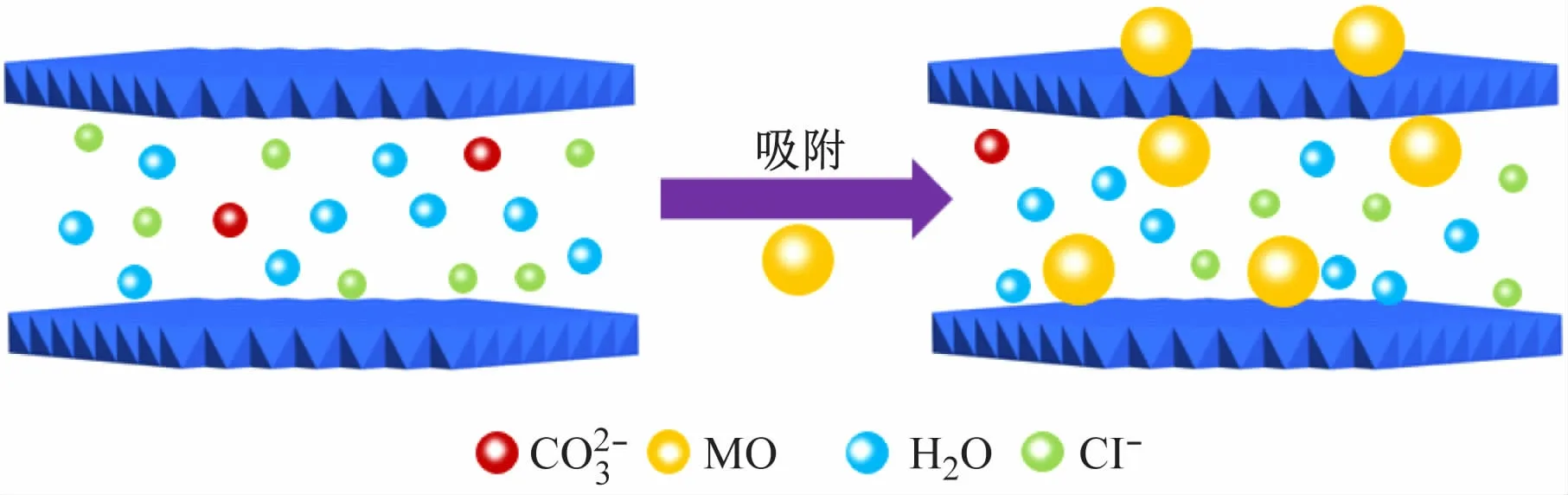
图10 E-CoAl-LDH吸附甲基橙过程示意图
本实验以问题为导向,包含前期调研、实验过程设计、实验结果表征分析及文章撰写等多个步骤的综合实验探索体系,学生在实践过程中需要将多门学科交叉运用,并且小组各成员之间需要合理分配个成员之间的实验操作分工及实验进行的时间和顺序,并同时做好小组间沟通,以便能够顺利高效完成整个实验体系。通过该综合性实验,提高学生基础理论知识和实验技能的掌握的同时开阔学生的视野,提升学生对当今学术前沿的理解,有助于提升学生的科研素养和专业技能知识水平。
