注射用修饰透明质酸钠凝胶热原试验探讨
2021-06-24王嘉铭曾裕聂永胜陆金健杨立峰
王嘉铭 曾裕 聂永胜 陆金健 杨立峰
(广东省医疗器械质量监督检验所,广州 510000)
随着现代医学科技的发展,注射用修饰透明质酸钠凝胶的研究也获得了较快的发展。透明质酸是一种天然直链多糖,由N-乙酰葡糖胺和葡萄糖酸双糖单位构成的线性多糖,分子量大,具有一定粘弹性特质[1]。在GB/T16886.11-2011医疗器械生物学评价第11部分全身毒性试验(附录F材料介导热原信息)中提到:对新型医疗器械没有必要都进行体内致热性试验,但材料如含有引起过热原反应的新化学成分或物质,则宜进行材料介导致热性评价[2],透明质酸钠类面部注射适用于中至深层真皮注射以纠正皱纹或重建软组织,作为一种植入人体内的新型生物材料[3],为了尽可能降低产品对患者的不良反应,在热原试验中对其开展正确的制备方法和注射剂量的研究至关重要[4]。
1 材料与方法
1.1 一般材料
试验样品:注射用修饰透明质酸钠凝胶;浸提介质:0.9%氯化钠注射液;试验动物:普通级新西兰兔(广州市白云区龙归兴科动物养殖场),未产并无孕,体重1.7kg以上。
1.2 试验方法[5]
取适用新西兰兔3只测定其体温,在测定正常体温符合要求后15min以内,自耳缘静脉缓缓注入规定剂量并温热至约38℃的供试品。然后每隔30min测量1次体温,共6次。以6次体温中最高的一次减去正常体温,即为该兔体温的升高温度(℃)。
1.3 结果评价
3只兔温度升高均低于0.6℃(或3只兔体温升高的总和低于1.3℃),判定该样品浸提液的热原检查符合规定。
2 不同的制备方法[6]和注射剂量[7]
(1)参照GB16886.12-2017[8],不规则产品浸提比例0.2g/mL,加入0.9%氯化钠注射液在37℃下浸提72h。取该制备条件下的浸提液,按10mL/kg的注射剂量进行试验。
(2)对(1)中制备的样品浸提液经3000rpm离心10min,用0.45μm 滤膜过滤作为试验液,按照10mL/kg的注射剂量进行试验。
(3)按照浸提比例0.1g/mL,加入0.9%氯化钠注射液在37℃下浸提72h。取该制备条件下的浸提液按照1mL/kg的注射剂量进行试验。
(4)对(3)中制备的浸提液用5μm过滤器过滤作为试验液,按照0.2mL/kg的注射剂量进行试验。
(5)对(3)中制备的浸提液用40μm过滤器过滤作为试验液,按照0.2mL/kg的注射剂量进行热原试验。
(6)对(3)中制备的浸提液用40μm过滤器过滤作为试验液,按照10mL/kg的注射剂量进行热原试验。
3 试验结果
制样方法和注射剂量按照(1)、(3)进行热原试验,兔在注射浸提液过程中反应异常,然后死亡。
制样方法(2)进行离心后浸提液变成凝胶状,无法注射导致无法进行热原试验。
制样方法和注射剂量按照(4)进行热原试验,试验过程中兔反应正常,但体温升高超过0.6℃,见表1。
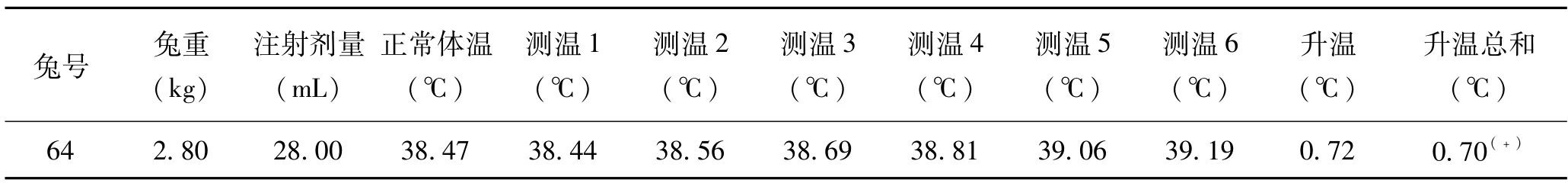
表1 热原试验结果(浸提比例:0.1g/ml,37℃72h,5μm过滤,注射剂量:0.2ml/kg)
制样方法和注射剂量按照(5)使用40μm的滤膜过滤后,按0.2mL/kg的注射剂量进行热原试验,试验过程兔反应正常,三只兔体温升高均低于0.6℃,且体温升高总和低于1.3℃,在该试验条件下,试验样品浸提液热原检查合格,见表2。
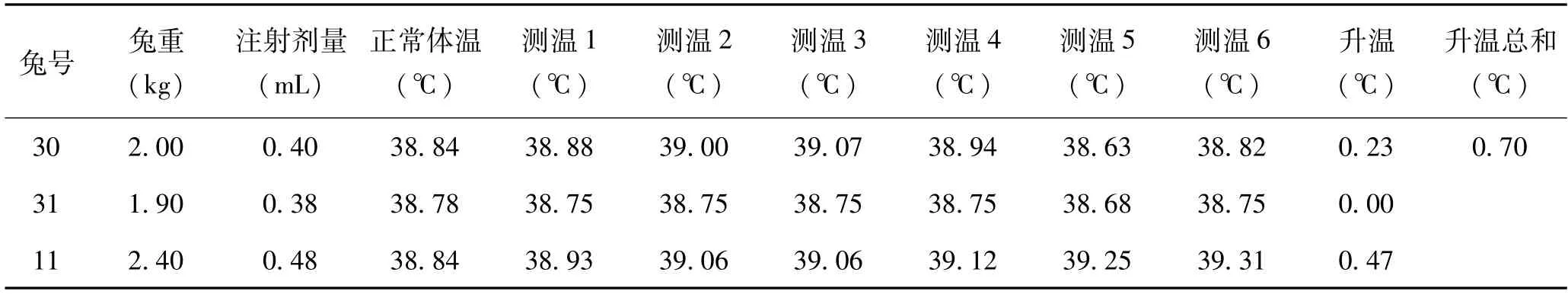
表2 热原试验结果(浸提比例:0.1g/ml,37℃72h,40μm过滤,注射剂:0.2ml/kg)
制样方法和注射剂量按照(5)使用40μm的滤膜过滤后,按10mL/kg的注射剂量进行热原试验,试验过程兔子反应正常,试验样品浸提液热原检查合格。见表3。
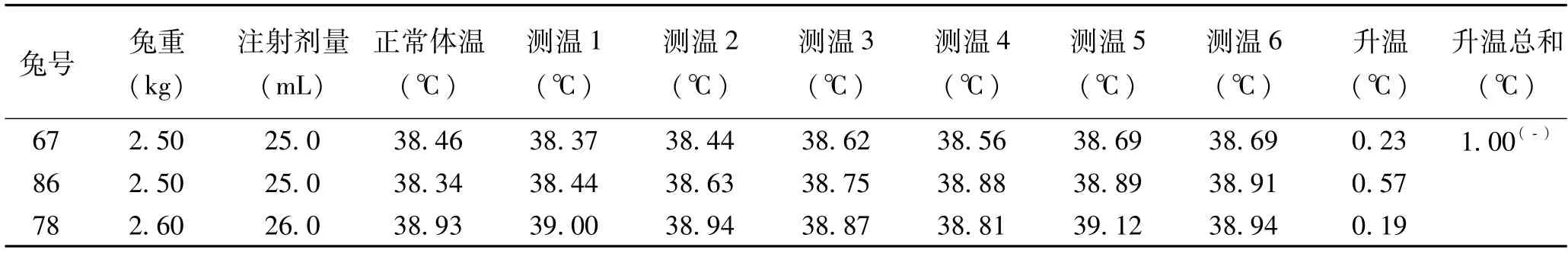
表3 热原试验结果(浸提比例:0.1g/ml,37℃72h,40μm过滤,注射剂量:10ml/kg)
4 讨论
该次热原试验的探讨,源于首次常规操作热原试验失败。按照GB/T16886.12制样原则,常规器械样品制备及注射剂量:0.2g/mL,37℃、72h,10mL/kg,造成了试验的异常,引起动物不必要死亡。经过整改后的制备方案使得试验正常进行,讨论如下。
观察制备方法(1)后的浸提液,肉眼观察无颗粒状出现,但可发现溶液粘稠,故有制备方法(2)将样品浸提液离心,经离心后,样品浸提液出现了凝胶状(样品与0.9%氯化钠注射液融合吸收)无法注射。这两种制备的方法说明样品按照0.2g/mL的浸提比例不适合热原试验操作的进行。粘稠的浸提液和凝胶状的浸提液都可能存在大颗粒透明孔径物质,通过兔耳缘静脉入血,造成兔异常反应和死亡。
降低浸提比例的制备方法(3),同时注射剂量由10mL/kg降低为1mL/kg(《GB/T14233.2-2005医用输血、输液、注射器具检验方法第二部分生物学试验方法》的最大注射剂量是10mL/kg)[9],但实验依然出现了兔异常反应和死亡。说明此浸提方法得出的浸提液依然存在肉眼观察不到的大颗粒浸提物质。
对制备方法(3)用5μm过滤器过滤(出现了过滤器无法滤下,滤膜破坏),再次降低注射剂量。注射进兔体内后,兔表现正常,但体温升高(见表1)。最终的整改制备方法是,加大过滤器的滤膜孔径。也借助于生产商的协助,进行了样品孔径的测量(见表4),由图中可以看出此种注射用修饰透明质酸钠凝胶颗粒最小孔径为66.897μm,再因为《中国人民共和国药典》0102注射剂,注射用浓溶液的规定:混悬型注射液中原料药物粒径应控制在15μm以下,含15~20μm(间有个别20~50μm)者,不应超过10%[10]。最终选择了40μm过滤器,取过滤液注射后,动物反应正常,体温正常,3只家兔温度升高均低于0.6℃,体温升高总和低于1.3℃(见表2)。
(4)由于上述试验方法采用过滤和降低注射剂量可以使得试验样品浸提液热原检查合格,但是降低剂量并没有办法充分评价产品的安全性[11],因而根据GB/T16886中规定的最大剂量再次进行热原试验,将浸提液通过40μm的过滤器后,按照10mL/kg的注射剂量进行试验,注射后动物反应正常,热原检验合格(见表3)。
注射用修饰透明质酸钠凝胶的热原试验,因其自身的产品特性,导致试验的特殊性,根据中华人民共和国药典2020版四部(0102注射剂)的试验方法中混悬型注射液中原液药物粒径的规定,借助激光粒度分析仪[12]对于样品孔径的测量(见表4)可以看出此类注射用修饰透明质酸钠凝胶粒度最小孔径为66.897μm,若不进行过滤处理,此粒径大小超过了中华人民共和国药典2020版四部(0102注射剂)中的注射用浓溶液的最大粒径规定,因而经讨论最初选择5μm的过滤器处理样品浸提液,结果出现很难滤过的现象,用注射器推动滤下浸提液,导致滤膜破裂。说明浸提液内依然有大分子颗粒通过破裂的滤膜进入注射液中导致体温升高。之后采用40μm的过滤器对样品浸提液进行过滤处理,按照GB/T16886中规定的注射剂量进行试验,试验动物反应正常,体温正常。故只要试验样品注射液的粒径大小符合注射标准,不需再降低注射剂量来进行试验。虽然标准中浸提液一般不应采用过滤、离心或其他方法来去除悬浮的粒子[5],但由于样品浸提液中的粒径不符合《中国人民共和国药典》0102注射剂的要求,也在实际的试验中得到验证,因此该产品的样品浸提液需要经过合适的过滤器过滤后,进行热原注射试验。
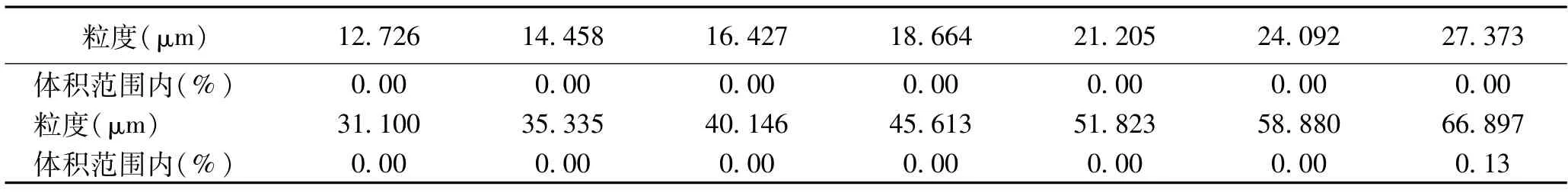
表4 激光粒度分布检测图
透明质酸钠类面部注射产品在生物医学的应用上要求有良好的生物安全性,因此通过正确处理样品浸提液进行热原试验可以为此类产品的生物安全性提供一定的依据。
