基于粒子特性研究特殊医学用途配方食品全营养乳液的稳定性
2021-06-22韩丽丽孙丰义陈朝青王学敏
韩丽丽,孙丰义,陈朝青,王学敏,周 昊,张 燕,何 梅,刘 鹭
(北京市营养源研究所,系统营养工程技术研究中心,北京100069)
特殊医学用途配方食品(Food for Special Medical Purpose,FSMP),是为了满足进食受限、消化吸收障碍、代谢紊乱或特定疾病状态人群对营养素或膳食的特殊需要,专门加工配制而成的配方食品。FSMP属于肠内营养,主要针对存在营养不足或营养风险但仍具有胃肠道功能的患者,在临床上主要起到营养支持和营养治疗作用[1-2]。相比于普通食品,特医法规(GB 29922-2013、GB 25596-2010)对FSMP全营养乳液的能量密度、蛋白、碳水、脂肪的供能比以及矿物质(12种)和维生素(13种)的含量有具体的要求,其蛋白、脂肪、碳水化合物的含量远高于类似的普通液态食品[3-5]。
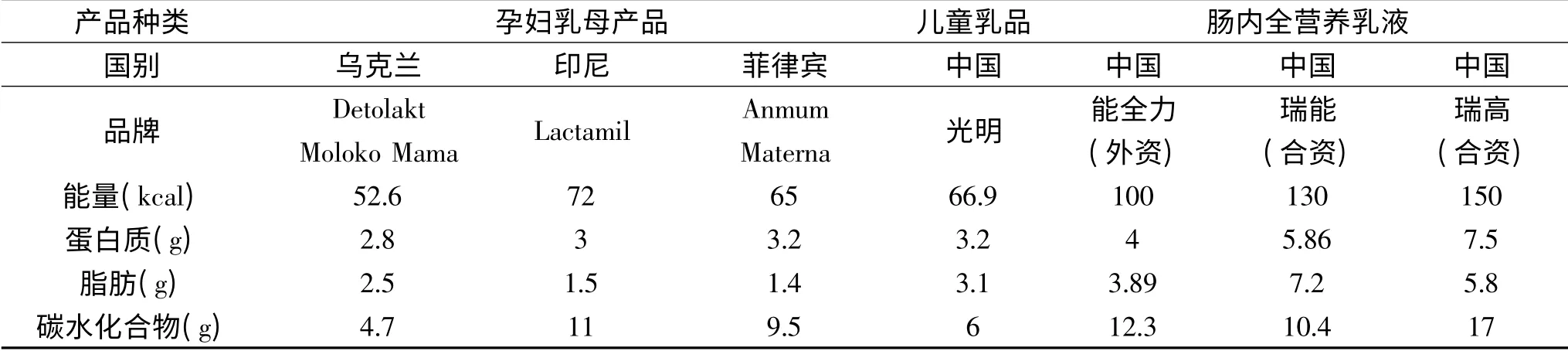
表1 部分乳制品与肠内全营养乳液能量及三大宏量营养素组成对比(100 mL)Table 1 Comparison of three macronutrients and energy of liquid dairy and total enteral nutrition emulsion(100 mL)
虽然FSMP全营养乳液的外观及组成比较接近于液态乳制品,但由于食品安全国家标准(GB 29922-2013、GB 25596-2010)对FSMP的营养素组成及其含量均有具体的要求,而目前专门针对FSMP全营养乳液的稳定性的研究较为少见。全营养乳液是一个成分复杂的缓冲体系,由蛋白质、脂肪、碳水化合物、维生素和矿物质类组成。它在热力学上属于不稳定体系,既有蛋白质等微粒形成的悬浮液、脂肪乳浊液,又有以糖、盐类形成的真溶液。其主要质量问题为加工及贮藏中出现沉淀、分层以及脂肪上浮等问题。从微观上表现为乳状液分散相颗粒的迁移(表现为沉淀和析水),或是分散相颗粒平均粒径大小的变化(表现为团聚和絮凝)。凡是影响全营养乳液中蛋白质稳定性的因素,破坏蛋白结构稳定性的因素都会影响产品的稳定性,例如稳定剂、乳液体系的pH、矿物质盐以及蛋白诱导胶凝。不适当的稳定剂或者pH会导致体系中蛋白平均粒径增大,易发生聚集、团聚;酪蛋白胶体钙与离子钙之间的盐类平衡被打破等都对产品稳定性造成影响[6-8]。乳液体系中微观粒子的平均粒径、电位以及体系pH的变化在一定程度上可以反映乳液体系的稳定性情况[12-14]。
粒度特征既可以从微观上确定乳状液分散相的组成特点,又可以从宏观上描述食品乳状液絮凝和聚结等过程。平均粒径分布分析是通过特定的仪器和方法对体系平均粒径特性进行表征的一种技术,可以从微观上阐明乳液体系中粒子的状态[12-13,15]。乳状液的其他性质如黏度等,也与其平均粒径密切相关[16-17]。本研究应用平均粒径、ζ-电位、离心沉淀率等手段研究微晶纤维素、结冷胶以及乳液体系p H对全营养乳液体系稳定性的影响;对货架期内全营养乳液体系中平均粒径、电势等稳定性特性进行测定分析,探讨影响全营养乳液的粒子变化规律,以期为特殊医学用途全营养乳液的开发提供参考。
1 材料与方法
1.1 材料与仪器
酪蛋白、乳清蛋白水解物、结冷胶 阿泽雷斯国际贸易(上海)有限公司;麦芽糊精 罗盖特贸易(上海)有限公司;白砂糖 北京糖业有限公司;维生素预混包、矿物质预混包 哥兰比亚营养品(苏州)有限公司;菜籽油、椰子油 益海嘉里集团;微晶纤维素 欣融实业有限公司。
AH-BASIC高压均质机 ATS工业系统有限公司;Nano ZS90电位及纳米粒度测定仪 马尔文仪器公司(中国);FE20 pH计 德国Sartorius公司;LUMsizer611快速稳定性分析仪 德国LUMisizer公司;Thermo Centrifuge X3R冷冻离心机 赛默飞世尔科技公司;RW20高速搅拌器及T25高速剪切仪 德国IKA magic LAB;Tomy-SX700全自动灭菌锅 日本Tomy Digital Biology公司;超高温灭菌设备ST20及无菌灌装设备CT20 上海顺仪实验设备有限公司;Brookfield DV-I Prime旋转粘度计 美国博勒飞公司。
1.2 实验方法
1.2.1 配方设计及依据 本配方的能量密度、三大营养素供能比以及营养素的含量参考《特殊医学用途配方食品通则》(GB 29922-2013)和中国营养学会膳食营养素参考摄入量(DRIs)以及专家共识的要求(包括优质蛋白含量、不饱和脂肪酸与饱和脂肪酸比例、营养素供能比、矿物质含量等)的设计[1-2]。本研究中的特殊医学用途全营养乳液能量密度为1 kcal/mL,蛋白质来源为酪蛋白、乳清蛋白水解物。脂肪来源为菜籽油、椰子油等。各营养素设计具体见下表所示:
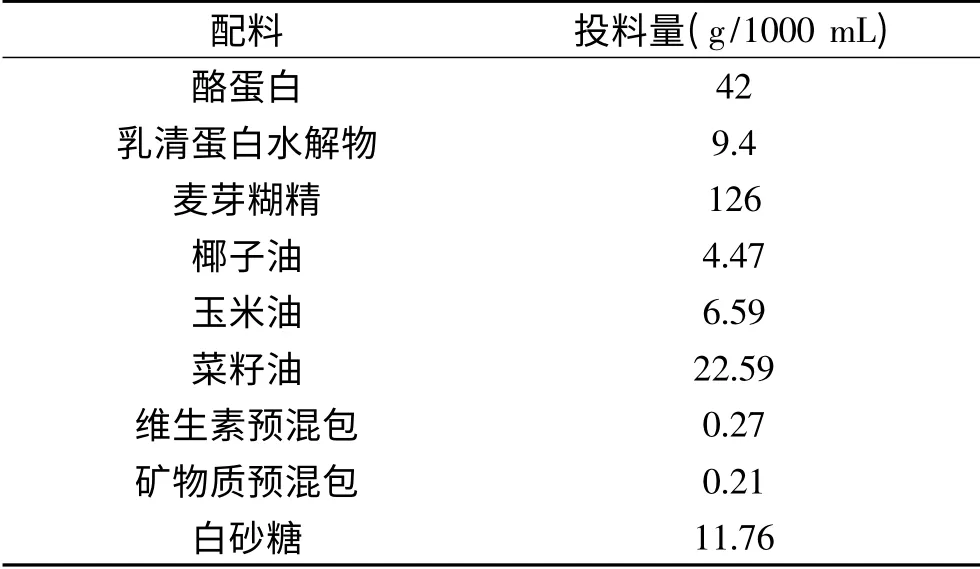
表2 特殊医学用途全营养乳液营养素设计Table 2 Formula design of total nutrient emulsion for FSMP
1.2.2 全营养乳液生产工艺流程 全营养乳液的工艺流程如图1所示。
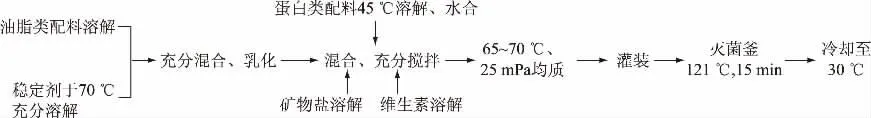
图1 特殊医学用途食品全营养乳液工艺流程Fig.1 Processing flow chart of total nutrient emulsion for FSMP
1.2.3 稳定剂对全营养乳液稳定性的影响 制备不同浓度的微晶纤维素(0.3、0.6、0.9、1.2、1.5、1.8 g/L)、不同浓度的结冷胶(0.05、0.1、0.15、0.2、0.25 g/L)的全营养乳液,利用杀菌釜灭菌。第2 d测定全营养乳液的平均粒径、电位、黏度、离心沉淀率的变化。考察不同稳定剂不同浓度对全营养乳液的稳定性的影响。
1.2.4 不同pH对全营养乳液稳定性的影响 制备0.1 g/L的结冷胶和0.6 g/L的微晶纤维素为稳定剂组成的全营养乳液,以0.1 mol/L盐酸或0.1 mol/L氢氧化钠溶液调节p H至6.2、6.27、6.42、6.58、6.68、6.82、6.95,经杀菌釜灭菌。测定常温下贮存第1 d和第20 d全营养乳液的平均粒径、电位、黏度、离心沉淀率的变化,考察p H对全营养乳液稳定性的影响。
1.2.5 全营养乳液货架期实验设计 按照图1的工艺配制一批全营养乳液,物料采用超高温瞬时灭菌工艺(137℃,15 s)灭菌,于(30±1)℃无菌灌装。将无菌灌装后的全营养乳液置于室温(25±2.5℃)环境下测定135 d。每隔15 d取样,测定样品的平均粒径、电位、黏度、p H、离心沉淀率的变化,分析其微观粒子特性变化的规律。
1.2.6 离心沉淀率(WHC)的测定 用吸管吸取25 mL待测样品于离心管中。测定样品质量m0后,放入离心机,以10000 r/min离心10 min后,取出离心管,除去上清液,静止倒置10 min后,测离心管中残余物的质量m。每个样品进行3次平行测定,取平均值。计算离心沉淀率。

1.2.7 ζ-电位的测定 室温下将待测样品与去离子水按照1∶1000稀释后,过0.45μm微滤膜过滤,利用纳米平均粒径电位分析仪对全营养乳液的ζ-电位进行测定,样品池选用DTS1060弯曲式毛细管样品池。每个样品测定3次,取算术平均值。
1.2.8 平均粒径的测定 同ζ-电位的测定,对样品进行前处理,将Zeta电位仪设置为平均粒径模式,测定其平均粒径。每个样品测定3次,取算术平均值。
1.2.9 p H测定 将样品置于25℃至恒温。利用p H计测定样品的p H,每个样品平行测定3次,取算术平均值。
1.2.10 黏度测定 将常温样品缓慢倒入200 mL容器内,将转子置于乳液内,液体没过转子刻度。测定参数:61号转子,50 r/min,30 s。共测定三次,取其平均值。
1.2.11 稳定性分析测定 采用快速稳定性分析仪对不同稳定剂使用方案下得到的全营养乳液进行稳定性分析。仪器通过离心加速分层和量化沉淀、悬浮的方法(STEP技术)快速分析液体的稳定性。本仪器采用近红外光全程监测分离过程中的粒子迁移行为,以时间和位置为参数,同步测量和记录样品的空间与时间消光图谱。仪器软件SEPView(6.3.116.7044)通过光透过率对时间积分,其曲线斜率作为不稳定系数。通过不稳定系数值比较样品的稳定性。不稳定系数值越大,在一定的时间内样品的透光率变化越快,即样品的移动分层速度变化越快,样品越不稳定;反之不稳定系数数值越小,样品越稳定[14-15]。
测定参数:温度25℃,离心力2300 g,光源875 nm;光因子系数1.00,每10 s扫描1次,共扫描300次。光学管:LUM 2 mm。
1.3 数据处理
所有测定均测定三次,取其平均值。采用Turkey分析法对结果进行显著性分析(P<0.05)。
2 结果与分析
2.1 胶体对全营养乳液稳定性的影响
蛋白质是全营养乳液中的三大宏量营养素之一。蛋白质是二次复溶于水中,这对蛋白质的热稳定性提出了极高的要求。这一复杂的体系不仅需要合适的工艺,还需要适量的稳定剂、乳化剂以及一定的体系条件(p H、金属离子浓度)以保持液体的稳定性[20-22]。本研究中所用的结冷胶、微晶纤维素都是阴离子多糖,可吸附在带正电荷的酪蛋白的表面,通过静电排斥力或空间位阻作用防止酪蛋白聚集沉淀,从而提高全营养乳液的稳定性[23]。
2.1.1 微晶纤维素对全营养乳液稳定性的影响 微晶纤维素(microcrystalline cellulose,MCC)是由纤维素原料经过稀酸水解并经过一系列处理得到的极限聚合度的产物,是一种可自由流动的纤维素晶体的天然聚合物[20,24]。微晶纤维素在溶液中经过高速剪切分散和均质之后,可以彻底分散在体系中,和水以氢键形式成三维网络结构,这种三维网络结构可以有效悬浮蛋白颗粒,阻止变性蛋白的聚集。MCC与其他亲水胶体不同之处在于MCC本身并不与水分子结合,只是分散在液体体系中,分散体系呈触变性;这种以氢键结合的微晶体网络体系没有糊状质感,口感清爽[6,21]。
本研究在全营养乳液的营养素配方基础上,考察不同浓度微晶纤维素对全营养乳液的稳定性的影响,比如平均粒径、黏度、电位等。乳液体系中粒子平均粒径及其分布是影响产品稳定性的一个重要因素,平均粒径越小,沉淀速度越慢,乳液更稳定[15,25]。如表3所示,随着微晶纤维素浓度的增大,从0.3增加到1.8 g/L,乳液体系中平均粒径变化幅度在521.53~583.23 nm之间。微晶纤维素添加浓度为0.6 g/L时,此时平均粒径(521.53 nm)最小(P<0.05)。当微晶纤维素浓度增加至0.9 g/L时,乳液中平均粒径浓度达至最大,为583.23 nm(P<0.05);此时微晶纤维素浓度继续增加,平均粒径开始减小;当微晶纤维素浓度达到1.8 g/L时,乳液平均粒径降到550.23 nm。

表3 不同浓度微晶纤维对全营养乳液体系的影响Table 3 Effect of various MCC concentrations on total nutrient emulsion
黏度也是影响稳定性的一个重要因素。高黏度的体系可以使分散相不容易聚集和凝聚,从而确保分散体系更加稳定。研究结果显示微晶纤维素浓度从0.3增加到1.8 g/L,全营养乳液的黏度从18.83增加至53.10 mPa·s;当微晶纤维素浓度小于1.5 g/L时,尽管黏度变化是显著的(P<0.05),但黏度幅度增加缓慢,仅由18.83 mPa·s增至38.40 mPa·s。
离心沉淀率是反映液体体系稳定性的一个指标。沉淀率越大,表明溶液悬浮性能较差,易发生蛋白沉淀等现象。当微晶纤维素浓度从0.3增加至0.6 g/L时,乳液的离心沉淀率显著降低至1.91%(P<0.05);随着微晶纤维素浓度继续增加至1.8 g/L,离心沉淀率显著增加,为2.47%(P<0.05)。在整个微晶纤维素浓度变化范围内,全营养乳液电位变化不明显(-20.77~-18.10 mV),没有显著性变化(P>0.05)。微晶纤维素主要依赖于三维网络结构的形成进而保持全营养乳液体系的稳定,与黏度关系较小。LUMisizer稳定性分析结果显示微晶纤维素浓度为0.3和0.6 g/L时,全营养乳液的不稳定性指数降低(P<0.05);随着其浓度的增加,不稳定指数显著性增加,体系不稳定性增加。

图2 不同浓度微晶纤维素的全营养乳液LUMiSizer稳定性图谱Fig.2 The dispersion analysis of LUMiSizer chromatograms of total nutrient emulsion with various concentrations of MCC
综合考虑平均粒径、黏度、离心沉淀率及不稳定性指数,微晶纤维素浓度的最适浓度为0.6 g/L,此时全营养乳液体系最稳定,此时的离心沉淀率也是最低,平均粒径也是最小。
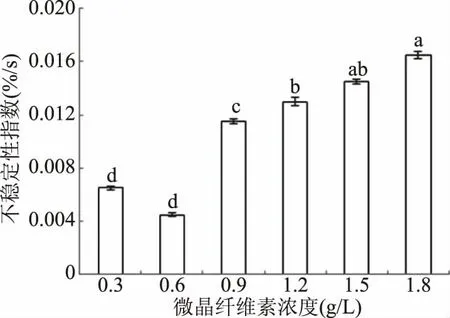
图3 不同浓度微晶纤维素的全营养乳液体系不稳定性指数Fig.3 The instability index of total nutrient emulsion with various concentrations of MCC
2.1.2 结冷胶对全营养乳液稳定性的影响 结冷胶是由伊乐假单胞菌(Pseudomonas elodea)发酵分泌的一种阴离子线性多糖,天然形成的结冷胶称为高酰基结冷胶(High Acyl Gellan Gum,HA)。高酰基结冷胶具有添加量小、热稳定性高、增稠性能明显和悬浮性优良等特性;相比于其他胶体,结冷胶还具有稳定酪蛋白胶束的作用[20,26]。结冷胶在高温下水溶液中分散为无序的随机线圈状态;在适宜的阳离子以及凝胶温度下,结冷胶的聚合物会聚合形成螺旋,最后形成三维结构[16,24,27]。
本文基于全营养营养素配方,考察了不同浓度的结冷胶对全营养乳液稳定性的影响。如表4所示,结冷胶对体系的黏度贡献很大。随着结冷胶浓度的微小增加,黏度幅度增长比较大:结冷胶浓度由0.05增加到0.25 g/L,体系黏度从14.57增加至54.20 mPa·s,口感稍感黏稠。离心沉淀率显示结冷胶浓度为0.1~0.15 g/L时,乳液的离心沉淀率为1.71%~1.75%,显著低于结冷胶浓度为0.2 g/L的全营养乳液(P<0.05)。但0.05~0.15 g/L的全营养乳液之间的离心沉淀率无显著性差异(P>0.05)。虽然乳液体系中的高黏度在一定程度上有利于乳液稳定性,减少乳液颗粒的聚集。本研究结果显示当结冷胶浓度高于0.15 g/L时,黏度持续增高,而离心沉淀率显著升高,表明稳定性不好。
本研究发现全营养乳液体系中平均粒径的变化与结冷胶浓度变化相反。随着结冷胶的浓度由0.05增加到0.25 g/L,乳液的平均粒径显著性降低(P<0.05),从813.47降低至642.57 nm。张帆[24]报道结冷胶浓度由0.05%增加到0.175%,β-胡萝卜素乳液乳液平均粒径由7μm逐渐减小到最低值(4μm);结冷胶浓度继续增加至0.2%,乳液平均粒径则开始增加至4.5μm。β-胡萝卜素乳液成分较为简单,主要为β-胡萝卜素和中链甘油脂肪,结冷胶此时主要起到乳化脂肪,作用于油滴表面降低表面张力,减少颗粒聚集;当结冷胶浓度增加超过一定范围,造成乳液微粒聚集,从而使平均粒径上升,乳液不稳定性增强[24]。全营养乳液成分较为复杂,含有蛋白质、脂肪、矿物质等。结冷胶等胶体不仅要作用于脂肪,作用于油滴表面,同时还要与油滴一起围绕在蛋白颗粒表面,降低表面吸附力,起到稳定体系的作用。因此全营养乳液体系和β-胡萝卜素乳液体系的平均粒径的变化不同。
研究结果还显示0.05~0.25 g/L的结冷胶浓度范围内的乳液体系的电位值变化不显著(P>0.05)。全营养乳液体系复杂,含有9~13种矿物质。本文推测全营养乳液中大量的金属离子对电位的影响远大于胶体对电位的影响。因此胶体浓度变化对体系电位的影响不明显。
LUMisizer稳定性分析结果显示,结冷胶浓度由0.05增长至0.1 g/L时,全营养乳液不稳定性指数显著降低(P<0.05);随着结冷胶浓度的增加,由0.1增长至0.20 g/L时,不稳定性指数显著增加(P<0.05)。综合平均粒径、离心沉淀率以及乳液不稳定指数,0.1~0.15 g/L的结冷胶制成的全营养乳液稳定性较好,平均粒径变化趋于平缓,为710.87~770.40 nm,离心沉淀率为1.71%~1.75%,此时黏度为21.70~23.13 mPa·s。
2.2 p H对全营养乳液稳定性的影响
全营养乳液属于肠内营养制剂,一般要求pH4~7左右。本研究中全营养乳液中的蛋白质为酪蛋白和部分水解乳清蛋白,皆为亲水亲油分子。液态环境的pH会影响蛋白质的空间结构的变化以及酪蛋白中胶体磷酸钙和离子钙的之间的动态平衡。pH还可以影响乳液表面集团的离子化程度,改变乳液液滴表面电荷密度,进而影响乳液中粒子的微观特性和稳定性。本研究通过调节全营养乳液不同的pH,考察p H对全营养乳液稳定性的影响。
乳液的电位反映了乳液体系中粒子的电荷水平。总体来说,电位绝对值越大,体系越趋于稳定。结果如图6所示,常温贮存第1 d,当乳液pH为6.2~6.58时,偏弱酸性,电位较低,在-23 mV左右波动;随着pH增加至6.95,电位下降到-25.07 mV。常温贮存20 d的乳液的电位相比于同pH的第1 d的电位都有所下降:pH6.2~6.42,电位下降至-24 mV;pH6.58~6.68,电位下降至-26.7 mV左右;p H6.82~6.95时,全营养乳液的电势降至-27.7 mV左右;基本来看,无论是贮存1 d还是贮存20 d,全营养乳液p H在偏弱碱性范围(pH6.82~6.95)的电位绝对值较高;当pH6.95时,贮藏20 d电位为-27.5 mV。

表4 不同浓度结冷胶对全营养乳液体系的影响Table 4 Effect of various gellan gum concentrations on total nutrient emulsion

图4 不同浓度结冷胶的全营养乳液LUMiSizer稳定性图谱Fig.4 The dispersion analysis of LUMiSizer chromatograms of total nutrient emulsion with various concentrations of gellan gum
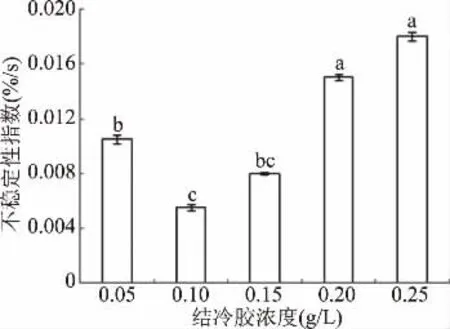
图5 不同浓度结冷胶的全营养乳液的不稳定性系数Fig.5 The instability index of total nutrient emulsion with various concentrations of gellan gum
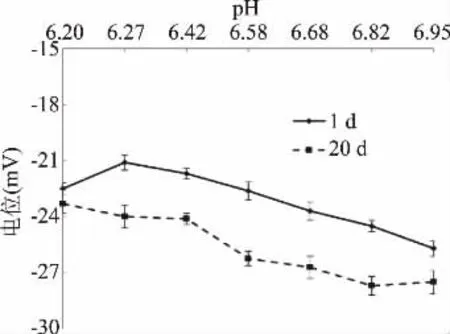
图6 不同pH下全营养乳液中电位的变化Fig.6 Effect of pH on Zeta potential of total nutrition emulsion
如图7所示,整个贮藏期内,随着贮存时间的增加,不同pH的全营养乳液的平均粒径都有相应的增加。平均粒径增大表明粒子相互聚集,不稳定性因素增高。全营养乳液pH从6.2增加到6.68,全营养乳液的平均粒径急速下降:平均粒径分别由1300 nm降至393 nm(第1 d)和由1369 nm下降至522 nm(第20 d)。当全营养乳液的pH继续升高至6.95,乳液的平均粒径则由393 nm增加到404 nm(第1 d)和由522 nm增加到603.5 nm(第20 d)。在整个贮藏期内,不同p H的乳液的平均粒径变化趋势一致,当pH为6.68时,乳液平均粒径最小。一方面液态环境的pH会影响蛋白质空间结构的变化以及酪蛋白中胶体磷酸钙和离子钙之间的动态平衡,进而影响到乳液微粒之间聚集程度;另一方面本研究所使用的结冷胶、微晶纤维素为阴离子多糖,随着pH减小,羧基质子化程度增加,乳液乳化能力降低,液滴间的静电斥力也随之减弱,乳液平均粒径增大。

图7 不同pH全营养乳液中平均粒径的变化Fig.7 Effect of pH on mean particle size of total nutrition emulsion
如图8所示,全营养乳液的pH从6.2增加到6.68时,全营养乳液的离心沉淀率持续降低。当pH为6.68时,乳液的离心沉淀率分别为1.79%(第1 d)和2.48%(第20 d);p H继续增加,由6.68增加至6.95时,离心沉淀率开始增加。当pH为6.95时,离心沉淀率分别增加至2.64%(第1 d)和3.1%(第20 d)。从乳液外观来看,偏弱酸性(p H6.20、p H6.27)的全营养乳液瓶壁上可见粗颗粒的分布;随着pH向中性或弱碱性(pH6.68~6.95)迁移,全营养乳液瓶壁光滑,未见粗颗粒。离心沉淀率的变化基本与平均粒径变化相一致。总体来看,pH为6.68时,离心沉淀率降至最低1.79%;随着贮存时间的增加,离心沉淀率也有所上升,贮存20 d后,离心沉淀率达到2.48%。总体来看,中性或弱碱性条件下(pH6.68~6.95),乳液中的粒子平均粒径较小,电位较大,离心沉淀率较小,此时体系较稳定。

图8 不同pH下全营养乳液的离心沉淀率Fig.8 Effect of pH on centrifugation sedimentation rate of total nutrition emulsion
2.3 全营养乳液货架期内稳定性变化
为了考察全营养乳液货架期的稳定性变化,本研究利用UHT灭菌、无菌灌装一批全营养乳液,置于常温下观察。全营养乳液135 d的电位变化如图9所示:贮藏期前期(第1~60 d),全营养乳液的电位一直不断下降,从-28 mV下降到-34 mV;贮藏期后半期(第60~135 d),电位缓慢下降,从-33.77 mV下降到-34.77 mV。
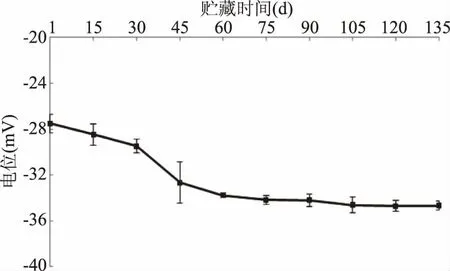
图9 常温下全营养乳液贮藏期间电位的变化Fig.9 Trends of Zeta potential of total nutrition emulsion during shelf life at room temperature
本研究中全营养乳液中的蛋白来源为酪蛋白和部分水解乳清蛋白。全营养乳液经过超高温灭菌、无菌灌装后,开始流通和销售。在热处理过程中,部分水解乳清蛋白变性、沉积于酪蛋白表面,蛋白颗粒发生聚集,乳液平均粒径增大。图10显示,135 d贮存期内,全营养乳液体系中平均粒径逐渐增大。贮藏期前期(第1~30 d),平均粒径基本维持在400 nm左右,变化不大;贮藏期中期(第30~45 d),平均粒径增大至约500 nm左右;贮藏期后期(第45~135 d),乳液的平均粒径基本变化幅度不大,维持在500 nm。随着贮存期的增加,一些变性的蛋白逐渐沉积于酪蛋白表面;同时附着在酪蛋白附近的脂肪液滴也逐渐吸引聚集,使得乳液体系中平均粒径逐渐增大。

图10 常温下全营养乳液贮藏期间平均粒径的变化Fig.10 Trends of mean particle size of total nutrition emulsion during shelf life at room temperature
图11 显示,贮藏期前期(第1~60 d)全营养乳液的离心沉淀率基本变化不大,约为1.8%左右;贮存期第60~105 d,离心沉淀率缓慢增加,从1.8%增加到2.3%;贮存期105~135 d,离心沉淀率变化不大,维持在2.3%左右。此时全营养乳液外观均一,有少许脂肪上浮,无沉淀。

图11 常温下全营养乳液贮藏期间离心沉淀率的变化Fig.11 Trends of centrifual sedimentation rate of total nutrition emulsion during shelf life at room temperature
全营养乳液在135 d贮藏期内pH变化如图12所示。不同杀菌处理会导致灭菌后全营养乳液的pH有所变化。同样的物料及配比,全营养乳液经UHT灭菌后,p H为7.02。总体来看贮藏于常温下的全营养乳液在整个贮藏期内p H呈下降趋势。图12显示全营养乳液的p H在贮藏期前期(第1~60 d)下降幅度很大,从7.02下降到6.57。贮藏后半期(第60~135 d),全营养乳液的pH下降趋于缓和,pH保持在6.57左右。贮藏期间内全营养乳液pH下降的原因很多:脂肪的氧化造成的水解、乳基原料中残余酶对蛋白和脂肪的降解生成游离氨基酸和脂肪酸、来自于酪蛋白的脱磷酸化作用、磷酸钙盐的形成[6,28-29]。本次贮存实验的样品是在UHT中试线上完成。在整个贮藏实验过程中,除了后期样品可观察到微量的脂肪上浮,未观察到胶凝现象和微生物污染现象。考虑到本研究中全营养乳液所用的原料与UHT中试线的情况,贮存期内全营养乳液pH的降低主要来自于脂肪的氧化降解以及热力加工所导致盐螯合、蛋白聚合造成体系pH变化。而体系p H的降低,又会反过来影响产品的稳定性。因此生产过程中阻氧对于保证全营养乳液体系稳定性非常重要。

图12 常温下全营养乳液贮藏期间pH的变化Fig.12 Trends of pH of total nutrition emulsion during shelf life at room temperature
3 结论
不同胶体对全营养乳液稳定性影响不同。微晶纤维素浓度对全营养乳液的平均粒径和黏度的变化幅度影响有限,对电位没有明显影响。微晶纤维素的适宜浓度为0.6 g/L,此时离心沉淀率和不稳定性指数分别为1.91%和0.0045。结冷胶浓度与全营养乳液的平均粒径成反比,与黏度成正比,结冷胶最适宜浓度为0.1 g/L。此时离心沉淀率为1.71%,不稳定性指数为0.0055。
p H对全营养体系的稳定性影响较大,p H微小变化会导致乳液平均粒径等特性发生明显变化,进而导致稳定性发生变化。弱酸性(6.2~6.58)范围内,易导致粒子互相聚集,易发生沉淀,体系不稳定。p H为6.68时,平均粒径最小,为393 nm,此时离心沉淀率最小,为1.79%;随着pH偏碱性移动(6.68~6.95),平均粒径又开始增高,离心沉淀率值开始变大。贮藏20 d,全营养乳液的同pH的全营养乳液的平均粒径、电位以及离心沉淀率的变化基本与储藏第1 d全营养乳液的粒子特性变化基本一致。
全营养乳液的平均粒径、电位、p H的变化主要在发生在货架期的前60 d,在这期间内,随着贮藏时间的增加,乳液中粒子不断发生聚集,变化到一定的程度进而影响到全营养乳液的稳定性。从货架期第60~105 d,全营养乳液的离心沉淀率增加至2.3%。从105~135 d,粒子特性基本保持不变。
