84例肺癌患者应用程序性死亡蛋白-1的免疫不良反应及护理
2021-06-21王艳何瑞仙翟敏锋苏伟才胡雪楠秦梦媛汪潘蓉黄秀秀
王艳,何瑞仙,翟敏锋,苏伟才,胡雪楠,秦梦媛,汪潘蓉,黄秀秀
(1.国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院a.内科;b.护理部,北京100021;2.北京大学 医学部,北京100191)
在我国,肺癌发病率和病死率都居恶性肿瘤之首[1-2]。化疗、放疗、手术是肺癌传统治疗手段,免疫治疗是近年来肺癌治疗新方法。随着程序性死亡蛋白-1(programmed death protein 1,PD-1)抑制剂的应用,晚期肺癌患者5年生存率从5%提高到16%[3]。PD-1抑制剂是目前临床应用最多的免疫检查点抑制剂,其治疗效果使更多肺癌患者受益。同时,该药也会发生皮肤毒性、内分泌毒性、肝脏毒性,甚至发生威胁患者生命的肺毒性和心脏毒性等反应,与传统化疗胃肠道反应、骨髓抑制等相比,具有一定的独特性,需要在护理工作中特别注意。目前,免疫不良反应在可控范围内,危及生命的毒性反应护理值得重视。经检索,对于PD-1免疫不良反应发生率、时间、程度及护理相关报道较少。笔者总结125例肺癌患者在笔者所在科室应用PD-1抑制剂后,发生免疫不良反应的特点及护理对策,报道如下。
1 临床资料
1.1 一般资料 便利选取2019年7月—2020年1月在医院接受PD-1抑制剂治疗的125例肺癌患者。纳入标准:(1)病理学确诊为肺癌,同期没有第二肿瘤;(2)接受PD-1抑制剂治疗;(3)年龄≥18岁;(4)无认知和交流障碍,能够电话随访。排除标准:有脑转移患者。本研究符合《赫尔辛基宣言》要求。
1.2 用药方案 采用PD-1抑制剂单药或PD-1抑制剂联合化疗药物治疗,按照推荐剂量2 mg/kg或3 mg/kg在静脉药液配置中心(PIVAS)进行配置,严格无菌操作,将PD-1抑制剂加入生理盐水100 mL中,使用无菌0.2 um过滤器输液器静脉滴注30~60 min,前后用生理盐水冲管,2~3周为1个治疗周期。
1.3 不良反应的分级和管理原则 遵循中国临床肿瘤学会(CSCO)免疫检查点抑制剂相关的毒性管理指南(2019版)[4],将毒性分为5个级别:G1,轻度毒性,无需住院,不推荐糖皮质激素治疗,可以继续使用PD-1治疗;G2,中度毒性,无需住院,局部使用糖皮质激素或口服全身使用,暂停PD-1治疗;G3,重度毒性,需住院治疗,全身口服或静脉糖皮质激素治疗,可请专科医师指导,停用PD-1;G4,危及生命的毒性,住院治疗并可收入加强护理病房,可请专科医师指导,全身静脉糖皮质激素治疗,永久停用PD-1;G5,与毒性相关的死亡。
1.4 统计学方法 使用SPSS 22.0对数据进行统计分析。所有数据收集由1人录入,1人核实,2人共同完成。用描述性统计方法描述一般资料,计数资料以例数、百分率(%)表示。
2 不良反应分析
2.1 肺癌患者免疫不良反应的构成比 125例患者中,84例出现免疫不良反应,男66例,占79%;年龄≥60岁43例,占51%;非小细胞肺癌75例,占89%,小细胞肺癌9例,占11%;PD-1抑制剂+化疗73例,占87%,PD-1抑制剂11例,占13%;65例(77%)患者只发生1种免疫不良反应。
2.2 免疫不良反应症状分类及程度分布 84例患者中,皮肤反应最多,31例,占37%;其次为甲状腺功能异常,29例,占35%;G1级42例(50%),G2级35例(42%),合计占92%。有15例患者终止治疗,除疾病进展5例外,其余10例为免疫不良反应,肺毒性-肺炎1例患者死亡;1例心脏毒性-心肌炎患者死亡。见表1。
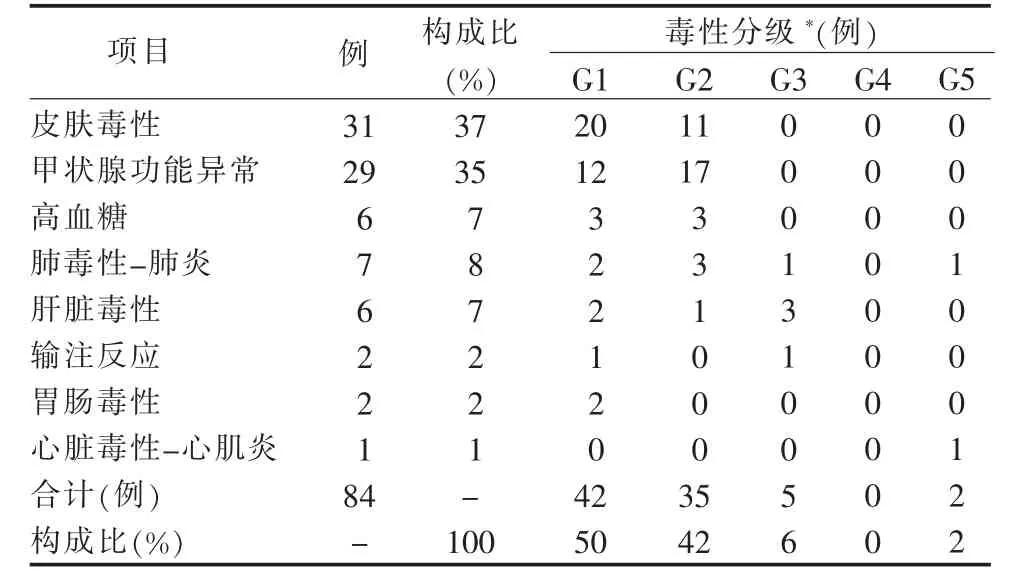
表1 84例肺癌患者免疫不良反应症状类别及程度分布
从表1可见,31例皮肤毒性患者为G1、G2级反应,且发生在第1、第2周期。其发生机制可能与PD-1/PD-L1和CTLA-4受体阻断介导的T细胞活化密切相关[5]。研究显示,皮肤毒性的发生率可达34%~40%[6],常发生在治疗早期[7],与本研究结果一致。皮肤毒性发生率高,且易于发现,因此护理上应尽早采用相应护理措施[8]。
从表1可见,29例甲状腺功能异常患者为G1、G2级反应,发生在第1、第2周期,5例甲状腺功能亢进患者发展为甲状腺功能减退[9]。发生机制可能与T细胞介导的甲状腺毒性[10]、甲状腺自身抗体对甲状腺组织的破坏[11]等有关。本组甲状腺功能减退患者,血清结果:促甲状腺激素(TSH)增高、游离T4降低。患者表现为乏力、皮肤苍白干燥、怕冷、体质量增加、便秘、抑郁等。
2.3 免疫不良反应发生时机 84例免疫不良反应主要发生在第1、第2周期,分别为36例和32例,占发生毒性反应的81%。皮肤毒性和甲状腺功能异常所占比例最多。见表2。
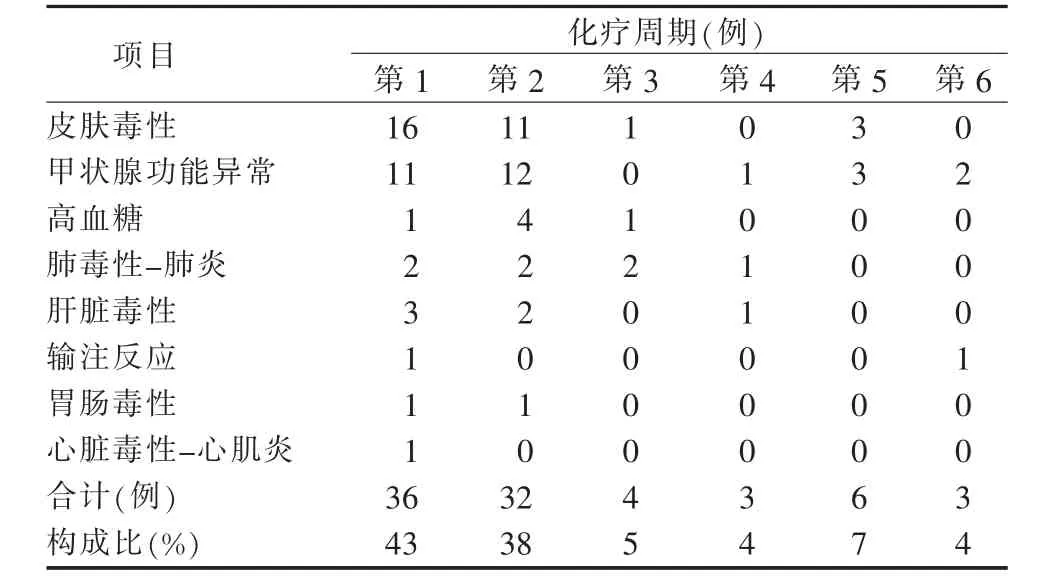
表2 84例肺癌患者免疫不良反应的发生时机
3 护理
3.1 注重评估观察与随访 本研究中,84例患者发生了不同程度的免疫不良反应,发生率67%(84/125)。其中,79%为男性,77%只发生1种不良反应,92%为轻中度。研究表明,化疗患者受多症状困扰[12],免疫治疗也存在相同的情况。为了预防和降低免疫不良反应,评估与观察为护理工作重点之首。在使用PD-1抑制剂治疗前,评估患者(尤其是男性患者)一般情况,询问感染HIV/HBV患者、既往抗肿瘤治疗情况等问题;评估影像学、血液学、皮肤黏膜检查等,尤其是自身免疫性疾病患者,保证治疗安全性。治疗中,观察用药后反应。出院后,定期电话或微信随访:症状、营养心理状况、用药情况及化验检查等,以便发现免疫不良反应是否加重或新出现,及时就诊并通知医师,根据反应级别对症治疗,做好相关护理。
3.2 常见免疫不良反应护理对策 从表1可见,81%免疫不良反应主要发生在化疗的第1、第2周期,皮肤毒性和甲状腺功能异常所占比例最多。针对此,提出护理对策如下。
3.2.1 将心理护理与健康宣教相结合 PD-1抑制剂作为肿瘤治疗的新药,单药治疗只有10%的适宜人群,在临床中免疫联合化疗可能更能够获益[9]。但是从经济压力、治疗效果,还有可能出现的免疫不良反应等问题上,势必会给癌症患者造成一定程度的紧张、焦虑情绪。治疗中为患者营造良好的病室环境,医生和护士床旁完成口头宣教,发放纸质版宣教小册子,并让患者复述以强化宣教效果,做好充分的心理准备,鼓励患者说出感受,帮助树立战胜疾病的信心,促进治疗顺利完成。
3.2.2 皮肤毒性护理 注意饮食清淡,避免辛辣、刺激食物;穿纯棉衣物,温水清洗,减少对皮肤的刺激;做好心理护理等。表1中,G1级20例患者手背、四肢、胸背部出现散在红色小点,伴有或不伴有瘙痒,局部使用润肤剂,外用糖皮质激素的软膏。G2级11例患者片状红疹,伴有瘙痒,以胸部最明显,在G1级治疗基础上,口服抗组胺药、糖皮质激素等,避免将皮肤抓破,出现感染现象[13]。同时,警惕Stevens-Johnson综合征/中毒性表皮坏死松解症(Stevens-Johnson syndrome/toxic epidermal necrosis,SJS/TEN)的发生,以免加重皮肤毒性程度,终止治疗。
3.2.3 甲状腺功能异常护理 本组出现29例甲状腺功能减退。给予温水洗澡,保持皮肤清洁,涂润肤乳,及时添加柔软、棉质衣物,注重保暖,提升体温;合理饮食,宜高蛋白、高维生素、高纤维、低脂饮食;适当活动,如散步、按摩腹部,以促进肠蠕动,减轻便秘;观察患者意识、精神状态,解释甲状腺功能减退原因,减轻焦虑、恐惧等心理,必要时可心理状态评估。
3.2.4 高血糖护理 本研究中,有6例患者出现高血糖,均顺利完成治疗。治疗期间监测患者血糖情况,必要时请内分泌科会诊。出院后定期随访,提供规范的健康教育:合理饮食,包括控制总热能、适量碳水化合物、充足食物纤维和蛋白质、控制脂肪摄入量;保持运动,每日餐后0.5~1 h进行散步、骑自行车、太极拳等活动,至少每周3次,每次0.5 h;定期监测血糖情况,坚持规律用药。
3.3 重度(G3级)以及致死性(G5级)不良反应的护理对策
3.3.1 肝脏毒性护理 文献报道发生率约为5%,中、重度的ALT/AST升高发生率约为1%~2%[4],这与本研究相似。本组中3例患者由于ALT>正常5~20倍ULN,总胆红素>正常3~10倍ULN,而停止使用PD-1抑制剂治疗。在护理中加强心理护理;指导患者戒烟、戒酒;多食高蛋白、高维生素、清淡、易消化饮食;适当运动,注意劳逸结合;定期检查肝功能,遵医嘱使用保肝药物、泼尼松等。现患者肝功能恢复正常。
3.3.2 输注反应护理 本研究中1例患者输液中出现寒战、体温39.5℃,呼吸困难,立即停止输入PD-1抑制剂,严格无菌操作更换输液器及生理盐水,给予心电监护,吸氧2 L/min,物理降温,苯海拉明和糖皮质激素治疗,1 h后体温降至38.0℃,3 h后体温降至正常,呼吸困难较前明显减轻,第2天缓解。同时做好生活护理,及时更换被服及病员服,做好解释,减轻心理压力。
3.3.3 肺毒性-肺炎护理 本组中2例G1级肺炎经治疗后继续完成后续治疗,5例发生肺毒性-肺炎患者终止治疗。有研究表明,约33%的患者无症状,仅有影像学的异常[14]。重度以上的肺炎发生率0%~
1.5%,是罕见但致命的严重不良事件[4]。本组中的肺炎死亡患者,因发热、胸闷、憋气告知主管医生,入院后,积极给予物理降温、低流量吸氧2 L/min[15-16],心电监护,严格无菌操作,住单间病房,病室每日通风2次,每次30 min,避免交叉感染等措施。监测各项检查,遵医嘱静脉滴入甲基泼尼松龙、抗感染治疗并补液维持水电解质平衡等营养治疗。给予心理支持,协助翻身叩背、更换衣物、保持床单位整洁等生活护理。此患者病情稍稳定转回当地治疗后死亡。
3.3.4 心脏毒性-心肌炎护理 本组中1例心脏毒性-心肌炎是致死的主要原因。本组中心脏毒性患者是护士在治疗后1周进行电话随访发现,患者主诉乏力、胸闷、胸痛,咳嗽1 d,护士立即让患者急诊就医,经过ECG和心梗标志物检查,静脉大剂量糖皮质激素治疗等[17],患者1 d后抢救无效死亡。通过上述情况,做好患者及家属的评估观察、心理护理、健康宣教很重要。特别要反复强调:如有胸闷、胸痛,憋气等可能危及生命的症状,需立即报告医生并就医,尽早发现,尽早治疗,提高患者及家属的警觉性,做好病情加重的思想准备。
