UPLC-PDA测定泽泻中两种活性成分并对不同产地药材的质量分析
2021-06-18张学花邢会香曹得辉毛喜孝
张学花,邢会香,刘 红,曹得辉,毛喜孝,郭 静
(青海普兰特药业有限公司,青海 西宁 810000)
泽泻为常用中药材之一,《神农本草经》中列为上品[1],为泽泻科植物东方泽泻Alismaorientale(Sam.)Juzep.或泽泻Alismaplantago-aquaticaLinn.的干燥块茎[2]。研究表明,泽泻具有利尿,降血糖、血脂及抗动脉粥样硬化,抗肾结石形成,抗肾炎活性,免疫调节等作用[3]。泽泻含有三萜类化合物、倍半萜类化合物、二萜类化合物、类脂、糖类等成分,其中三萜类是泽泻萜类化合物的主要化学成分,包括泽泻醇A、泽泻醇B及其衍生物[4],泽泻醇B是利尿成分[5],23-乙酰泽泻醇B可用于研制新型抗肿瘤药物[6]。中国药典2015版仅测定23-乙酰泽泻醇B的含量[7],2020版药典测定23-乙酰泽泻醇B和23-乙酰泽泻醇C的含量[2],经研究发现泽泻植株无论哪个部位泽泻醇B与23-乙酰泽泻醇B含量均最高,23-乙酰泽泻醇C含量最少[8],因此控制泽泻药材中含量较高的泽泻醇B和23-乙酰泽泻醇B对于控制药材质量显得尤为重要。
1 材料
1.1 仪器
ACQUITY UPLC H-CLASS 超高液相色谱仪(ACQUITY UPLC PDA eLambda检测器,Waters),MS105型十万分之一电子分析天平(METTLER TOLEDO),ML-204T-02型万分之一电子分析天平[梅特勒-托利多仪器(上海)有限公司],JP-080ST型超声清洗仪(深圳市洁盟清洗设备有限公司有限公司)。
1.2 药材与试剂
泽泻醇B对照品(NATURE,批号:18649-93-9,纯度:95.0%),23-乙酰泽泻醇B对照品(中国食品药品检定研究院,批号:111846-201705,纯度:99.7%);泽泻药材共20批次,产地分别为江西省抚州市、四川省眉山市、广西省贵港市;甲醇、乙腈均为进口色谱纯,磷酸为分析纯,水为屈臣氏蒸馏水。
2 方法与结果
2.1 色谱条件
色谱柱:ACQUITY UPLC BEH C18(100×2.1mm,1.7μm);流动相:乙腈-0.1%磷酸;梯度洗脱,洗脱程序为:0-1.0min(60∶40)、1.0-2.0min(48∶52)、2.0-7.0min(48∶52)、7.0-8.0min(57∶43)、8.0-12.0min(57∶43)、12.0-13.0min(80∶20)、13.0-16.0min(80∶20)、16.0-17.0min(60∶40);流速为0.50mL/min;检测波长为208nm;进样量为5μL。理论板数按泽泻醇B峰计算应不低于3500。
2.2 溶液的制备
2.2.1 空白溶液 70%甲醇水溶液。
2.2.2对照品溶液 取泽泻醇B对照品、23-乙酰泽泻醇B对照品适量,精密称定,加70%甲醇水溶液分别制成每1ml含泽泻醇B 0.1mg、23-乙酰泽泻醇B50μg的溶液。
2.2.3供试品溶液 取本品粉末(过三号筛)约1g,精密称定,置具塞锥形瓶中,精密加入70%甲醇水溶液50mL,称定重量,超声处理10min,放冷,再称定重量,用70%甲醇水溶液补足减失的重量,摇匀,用0.22μm微孔滤膜滤过,取续滤液备用。
2.3 系统适用性试验
按照2.2方法分别制备得到对照品溶液和供试品溶液,按2.1项下色谱条件进行测定,记录色谱。结果显示对照品连续进样5针,泽泻醇B峰面积的RSD为0.24%,保留时间的RSD为0.46%,对照品和供试品溶液中泽泻醇B和23-乙酰泽泻醇色谱峰与前后杂质峰分离度均大于1.50,泽泻醇B色谱峰的理论塔板数均不小于3500,提示该色谱系统系统适用性良好。
2.4 专属性试验
按照2.2方法分别制备得到空白溶液、对照品溶液、供试品溶液,按2.1项下色谱条件进行测定,记录色谱,见图1。结果显示空白溶液对主色谱峰无干扰,对照品和供试品溶液中主色谱峰保留时间一致。另采用PDA检测器对对照品溶液、供试品溶液中的主色谱峰进行峰光谱扫描和纯度检测。结果显示对照品和供试品溶液中主色谱峰纯度角度均小于纯度阈值,纯度符合要求,无阴性干扰。具体数据见表1。本试验提示该方法专属性良好。
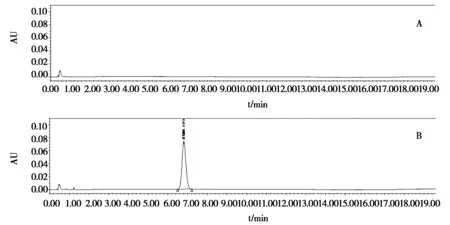

图1 泽泻及其对照品高效液相色谱图

表1 泽泻和对照品主色谱峰纯度角度和纯度阈值列表
2.5 线性关系考察
2.5.1泽泻醇B对照品线性关系考察 精密称定泽泻醇B对照品20.16mg,加70%甲醇水溶液制成192μg/ml的泽泻醇B对照品母液。分别精密量取适量上述母液,稀释配制成浓度为0.96、48、96、144、192μg/ml的系列对照品溶液。按2.1项下色谱条件进行测定,记录色谱。以质量浓度(X,μg/ml)为横坐标、峰面积(Y)为纵坐标进行线性拟合,得回归方程Y=10477X+923.58(r=0.9999)。结果表明,泽泻醇B对照品在0.96-192μg/ml线性关系良好。
2.5.223-乙酰泽泻醇B对照品线性关系考察 精密称定23-乙酰泽泻醇B对照品20.33mg,加70%甲醇水溶液制成0.203μg/ml的23-乙酰泽泻醇B对照品母液。分别精密量取适量上述母液,稀释配制成浓度为10.150、25.375、50.750、76.125、101.500μg/ml的系列对照品溶液。按2.1项下色谱条件进行测定,记录色谱。以质量浓度(X,μg/ml)为横坐标、峰面积(Y)为纵坐标进行线性拟合,得回归方程Y=9290.7X+2520.7(r=1.0000)。结果表明,23-乙酰泽泻醇B对照品在10.150-101.500μg/ml线性关系良好。
2.6 重复性试验
由实验员(甲)分别取泽泻药材粉末(过三号筛)约1g,平行6份样品,精密称定,按照2.2.3方法制备得到6份供试品溶液。按2.1项下色谱条件进行测定,记录色谱。结果泽泻醇B和23-乙酰泽泻醇B含量的RSD分别为2.2%、2.1%,提示该方法重复性良好。
2.7 中间精密度试验
由另外一名实验员(乙)分别取泽泻药材粉末(过三号筛)约1g,平行6份样品,精密称定,按照2.2.3方法制备得到6份供试品溶液。按2.1项下色谱条件用另一台G18QSM448A超高液相色谱仪进行测定,记录色谱。结果甲乙两名实验员在不同仪器上测得泽泻醇B和23-乙酰泽泻醇B含量的RSD分别为3.4%、3.7%,提示该方法中间精密度良好,具体数据见表2。

表2 中间精密度试验结果(n=9)
2.8 加样回收试验
取已知含量的泽泻药材粉末(过三号筛)约0.5g,平行9份样品,分为3组,分别加入3个质量分数水平(50%、100%和150%)的泽泻醇B和23-乙酰泽泻醇B对照品。按照2.2.3项下溶液制备方法制备得到9份供试品溶液。按2.1项下色谱条件进行测定,记录色谱并计算加样回收率,结果见表3。

表3 回收率试验结果(n=9)
2.9 稳定性试验
取2.2.3项下供试品溶液适量,分别置于室温下放置0、2、4、8、12、16、24h时按2.1项下色谱条件进行测定,记录色谱。结果供试品中泽泻醇B和23-乙酰泽泻醇B色谱峰峰面积的RSD值分别为0.8%和0.8%。结果表明供试品在70%甲醇水溶液中24h内稳定性良好,具体数据见表4。
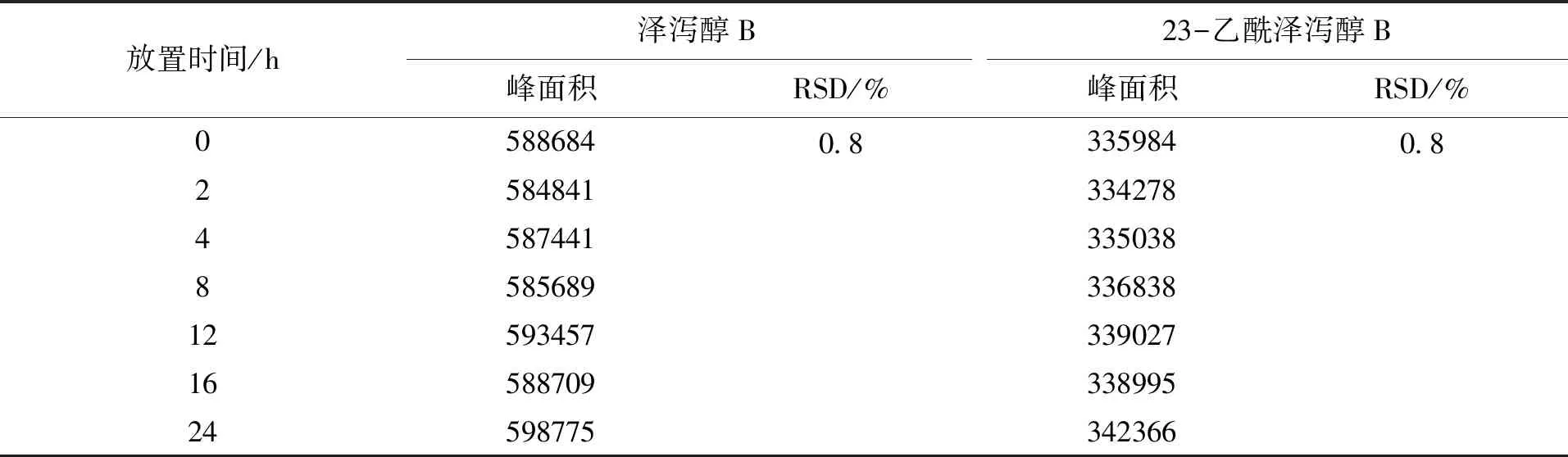
表4 稳定性试验结果
2.10 耐用性试验
本研究中耐用性试验是通过微调测试条件中的单个变量观察结果的不受影响程度,改变的测试变量包括流动相组成、流速、柱温、色谱柱。结果表明该方法耐用性良好,具体数据见表5。
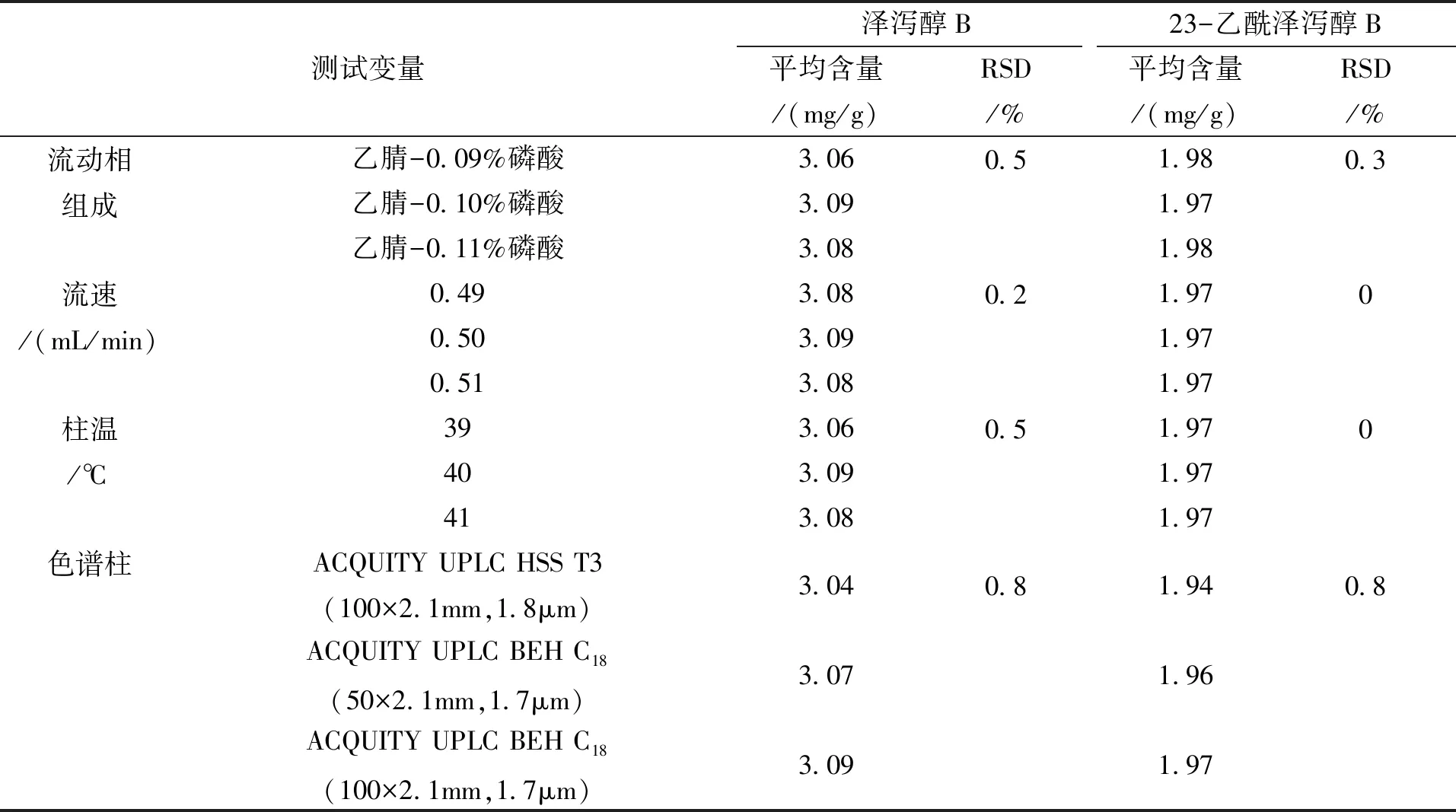
表5 耐用性试验结果
2.11 样品含量测定
取20批次泽泻样品适量,按照2.2.3方法制备供试品溶液,再按2.1项下色谱条件进行测定,双样双针,记录色谱并计算样品含量,结果见表6。
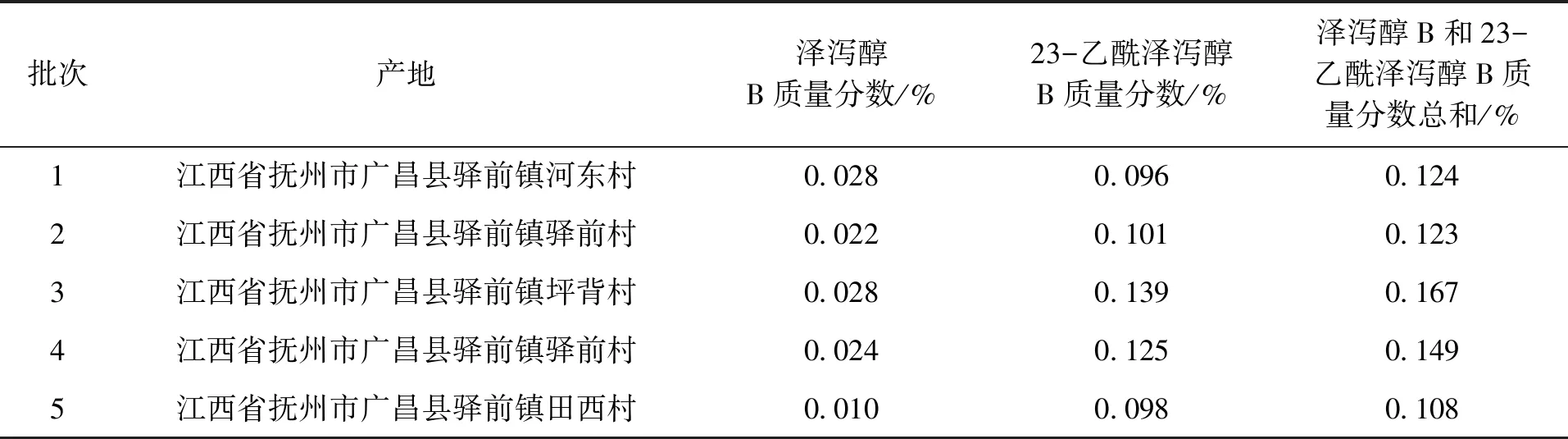
表6 泽泻样品中泽泻醇B和23-乙酰泽泻醇B含量测定结果(n=2)

续表6
3 讨论
3.1 色谱条件的选择
本研究考察了柱温、流速、进样体积对色谱峰分离的效果,结果当柱温30℃、流速0.35ml/min、进样体积10μl时峰形均未达到要求,柱温40℃、流速0.50ml/min、进样体积5μl时峰形符合要求。
3.2 提取条件的选择
本研究考察了不同比例和不同类别的提取溶剂(30%、50%、70%甲醇水溶液,50%乙腈水溶液和50%乙醇水溶液)进行提取,同时考察了不同提取方式(超声和回流)、不同提取时间(10、20、30min)和不同溶剂量(10、25、50、100ml)对泽泻醇B和23-乙酰泽泻醇B含量的影响,结果发现提取溶剂和溶剂量对结果有较显著的影响,而提取方式和提取时间对含量结果影响较小,因此最终确定最佳提取条件为50ml 70%甲醇水溶液超声提取10min。
4 结论
综上所述,该方法操作简单,可以同时快速测定泽泻中含量较高的三萜类成份泽泻醇B和23-乙酰泽泻醇B成分的含量,且重复性、准确度及耐用性良好,本研究为今后药典中建立合理的泽泻药材质量标准奠定了良好的基础。用本研究方法分析20批不同产地的泽泻药材,江西省、四川省、广西省泽泻醇B和23-乙酰泽泻醇B总含量差异较大,其中四川的总含量较高,这为药材的资源评价和合理使用提供科学参考。
