HPLC法测定藏药三果汤中没食子基儿茶素没食子酸酯和表没食子基儿茶素没食子酸酯的含量
2021-06-17林艾和
黄 宽 林艾和 范 源,2*
1.云南中医药大学,云南 昆明 650500;2.云南中医药大学第二附属医院,云南 昆明 650216
三果汤又名哲布汤,由诃子(Terminaliachebula)、毛诃子(Terminaliabellirica)和余甘子(Phyllanthusemblica)3味药组成,为藏医中重要的基础方,《四部医典》中记载,其具有治疗瘟疫、紊乱热症、促使热症成型的作用[1]。现代研究表明,三果汤主要含鞣质酚酸类成分[2],具有抗菌[3]、抗炎[4-5]、抗肿瘤[6-7]、抗氧化[8]、抗辐射[9]、降糖[10]、降脂[11]、肝肾损伤的保护[12-13]等药理作用。没食子基儿茶素没食子酸酯(gallocatechin gallate,GCG)、表没食子基儿茶素没食子酸酯(epigallocatechin gallate,EGCG)为儿茶素类物质,具有抗氧化、降脂、抗肿瘤、抗血栓等作用以及清除自由基活性等[14-18]。目前,尚无对三果汤中这两个成分进行定量分析的报道,为更全面地评价三果汤的质量,本研究建立建立新的HPLC方法对三果汤中EGCG和GCG成分的含量进行定量测定。
1 仪器与试剂
Agilent 1200高效液相色谱仪(美国Agilent公司),色谱柱为 Agilent Zorbax C18键合硅胶柱(150 mm×4.6 mm,5 μm);DFY-600摇摆式高速万能粉碎机(永康式速锋工贸有限公司);T-1000型电子天平(上海浦春计量仪器有限公司);AB265-SMETTLER TOLEDO十万分之一分析天平(Mettler-tolido international trade(Shanghai) co.LTD)。
表没食子基儿茶素没食子酸酯(EGCG批号:wkq20051208,四川省维克奇生物科技有限公司)、没食子基儿茶素没食子酸酯(GCG批号:wkq20051403,四川省维克奇生物科技有限公司);诃子、毛诃子、余甘子(批号:20190803,安国市旭芳中药材经营有限公司)。甲醇、乙腈为色谱纯,其余试剂为分析纯,水为超纯水。
2 方法与结果
2.1 色谱条件 色谱柱为Zorbax C18(4.6 mm×250 mm,5 μm);流动相:乙腈(A)-0.1%磷酸(B),梯度洗脱(0~8 min,8%~10% A;8 ~20 min,10%~15% A;20~50 min,15%~30% A;流速:1.0 mL·min-1;检测波长:280 nm;柱温:25 ℃;进样量:10 μL。理论塔板数按EGCG计算应不低于5000,分离度均大于1.5。色谱图如图1所示。
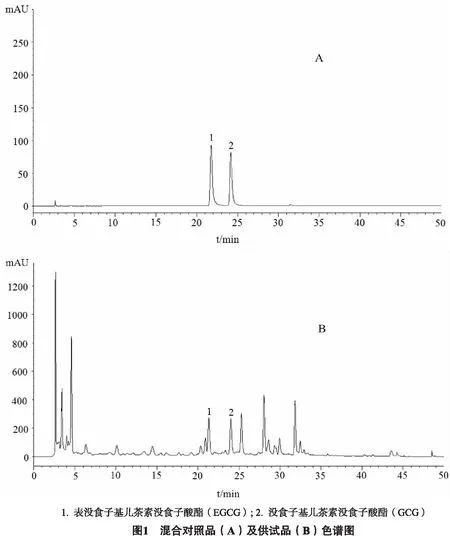
2.2 溶液的制备
2.2.1 混合对照品溶液 分别精密称取EGCG、GCG对照品2.31 mg、0.84 mg,置于10 mL量瓶中,用甲醇配制成EGCG、GCG浓度分别为0.2310 mg·mL-1和0.0840 mg·mL-1的混合对照品溶液。放置于4℃冰箱保存,临用时放置至室温。
2.2.2 供试品溶液 根据传统藏医药中三果汤处方配比,诃子、毛诃子和余甘子3种药材去核后按1∶1∶1的比例水煎制得[19],称取取诃子、毛诃子、余甘子药材(去核)各1.0 g,捣碎,加入100 mL馏水,浸泡30 min,煎煮3次,每次20 min,过滤,合并3次滤液,浓缩定容至50 mL容量瓶中,冷藏备用。制备成含生药0.5 g·mL-1的三果汤水提物,吸取备用三果水提物1 mL,加50%甲醇定容于10 mL容量瓶中,用0.45 μm的微孔滤膜进行过滤处理,即得到样品溶液。
2.3 线性关系考察 分别精密称取EGCG、GCG对照品11.55 mg、4.20 mg,置于50 mL量瓶中,用甲醇配制成EGCG、GCG浓度分别为0.2310 mg·mL-1和0.0840 mg·mL-1的混合对照品储备液。精密吸取混合对照品储备液各1、2、4、6、8、10 mL于10 mL量瓶中,分别加甲醇稀释,得到EGCG分别为0.0231、0.0462、0.0924、0.1386、0.1848、0.2310 mg·mL-1;GCG分别为0.00840、0.0168、0.0336、0.0504、0.0672、0.084 mg·mL-1的6份不同质量浓度的混标溶液,精密吸取上述各溶液10 μL进样。以质量浓度(mg·mL-1)为横坐标(X),峰面积(mAU*s)为纵坐标(Y)进行线性回归,绘制标准曲线进行回归分析。EGCG回归方程为Y=1391.4X-23.937,r=0.9996,表明EGCG在0.0231~0.2310 mg·mL-1范围内EGCG的峰面积与质量浓度呈现良好的线性关系。GCG回归方程为Y=3489.7X-59.47,r=0.9991,表明GCG在0.0084~0.0840 mg·mL-1范围内GCG的峰面积与质量浓度呈现良好的线性关系。

表1 线性关系考察结果
2.4 精密度试验 精密吸取“2.2.2”项下混合对照品溶液,在“2.1”项条件下连续进样6次,结果显示EGCG、GCG峰面积RSD分别为0.53%、0.67%,表明仪器精密度良好。
2.5 稳定性试验 取同一份供试品溶液,在“2.1”项条件下,分别于2、4、6、8、10、12 h进样,结果显示EGCG、GCG在10 h内峰面积的RSD值分别为0.91%、1.14%,表明供试品溶液在12 h内稳定性良好。
2.6 重复性试验 取同一批诃子、毛诃子、余甘子药材6份,按“2.2.3”项下方法制备供试品溶液,精密吸取6份供试品溶液各10 μL进样,结果显示EGCG、GCG平均含量为12.26 mg/g、5.23 mg/g, RSD分别为1.51%、1.47%,表明该方法重复性良好。
2.7 加样回收率试验 精密称取9份已知含量的诃子、毛诃子、余甘子药材各0.5 g,按1∶1∶1配制成三果汤,分别按照药材含有量的80%、100%、120%加入混合对照品,按“2.2.3”项下方法制备供试品溶液,精密吸取10 μL在“2.1”项条件下进样。结果见表2。其中,供试品溶液以10 μL进样分析,测得EGCG和GCG均在标准曲线线性范围内。

表2 加样回收率试验 (n=9)
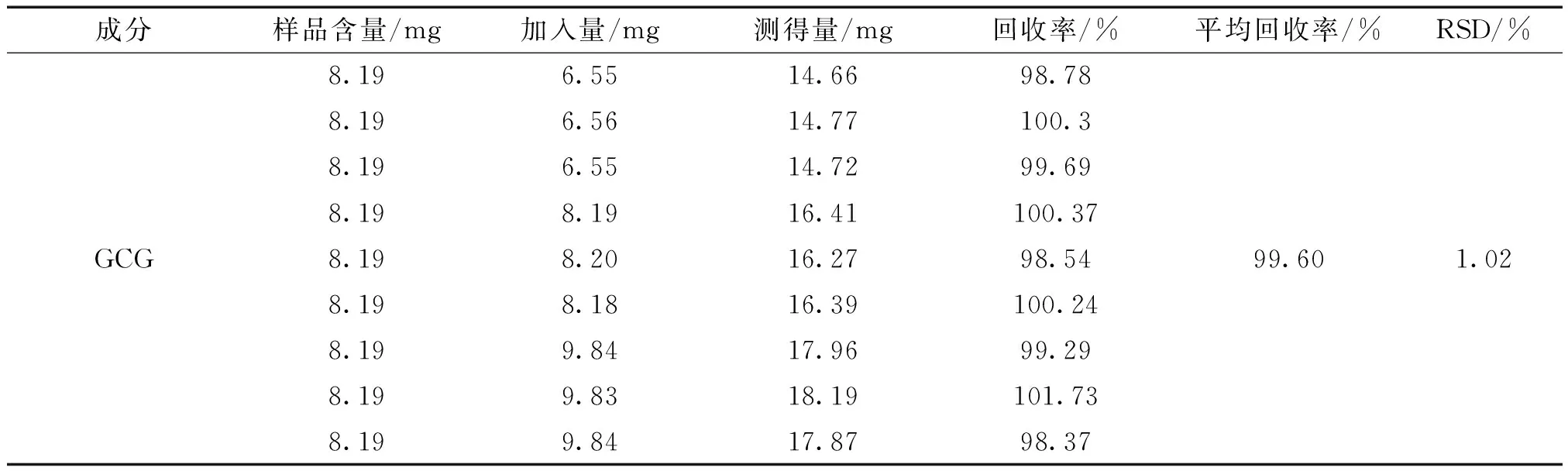
续表2 表2 加样回收率试验 (n=9)
2.8 含量测定 取6份不同批次三果汤样品,按“2.2.2”项下方法制备供试品溶液,在“2.1”项下条件下进样,计算EGCG和GCG成分含有量,结果见表3。
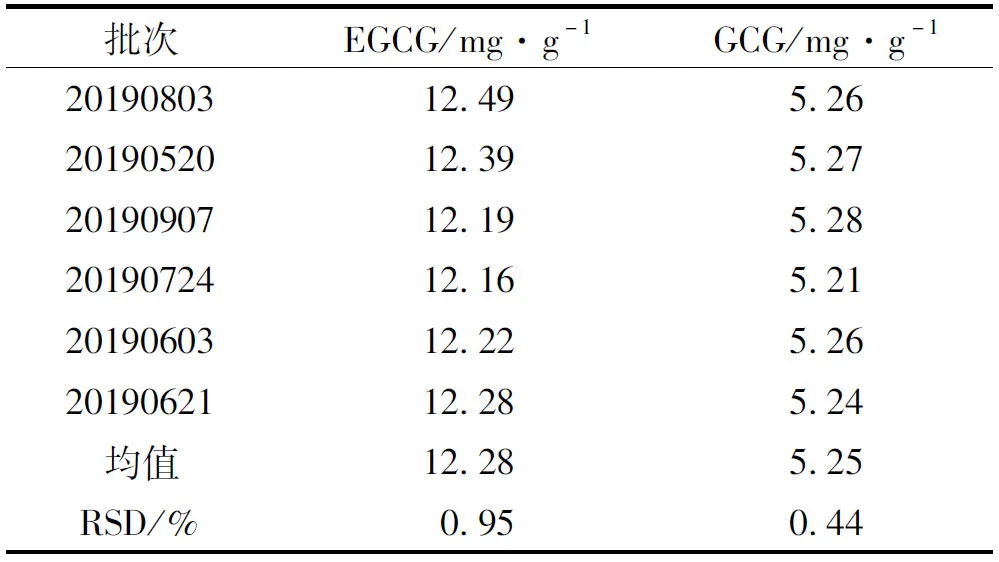
表3 含量测定结果
3 讨论
本试验分别对不同流动相系统进行考察,乙腈(甲醇)-0.1%磷酸、乙腈(甲醇)-0.2%磷酸等流动相系统,结果表明,乙腈-0.1%磷酸水溶液作流动相进行梯度洗脱时,分离度较好且峰形尖锐。同时对柱温(25、30、35℃)和流速(0.85、1.0、1.25、1.5 mL·min-1)进行了优化。结果显示,柱温25 ℃、流速 1.0 mL·min-1时分离效果好。本研究以EGCG和GCG作为三果汤水提物质量控制指标,建立了HPLC同时测定三果汤水提物中EGCG和GCG含量的方法。该方法简便可行,结果准确,可有效控制三果汤水提物的质量,为藏药三果汤的药效物质基础研究提供基础。
