新旧两版指南对浸润性乳腺癌HER-2基因扩增的判读影响
2021-06-17杨向红
张 莹,王 哲,杨向红
乳腺癌是全球女性常见的恶性肿瘤之一,近年乳腺癌的发病率逐年升高,并呈年轻化趋势[1]。有研究发现,曲妥珠单抗对浸润性乳腺癌组织中HER-2基因扩增患者的分子靶向治疗取得较好疗效,因此明确HER-2基因状态对乳腺癌患者治疗尤为重要[2]。目前HER-2检测方法有免疫组化(immunohistochemistry, IHC)、荧光原位杂交(fluorescence in situ hybridization, FISH)、显色原位杂交(chromogenic in situ hybridization, CISH)、双色银染原位杂交(dual-color in situ hybridization, DISH)等。本文采用IHC和FISH两种方法进行HER-2蛋白表达和基因扩增检测,分析其一致性;应用《乳腺癌HER-2检测指南(2014版)》[3](简称旧版指南)和《乳腺癌HER-2检测指南(2019版)》[4](简称新版指南)进行判读,探讨新旧两版指南对判读结果的影响,旨在为临床靶向用药提供参考。
1 材料与方法
1.1 材料收集2019年1月~2020年10月中国医科大学附属盛京医院存档的乳腺浸润性导管癌组织石蜡标本698例,其中手术切除标本575例,粗针穿刺标本123例。所有患者均为女性,年龄23~84岁,中位年龄53岁,术前均未接受新辅助治疗。采用IHC和FISH法进行HER-2蛋白表达和基因扩增检测,根据新旧两版指南判读标准,由两位病理医师阅片判读。
1.2 方法
1.2.1IHC 标本均经10%中性福尔马林固定,石蜡包埋,连续3 μm厚切片3张,分别进行HE、IHC、FISH染色。IHC使用HER-2/neu兔单克隆抗体(4B5,罗氏诊断公司),Ventana BenchMark XT 全自动免疫组化仪检测,每例标本均设有阴、阳性对照。
1.2.2FISH 使用HER-2基因扩增检测试剂盒(北京金菩嘉公司)。(1)石蜡切片65 ℃烤片2 h,常规脱蜡。(2)预处理:100%乙醇脱二甲苯5 min,去离子水3 min,水煮20 min。(3)酶消化:37 ℃预热的胃蛋白酶工作液中消化10 min。(4)梯度乙醇脱水。(5)变性及杂交:滴加探针混合液,盖玻片,封片胶封固,85 ℃ 5 min,42 ℃孵育16~18 h。(6)杂交后处理:46 ℃ 2×SSC洗涤5 min,46 ℃ 0.1%NP-40洗涤2 min,70%乙醇3 min,暗处自然干燥。(7)DAPI(4′6-二脒基-2-苯基吲哚)复染、封片。(8)荧光显微镜下判读。
1.3 结果判读IHC结果判读:根据旧版指南无染色或≤10%的浸润癌细胞呈不完整的、微弱的细胞膜染色为0;>10%的浸润癌细胞呈不完整的、微弱的细胞膜染色为1+;>10%的浸润癌细胞呈弱~中等强度的完整细胞膜染色,或≤10%浸润癌细胞呈强而完整的细胞膜染色为2+;>10%的浸润癌细胞呈强而完整且均匀的细胞膜染色为3+。新版指南与旧版指南判读结果基本相同。
FISH结果判读:在低倍镜下观察整张FISH切片,判断检测质量以及是否存在HER-2基因扩增的异质性。找到至少2个浸润癌区域,随机计数30个浸润癌细胞中的双色信号(要求细胞核大小一致、核边界完整、DAPI染色均一、细胞核无重叠、信号清晰)。双探针FISH判读标准详见图1、2。

图1 旧版指南HER-2双探针FISH检测判读标准:a表示均质、连续的浸润细胞,且占浸润癌的10%以上
1.4 统计学方法采用SPSS 17.0软件进行统计学分析,对IHC与FISH法检测的HER-2蛋白表达与基因扩增结果进行Kappa一致性分析及Spearman等级相关分析,本实验以P<0.05为差异有统计学意义。
2 结果
2.1 旧版指南判读在698例乳腺浸润性导管癌患者中,IHC法进行HER-2蛋白检测,合计检测HER-2(0)、HER-2(1+)患者116例,检出率为16.6%(116/698);HER-2(2+)患者402例,检出率为57.6%(402/698);HER-2(3+)患者180例,检出率25.8%(180/698)(图3)。

图3 HER-2蛋白表达,Ventana Ultraview DAB 法:A.HER-2(0);B.HER-2(1+);C.HER-2(2+);D.HER-2(3+)
FISH法进行HER-2基因扩增检测,HER-2基因扩增阳性284例,检出率为40.7%(284/698);HER-2基因扩增阴性364例,检出率为52.1%(364/698);HER-2基因扩增结果不确定50例,检出率为7.2%(50/698)。

图2 新版指南HER-2双探针FISH检测判读标准:a表示IHC检测HER-2(3+)呈阳性;HER-2(0)、HER-2(1+)、HER-2(2+)均呈阴性
2.2 新版指南判读在698例乳腺浸润性导管癌中,FISH法检出HER-2基因扩增阳性279例,检出率为40.0%(279/698);FISH法检测HER-2基因扩增阴性419例,检出率为60.0%(419/698)。IHC法检测HER-2蛋白表达结果与旧版指南判读结果一致。
2.3 新版与旧版指南判读分析与旧版指南判读结果相比,新版FISH法检测HER-2基因扩增阳性由40.7%降至40.0%,FISH法检测HER-2基因扩增结果不确定由7.2%降至0,FISH法检测HER-2基因扩增阴性由52.1%升至60.0%。在698例FISH法检测HER-2基因扩增结果中,642例新旧两版判读结果相同,一致率为92.0%(642/698),56例两版判读结果不同(8.0%,56/698)。56例中旧版指南FISH法检测HER-2基因扩增阳性而新版指南为阴性的6例,旧版指南FISH法检测HER-2基因扩增结果不确定而新版指南为阳性1例,旧版指南FISH法检测HER-2基因扩增不确定而新版指南阴性49例(图4)。
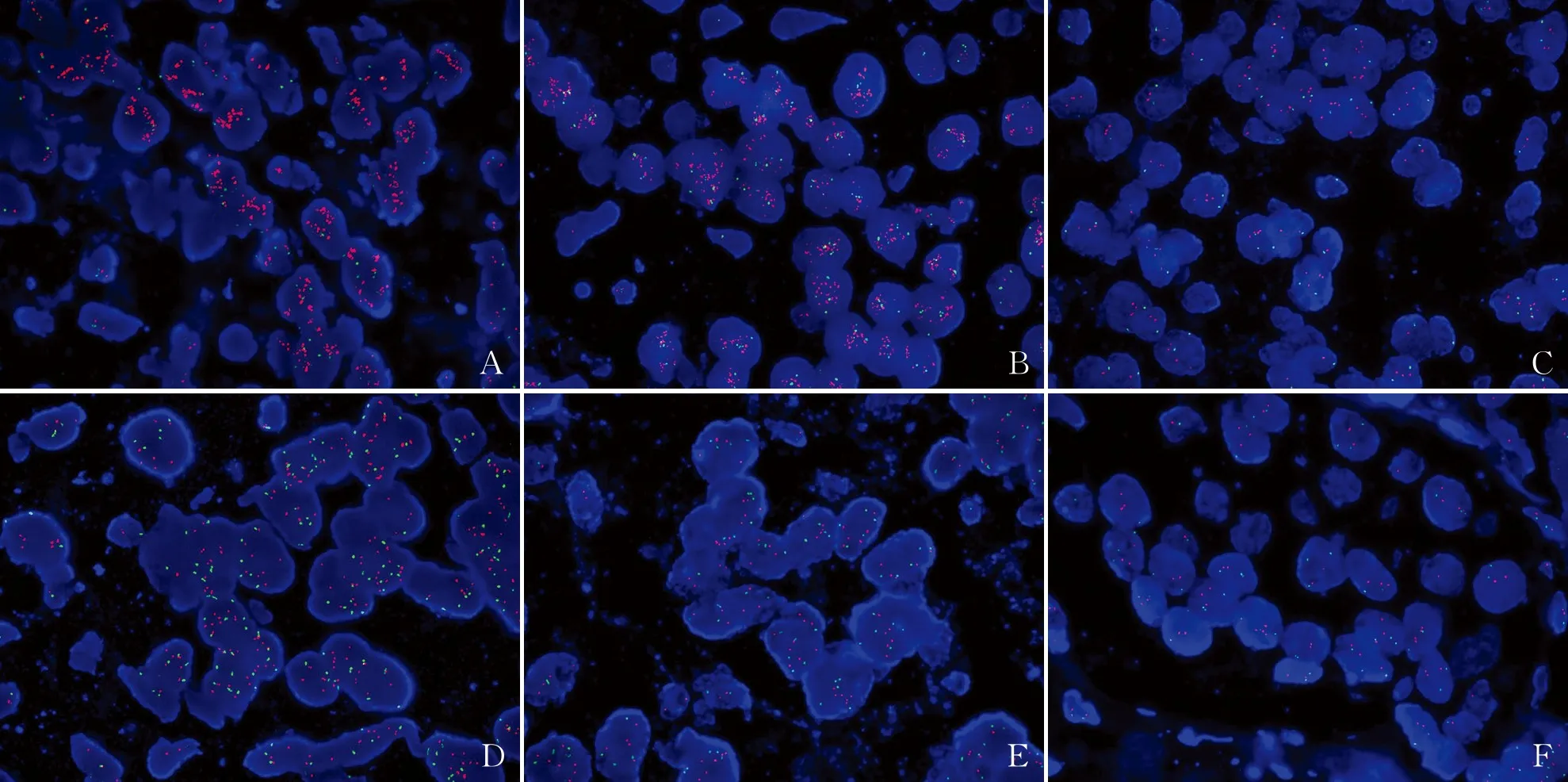
图4 FISH法检测HER-2基因扩增结果(HER-2呈红色,CEP17呈绿色):A.HER-2信号连接成簇;B.HER-2/CEP17比值≥2.0,平均HER-2拷贝数≥4.0信号/细胞;C.HER-2/CEP17比值≥2.0,平均HER-2拷贝数<4.0信号/细胞;D.HER-2/CEP17比值<2.0,平均HER-2拷贝数≥6.0信号/细胞;E.HER-2/CEP17比值<2.0,平均HER-2拷贝数≥4.0且<6.0信号/细胞;F.HER-2/CEP17比值<2.0,平均HER-2拷贝数<4.0信号/细胞
2.4 IHC与FISH法检测HER-2蛋白表达与基因扩增的一致性分析根据旧版指南判读,IHC法检测HER-2蛋白表达0、1+与FISH法检测HER-2基因扩增阴性符合率为88.8%(103/116),IHC法检测HER-2蛋白表达2+与FISH法检测HER-2基因扩增阳性符合率为27.9%(112/402),IHC法检测HER-2蛋白表达3+与FISH法检测HER-2基因扩增阳性符合率为92.8%(167/180)。IHC与FISH法检测HER-2蛋白表达与基因扩增的总一致率为54.7%(382/698),结果存在一致性(Kappa=0.277,P<0.001),且呈正相关(r=0.608,P<0.001,表1)。

表1 旧版指南IHC与FISH法检测HER-2蛋白表达与基因扩增的一致性分析
根据新版指南判读,IHC法检测HER-2蛋白表达0、1+与FISH法检测HER-2基因扩增阴性符合率为97.4%(113/116),IHC法检测HER-2蛋白表达2+与FISH法检测HER-2基因扩增阳性符合率为26.9%(108/402),IHC法检测HER-2蛋白表达3+与FISH法检测HER-2基因扩增阳性符合率为93.3%(168/180)。IHC与FISH法检测HER-2蛋白表达与基因扩增的总一致率为55.7%(389/698),结果存在一致性(Kappa=0.251,P<0.001),且呈正相关(r=0.641,P<0.001,表2)。

表2 新版指南IHC与FISH法检测HER-2蛋白表达与基因扩增的一致性分析
3 讨论
HER-2基因属于EGFR家族成员之一,主要通过与家族其他成员形成异二聚体与配体结合,激活下游信号传导途径,从而促进肿瘤的发生与发展[5-7]。研究发现,在乳腺癌、胃癌、肺癌、结直肠癌中均检测出HER-2基因扩增或HER-2蛋白的过表达,13%~20%的乳腺癌患者HER-2检测阳性,并有部分患者从分子靶向治疗中获益[8-10]。因此,明确HER-2基因状态对乳腺癌患者的个体化治疗尤为重要。
根据新版指南判读,本组FISH法检测HER-2基因扩增阳性检出率为40.0%,IHC法检测HER-2蛋白表达3+检出率为25.8%,IHC法检出率与文献报道基本一致[11-12]。由于FISH法检测参照的判读标准不同,导致文献报道的FISH法检测HER-2基因扩增阳性检出率不一[11-13]。本组通过对698例浸润性乳腺癌患者的IHC和FISH结果以旧版指南再判读发现,新版指南结合了HER-2/CEP17比值、平均HER-2拷贝数和IHC结果综合评估,取消了FISH法检测HER-2基因扩增的不确定结果,使不确定结果由7.2%降至0。FISH法检测HER-2基因扩增阳性由40.7%降至40.0%,FISH法检测HER-2基因扩增阴性由52.1%升至60.0%,为临床提供了更明确的HER-2基因状态。此外在698例中,有56例新旧两版指南判读结果不同,其中6例为HER-2/CEP17比值≥2,平均HER-2拷贝数<4.0信号/细胞,在新版指南中FISH结果为阴性,现有的临床试验数据中,缺乏充分依据显示此部分患者能从靶向治疗中获益[14-15],新版指南判读结果与临床试验数据相符。另有50例为HER-2/CEP17比值<2,平均HER-2拷贝数≥4.0且<6.0信号/细胞,根据新版指南判读,1例结合IHC 3+结果,FISH结果为阳性,49例结合IHC 0、1+、2+结果,FISH结果为阴性。此部分患者能否从靶向治疗中获益目前尚不确定,需要更充分的循证医学依据[16-17]。
本组结果显示,根据新旧两版指南判读,IHC与FISH法检测HER-2蛋白表达与基因扩增结果均存在一致性(Kappa=0.277,P<0.001;Kappa=0.251,P<0.001),且均呈正相关(r=0.608,P<0.001;r=0.641,P<0.001),与文献报道一致[18-19]。经对比分析发现,根据新版指南判读,IHC法检测HER-2 (0、1+)、(3+)与FISH法检测HER-2基因扩增结果的符合率明显增加(97.4%,93.3%),IHC法检测HER-2 (2+)与FISH法检测结果符合率降低(26.9%),IHC与FISH法检测的总一致率略有提高(55.7%)。新版指南中部分结果结合IHC综合判读,提高了IHC与FISH法检测结果的一致性。同时本组结果也进一步验证了指南中提出的,IHC法检测HER-2(0)、(1+)判为阴性,HER-2(3+)判为阳性,HER-2 (2+)一致率较低,需应用FISH法进行HER-2基因扩增状态检测,为临床提供多角度更精准的靶向治疗依据。此外,指南中还提出所有乳腺原发性浸润性癌均应进行HER-2检测,只要能获取肿瘤组织,对复发灶、转移灶也应进行HER-2检测。本组698例均为原发性浸润性乳腺癌,对复发灶、转移灶HER-2检测结果需跟踪患者后续治疗以进一步分析。
此外,在595例计数17号染色体着丝粒CEP17信号中发现平均CEP17拷贝数≥3信号/细胞者有128例(21.5%,28/595)。近年有研究显示整条17号染色体的多体罕见,CEP17的增加并不能代表整条17号染色体多体,部分乳腺癌中存在HER-2基因与着丝粒的共扩增[20]。17号染色体的异常与乳腺癌的预后或靶向治疗是否相关,尚未有明确报道,有待于进一步分析。
综上所述,新旧两版指南IHC与FISH法检测HER-2蛋白表达与基因扩增结果均存在一致性,且两者均呈正相关。新版指南结合HER-2/CEP17比值、平均HER-2拷贝数和IHC结果综合评估,取消了FISH法检测HER-2基因扩增的不确定结果,使其阴性率有所增加,为临床提供了更完善的靶向治疗依据。
