基于CBCT 的宫颈癌放疗摆位误差及不同配准方式分析
2021-06-17许新明牛书雷高灵灵
许新明,张 超,王 陶,张 坤,牛书雷,高灵灵,李 腾,杨 健
(沧州市人民医院放疗中心,河北 沧州 061000)
放射治疗是宫颈癌的主要治疗方法之一,宫颈癌的常规放疗毒副反应较大,包括骨髓抑制、放射性直肠炎、放射性膀胱炎等[1],图像引导放射治疗(image-guided radiotherapy,IGRT)可较好地纠正摆位误差,从而降低放射性毒副反应的发生[2]。IGRT 的图像配准方式包括骨性配准、灰度配准、银夹配准、手动配准等。宫颈癌的图像配准方式主要是前两种,而各放疗中心选择配准方式不尽相同[3,4]。本研究通过采集13 例宫颈癌术后患者放疗期间的锥形束CT(cone beam computed tomography,CBCT)数据,对摆位误差进行统计分析,进一步探讨不同配准方式的差异。
1 资料与方法
1.1 一般资料 选取2019 年4 月~12 月沧州市人民医院放疗中心收治的13 例宫颈癌术后放疗患者,年龄45~68 岁,平均年龄57.69 岁,体重49~98 kg,平均体重67.69 kg,身高150~167 cm,平均身高156.62 cm。ⅠB 期3 例,ⅡA 期9 例,ⅡB 期1 例。本研究经医院伦理委员会审核批准,所有受试者均知情并签署知情同意书。
1.2 纳入及排除标准 纳入标准:①东部肿瘤协作组(eastern cooperative oncology group,ECOG)体力状况评分0~2 分;②宫颈癌子宫+双侧附件切除术后;③年龄18~70 岁。排除标准:①Ⅲ~Ⅳ度骨髓抑制;②既往溃疡性结肠炎、原发膀胱炎;③既往接受直肠、膀胱手术;④碘造影剂过敏;⑤远处转移。
1.3 方法
1.3.1 定位方法 行盆腔CT 定位前及每次治疗前1 h排空尿液,饮用500 ml 水充盈膀胱[5]。每日固定时间排便,以实现治疗重复性。定位时患者仰卧位,头垫B/C 枕,双手抱肘于额前,采用体部低温热塑膜联合体板(华光普泰,HYX-UTS-CM)固定。应用CT 模拟定位机(荷兰飞利浦,Brilliance 16 排螺旋CT)行模拟定位增强扫描,扫描范围为腰1 椎体上缘到坐骨结节下5 cm,层厚3 mm,层间距3 mm。扫描图像由MOSAIQ 网络传输至Monaco(瑞典医科达,V5.11.03)治疗计划系统,进行靶区勾画和治疗计划设计。
1.3.2 CBCT 扫描 治疗前利用加速器机载XVI 系统实施kV 级CBCT 扫描,扫描条件:准直器:M20,滤线器:F1,顺时针扫描-180°~180°,180°/min,扫描条件120 Kv,1056 mAs,剂量率600 Mu/min,扫描帧数5.5 Hz,图像重建矩阵数1024×1024,辐射剂量为22 mGy。所有患者每周进行1 次CBCT 扫描,其中12 例患者各行5 次有效CBCT 图像扫描,1例患者行4 次有效CBCT 图像扫描,共获取64 幅CBCT 图像。
1.3.3 CBCT 图像配准 采集CBCT 图像与定位CT图像配准,配准范围:全体廓范围,即CBCT 扫描的整体图像范围[6,7]。配准方法:采取骨性配准及灰度配准两种方法分别进行图像配准。配准参考点:计划等中心点。配准后获得6 维治疗床x(左右)、y(头脚)、z(前后)轴及分别以x、y、z 轴旋转形成相应的Rx、Ry、Rz旋转方向上的摆位误差数据,平移坐标轴分别以左、头、前为正,旋转坐标轴以顺时针方向为正,反之为负。
1.4 统计学方法 采用SPSS 24.0 软件进行数据分析,计量资料以()表示,不同配准方式摆位误差数据比较采用两个配对样本的Wilcoxon 符号秩和检验,不同坐标轴摆位误差比较采用多个独立样本的秩和检验,P<0.05 为差异有统计学意义。
2 结果
2.1 骨性配准 考虑方向时在x、y、z 轴平移误差分别为(0.07±0.29)cm、(-0.26±0.75)cm、(-0.01±0.21)cm,Rx、Ry、Rz轴旋转误差分别为(0.47±1.61)°、(-0.44±1.09)°、(-0.38±1.53)°,不考虑方向时在x、y、z 轴平移误差分别为(0.25±0.17)cm、(0.64±0.46)cm、(0.15±0.15)cm,Rx、Ry、Rz轴旋转误差分别为(1.17±1.19)°、(0.89±0.76)°、(1.20±1.02)°,见图1。x、y、z 轴上0.3 cm以内的摆位误差分别占70.31%、35.94%、93.75%,Rx、Ry、Rz轴上3°以内的摆位误差分别占93.75%、96.88%、92.19%,见图2。平移误差:y 轴>x 轴>z 轴,差异有统计学意义(Z=-4.606、3.139,P<0.05)。
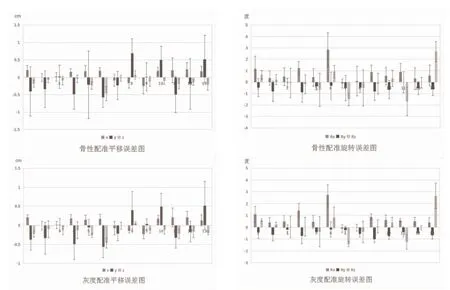
图1 宫颈癌术后患者摆位误差图
2.2 灰度配准 考虑方向时在x、y、z 轴平移误差分别为(0.07±0.19)cm、(-0.09±0.46)cm、(-0.16±0.17)cm,Rx、Ry、Rz轴旋转误差分别为(0.73±0.83)°、(-0.52±0.43)°、(0.07±1.12)°,不考虑方向时在x、y、z 轴平移误差分别为(0.17±0.11)cm、(0.35±0.31)cm、(0.20±0.13)cm,Rx、Ry、Rz轴旋转误差分别为(0.78±0.78)°、(0.59±0.33)°、(0.82±0.76)°,见图1。x、y、z 轴上0.3 cm以内的摆位误差分别占92.19%、73.44%、96.88%,Rx、Ry、Rz轴上3°以内的摆位误差分别占95.31%、100.00%、98.44%,见图2。平移误差:y 轴>x 轴,差异有统计学意义(Z=-3.333,P<0.05)。
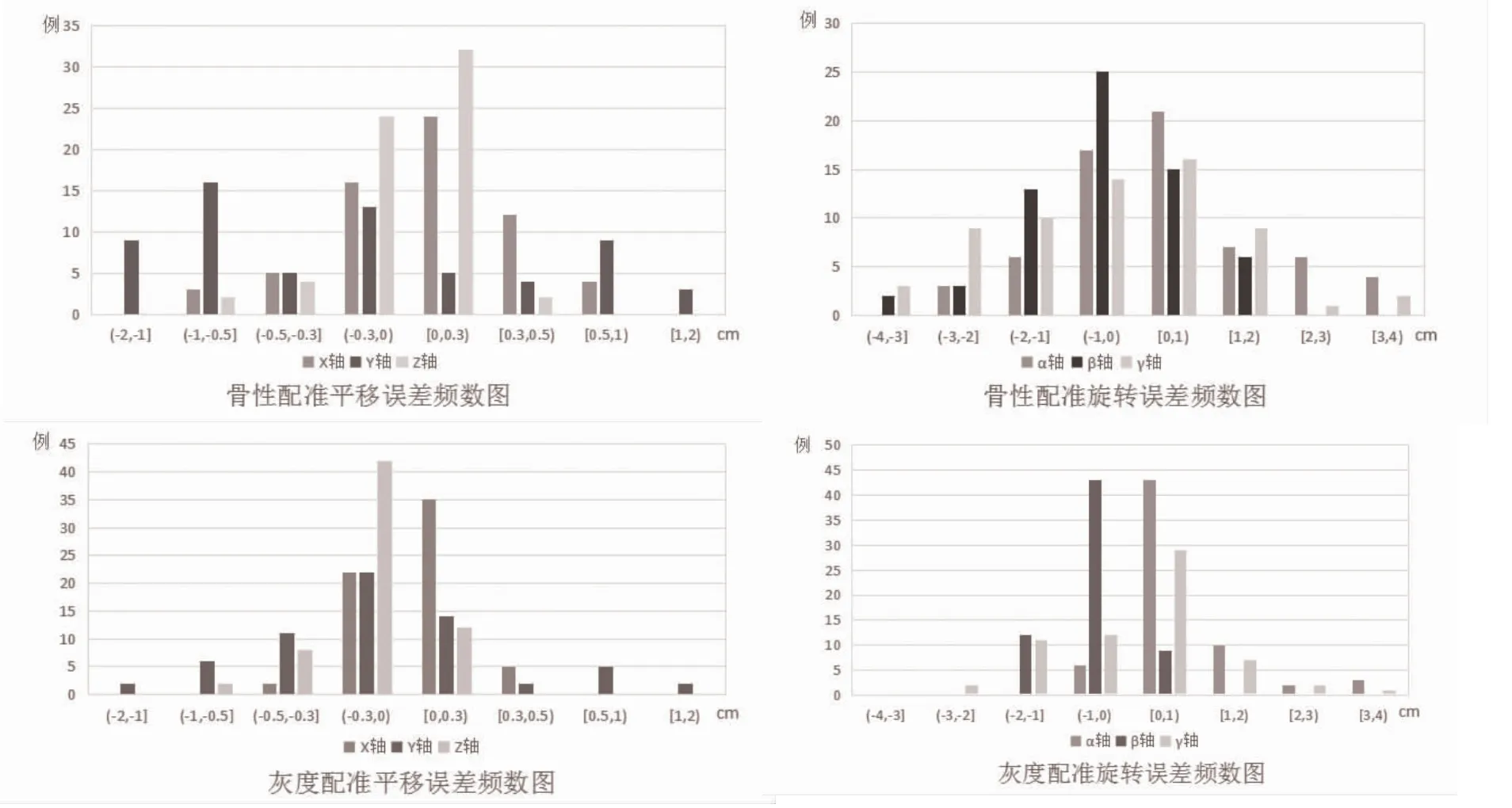
图2 宫颈癌术后患者摆位误差频数图
2.3 宫颈癌术后患者CBCT 图像不同配准方式摆位误差比较 扫描获取摆位误差数据不符合正态分布,行非参数检验,在x、y、z 轴及Rx、Ry、Rz轴上骨性配准与灰度配准比较,差异有统计学意义(P<0.05),见表1。
表1 宫颈癌术后患者CBCT 图像不同配准方式摆位误差比较()
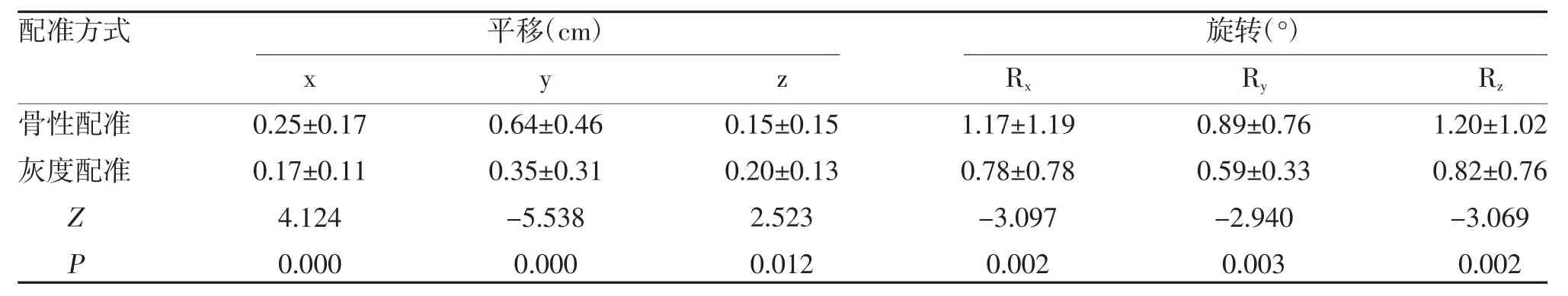
表1 宫颈癌术后患者CBCT 图像不同配准方式摆位误差比较()
3 讨论
患者在放疗过程中存在着治疗体位与定位体位在三维空间坐标系中的平移和旋转摆位误差[8]。摆位误差分为系统误差和随机误差,系统误差为实际治疗和模拟定位间的差异,体现了患者治疗过程中分次间治疗位置重复性差异;随机误差随机误差多由患者位置及器官运动变化引起,体现了分次内治疗时重复性差异[9,10]。与此对应,造成摆位误差因素也可归纳为两类,一类为设备因素,即放疗设备和材料造成的误差,相当于系统误差;另一类为人为因素,即患者和技术员治疗摆位所造成的误差,相当于随机误差[5,11]。
IGRT 技术可实现摆位误差的在线或离线校正,图像配准是IGRT 的关键技术环节之一,图像配准技术的精确性直接关系到位置校准的可靠性,从而影响临床治疗疗效以及危及器官的受量[12,13]。许峰等[14]利用IGRT 研究不同部位肿瘤的摆位误差,头颈部肿瘤均采用骨性自动匹配,胸部肿瘤采用软组织自动匹配,腹盆部匹配采用骨性或软组织匹配,数据显示摆位误差在x、y、z 方向分别为头颈部(-0.3±1.5)、(-0.3±1.6)、(0±1.3)mm,胸部(-0.6±2.9)、(-0.2±5.6)、(0.7±3.2)mm,腹盆部(-0.8±2.1)、(-0.3±5.9)、(0.1±2.6)mm,显示不同部位肿瘤的放疗随机误差在头脚方向均大于其他方向。本研究显示头脚方向摆位误差为(-0.26±0.75)cm(骨性配准),而0.3 cm以上的摆位误差占比高达64.06%,高于其他方向,与文献报道类似。可能与患者左右方向由体膜固定,前后方向受治疗床限制,而头脚方向则无刚性限制等因素有关。
Astreinidou E 等[15]发现1°的旋转误差对原发性肿瘤的覆盖无影响,但对选择性淋巴结的覆盖有轻微影响。Fu W 等[16]研究显示旋转角度误差即使达到3°,等效均匀剂量和肿瘤控制率的变化仍在2%以内,对诸如直肠和膀胱等敏感结构的影响也可以忽略不计。王占宇等[17]研究显示头颈部肿瘤3 mm 和3°内单一方向摆位误差对靶区和危及器官影响有限。本研究不同配准方式得出旋转误差大多数在2°以内,Rx和Rz方向误差稍大,平均为1.2°左右,故对靶区及危及器官的影响不大。从数据中可以看出,第6 例患者Rx轴和第13 例患者Rz轴向分次间摆位误差均高于其他患者,经进一步分析,考虑原因为行CT 定位时因患者不熟悉体位或情绪紧张所致的摆位误差较大,而后续治疗时熟悉了放疗过程,体位更加放松自如,与技术员配合更加默契。也提示临床医师校位时应注意观察,必要时可选择重新定位以减小摆位误差。
图像配准的精度受多种因素的影响,主要包括所配准图像的质量、不同配准算法和不同配准范围及方式等[6,7]。既往多项研究表明[6,18,19],乳腺、肺、肝部肿瘤配准多以灰度配准为主,而头颈部肿瘤则以骨性配准为主[14,20],原因可能与肿瘤周围感兴趣区的组织类型有关,乳腺、肺、肝感兴趣区多为软组织器官且活动度较大,头颈部肿瘤的感兴趣区主要为骨骼属刚性结构,位置相对固定,因此采用不同配准参考方式。对于宫颈癌的放射治疗而言,采用骨性配准和灰度配准的都有[3,4]。从本研究可以看出,宫颈癌术后放射治疗采用骨性配准,摆位误差差异较大,而采用灰度配准得出的摆位误差则更多集中在3 mm 及1°以内,数据差异较小。统计学分析表明,两者之间的差异有统计学意义,表明宫颈癌术后放疗骨性配准与灰度配准之间差异不容忽视。考虑与盆腔特殊解剖结构及靶区设置有关,照射靶区以宫旁、阴道残端及盆腔淋巴引流区的预防照射为主,其解剖位置基本与盆腔诸骨毗邻,照射范围与位置相对固定;而危及器官则以膀胱、直肠等软组织器官为主,放疗分次间解剖位置偏差可能较大。宫颈癌术后放疗建议采用骨性配准,以达到更好的靶区覆盖和精准性。而灰度配准可能会使膀胱、直肠等危及器官得到更好的保护,但是会造成靶区漏照。
综上所述,宫颈癌放疗患者由于放疗范围大,解剖结构复杂,摆位误差相对较大。采用IGRT 技术可有效纠正摆位误差,提高放疗精度及治疗效果。宫颈癌术后放疗建议采用以骨性配准方法,以期获得更为准确的摆位误差。
