光学相干断层扫描血管成像扫描信号强度对视盘周围血管密度的影响
2021-06-15周立军沈沛阳何宇深曹艺冼碧琨孔祥斌
周立军,沈沛阳,何宇深,曹艺,冼碧琨,孔祥斌
(南方医科大学附属佛山医院眼科,广东 佛山 528000)
视盘是视神经的重要组成部分,其丰富的血流供应是维持正常功能的重要保障[1-2]。有研究[3-4]发现在视神经相关的疾病中视盘血流会发生改变,如在早期青光眼的患者中发现这类患者的视盘血流会出现显著的降低,因此视盘血流常常被认为是管理和检测视神经疾病的一个重要标志物[5]。既往在检查视盘血流时,常常使用超声多普勒或者眼底荧光血管造影等,但一直面临不能准确定量或有创性等不足[6-7]。最近在相干断层扫描成像(optical coherence tomography,OCT)基础上发展起来的光学相干断层扫描血管成像(optical coherence tomography angiography,OCTA)技术由于具有检查快速无创,且能进行血流定量,可以实现血流的可视化等优点,目前已经用于视网膜和视盘血流的检查[8-9]。
在使用OCTA检查过程中,研究者[10-11]发现视网膜或视盘血流密度不仅与疾病的种类、年龄和眼轴等有关,也与OCTA扫描信号强度(scanning signal intensity,SSI)有关[12-14]。SSI是一个关于成像质量的重要参数,在血流密度的临床应用或研究中,为保证图片的质量,常常要求OCTA-SSI要至少达到一定的强度才能视为有效扫描(如蔡司OCTA的SSI为0~10,一般要求SSI至少为7)[14],但对于这些符合质量要求的OCTA图像,SSI是否仍然会对视网膜或视盘血流产生常影响以及可能产生什么样的影响,目前少有报道。
1 对象与方法
1.1 对象
本研究为2019年5月至2020年4月在佛山市第二人民医院进行的单中心横断面研究。研究方案已获得佛山市第二人民医院医学伦理委员会的批准(KJ20190012),并在中国临床研究网进行了注册(ChiCTR1900024921),本研究遵循赫尔辛基宣言,受试者在接受检查前均签署知情同意书。
参与研究的受试者来源于眼科门诊,体验中心及社区筛查的健康者。入组标准:最佳矫正视力≥0.8,眼压<21 mmHg(1 mmHg=0.133 kPa),裂隙灯及眼底检查均正常。排除标准:既往眼部手术史或外伤史;明显的屈光介质浑浊而影响成像;高度近视(球镜大于-6.00 D或者眼轴大于26 mm);患有高血压、糖尿病或其他全身疾病。
1.2 方法
受试者均接受了视力、眼压、裂隙灯、眼轴和OCTA检查。最佳矫正视力使用国际标准视力表检查,眼压采用自动眼压计连续测量3次取其平均值。使用眼球生物测量仪Lenstar测量眼轴。用蔡司OCT(Cirrus 5000 HD-OCT)的200×200扫描获取视盘面积,同时记录受试者的身高、体重和血压指标,并计算BMI。
OCTA检查:使用蔡司OCTA对所有受试者进行视盘扫描检查。蔡司OCTA使用波长为840 nm光源,每秒可进行68 000次A扫描。在水平和垂直方向上每个B扫描含有350个A扫描,并使用机器所自带软件利用光学微血管造影(optical micro angiography complex,OMAG)算法自动获取相应区域和层次的血管密度[15-16],其中血管密度定义为单位面积的血管长度(一定区域血管长度的总和/一定区域的面积)。为获得视盘的血管密度,将以视盘为中心的6 mm×6 mm扫描模式与实时眼动追踪系统配合使用,测量厚度为从内界膜到内丛状层的距离。蔡司OCTA仪器自带的早期糖尿病视网膜病变治疗研究(early treatment diabetic retinopathy study,ETDRS)图表将视盘血管密度自动分为中心环、内环、外环和整圆(图1A)。我们通过计算(整圆的血管长度-中心圆的血管长度)/(整圆的面积-中心圆的面积)得到视盘周围血管密度(图1B)。根据既往研究的结果[12],为保证图片质量,我们将OCTA-SSI≥7的OCTA图像纳入研究。

图1 视盘6 mm×6 mm OCTA 扫描成像Figure 1 Optical coherence tomography angiography 6 mm×6 mm scan image on the optic disc
1.3 统计学处理
2 结果
2.1 人群一般资料
本研究最终纳入符合条件的186名受试者共359眼,其中男85例(45.70%),女101例(54.30%),年龄18~84(47.86±17.86)岁,359眼的平均图像SSI为7~10(9.07±1.0),视盘周围血管密度为5.36~19.88 (17.75±1.99) mm-1。不同变量的临床特征总结见表1。
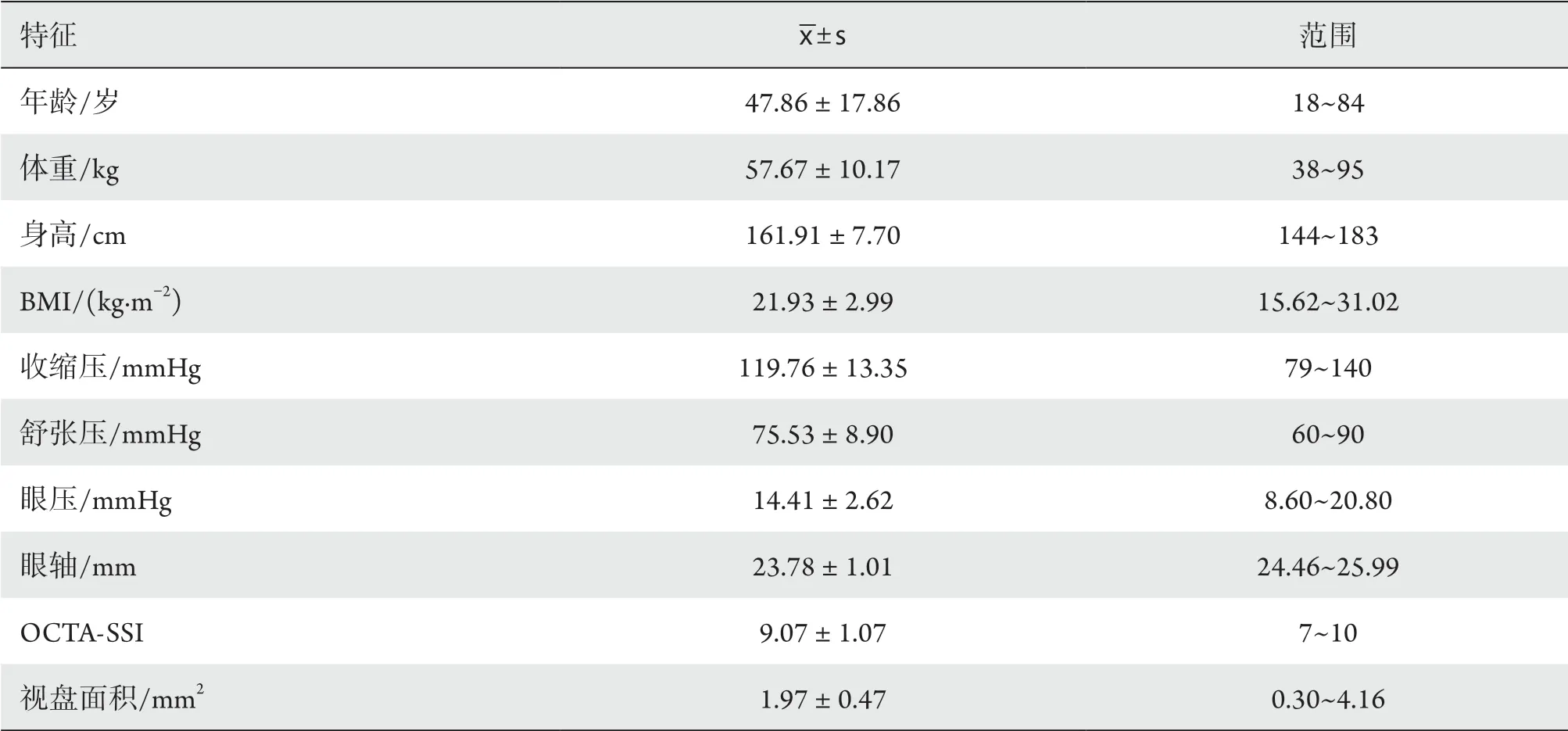
表1 入组人群的一般人口学特征Table 1 Demographic and clinical characteristics of study participants
2.2 单因素分析结果
为研究不同因素对视盘周围血管密度的影响,首先利用广义估计方程进行单因素分析,结果显示:视盘周围血管密度与SSI呈显著正相关,SSI每提升1个信号强度,视盘周围血管密度会相应增加1.0240 mm-1(P<0.001);与眼轴呈负相关,眼轴为增加1 mm,视盘周围血管密度会降低0.5120 mm-1(P<0.001)。视盘周围血管密度与年龄、性别、身高、体重、BMI及血压无显著相关性(P>0.1,表2)。

表2 视盘周围血管相关因素的单因素分析Table 2 Univariate analysis of the associated factors of peripapillary vessel density
2.3 多因素分析结果
将性别、年龄、视盘面积及在单因素分析中P>0.2的变量一起纳入广义估计方程进行多因素分析,结果显示:在校正年龄和性别后,视盘周围血管密度依然与SSI呈显著正相关(β=0.9721,P<0.001),与眼轴(β=-0.4157,P<0.001)和视盘面积(β=-0.3239,P<0.001)均呈显著负相关 (表3)。

表3 视盘周围血管相关因素的多因素分析Table 2 Multivariate analysis of the associated factors of peripapillary vessel density
3 讨论
本研究结果显示:OCTA-SSI与视盘周围血管密度呈显著正相关,在校正年龄、性别、眼轴及视盘面积后,每增加1个信号强度,可以使视盘周围血管密度增加0.9721 mm-1。提示即使纳入了符合条件的OCTA图像(蔡司OCTA通常要求SSI>7),SSI依然会显著影响视盘周围的血管密度,因此在评估视盘周围血管密度时,应该考虑SSI的影响。
视盘周围血管密度不仅与疾病相关,而且也有OCTA图片质量密切相关[17-18]。OCTA扫描的图片质量与患者的合作程度、眼底健康情况及屈光状态等多种因素相关,为保证OCTA的图片质量,常常要求达到一定信号强度[14]。如蔡司OCTA要求SSI>6 (0~10),海德堡OCTA要求SSI>15(0~40),而RTVue OCTA要求SSI>35 (0~100)[19]。Lim等[13]利用蔡司OCTA 检测了259名患者的259眼视盘血管情况,通过6 mm×6 mm扫描得到了扫描信号≥7的图像,根据OCTA扫描信号强度的大小分为SSI-7、SSI-8、SSI-9和SSI-10四组,比较了不同SSI组的视盘血管密度,结果显示:SSI是影响视盘周围血管的显著因素,尽管SSI-9与SSI-10没有明显差异。虽然没有将SSI分组,但是本研究通过单因素和多因素分析均证实SSI与视盘周围血管密度显著相关,这个结果与Lim等[13]的结论一致。另外,本研究也显示眼轴长度与视盘周围血管密度显著负相关,这可能与视盘周围的神经纤维层的厚度有关。眼轴越长,视盘周围纤维层的厚度就越薄,所需的供养就越少[10,20]。
理论上,随着年龄的增加,黄斑区的血管可能为部分萎缩退化,黄斑中心凹无血管区会扩大,因此黄斑区的血管密度应该会降低,视盘的血管密度也可能存在类似的变化。但目前关于年龄与视盘区血管的关系实际上有不同的报道。Jo等[11]的研究显示:随着年龄的增加,视盘区的血管密度会降低。但也有研究[21]认为视盘血管密度与年龄无关,本研究也得出了类似的结论。造成这种结果的差异,可能与研究设计、入组人群及检测仪器的算法不同有关。
本研究也存在一些不足之处:尽管排除了高度近视的受试者,但纳入了部分患有近视的参与者。有研究[22]显示:近视可能会对眼底采集的图片产生放大效应,因此需要校正,本研究并没有校正这种放大作用,对于近视人群,本研究可能会低估视盘周围血管密度。这种放大效应需要在以后的研究中进一步进行评估。另外,因为视盘有较为粗大的血管出入,会产生投影[23],本研究也没有去掉大血管进行再评估,这可能对研究结果产生相应的影响。最后,本研究仅纳入了成人受试者,而对于儿童是否也有类似的结果,需要在以后的工作中对儿童人群进一步探讨。
综上,本研究在校正了双眼数据的相关性及年龄和性别的影响之后,除了眼轴会显著影响视盘周围的血管密度外,即使纳入OCTA-SSI大于7的图像,SSI依然与视盘周围血管呈显著正相关,因此在以后的临床和科研工作中,除了考虑眼轴对视盘周围的血管密度产生的影响外,还需要考虑OCTA-SSI的影响。
