基于中药液、固体物料指标成分含量相关性的膜工艺评估方法创新研究
——以杜仲叶水提液为例
2021-06-11钟文蔚郑东阳邹洪荟卓泽伟郭立玮
钟文蔚 ,郑东阳 ,邹洪荟 ,卓泽伟 ,郭立玮
1.广州中国科学院先进技术研究所 中药与天然产物研发部,广东 广州 511458
2.广州南沙资讯科技园有限公司博士后科研工作站,广东 广州 511458
3.广东药科大学,广东 广州 511436
4.广东医科大学,广东 东莞 524023
5.南京中医药大学 植物药深加工工程研究中心,江苏 南京 210023
6.中药提取分离过程现代化国家工程研究中心,广东 广州 510240
杜仲叶是杜仲科植物杜仲Eucommia ulmoidesOliv.的干燥叶,具有降血压、调血脂、降血糖、抗炎、抗病毒、抗疲劳、强筋健骨、抗衰老的功效。近年来,随着绿色制造观念在各行各业的大力推广,杜仲叶提取物作为大健康产品,如绿色食品与饲料添加剂的应用研究日益广泛。文献报道杜仲叶的水提取、精制过程,大多采用醇沉的工艺。近年来,膜集成工艺替代水醇法,已成为中药水提液澄清、精制工序的重要升级换代技术,有力地促进了中药绿色制造的进程[1-6]。
但如何将不同孔径的膜进行优化组合,以及各级膜截留液的“顶洗”(在超滤过程中加入纯溶剂[1],通常为水,以增加总渗透量,带走残留在截留液里的目标成分,达到提高回收率的目的)程序设计合理性,仍要由多次“试错”才能决定,其主要评估因素是精制过程最终产物干浸膏(固含物)中的中药指标成分含量[7]。能否通过对膜过程液态物料中间体指标性成分的含量检测结果,推测、判断其最终产物干浸膏(固含物)的指标性成分含量,从而确认膜工艺流程设计的科学与合理性,成为中药澄清精制膜工艺流程设计的技术瓶颈。
本实验旨在通过探索液体物料与其干浸膏(固含物)中指标性成分的相关性模型,为膜澄清工艺过程液体物料中间体提供估算最终固体成品成分含量方法,建立以膜工艺过程液体物料中间体指标性成分含量直接评估膜澄清、精制工艺优化与否的创新模式,为实现中药膜过程智能控制提供技术支撑。
1 仪器与材料
200 nm 陶瓷膜(ZrO2),江苏久吾高科技股份有限公司;截留相对分子质量(Mw)10 000 膜(PES),厦门国初科技有限公司;截留Mw3500 超滤膜(GK1812),美国通用电气公司;Waters 2996 高效液相色谱仪,美国沃特世公司;安捷伦Eclipse Plus C18色谱柱(100 mm×4.6 mm,3.5 μm),美国安捷伦科技公司;MV-1800 紫外分光光度计,上海美谱达仪器有限公司;JW-t-0.1B-316 陶瓷膜实验设备,江苏久吾高科技股份有限公司;WTM-0806D 平板膜评价仪,杭州沃腾膜工程有限公司。
杜仲叶,产于江西井冈山,经本课题组郭立玮教授鉴定,为杜仲科杜仲属植物杜仲Eucommia ulmoidesOliv.的干燥叶[8],干燥至恒定质量后磨成粉末后过80 目筛网备用。对照品绿原酸(批号C109403,质量分数≥98%)、芦丁(批号R189033,质量分数≥95%)、没食子酸(批号G131992,质量分数≥99%)、葡萄糖(批号G116300,质量分数≥98%)购于上海阿拉丁生化科技股份有限公司;对照品牛血清白蛋白(批号A80132,质量分数96%)购于上海麦克林生化科技有限公司。甲醇、磷酸为色谱纯,水为超纯水其余试剂均为分析纯。
2 方法
2.1 杜仲叶提取液制备
本课题组前期对杜仲叶的水提过程进行了正交实验设计和验证,因此本实验使用的提取方法按前期课题组优选的提取方法进行提取。称粉碎的杜仲叶1000 g 至5 L 提取罐,70 ℃加10 倍量纯水提取1 h,滤过后取滤渣再加10 倍量纯水70 ℃提取1 h,滤过,合并2 次滤液,得杜仲叶水提液12 L(W1)。测量其指标性物质含量。
2.2 陶瓷膜微滤
将W1 经200 nm 陶瓷膜微滤澄清,测量其透过液(W2)中的指标性物质含量。
2.3 微滤澄清后透过液进行超滤
将200 nm 陶瓷膜澄清后的W2 分别过截留Mw10 000、3500 超滤膜,得到透过液(W3、W4),分别测量透过液中指标性物质含量。杜仲叶水提液澄清、精制的膜集成实验流程设计图见图1。

图1 杜仲叶水提液澄清、精制的膜集成实验流程设计图Fig.1 Process flow diagram of clarification and refinement of aqueous extracts of Eucommiae Folium via integrated membrane process
2.4 水提液中相关物质含量检测方法
绿原酸、蛋白质、固含量测定依据《中国药典》2020年版[8],总黄酮含量测定采用NaNO2-Al(NO3)3- NaOH 显色法[9],总多酚含量测定采用福林酚显色法[10],杜仲粗多糖含量测定采用硫酸-苯酚法[11]。所有数据取2 次试验数据平均值。
2.5 固含物成分的检测方法
精密称取1 g 固体粉末,用水溶解后定容至10 mL,测量其相应物质含量,可得到1 g 固含物中成分含量。
3 结果和讨论
3.1 杜仲叶水提液陶瓷微滤和超滤处理后相关化学物质含量变化对比
杜仲叶水提液陶瓷微滤和超滤处理后相关化学物质含量变化对比见表1。除了《中国药典》2020年版[8]中的指标性成分绿原酸外,杜仲多糖[12]、杜仲黄酮和多酚[13]也属于杜仲叶中含量较高的有效成分,具有抗氧化等功效。表1 中绿原酸为指标成分,以膜过程截留率低为优;总黄酮和粗多糖亦为有效物质,以膜过程截留率低为优;总蛋白为大分子杂质,宜去除,以膜过程截留率高为优。
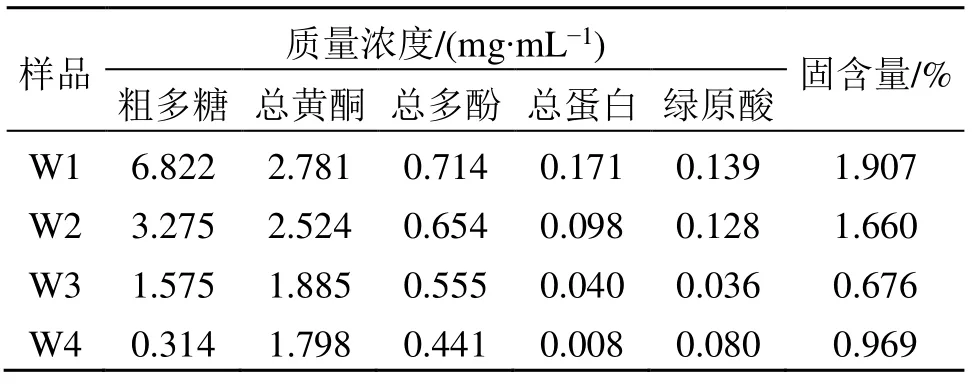
表1 杜仲叶水提液微滤和超滤处理前后相关化学物质含量变化Table 1 Comparison of chemical compositions in aqueous extracts of Eucommiae Folium
由表1 可知,经200 nm 陶瓷膜(W2)、200 nm陶瓷膜+Mw10 000 超滤膜(W3)、200 nm 陶瓷膜+Mw3500 超滤膜(W4)3 种不同膜过程处理后,杜仲水提液的总蛋白大分子物质虽然被不同程度去除,但其中指标成分绿原酸、粗多糖及总黄酮、总多酚等有效物质的含量也呈现下降的趋势。现有研究只针对水提液中物质的截留率,但未有报道指导如何科学、合理地评估膜过程对杜仲叶水提液澄清、精制作用。
3.2 不同膜过程处理后提取液固含物中相关成分的分析
对于杜仲水提液原液及经过不同膜集成过程后的各透过液进行浓缩、干燥,并测定固体中指标性成分物质含量,分别标注为G1(水提液原液浓缩干燥)、G2(200 nm 陶瓷膜透过液浓缩干燥)、G3(200 nm 陶瓷膜+Mw10 000 超滤膜透过液浓缩干燥)、G4(200 nm 陶瓷膜+Mw3500 超滤膜透过液浓缩干燥)。按照上述“2.4”项方法,可得到干燥固体所含相关成分数据(表2)。其中,绿原酸可作为杜仲叶水提液的指标性药效物质,而蛋白质可作为必须通过澄清精制工艺去除的大分子物质的代表。
由表2 可知,样品G4,大分子物质的代表蛋白质的含量最低,仅为0.85 mg/g,而指标性成分的代表绿原酸的含量最高,高达8.88 mg/g,显著高于G1、G2、G3。说明200 nm 陶瓷膜+Mw3500 超滤膜工艺的澄清、精制效果优于其他的膜工艺。

表2 干燥固体的成分分析Table 2 Chemical compositions of dried solids
该实验结果虽然对表1 的结果起到佐证、确认的作用,但毕竟过程比较繁杂,直到实验研究最后阶段,才能获取膜工艺过程液体物料干燥后固含物中指标性成分的含量。可借助“化学工程”领域常用的物料衡算原理,探寻更为简洁的方法。
3.3 基于“物料衡算”原理的液、固体物料指标成分含量相关性研究
在中药制药过程中,大部分物料(制剂)最终会被浓缩、干燥成固体形态(即干浸膏或喷干粉)。根据“物料衡算”的一般原理,以下公式(1)、(2)成立。

式(1)与(2)的定义不同,由式(2)可知,总固体质量由指标成分物质与其他固体物质共同组成。而式(1)中,分母仅为液体物料的质量,从而水提液中某指标成分的质量浓度并不等同于该指标成分在干浸膏(固体中间体)中的质量分数。例如,实验中发现,尽管在过超滤膜后绿原酸在水提液中含量有所减少(表1 中W4 小于W2),但也同时发现在过完Mw3500 超滤膜的干浸膏中绿原酸含量却有所增加(表2 中G4 大于G2)。其结果是,经200 nm 陶瓷膜+Mw3500 超滤膜处理后,指标成分绿原酸在澄清、精制工艺最终产物干浸膏的纯度提高了。就基于膜过程的中药制药分离技术而言,液体物料贯穿工艺流程主体,如何遵照“物料衡算”原理,寻找澄清、精制工艺最终产物干浸膏中指标成分含量与流程关键工序液体中间体指标成分含量的相关性,对于膜集成工艺路线设计事关重大,是中药膜过程智能化亟需解决的生产实际问题。
文献报道[14],经对118 种《中国药典》2020年版中药单方、复方的水提液(按药典方法配制)的固含量测试实验,发现中药提取液原液固含量普遍远小于溶剂质量(表3)。

表3 118 种中药单方、复方水提液固含率测试结果Table 3 Solid contents of 118 types aqueous TCM extracts
因此,作如下理论推导:根据表3 的数据,可认为,对于中药提取液原液而言,其总固体质量远小于水(溶剂)质量,因此公式(3)成立。

由式(5),可利用某指标性成分在水提液中的浓度与固含率,简便得出固体干浸膏(固体制剂)的指标性成分质量。不必再等到全部工艺过程结束,即可以由膜工艺中间液体物料中某指标成分的含量判断该工艺设计是否可以达到预期结果。
为验证本方法的科学性与可行性,开展了相关实验。由表4、5 可知,无论是绿原酸,还是蛋白质,它们在同一工艺过程节点干浸膏中含量的实测值与估算值都极为接近。
根据上述方法,可由表1 中指标成分绿原酸在液体物料中的含量、固含量,推导出3 种膜工艺过程最终产物干浸膏中绿原酸的含量。
由上述计算结果可知,G4 中绿原酸的含量最高,即可认为200 nm 陶瓷膜+Mw3500 超滤膜是本实验的最佳膜集成工艺。
作为实际生产中对膜澄清、精制工艺科学、合理性判断的一种简便方法,式(5)虽有一定局限性,但作为解决复杂体系膜工程化问题的手段,则表现出较大的灵活性和实用性。
4 结语
中药制药工艺是影响中药质量最为关键的因素之一,本研究创造性地建立液、固体物料指标成分含量相关性模型,并将其对中药制药中间体最终产物质量推测的结果,作为工艺优选的依据,为在实际中药生产领域实现“前瞻性”设计提供了技术支撑。本研究针对“过程的开发及优化”,引进“化工过程控制”原理:对于复杂的化工过程,不能满足于在现有装置上通过测试获得所需的对象动态特性知识,更重要的是,在对象处于设计阶段,就能利用计算方法预估其特性,以改变“黑匣”无知状态,指导工艺设计中的原理性设计。据此所开展的面向中药澄清精制膜工艺过程评估模式创新,不仅为中药制药学与现代科学全面兼容提供了新方法,而且也为构建“中药制药分离过程工程原理”理论体系提供了新视野。
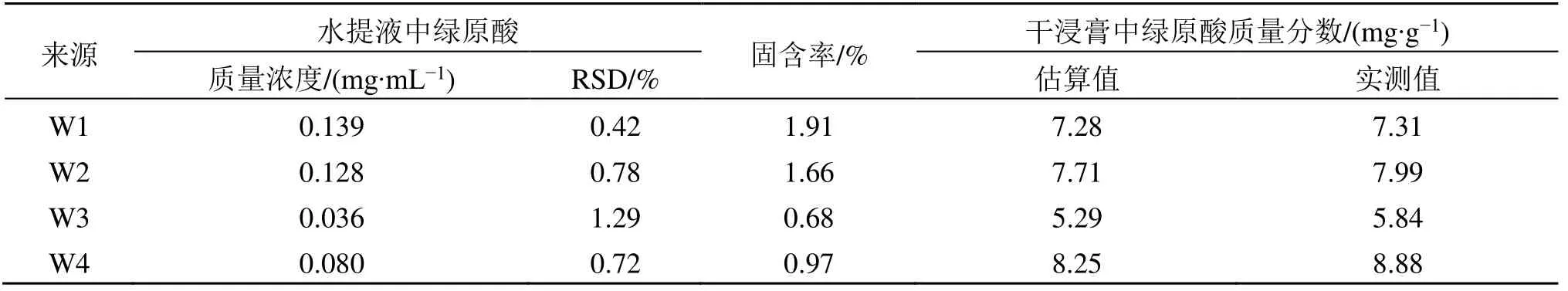
表4 杜仲叶水提液澄清、精制膜集成工艺过程中绿原酸的物料衡算Table 4 Mass balance analysis of chlorogenic acid in aqueous extracts of Eucommiae Foliumvia integrated membrane process of clarification and refinement
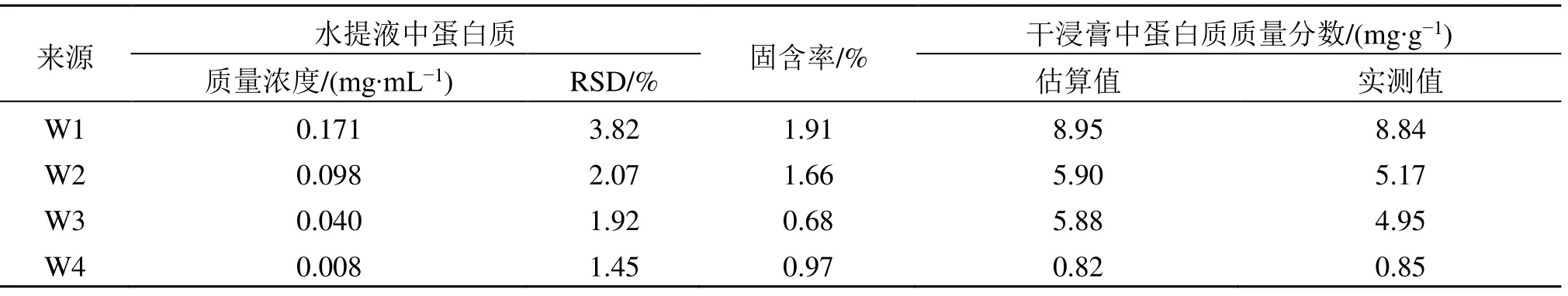
表5 杜仲叶水提液澄清、精制膜集成工艺过程中蛋白质的物料衡算Table 5 Mass balance analysis of proteins in aqueous extracts of Eucommiae Folium via integrated membrane process of clarification and refinement
志谢:广州中国科学院先进技术研究所中药绿色制造工艺研发与质量控制实验室的高效液相设备,宋宏臣博士及其课题组成员提供陶瓷膜设备,何敬愉博士对前期实验提供的帮助。
利益冲突所有作者均声明不存在利益冲突
