安罗替尼在晚期非小细胞肺癌真实世界非一线治疗中的临床效果▲
2021-06-09韦婷婷赵迎喜许克忠龙亚秀
韦婷婷 蓝 柳 赵迎喜 许克忠 龙亚秀
(1 广西来宾市人民医院肿瘤科,来宾市 546100,电子邮箱:285977772@qq.com;2 广西科技大学第二附属医院肿瘤放射治疗三病区,柳州市 545006)
肺癌是全球发病率较高的恶性肿瘤,其中非小细胞肺癌(non-small cell lung cancer,NSCLC)占肺癌的80%~85%[1]。大多数患者诊断时已属晚期,对于局部晚期或晚期NSCLC患者,化疗、靶向治疗和免疫治疗仍然是最重要的治疗手段,但仍有大部分患者在经标准一线或二线治疗后未能达到完全缓解,甚至出现疾病进展,若此时患者身体状况尚可,需给予有效且安全的药物治疗来控制肿瘤、延长生存时间。近年来,采用分子靶向药物治疗表皮生长因子受体(epidermal growth factor receptor,EGFR)突变、间变性淋巴瘤激酶突变和C-ros原癌基因1-受体酪氨酸激酶基因突变患者,可改善患者的预后[2],但无基因突变患者不能从该治疗中获益,且基因突变阳性患者对靶向药物疗的耐药现象也成为肺癌治疗中亟待解决的瓶颈问题,大多数酪氨酸激酶抑制剂(tyrosine kinase inhibitor,TKI)仅能延长无进展生存期(progression-free survival,PFS),对总生存时间(overall survival,OS)的改善作用不明显[3],因此探寻新的靶向药物用于治疗局部晚期或晚期NSCLC成为研究趋势。安罗替尼(AL3818)是一种新的抗肿瘤血管生成和抑制肿瘤细胞增殖的多靶点小分子TKI[4],由于其作用于这些靶点的半抑制浓度值低,故血药浓度低,副作用小,因此与其他TKI药物相比有着明显的优势[5]。本研究探讨安罗替尼在晚期肺癌真实世界非一线治疗中的疗效和安全性,现报告如下。
1 资料与方法
1.1 临床资料 回顾性分析2018年12月至 2019年6月广西来宾市人民医院和广西科技大学第二附属医院收治的48例NSCLC患者的临床资料。纳入标准:(1)经病理和影像学确诊为晚期(ⅢB/Ⅳ期)NSCLC;(2)至少有1个可测量病灶;(3)本次就诊前已经一线或多线治疗失败(进展或复发),且肿瘤仍持续生长;(4)仅单独口服盐酸安罗替尼2个周期以上,不同时进行其他方法治疗。同时满足以上4个条件的患者纳入本研究,本研究不设排除标准。其中男性28例、女性 20例,年龄43~71(60.6±8.8)岁;美国东部肿瘤协作组体能状态(Eastern Cooperative Oncology Group-performance status,ECOG-PS)评分≤1分14例,2分28例,3分6例;腺癌32例,鳞状细胞癌16例;有脑转移10例,无脑转移38例;EGFR突变阳性16例;既往接受EGFR-TKI治疗22例,抗血管生成药物+化疗5例,单纯化疗21例。本研究经广西科技大学第二附属医院医学伦理委员会批准,所有患者均对本研究知情并签署知情同意书,自愿参与。
1.2 治疗方法 所有患者口服盐酸安罗替尼胶囊(正大天晴药业集团股份有限公司,生产批号200413283)进行治疗:早餐前顿服安罗替尼8~12 mg,1次/d,连续服用2 周后停药1 周,即3 周(21 d)为1个周期。所有患者均口服盐酸安罗替尼2个周期或以上。
1.3 随访和病情评价 每2周对患者进行1次随访,每用药2个周期评估1次疗效,直至患者死亡或研究截止时间(2019年12月30日),以先发生者为准。参照世界卫生组织实体瘤疗效评估标准(RECIST 1.1)[6]评估疗效。主要观察指标为PFS,次要观察指标包括OS、疾病控制率(disease control rate,DCR)和不良事件(高血压、疲劳、食纳下降、手足综合征、口咽痛、咯血、皮疹、促甲状腺素升高、高三酰甘油血症)。DCR=(完全缓解+部分缓解+病情稳定)例数/总例数×100%。其中,完全缓解指所有目标病灶完全消失;部分缓解指所有可测量目标病灶的直径总和缩小≥30%;疾病进展指目标病灶的直径和相对增加≥20%;疾病稳定指靶病灶减小的程度没达到部分缓解,增加的程度也没达到疾病进展水平,介于两者之间[6]。用药不良事件性质和严重程度的评价参照美国国家癌症研究所通用毒性反应标准(NCI-CTC v3.0)[7],分为0~Ⅳ级。
1.4 统计学分析 采用SPSS 24.0软件进行统计分析。计数资料以例数和率(%)表示,组间比较采用χ2检验;计量资料以(x±s)表示,组间比较用成组设计t检验;生存分析用Kaplan-Meier法;PFS和DCR的比较采用log-rank检验;采用Cox逐步向前回归法分析影响PFS的因素。Log-rank检验时以P<0.10为差异有统计学意义,其余检验均以P<0.05为差异有统计学意义。
2 结 果
2.1 治疗情况 48例NSCLC患者采用安罗替尼治疗5~30周,中位治疗时间为12周;随访时间4.5~21.6个月,中位随访时间为9.9个月。治疗过程中有3例患者出现Ⅲ级手足综合征、5例患者出现Ⅲ~Ⅳ级高血压,其中有5例(10.4%)患者的治疗剂量调整为10 mg/d,2例(4.2%)患者的治疗剂量调整为8 mg/d,1例Ⅲ级高血压患者因咯血而终止治疗。所有患者均进行疗效和不良反应评价。
2.2 客观疗效评价 48例NSCLC患者经治疗后均无完全缓解者,部分缓解24例(50.0%),病情稳定10例(20.8%),疾病进展或者死亡14例(29.2%),DCR为70.8%(34/48)。
2.3 生存情况 Kaplan-Meier生存分析结果显示,48例NSCLC患者的中位PFS为6.5个月(95%CI:4.4~7.0),中位OS为9.9个月(95%CI:8.7~11.6),见图1。
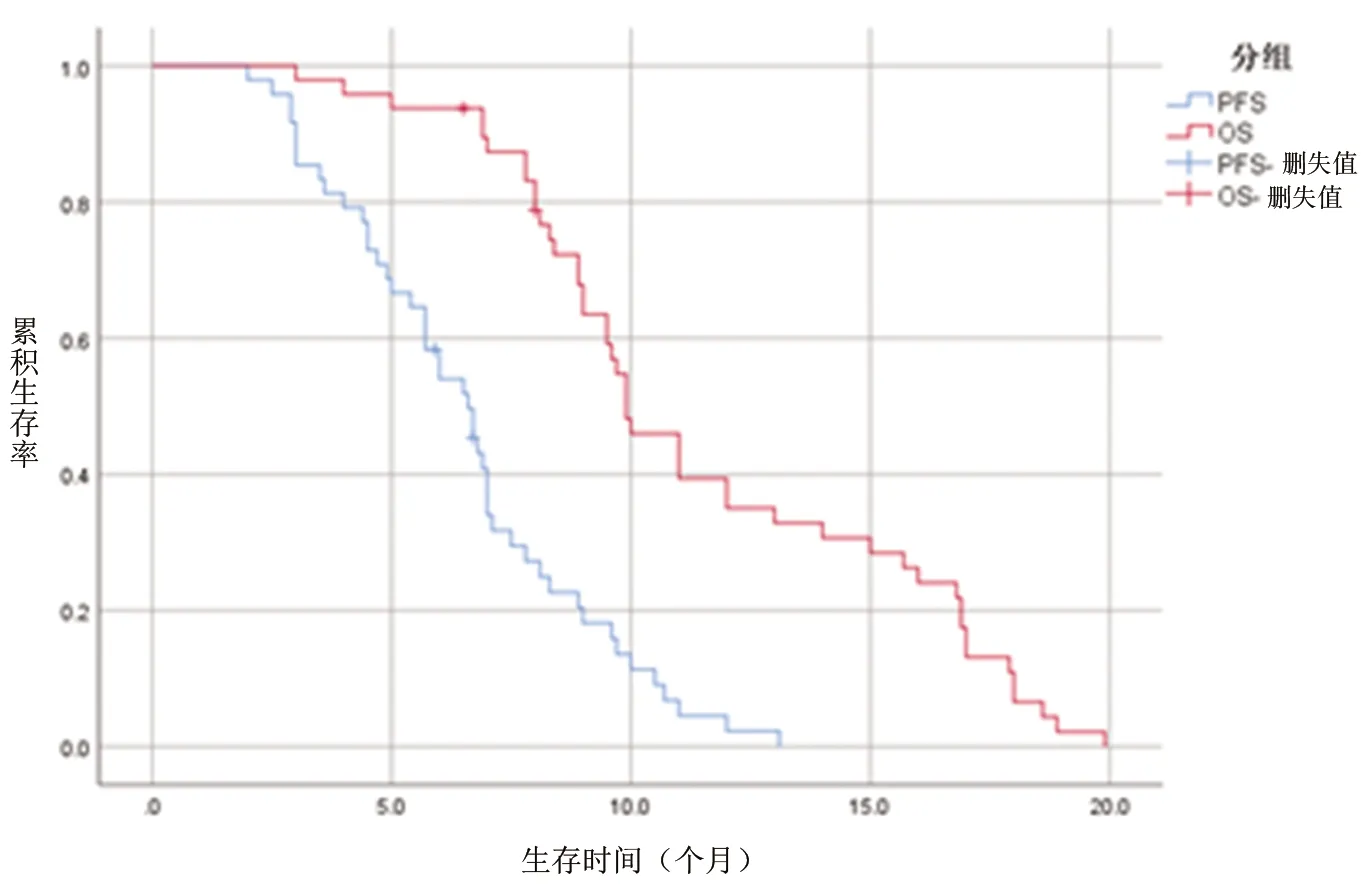
图1 48例晚期NSCLC患者的无进展生存曲线及总生存曲线
2.4 不同临床特征NSCLC患者DCR和PFS的比较 单因素分析结果显示,是否有脑转移、转移灶个数、EGFR状态可能与DCR相关,是否有脑转移、转移灶个数、EGFR状态可能与PFS相关(均P<0.05)。见表1。
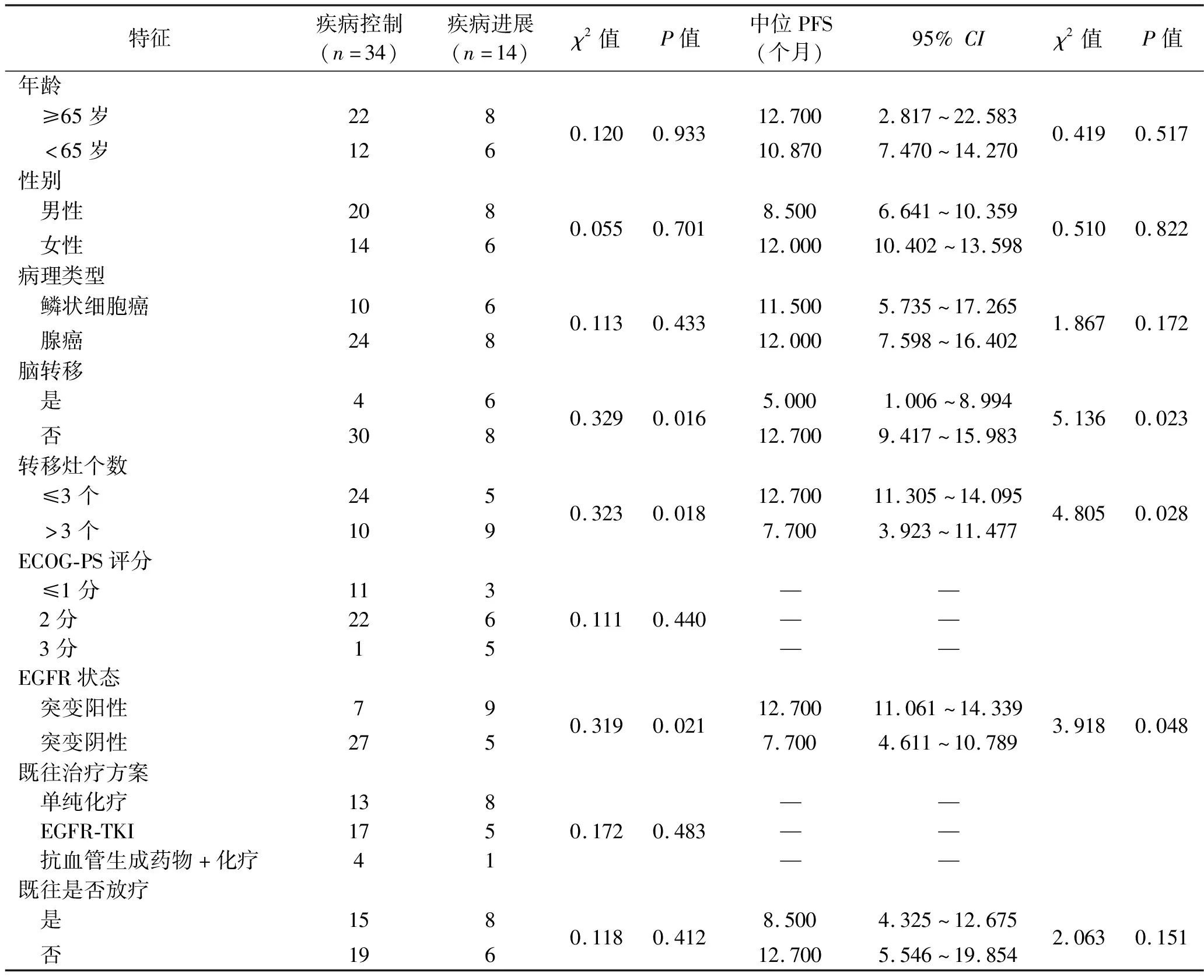
表1 不同临床特征患者的疾病控制情况及PFS的比较(n=48)
2.5 影响NSCLC患者PFS的多因素Cox回归分析 以患者治疗后的PFS为因变量,以单因素分析具有统计学意义(P<0.10)的变量(脑转移情况、转移灶个数、EGFR状态)和临床上认为与PFS相关的变量(ECOG-PS评分、既往放疗情况)作为协变量,纳入Cox回归模型中,采用向前法进行分析(变量赋值情况见表2)。结果显示,无脑转移、转移灶个数<3个、EGFR突变阳性是NSCLC患者接受安罗替尼治疗后PFS延长的保护因素(均P<0.05)。见表3。
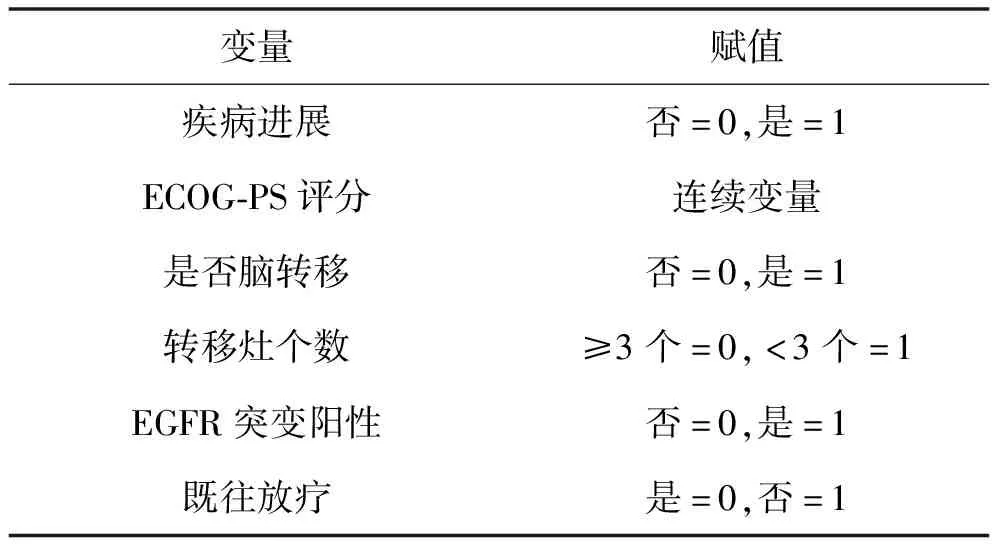
表2 变量赋值情况
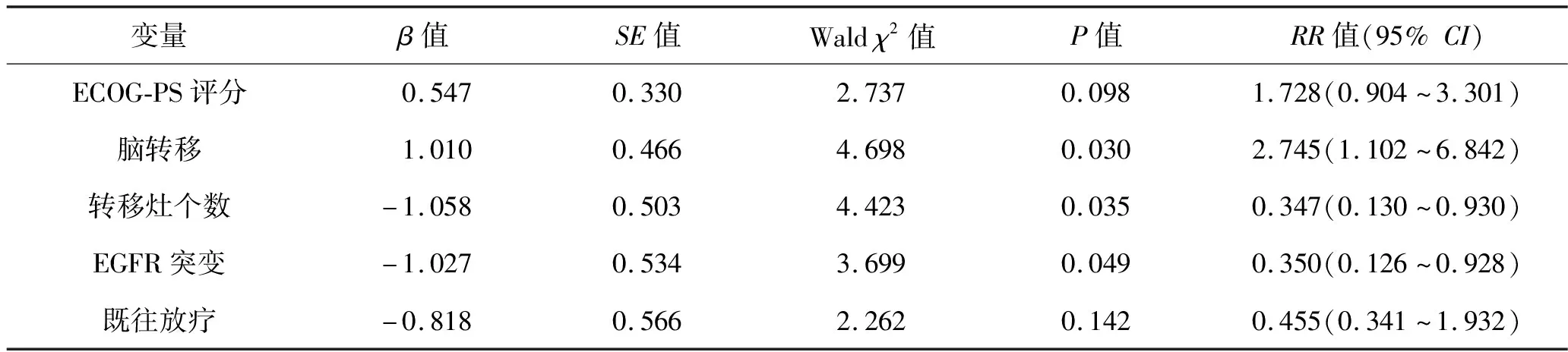
表3 NSCLC患者疾病进展影响因素的多因素Cox回归分析结果
2.6 不良反应 本研究中Ⅰ~Ⅱ级不良反应,以食欲下降、疲劳、高血压、手足综合征为主,而促甲状腺素升高、高三酰甘油血症、口咽痛、皮疹的发生率较低;Ⅲ级~Ⅳ级不良反应中,高血压5例、手足综合征3例、咯血1例。见表4。其中大多数高血压和手足综合征发生在开始用药后的第2~4周内。
3 讨 论
得益于放化疗及靶向药物治疗的进步,晚期NSCLC患者生存时间较以往明显延长,但随着治疗时间推移,患者逐渐对靶向药物(EGFR/间变性淋巴瘤激酶)或化疗药物耐药,对于此类经历三线及三线以上治疗失败的患者,目前并没有标准的治疗方案[8]。而既往关于化疗用于晚期NSCLC三线治疗的研究,多为回顾性或小样本量研究,循证医学证据不充分。针对目前抗血管生成药物或TKI虽然能延长PFS,但OS无显著获益的现状[9],国内外学者开展了多项临床研究,旨在建立晚期NSCLC三线治疗的标准方案,从已经公布的研究结果来看,我国自主研发的新药安罗替尼治疗具有明显的优势[10-11]。
目前已公布的Ⅱ期和Ⅲ期临床试验结果显示,安罗替尼可明显改善NSCLC患者的目标应答率和DCR[10-11]。其中最具有代表性的是ALTER0303研究[10],该研究显示,相比于安慰剂组,安罗替尼单药组的PFS及OS均显著延长,不同病理类型、驱动基因突变状态、既往治疗模式患者以及老年患者均能从安罗替尼治疗中获益,该药展现了良好的抗肿瘤疗效,尤其是对于治疗方式相对较局限的鳞癌患者,安罗替尼组的OS较安慰剂组延长了4.7个月。故2018年版专家共识将安罗替尼在无驱动基因突变、非鳞癌的Ⅳ期NSCLC患者的三线治疗中作为Ⅰ级推荐(1类证据)[12-13]。
真实世界研究是相对于随机对照试验(randomized controlled trial,RCT)“理想世界”而言的。RCT 研究采用了随机化、盲法、严格质控等措施来规范研究过程,故其研究对象不一定能代表应用某些治疗手段的所有患者群[14]。而真实世界研究侧重于基于现实中个体化的诊疗方式来评价治疗方法的真实有效性和安全性,其不仅在研究样本的基线数据上与 RCT 有差异,而且在后续的治疗上,除了主要的干预措施一致外,还存在次要干预措施以及其他诸多方面的差异[15]。本研究定位于真实世界的用药人群,部分患者ECOG评分>1分,甚至达3分,包括一线、二线甚至是三、四线治疗失败的患者,但纳入研究对象时没有设立类似于RCT的严格纳入和排除标准,而是通过对符合要求的人群进行集中监测,观察盐酸安罗替尼在临床中的真实有效性及安全性,为临床用药提供参考。
在ALTER0303 研究[10]中,安罗替尼组的中位OS较安慰剂组长 3.3 个月(9.6个月比6.3 个月;HR=0.68,95%CI:0.54~0.87;P=0.002);PFS 延长 4.0 个月(5.4个月比1.4 个月;HR=0.25,95%CI:0.19~0.31;P<0.001),且安罗替尼组的客观缓解率和DCR等次要指标也均优于对照组(P<0.001);亚组分析结果显示,EGFR突变阳性或阴性的腺癌或鳞癌患者都能从安罗替尼治疗中在 OS 和 PFS 方面双重获益[11]。而本研究中,NSCLC患者的DCR为 81.25 %,中位PFS为6.5个月,中位OS为9.9个月,虽然老年患者(≥65岁)占了大部分,且有一半的患者ECOG评分为2分,甚至有12.5%的患者ECOG达3分,但PFS及OS时间均略长于ALTER0303研究。原因考虑为本研究纳入了一部分一线治疗失败后未进行二线治疗,直接使用安罗替尼治疗的患者。这也体现了真实世界的情况,部分EGFR突变阴性的晚期NCSCL老年患者在进行一线化疗失败后,虽然身体的一般情况良好,但因考虑年龄以及生活质量因素拒绝行二线化疗,而超出说明书适应证直接使用安罗替尼治疗或联用其他抗肿瘤药物,这也取得一定疗效。
本研究结果显示,NCSCL患者行安罗替尼治疗后的PFS与是否有脑转移、转移灶个数和EGFR突变状态相关(均P<0.05),而与ECOG评分、性别、年龄、病理类型、既往治疗方式无明显相关性(均P>0.05)。这与ALTER0303RCT研究[10]的结论有部分不一致,考虑与本研究的样本量小不能进行分层分析,以及真实世界中人群用药周期差异相关。
ALTER0303 研究通过扩大样本量进一步验证安罗替尼的安全性。该研究中主要不良反应包括乏力、高血压、手足综合征、高三酰甘油血症、厌食等,通过对症治疗或调低药物治疗剂量等方式可有效地得到控制;最常见的Ⅲ级以上不良事件包括高血压(13.6%)、低钠血症(8.2%)、γ-谷氨酰转移酶升高(5.4%),有24例受试者因Ⅲ级以上不良事件下调安罗替尼剂量至10 mg,2例下调至8 mg[11]。本研究中,胃肠道反应、疲劳高血压、手足综合征、促甲状腺素升高、高三酰甘油血症、口咽疼痛、皮疹均为靶向治疗药物的常见不良反应,给予对症处理后可缓解;Ⅲ~Ⅳ级不良反应包括高血压5例、手足综合征3例,其中5例患者的剂量调整为10 mg/d,2例患者的剂量调整为8 mg/d,1例因咯血而终止治疗。最早出现的不良反应为胃肠道反应,一般多在治疗后1~2周出现,给予止泻药物治疗后均可缓解;其次是高血压(收缩压及舒张压均有升高,以舒张压升高最明显),最早发生于治疗后第2~3周,给予降压药物后多数患者的血压均可控制在正常范围内,2例Ⅲ级和1例Ⅳ级高血压患者在联用降压药情况下,安罗替尼减量至10 mg后患者血压恢复正常,1例Ⅲ级和1例Ⅳ级高血压患者安罗替尼减量至8 mg后血压恢复正常。手足皮肤反应多出现在治疗第3~4周,多为Ⅰ~Ⅱ级,给予尿素维生素E软膏、莫匹罗星软膏以及维生素B12外敷后皮疹可控制,2例Ⅲ级患者安罗替尼减量至10 mg后可控制,1例Ⅲ级患者安罗替尼减量至8 mg后可控制。本研究中大部分的不良反应在ALTER0303临床试验中也出现,但Ⅲ~Ⅳ级不良事件发生率与ALTER0303研究有差异。原因考虑为:在真实世界中,患者无明确的纳入和排除标准,不同的人群对药物的反应有差异;因受经济、意愿等因素的影响,患者的治疗时间较RCT研究明显减少(中位治疗时间12周比18周)。本研究中有1例患者出现咯血,提示临床使用安罗替尼时需警惕咯血的发生,严格排除中心型鳞状细胞癌和高危咯血风险患者。本研究纳入了6例ECOG-PS评分为3分的患者,口服安罗替尼10 mg可耐受,不良反应多为Ⅰ~Ⅱ级,较其他患者无明显加重,这提示在真实世界中安罗替尼应用于体能较差的患者时安全性仍较高。
目前已有研究表明部分生物标记物可以预测安罗替尼的疗效,例如循环血管内皮细胞(circulating endothelial cell,CEC)表达水平下降的患者接受安罗替尼治疗后PFS较CEC表达水平正常的患者延长,提示CEC是预测安罗替尼疗效的敏感标志物[16]。Lu等[17]发现,趋化因子CXCL2水平的变化可用于预测和监测安罗替尼治疗晚期NSCLC患者的效果。故下一步的研究中,我们将进一步扩大样本量,并纳入CXCL2、CEC、循环DNA等预测因子,探寻这些预测因子是否能真实地预测安罗替尼治疗NSCLC的效果,进一步明确安罗替尼的疗效并确定优势人群。
综上所述,安罗替尼在晚期 NSCLC二线及二线以上治疗中安全、有效,其中无脑转、转移病灶数<3个、EGFR突变阳性的患者PFS获益更大,这可为晚期 NSCLC多线化疗、EGFR-TKI治疗失败的患者提供新的治疗机会,延长其生存时间。尤其是老年或一般情况不良的患者,口服安罗替尼后副反应无明显加重。在今后的Ⅲ期临床试验和真实世界研究中,一方面,可以纳入分子预测因素,以进一步确定安罗替尼治疗的优势人群;另一方面,可以就安罗替尼治疗时机前移进行一系列研究,例如对一线化疗后未达完全缓解的患者使用安罗替尼进行维持治疗,或者比较一线治疗失败的患者采用二线标准化疗与采用二线标准化疗联合安罗替尼治疗的疗效差异。
