贝诺酯的合成方法改进
2021-06-08陈启绪张永春任继波曹智超刘圣玮宋子龙王明君袁文鹏
陈启绪,张永春,任继波,曹智超,刘圣玮,宋子龙,祁 祺,王明君,袁文鹏*
(1.齐鲁工业大学(山东省科学院)山东省科学院菏泽分院,山东省生物工程技术创新中心,山东菏泽 274000;2.齐鲁工业大学(山东省科学院)化学与化工学院,山东 济南 250353)
贝诺酯又名扑炎痛、苯诺来、解热安,化学名:2-乙酰氧基苯甲酸对乙酰氨基苯酯,是由对乙酰氨基酚和阿司匹林化学结构经拼合形成的酯化前药,属于非甾体抗炎解热镇痛药[1]。贝诺酯具有对胃肠道刺激性小、毒性低、作用时间长等特点,在临床上得到广泛应用[2]。贝诺酯的现有合成方法(图1)[3-6]:乙酰水杨酸通过氯代反应生成乙酰水杨酰氯,然后与对乙酰氨基酚的钠盐反应,生成贝诺酯,反应收率在65%~80%之间。现有的贝诺酯合成方法中,乙酰水杨酸的氯代方法有氯化亚砜/吡啶体系氯代[5-6]、草酰氯/吡啶体系氯代[7]、光气氯代[8]、固体三光气氯代[9-10]。这些氯代试剂中,氯化亚砜、草酰氯、光气在使用过程中,会产生强烈的刺激性气味,实验过程不安全;固体三光气可以看作三分子氯气,使用量需在1 倍当量以上,同时后处理过程中产生三倍当量的废水。此外,这些合成方法均需尾气吸收装置,实验装置复杂,操作不便。Vilsmeier 试剂在医药和化工领域有十分广泛的应用[11-12],除了作为酰化试剂使用外,还能作为氯代试剂使用。本研究先用固体三光气(BTC)和DMF 反应制备新型Vilsmeier 试剂[13],然后将Vilsmeier 试剂与乙酰水杨酸在缚酸剂催化下反应,制备乙酰水杨酰氯,对乙酰氨基酚和碱反应生成钠盐,最后将乙酰水杨酰氯与钠盐反应制得贝诺酯。对实验进行了优化,以Vilsmeier 试剂、乙酰水杨酸为原料,三乙胺为缚酸剂制备贝诺酯,反应收率为70%~80%,实验过程中气味小、实验装置简单(无需尾气接收装置),减少了废水废气的产生,更安全环保。

图1 现有的贝诺酯合成方法的路线Fig.1 The route of existing synthetic methods for benorilate
1 实验部分
1.1 实验仪器及试剂
(1)仪器:磁力电动搅拌机、低温恒温搅拌反应浴、循环水式真空泵(巩义市予华仪器有限责任公司);三口瓶、温度计、抽滤瓶、全自动熔点仪(济南海能仪器有限公司)等。
(2)试剂:固体三光气、N,N-二甲基甲酰胺、乙酰水杨酸(含量大于99%)、三乙胺、吡啶、碳酸氢钠、对乙酰氨基酚(含量大于99%)、氢氧化钠、95%乙醇、石油醚、乙酸乙酯、无水氯化钙、活性炭,以上试剂均为国药分析纯。
1.2 实验原理
贝诺酯的改进合成原理如图2 所示。

图2 合成贝诺酯的改进方法Fig.2 The improved method for the synthesis of benorilate
1.3 实验步骤
1.3.1 乙酰水杨酰氯的制备
在装有温度计、磁力电动搅拌器的250 mL三口烧瓶中加入60 mL 溶剂DMF,控温0 ℃~5 ℃,分批加入6.58 g(22.2 mmol)固体三光气。加入后,升温到室温搅拌30 min,制得66.6 mmol Vilsmeier 试剂。控温5 ℃下向Vilsmeier 试剂中加入10.0 g(55.5 mmol)乙酰水杨酸,逐滴加入66.6 mmol三乙胺缚酸剂,室温条件下反应3 h,然后将反应液转移至恒压漏斗中,密封备用。
1.3.2 贝诺酯的制备
精确称取10.0 g (66.2 mmol)扑热息痛(对乙酰氨基酚)和100 mL 水,加入装有搅拌桨、温度计的500 mL 三口烧瓶中。将反应液降温至5 ℃左右,在搅拌下逐滴加入氢氧化钠溶液(3.6 g 固体氢氧化钠,20 mL 水配成)。滴加完毕后,缓慢滴入第一步制得的乙酰水杨酰氯(20 min 滴毕),控温8 ℃~12 ℃,滴毕,用15 mL DMF 荡洗恒压滴液漏斗并滴加至反应液中,使反应液的pH 在9~10 之间,搅拌反应30 min 后,补加150 mL 水,搅拌析晶30 min 后,抽滤,用水冲洗至中性,烘干,得粗品13.98 g,摩尔收率为80.4%,熔点为174 ℃~175.3 ℃(与文献报道的174 ℃~178 ℃[5]、174 ℃~175 ℃[14]一致)。TLC 显示:得到的产品与对照品一致,无其他杂质点,展开剂为V(石油醚):V(乙酸乙酯)=5:1 的混合溶剂。1H NMR (CDCl3,400 MHz) δ:8.22~8.20(m,1H,CONH),7.69~7.11(m,8H,ArH),2.33 (s,3H,CH3),2.16 (s,3H,CH3);13C NMR(CDCl3,400 MHz) δ:169.92,168.41,163.21,151.16,146.58,135.97,134.70,132.26,126.28,124.03,122.47,122.08,120.96,24.47,21.06(与文献报道[9]一致)。元素分析,C17H15NO5实测值(计算值):C 为65.13%(65.17%),H 为4.86%(4.83%),N 为4.49%(4.47%)。
2 实验结果与分析
参考贝诺酯的现有合成方法,以Vilsmeier 试剂为氯代试剂,丙酮为反应溶剂,经过试验无法得到贝诺酯产品。由于Vilsmeier 试剂是常用的氯代试剂,该反应理论上没有问题,推测反应溶剂不适合Vilsmeier 试剂体系,因此先对反应溶剂进行了考察。
2.1 反应溶剂对反应结果的影响
本组实验Vilsmerier 试剂与乙酰水杨酸投料摩尔比均为1.2:1,吡啶为缚酸剂,反应温度为15 ℃~25 ℃,其他条件均相同,考察不同溶剂对反应结果的影响,结果见表1。

表1 不同溶剂对反应收率的影响Tab.1 Effects of different solvents on the reaction yield
从表1 中可以得出,用丙酮、DMSO 作反应溶剂,反应收率低;二甲苯反应收率适中,但是产品的颜色较深;DMF、甲苯、四氢呋喃反应收率较高,DMF 为较优的反应溶剂。
2.2 缚酸剂对反应结果的影响
本组实验均以DMF 为反应溶剂,Vilsmerier试剂与乙酰水杨酸的投料摩尔比为1.2:1,反应温度为15 ℃~25 ℃,考察缚酸剂对反应结果的影响,结果见表2。

表2 缚酸剂对反应结果的影响Tab.2 Effects of acid acceptors on reaction results
由表2 可得出,有机碱作缚酸剂的反应收率优于无机碱,其中三乙胺优于吡啶,三乙胺为较优的缚酸剂,反应收率可达80.4%。
2.3 Vilsmerier 试剂投料量对实验的影响
本组实验以DMF 为反应溶剂,三乙胺为缚酸剂,反应温度为15 ℃~25 ℃,其他条件均相同,考察Vilsmeier 试剂的投料量对实验结果的影响,结果见表3。

表3 乙酰水杨酸和Vilsmerier 投料比对反应的影响Tab.3 Effects of acetyl salicylic acid and Vilsmerier feeding ratio on reaction
从表3 中可得出,随着Vilsmerier 试剂投料量的增加,反应收率也进一步提高;当Vilsmerier试剂为1.2 倍当量时,反应收率达到最高;再增加Vilsmerier 试剂的量时,反应收率有一定的下降,产品的性状也会变差,这是由于Vilsmeier 试剂作为活泼的氯代试剂,底物乙酰水杨酸含有羧酸基团和酯基,升高温度致使原料和生成的贝诺酯不稳定,易降解,具体见2.4 反应温度对实验的影响。
2.4 反应温度对反应结果的影响
本组实验的反应溶剂为DMF,Vilsmerier 试剂与乙酰水杨酸投料摩尔比为1.2:1,缚酸剂为三乙胺,其他条件均相同,考察反应温度对反应结果的影响,结果见表4。
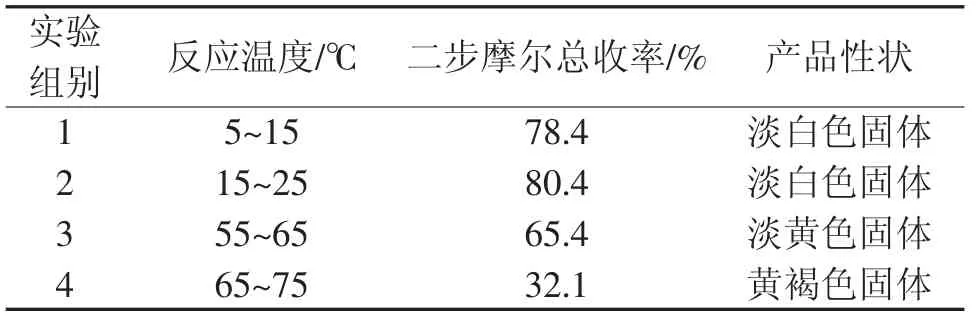
表4 温度对反应结果的影响Tab.4 Effects of temperature on reaction results
由表4 的结果可以看出,反应在较低温度条件下,反应收率较高,随着反应温度的升高,反应收率反而下降,产品颜色也逐渐变深。这是由于反应温度较高时,会导致原料乙酰水杨酸分解,形成邻羟基苯甲酸,易产生分子间缩合或者发生氧化聚合,形成多聚深色杂质[7]。因此较佳的反应温度为室温,在15 ℃~25 ℃之间。
3 结论
本合成方法采用DMF 与BTC 反应制备Vilsmerier 氯代试剂,再与乙酰水杨酸反应制得乙酰水杨酰氯,最后与对乙酰氨基酚钠盐反应,制得贝诺酯粗品,二步反应摩尔总收率可达80.4%。用Vilsmeier 试剂替代传统的氯代试剂,实验过程中气味小,更安全;氯代试剂的使用量少,产生的废水量少,更环保;无需尾气接收装置,实验装置简单;反应过程中,室温即可进行反应,无需加热,反应条件温和。本文提供了一种贝诺酯的合成方法和确证的核磁谱图,该方法易于放大、操作更安全,有望应用于工业化生产。
