应用全模型迭代重建技术的低剂量CT肝脏体积测定的临床应用价值
2021-06-07樊荣荣施晓雷
樊荣荣,施晓雷,钱 懿,望 云,萧 毅
海军军医大学长征医院放射诊断科,上海 200003
多种肝脏疾病会导致肝脏体积发生变化。对于某些肝脏疾病,例如肝硬化,肝脏体积的变化能够在一定程度上反映其病变程度。合理监测肝脏体积,尤其是更加细化的肝段体积比(liver segmental volume ratio,LSVR),即肝Ⅰ~Ⅲ段体积与肝Ⅳ~Ⅷ段体积之比[1],对于肝硬化的诊断、评估、治疗及随访具有重大的意义。肝脏储备功能是指肝脏应对生理负荷增加时可动员的额外代偿潜能[2]。手术是治疗肝脏疾病的最主要手段,术前精准评估肝脏储备功能,在制订手术方案、减少术后并发症方面具有重要的价值[3]。
多层螺旋计算机体层成像(computed tomography,CT)具有操作方便、快捷的优势,目前广泛应用于测量肝脏体积[4]。肝脏体积的测定需要采用CT增强扫描图像,且肝脏疾病患者需要多次随访检查,降低其辐射剂量很有必要,但是普通低剂量CT扫描会影响肝脏边缘及肝段分界标志的锐利度,影响肝脏体积测定的准确性。研究[5-7]表明,新一代的全模型迭代重建(iterative model reconstruction,IMR)与传统滤波反投影(filter back projection,FBP)重建相比,能够在降低辐射剂量的前提下,改善图像质量。然而,低剂量CT对肝脏体积定量测定有无影响,尚未见相关报道。本研究通过比较常规剂量FBP重建与低剂量(管电压、管电流分别为80 kV、150 mA)IMR的肝脏体积,探讨低剂量条件下,应用IMR技术能否准确重建肝脏图像,并测量肝脏及肝段体积。
1 资料和方法
1.1 一般资料
本研究为前瞻性设计,所有入选者检查前均已签署知情同意书。纳入2018年5月—8月因病情需要行上腹部增强CT检查的患者。排除标准:① 严重心、肾功能不全患者;② 碘过敏患者;③ 运动或金属伪影较重,影响观察者;④ 肝脏病变、肝脏术后或介入治疗后患者;⑤ 体重指数(body mass index,BMI)超过28 kg/m2。共40例患者纳入研究,其中男性21例,女性19例;年龄38~74岁,平均年龄(57±11)岁。
1.2 CT检查方法
1.2.1 扫描方法和参数
采用荷兰Philips公司的Brilliance iCT 256层CT扫描仪行上腹部平扫和肝脏3期增强扫描。患者取仰卧位,扫描范围从膈顶至肝下缘。所有患者上腹部平扫、动脉期及门静脉期扫描均采用常规剂量,管电压为120 kV,管电流根据患者BMI自动生成;其他参数均一致,准直为128×0.625 mm,螺距为0.914,机架旋转时间为0.4 s/周,矩阵512×512,视野(field of view,FOV)为32 cm×32 cm,重建层厚、间隔均为1 mm。延迟期扫描采用低剂量,管电压、管电流分别为80 kV、150 mA。增强扫描采用高压注射器经前臂静脉以3 mL/s的流率注射对比剂(含碘350 mg/mL),对比剂注射总量根据患者BMI计算。注射对比剂后30、60 s分别行动脉期及门静脉期扫描,注射对比剂100 s后行低剂量延迟期扫描。
1.2.2 图像后处理方法
将患者的常规剂量下门脉期原始数据进行FBP重建重组,标记为A组;将低剂量下延迟期原始数据进行IMR Soft Level 1重组,标记为B组。将2组原始图像传输至Philips星云工作站的肝脏分段(liver segmentation)软件对肝脏进行三维重建。软件根据阈值自动识别肝脏轮廓,人工对软件识别错误的组织进行修饰,去除胆囊、肝内较大血管以及肝裂间脂肪,根据Couinaud分段测定肝脏总体积、肝Ⅰ~Ⅷ段体积及LSVR。
1.3 图像分析
在Philips星云工作站上对图像质量进行主观评价。由主要从事腹部CT诊断工作的1名主治医师和1名住院医师采用盲法对两组图像的质量进行评分,以便评价2名医师评分的一致性;再由2名医师共同评分,意见不一致时邀请第3名医师共同讨论,以得到一致意见用于比较图像质量。评分标准如下。① 肝脏边缘锐利度:1分,边缘显示不清,存在伪影;2分,边缘模糊,可能存在伪影;3分,边缘较锐利,无伪影干扰;4分,边缘清晰锐利。② 肝段分界标志锐利度:1分,肝段分界显示不清,与肝实质对比度差;2分,边缘模糊,与肝实质对比度欠佳;3分,边缘较清,与肝实质对比度较佳;4分,边缘清楚,与肝实质对比度极佳。
计算机自动记录扫描的CT剂量容积指数(CT dose volume index,CTDI)、长度乘积(dose length produce,DLP),有效剂量(effective dose,ED)=DLP(mGy·cm)×k,k为肝脏转换系数[0.015 mSv/(mGy·cm)][8]。
1.4 统计学处理
采用SPSS 21.0软件进行统计学分析。2名医师对各组图像质量主观评分的一致性采用kappa检验,其中kappa值≤0.4为一致性差,0.4<kappa值≤0.6为一致性中等,0.6<kappa值≤1.0为一致性好。对A、B两组之间的主观评价指标采用Wilcoxon符号秩检验;两组辐射剂量、肝脏总体积、肝段体积、LSVR的比较采用配对样本t检验。对肝脏总体积及肝段体积进行正态分布及方差齐性检验,符合正态分布者用±s表示;否则用中位数表示。P<0.05为差异有统计学意义。
2 结 果
2.1 主观评价
2名医师对图像质量主观评分的一致性均较好,2名医师对A、B两组图像(图1、2)进行肝脏边缘锐利度、肝段分界标志锐利度评分,其中肝脏边缘锐利度kappa值分别为0.613、0.617,肝段分界标志锐利度kappa值分别为0.661、0.611(表1);两组评分差异有统计学意义(P<0.05),A、B组肝脏边缘锐利度评分的中位数分别为3、4分;A、B组肝段分界标志锐利度评分的中位数分别为3、4分(表2)。

表1 2名医师对两组重建图像质量主观指标评价一致性检验 M(P25,P75)
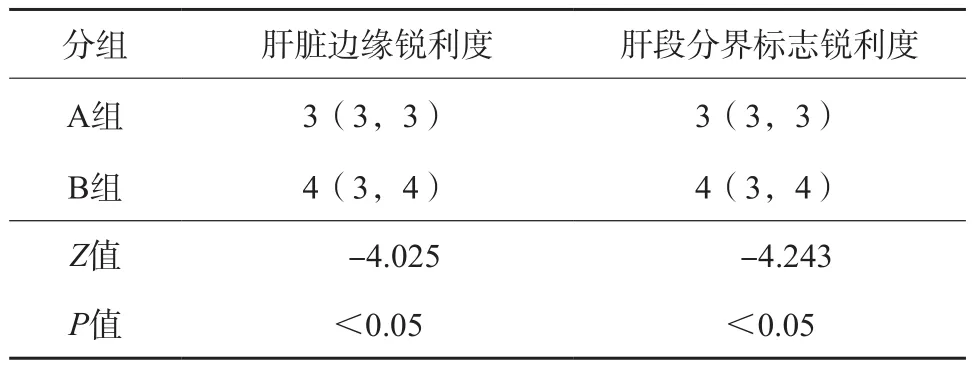
表2 肝脏延迟期扫描两组重建图像质量主观指标比较 M(P25,P75)
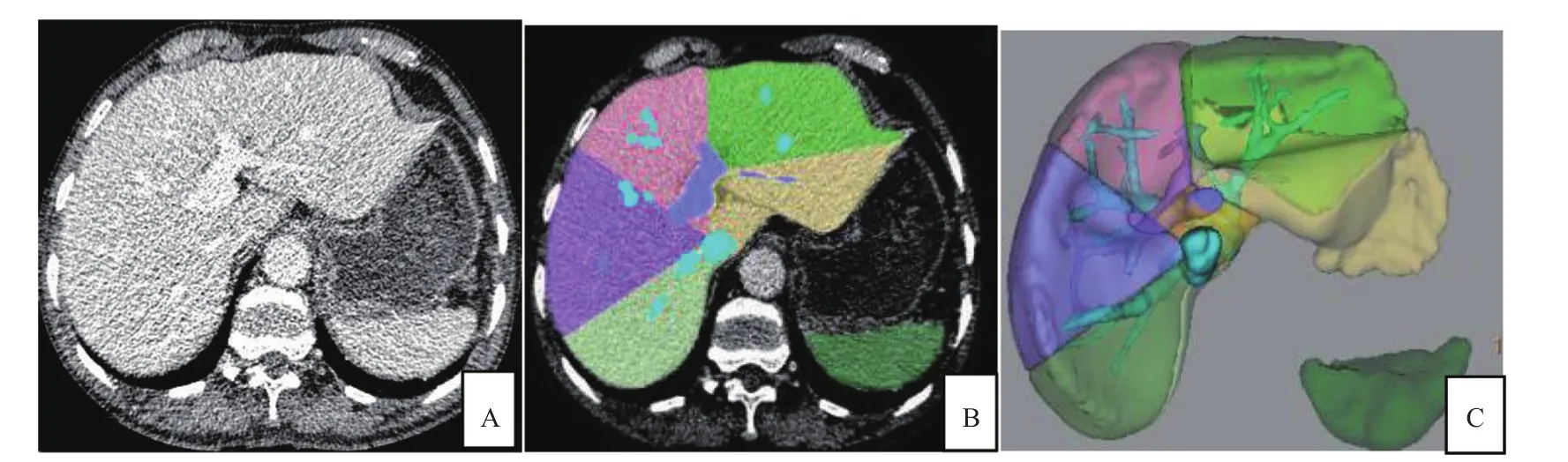
图1 常规剂量A组的腹部增强CT门脉期图像
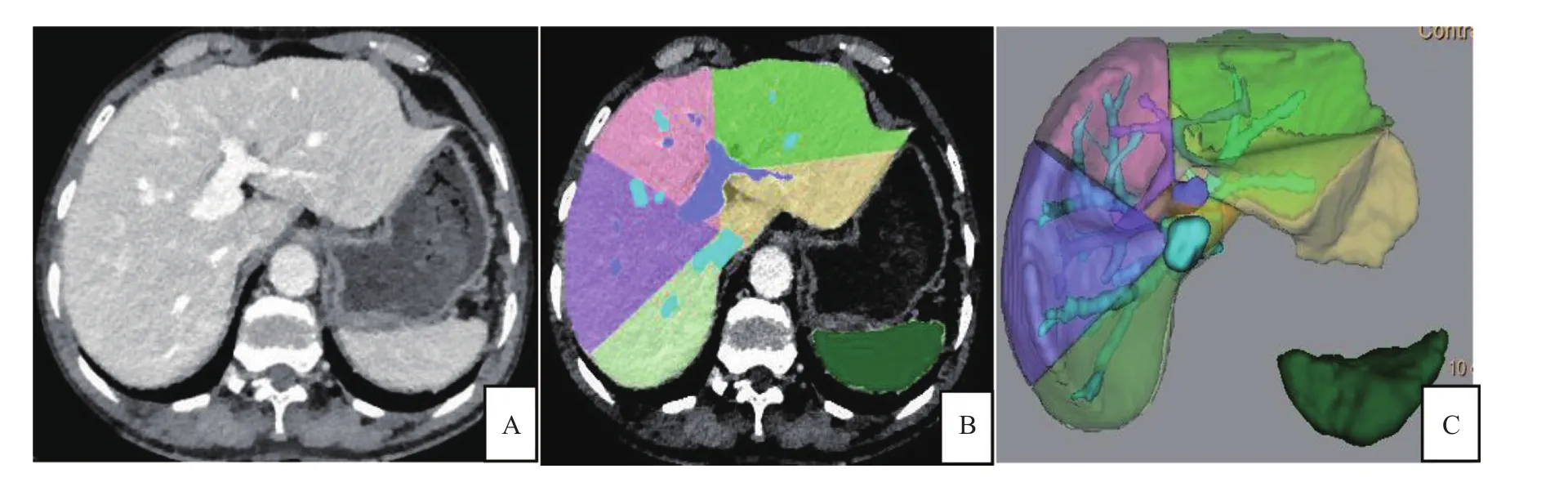
图2 低剂量B组的腹部增强CT延迟期图像
2.2 肝脏总体积、肝段体积及LSVR
A、B组肝脏总体积、肝Ⅰ~Ⅶ段体积、LSVR见表3。两组之间差异均无统计学意义(P>0.05)。
表3 两组重建图像肝脏总体积、肝段体积、LSVR比较±s
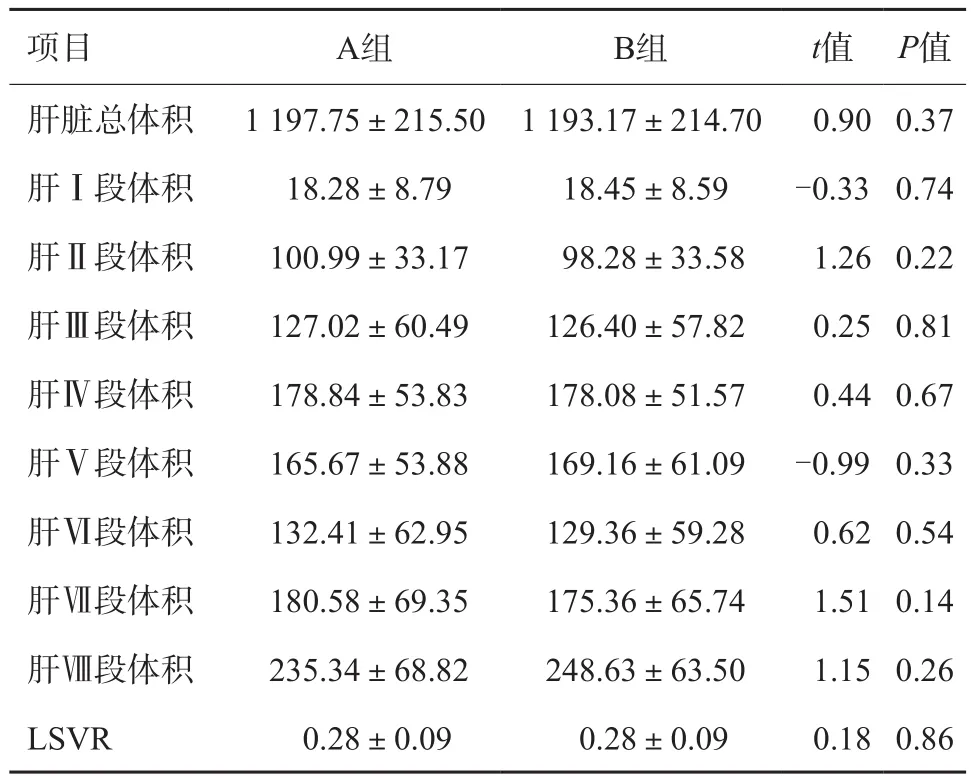
表3 两组重建图像肝脏总体积、肝段体积、LSVR比较±s
项目 A组 B组 t值 P值肝脏总体积 1 197.75±215.50 1 193.17±214.70 0.90 0.37肝Ⅰ段体积 18.28±8.79 18.45±8.59 -0.33 0.74肝Ⅱ段体积 100.99±33.17 98.28±33.58 1.26 0.22肝Ⅲ段体积 127.02±60.49 126.40±57.82 0.25 0.81肝Ⅳ段体积 178.84±53.83 178.08±51.57 0.44 0.67肝Ⅴ段体积 165.67±53.88 169.16±61.09 -0.99 0.33肝Ⅵ段体积 132.41±62.95 129.36±59.28 0.62 0.54肝Ⅶ段体积 180.58±69.35 175.36±65.74 1.51 0.14肝Ⅷ段体积 235.34±68.82 248.63±63.50 1.15 0.26 LSVR 0.28±0.09 0.28±0.09 0.18 0.86
2.3 辐射剂量
A组的平均CTDI为10.26±2.09,平均DLP为(296.00±68.03)mGy·cm,平均ED为(4.44±1.02)mSv;B组的平均CTDI为2.9,平均DLP为(83.5±6.3)mGy·cm,而平均ED为(1.25±0.01)mSv。两组CTDI与DLP差异均有统计学意义(P<0.001),B组辐射剂量较A组平均减少了75%以上。
3 讨 论
3.1 低剂量CT测量肝脏及肝段体积的意义
肝脏体积是反映某些肝脏疾病(例如肝硬化)病变程度以及评价肝脏储备能力的主要指标,在某些方面甚至被视为与Child-Pugh分级同等重要[9]。对于肝硬化来说,除了肝脏总体积的变化以外,还会导致肝脏比例失调,即肝尾状叶及肝左外叶体积增大,肝右叶及肝左内叶体积缩小,此时肝脏总体积不能完全反映肝脏比例失调程度,还需要测量更为细化的肝段体积,并计算肝脏体积比。Couinaud分段根据肝脏的解剖和功能将肝脏分为8段,即肝Ⅰ~Ⅷ段,是肝脏的独立切除单位,手术前精确评估独立的肝段体积及肝脏体积比对手术方案的制订、术中精准切除病灶及减少术后并发症方面亦具有重要意义。
CT检查操作简单、扫描时间短、空间分辨率高、后处理功能强大,测量肝脏体积较为准确[10],在临床上最为常用。与CT相比,B超测量肝脏体积受检查者主观因素影响,在操作技术方面的要求也较高[11];磁共振成像(magnetic resonance imaging,MRI)较CT检查花费多,且扫描时间长,不利于急症患者及幽闭恐惧症的患者,并且易发生不同类型的伪影,受患者呼吸伪影、肝脏边缘伪影及肝脏近膈顶处容积效应的影响都会导致MRI测量的肝脏体积偏大。
肝脏体积的测定,尤其是肝段体积划定需要采用CT增强扫描图像,且肝脏疾病患者常需要多次随访检查来监测病情变化和治疗效果,存在辐射较大的问题。如能采用低剂量CT测定肝脏及肝段体积,将明显降低患者的辐射剂量,从而减少因腹部行多期增强CT辐射剂量较大导致的健康隐患。
3.2 IMR在低剂量CT肝脏及肝段体积测量中的应用价值
单纯降低辐射剂量会导致CT图像质量下降,影响肝脏边缘及肝段分界标志锐利度,导致肝脏体积尤其是肝段体积测定不准确。
IMR是美国食品药品监督管理局(Food and Drug Administration,FDA)认证的新型的全迭代重建技术,其通过更多的迭代次数、更为复杂的迭代运算,采用更加完整、全面的系统模型进行对比校正,最终得到低噪声、高分辨率的CT图像[13]。IMR技术降低辐射剂量的能力在腹部CT增强检查中已经得到了证实,并能够在低剂量下保证图像质量,不影响诊断[12-13]。我们的前期研究[13]亦表明,在低剂量条件下,采用IMR能够显著降低图像噪声,提高图像的低对比分辨率,改善图像质量,不会影响病灶检出和常规诊断。但其在肝脏及肝段体积测量方面的应用研究尚未见报道。
CT测量肝脏体积分为手工法测量和三维重建半自动法测量两种。研究[14]表明,半自动法测量具有测量准确、速度较快的优势,故本研究采用半自动法测量肝脏体积。半自动法是根据软件自动识别肝脏解剖及肝密度将所绘层面自动延伸,然后手工微调即可。半自动法测量肝脏总体积时,肝脏边缘锐利度越高,软件勾勒的肝脏总体积越准确。另外,肝段体积测量需要人工根据肝段分界标志锐利度进行肝段划分,因此肝段分界标志锐利度越高,肝段划分越准确。本研究的主观评价证实,低剂量条件下应用IMR技术能够提高肝脏边缘锐利度及肝段分界标志锐利度。客观评价方面,本研究在肝脏总体积及肝段体积的定量测量中,A、B组之间差异无统计学意义,说明低剂量下应用IMR技术能够准确地测定肝脏及肝段体积,并计算相应的LSVR。
本研究将B组管电压、管电流分别设置为80 kV、150 mA,平均有效剂量为(1.25±0.01)mSv,较A组常规剂量的有效辐射减低至少75%以上,并且能够同样准确地应用重建肝脏图像测量肝脏总体积、肝段体积,以及计算LSVR,这对于需要长期监测肝脏疾病进程、评估治疗效果及随访肝脏储备功能的患者具有重要价值。
综上所述,低剂量条件下应用IMR比FBP重建常规剂量扫描可明显降低辐射剂量,提高肝脏边缘锐利度及肝段分界标志锐利度,可改善低剂量下肝脏图像质量,准确测量肝脏总体积及肝Ⅰ~Ⅷ段体积的定量数据,并计算得到LSVR。
