131I治疗甲状腺乳头状癌临床疗效及对甲状腺相关抗体和基质金属蛋白酶水平的影响
2021-06-02,,
, ,
(湖南中医药高等专科学校附属第一医院内分泌科,湖南省株洲市412000)
甲状腺癌近年来发病率出现了快速升高的趋势,是目前最常见的内分泌系统恶性肿瘤[1-2]。甲状腺乳头状癌(papillary carcinoma of thyroid,PTC)是甲状腺癌中的常见病理类型,其发病率有逐年升高的趋势,是临床上导致死亡的重要原因[3-4]。目前临床上通常采用手术合并碘131(131I)治疗甲状腺癌,且其安全性和有效性已经得到广泛的认可[5]。研究显示,基质金属蛋白酶可调控多种恶性肿瘤细胞的发病过程[6-7];甲状腺过氧化物酶抗体(thyroid peroxidase antibody,TPO-Ab)和抗甲状腺球蛋白抗体(anti-thyroglobulin antibody,anti-TGAb)是自身免疫性甲状腺疾病患者血清中的常见自身抗体,其与受体结合后能够激活NK细胞,而攻击靶细胞,导致甲状腺细胞破坏[8-9]。本研究旨在分析131I治疗甲状腺乳头状癌患者临床疗效及对甲状腺相关抗体及基质金属蛋白酶水平的影响,为临床治疗提供参考。
1 资料和方法
1.1 研究对象
选择本院住院2012年1月—2016年1月甲状腺乳头状癌患者90例,其中男38例,女52例,年龄53~77岁,平均(65.6±11.7)岁,所有患者均经病理检查确诊为乳头状癌。其中肺部转移20例,颈部淋巴结转移70例;低危患者35例,中危患者50例,高危患者5例。本研究经本院伦理委员会批准,所有患者均知情同意。
纳入标准:①甲状腺右侧腺叶含有癌灶或甲状腺双侧均含癌灶;②无手术禁忌证;③初次行甲状腺手术者;④病理证实为PTC(穿刺或冰冻或常规)。排除标准:①并发其他恶性肿瘤患者;②严重的代谢系统疾病患者;③严重的神经系统疾病患者或认知功能障碍患者;④临床资料不完整或不同意本研究患者;⑤严重的心肾功能异常患者。
1.2 131I治疗方案
在患者手术后4周进行131I治疗。所有患者在本研究前均停止服用左甲状腺素钠片3周,禁止摄入碘4周,若近期已接受CT检查,则131I治疗推迟至检查1~2月后进行。
所有患者均接受一次性空腹口服131I治疗:无一次性口服剂量转移者为100 mCi,有淋巴转移者为150 mCi,有肺转移者为200 mCi。口服131I后患者即入隔离病房观察,禁食2 h,住院期间和出院后1月内禁止摄入碘。嘱咐患者口含维生素C片防止放射性腮腺炎,口含柠檬片促进唾液腺分泌,口服伊托必利(50 mg/次,一日3次)护胃,督促患者多饮水。在服用131I 48 h后开始口服左甲状腺素钠片(50~100 μg/天),服用时间为6月左右。患者出院后定期随访,131I治疗6月后复查评价疗效。
1.3 观察指标
分别于治疗前和口服131I治疗6月后,抽取患者治疗前后空腹静脉血,1 500 r/min离心10 min后分离血清,进行治疗前后相关指标的检测。采用全自动生化分析仪分析白细胞数、血小板数、红细胞数和淋巴细胞数变化,并检测肝肾功能相关蛋白血肌酐(blood urea nitrogen,BUN)、谷丙转氨酶(alanine aminotransferase,ALT)、谷草转氨酶(glutamic oxaloacetic transaminase,AST)和碱性磷酸酶(alkaline phosphatase,ALP)水平的变化。放射免疫法分析血清TPO-Ab、anti-TGAb水平变化。酶联免疫吸附测定法分析血清基质金属蛋白酶2/9(metalloproteinase 2/9,MMP2/9)和基质金属蛋白酶抑制剂(inhibitor of metalloproteinase 1/2,TIMP1/2)水平变化。MMP2及MMP9检测试剂盒购自Omega公司;TIMP1检测试剂盒购自Santa Cruz公司;TIMP2检测试剂盒购自R&D公司。所有检测操作均按照试剂盒说明书进行。
1.4 治疗效果判定
①完全缓解(complete remission,CR):患者在接受治疗以后,肿瘤完全消失,且消失时间在1月以上;②部分缓解(partial remission,PR):患者在接受治疗后,肿瘤病灶有消失,且最大直径及最大垂直直径的乘积降低程度高于50%,同时未发现有新发病灶,维持状态在1月以上;③稳定(stable disease,SD):患者在接受治疗后,病灶的最大直径及最大的垂直直径的乘积出现降低,但降低的程度低于50%;④进展(progressive disease,PD):患者在接受治疗后,肿瘤的病灶未出现变小的现象或出现体积增大的现象。总有效=CR+PR+SD。
1.5 统计学方法
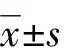
2 结 果
2.1 131I治疗甲状腺乳头状癌临床疗效
90例甲状腺乳头状癌患者经131I治疗后,完全缓解患者18例(20.00%),部分缓解患者49例(54.44%),稳定患者11例(12.22%),进展患者12例(13.34%),总有效率为78例(86.66%)。
2.2 131I治疗前后甲状腺相关抗体水平的变化
与131I治疗前比较,131I治疗后患者血清中TPO-Ab及anti-TGAb水平均明显降低(P<0.05;表1)。
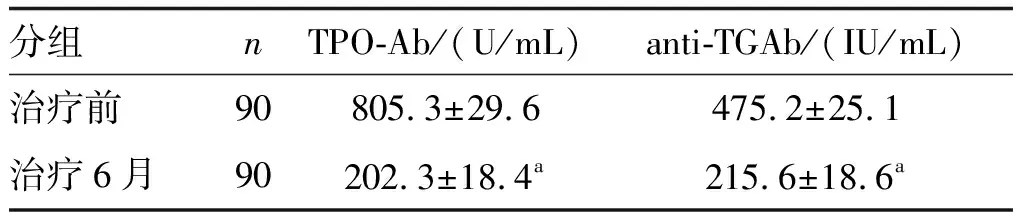
表1 131I治疗甲状腺乳头状癌前后血清甲状腺相关抗体水平的变化
2.3 131I治疗前后基质金属蛋白酶水平的变化
与131I治疗前比较,131I治疗后患者血清中MMP2/9及TIMP1/2水平均明显降低(P<0.05;表2)。
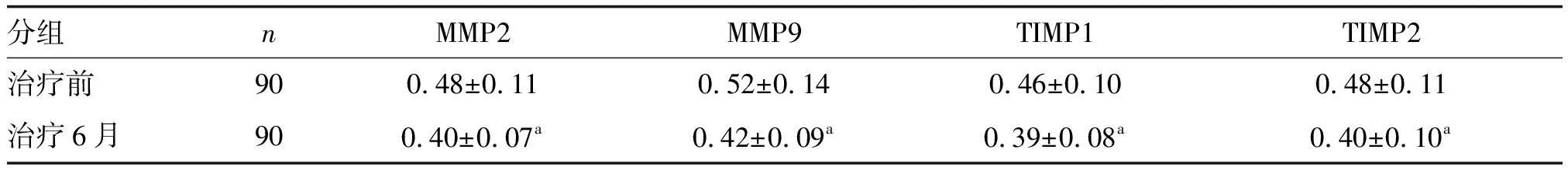
表2 131I治疗甲状腺乳头状癌前后血清基质金属蛋白酶水平的变化
2.4 131I治疗前后血细胞及肝肾功能指标的变化
与131I治疗前比较,131I治疗后患者白细胞、血小板、淋巴细胞、红细胞、BUN、ALT、AST及ALP水平无明显变化(P>0.05;表3)。
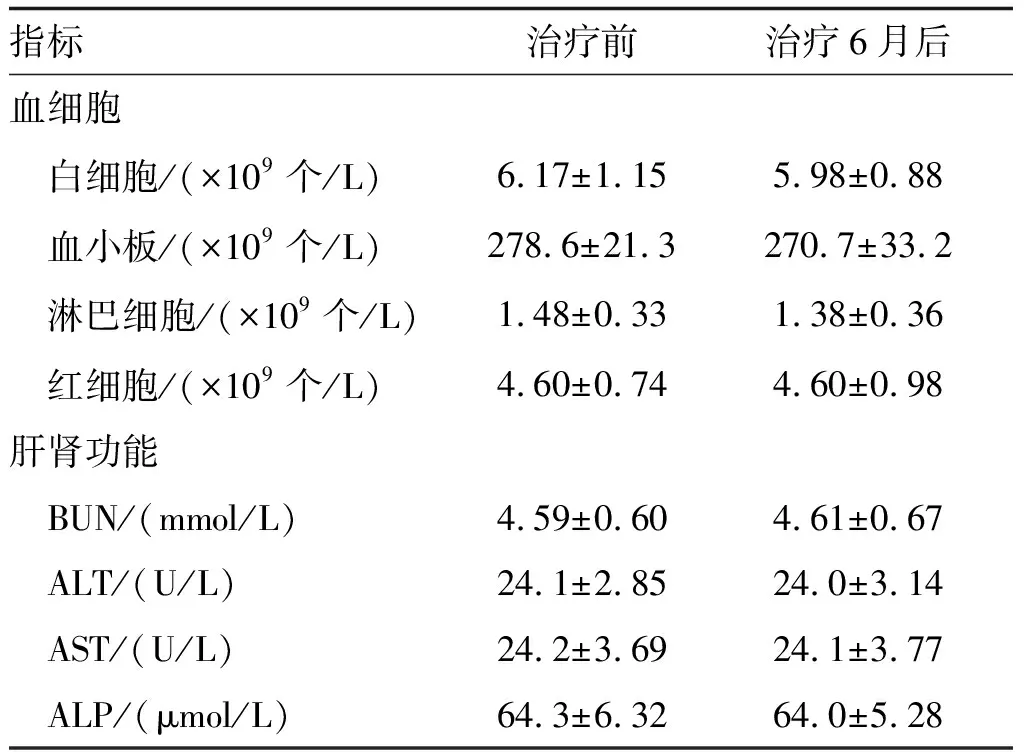
表3 131I治疗甲状腺乳头状癌前后血细胞和肝肾功能指标的变化 (n=90)
3 讨 论
放射性131I治疗是临床治疗甲状腺乳头状癌的主要方式之一,该治疗方式的临床疗效早已得到认可,同时安全性也较高,无明显不良反应。但围绕131I治疗后患者体内基质金属蛋白酶及其抑制剂和甲状腺相关抗体水平变化的研究较少。本研究在分析131I治疗甲状腺乳头状癌患者临床疗效及对甲状腺相关抗体及基质金属蛋白酶水平的影响时发现,90例甲状腺乳头状癌患者经131I治疗后完全缓解患者18例(20.00%),部分缓解患者49例(54.44%),稳定患者11例(12.22%),进展患者12例(13.34%),总有效率为86.66%;与131I治疗前比较,接受131I治疗6月后患者血清中TPO-Ab、anti-TGAb、MMP2/9及TIMP1/2水平均明显降低,而白细胞、血小板、淋巴细胞、红细胞、BUN、ALT、AST及ALP水平无明显变化,表明131I治疗甲状腺乳头状癌患者有较好临床疗效,且明显降低患者血清中甲状腺相关抗体及基质金属蛋白酶水平,不会影响患者的肝肾功能,安全性高。
有研究表明,131I对多种恶性肿瘤均有较好的效果,但关于其在治疗过程中对患者体内基质金属蛋白酶水平变化影响的研究较少[5,10]。基质金属蛋白酶及其抑制剂在恶性肿瘤细胞的增殖过程中具有重要的调控作用,且药物抑制肿瘤细胞增殖的过程中,基质金属蛋白酶的表达出现下降趋势[11-12]。针对乳腺癌患者的研究显示,MMP-11在患者体内的水平与循环肿瘤细胞具有相关性,该蛋白能促进肿瘤细胞的形成,其机制可能是对肿瘤的微环境进行了改变[13-14]。以往的研究也发现基质金属蛋白酶对口腔癌的早期诊断具有重要意义,同时还可作为口腔癌患者临床分期和病理分级的参考指标,在口腔癌患者病情预估和疗效评估等方面也具有临床参考价值[15]。本研究发现,与131I治疗前比较,接受131I治疗6月后患者血清中MMP2/9及TIMP1/2水平均明显降低,表明131I治疗甲状腺乳头状癌患者可明显降低患者血清中甲状腺相关抗体及基质金属蛋白酶水平。
甲状腺过氧化物酶抗体和抗甲状腺球蛋白抗体在多种甲状腺疾病如慢性淋巴细胞性甲状腺炎、甲状腺功能亢进症、原发性甲状腺功能减退症中均呈现明显的异常,但是目前尚无患者血清中上述因子水平在接受131I治疗后变化的相关研究[8,16-17]。本研究也发现与131I治疗前比较,接受131I治疗6月后患者血清中TPO-Ab、anti-TGAb水平均明显降低,表明131I治疗甲状腺乳头状癌患者有较好临床疗效,且此过程可能与影响血清中甲状腺相关抗体水平有关。
已有证据显示,131I治疗的安全性相对较高,但部分患者也会出现乏力、食欲减退、恶心等不良反应。但在本次研究中未出现明显的不良症状。因此,131I治疗甲状腺乳头状癌患者有较好临床疗效,且明显降低患者血清中甲状腺相关抗体及基质金属蛋白酶水平,不会影响患者的肝肾功能,安全性高。
