锂离子负极材料VS4的制备与性能表征*
2021-05-24张学政邵亚川孙会兰
张学政,邵亚川,张 迪,孙会兰,王 波
(河北科技大学 材料科学与工程学院,石家庄 050018)
目前,科技的进步与发展是建立在消耗化石能源的基础之上的.随着能源危机的日益严重,人们开始转向低成本新型能源的研究,伴随着新型能源技术的发展,新型能源材料领域研究进程也得到了相应推进[1-2].现今,作为已经商业化的锂离子电池,由于其理论能量密度高、循环寿命长、安全性能高、自放电率低等特点而得到了广泛应用[3].但是由于其他电池技术的发展并不成熟,锂离子电池仍然会在一段时间内占据市场主流,而锂元素具有资源短缺和地理分布不均的特点[4-5],因此,充分高效利用现存的锂资源依然是一个研究热点.目前商业化的锂离子电池以石墨作为负极材料,理论比容量为372 mA·h/g,不足以应对未来能源市场的竞争,因此,需要研究并制备新型的负极材料来取代传统石墨材料[6].过渡金属的硫化物具有良好的储能性能,且相较于对应的氧化物具有更高的机械稳定性和电导率[7].硫化锰理论比容量高达616 mA·h/g,且其制备方法简单,但其在锂离子嵌入/脱嵌过程中同纯硅负极一样具有较大的体积效应,这种体积效应使得电池的循环寿命严重下降[8].四硫化钒(VS4)层间距可达0.58 nm,较大的层间距有利于锂离子的快速、稳定传输[9].良好的体积膨胀承受能力有利于保持材料结构的稳定[10],且较高的硫含量可使材料具有较高的理论比容量[11-13].目前,诸多研究方法都制备出了VS4负极材料[14-16],但这些制备方法较为复杂,所需成本较高,不利于大规模应用.因此,本文以Pluronic F-127为分散剂和造孔剂,以偏钒酸铵、硫代乙酰胺为原料,分别以甲醇和乙二醇为反应溶剂,选用反应产物形貌更好且操作简单的溶剂热法来制备VS4负极材料.以甲醇作为溶剂制备VS4负极材料后,当电流密度为0.6 A/g、循环1 000次时,电池的放电比容量仍能达到280 mA·h/g,此时其库伦效率能够保持为99%,故所制备的电池有望应用至实际生产中.
1 实 验
1.1 负极材料的制备
以偏钒酸铵NH4VO3(分析纯)、硫代乙酰胺(纯度不低于98%)为原料,以Pluronic F-127为分散剂和造孔剂,分别以色谱级甲醇(纯度不低于99.9%)和乙二醇(纯度大于99%)为反应溶剂制备VS4负极材料.VS4、硫代乙酰胺、Pluronic F-127的质量分数分别为17.7%、57%、25.3%.
称取适量Pluronic F-127、NH4VO3放入去离子水中,搅拌至溶液呈乳白色直至出现白色药品沉淀,利用锡箔纸封住杯口,采用磁力搅拌器在60 ℃条件下进行加热并搅拌20 min直至溶液呈淡黄色.随后将适量硫代乙酰胺加入甲醇溶液,利用磁力搅拌器在60 ℃条件下搅拌30 min直至溶液呈黑灰色.将得到的溶液放入反应釜中并在真空干燥箱内保温12 h,得到黑灰色浓稠液体,之后将得到的浓稠液体放入真空干燥箱中在60 ℃条件下干燥10 h,得到最终产物VS4-甲醇负极材料.当采用乙二醇作为溶剂时,只需将上述实验过程中的甲醇替换为乙二醇,其余步骤不变,即可得到VS4-乙醇负极材料.
1.2 电池的组装和测试
将产物VS4-甲醇(或VS4-乙二醇)、SuperP、聚偏二氟乙烯(PVDF)按照7∶2∶1的质量比混合后放入研钵中研磨均匀,加入N-甲基吡咯烷酮(NMP)后均匀涂敷于铜箔上.将铜箔放入真空干燥箱中,待其干燥后剪切成直径为10 mm的负极电极片,并再次进行干燥.以LiPF6溶液为电解液、Celgard2400为隔膜,在氩气氛围下的真空手套箱中进行电池组装并装配得到半电池.分析VS4-甲醇(VS4-乙二醇)作为电极材料时电池的电化学性能.
2 结果与分析
2.1 XRD分析
图1为实验产物的XRD图谱.由图1可见,实验产物的衍射线都很尖锐,不存在明显杂峰,表明实验产物结晶度很高,杂质相很少且纯度较高.观察图1可以发现,21-1434#PDF标准图谱在16.99°和17.08°时出现两大强峰,且与VS4的特征晶面(110)和(020)相对应,因而可以断定实验产物确实为VS4负极材料,即以甲醇和乙二醇为溶剂能够成功制得VS4负极材料.

图1 实验产物的XRD图谱Fig.1 XRD spectrum of experimental product
2.2 TEM分析
图2为VS4-甲醇负极材料的TEM图像.由图2a、b可见,很多较长的纳米分枝从中心处延伸出来,VS4-甲醇负极材料整体呈规则海胆状形态,纳米微团直径约为2~4 μm.由图2c可以观察到,VS4-甲醇负极材料的大多数纳米分枝具有直边和规则端,且分枝长、数量多、不易团聚.这种纳米结构不仅可以缩短锂离子的扩散长度,而且能够增大活性材料与电解质溶液的界面面积,从而便于锂离子扩散和电子传输,并提高充放电过程中锂离子在电解质溶液中的动力学条件,因而有利于增强VS4-甲醇负极材料的电化学性能.由图2d可见,VS4-甲醇负极材料微观组织的纳米分枝表面并非光滑,而是粗糙不平的,坑坑洼洼的表面能为锂离子提供更多的电化学活性位点,从而提高锂电池的充放电效率和容量.由图2e可以清晰观察到VS4-甲醇负极材料的晶格条纹,其层间距较小(约为0.295 nm).由图2f可以观察到VS4的衍射花样由整齐排列的斑点组成,表明该材料属于晶体型.

图2 VS4-甲醇的TEM图像Fig.2 TEM images of VS4-methanol
图3为VS4-乙二醇负极材料的TEM图像.由图3a、b可见,与VS4-甲醇负极材料相比,VS4-乙二醇负极材料的微观结构呈不规则海胆状形态,纳米微团直径约为1.5~3 μm,表面分枝杂乱无章或交织成网状.由图3c可见,VS4-乙二醇负极材料的纳米分枝与VS4-甲醇负极材料相比不够坚挺、易团聚且数量较少,因而所能提供的锂离子活性位点较少.由图3d可见,VS4-乙二醇负极材料的分枝缠绕在一起,负极材料表面积发生堆叠,空隙结构减少,这也是其所能提供的锂离子活性位点较少的原因之一.由图3e可以清晰观察到VS4-乙二醇负极材料的典型层状结构,且层间距较大(约为0.56 nm).由图3f可见,VS4-乙二醇负极材料的衍射花样为半径不同的同心圆,表明该物质属于非晶型.

图3 VS4-乙二醇的TEM图像Fig.3 TEM images of VS4-glycol
2.3 电化学性能分析
图4为VS4-甲醇和VS4-乙二醇电极在0.4 A/g电流密度下的充放电比容量循环曲线.由图4可见,VS4-乙二醇电极的首次放电比容量可以达到1 275 mA·h/g,VS4-甲醇电极的首次放电比容量为1 200 mA·h/g.电极循环持久性的优越性体现在多次放电后比容量仍然能够达到一个较高的稳定值.经过50次循环后,VS4-乙二醇电极的放电比容量迅速缩减为103 mA·h/g,仅仅为首次放电比容量的8.1%.出现上述现象的原因为:VS4-乙二醇负极材料的微观结构呈不规则海胆状形态,且分枝缠绕在一起,其所能提供的锂离子电化学活性位点较少.观察图4可以发现,经过50次循环后VS4-甲醇电极的放电比容量约为200 mA·h/g,明显高于VS4-乙二醇电极.这是因为:一方面,VS4-甲醇负极材料的微观结构呈规则海胆状形态,纳米分枝较长、数量较多,电极表面粗糙,从而可为锂离子提供更多的电化学活性位点;另一方面,VS4-甲醇负极材料的每个纳米分枝形态坚挺,不会发生交错缠绕现象,空隙结构相对较多,可以增加活性材料与电解质溶液的接触面积,从而有利于锂离子的快速转移,进而提高电池的充放电速率.通过比较VS4-甲醇电极与VS4-乙二醇电极的比容量循环性能可知,VS4-甲醇电极的比容量循环性能更加优越.

图4 不同电极的充放电比容量循环曲线Fig.4 Charge and discharge specific capacity cycle curves of different electrodes
对VS4-甲醇电极多次充放电的比容量循环性能进行测试.图5为VS4-甲醇在0.6 A/g电流密度下的充放电比容量循环曲线.由图5可见,VS4-甲醇电极具有稳定的比容量循环性能.经过400次循环后,VS4-甲醇电极的放电比容量接近平稳且约为300 mA·h/g.经过1 000次循环后,VS4-甲醇电极的放电比容量仍可达到280 mA·h/g,此时其库伦效率能够保持为99%.由图5可见,VS4-甲醇电极的充放电比容量循环曲线的变化趋势为:首先急剧下降,再缓慢上升最后趋于平稳.VS4-甲醇电极的充放电比容量下降的原因为:1)电极材料与电解液发生反应,在固液两相的相界面上生成不溶性固体产物并沉积于负极材料上,从而形成了SEI膜,消耗了锂离子;2)在充放电过程中,通过锂离子在电极之间的重复往返嵌入/脱嵌所产生的动力学作用力造成负极材料的构架结构和SEI膜的塌陷损坏和不稳定,从而使得电池的容量发生快速衰减.VS4-甲醇电极的充放电比容量上升的原因为:1)经过初始循环后,电池内部化学物质得到活化,负极材料表面的活性位点数量增大;2)SEI膜逐渐稳固并增大了表面积,从而起到支撑负极材料结构的作用.
图6为不同电流密度下VS4-甲醇电极的倍率性能曲线.将VS4-甲醇电极分别在不同电流密度下进行充放电循环操作,每10次循环为一个周期,10次循环之后改变电流密度再次进行充放电循环.由图6可见,VS4-甲醇电极在0.2、0.4、0.6和1 A/g电流密度下的平均放电比容量分别约为600、300、240和150 mA·h/g.除了前3次循环外,VS4-甲醇电极在不同电流密度下的比容量曲线均趋于直线,库伦效率均保持在95%以上.当电流密度从1 A/g返回到0.2 A/g,VS4-甲醇电极的放电比容量可以回升到550 mA·h/g,可以达到在0.2 A/g电流密度下循环放电比容量的92%左右,表明VS4-甲醇电极具有良好的倍率性能.

图5 VS4-甲醇的充放电比容量循环曲线Fig.5 Specific charge and discharge capacity cycle curves of VS4-methanol
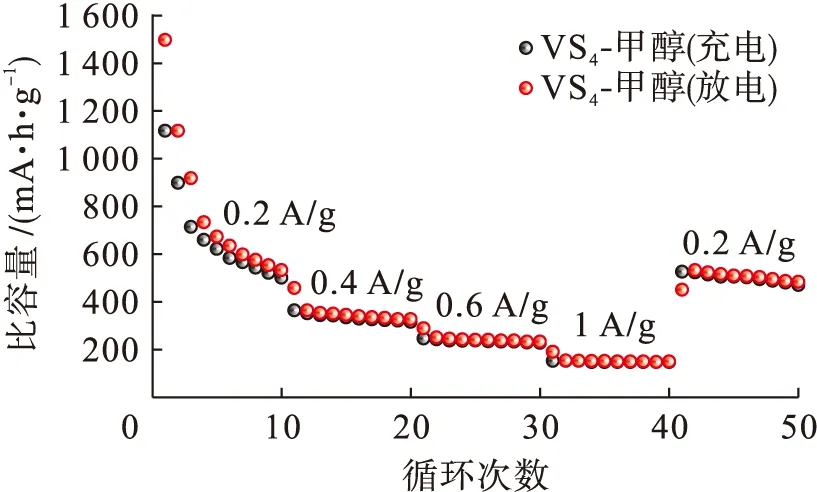
图6 不同电流密度下VS4-甲醇的倍率性能曲线Fig.6 Multiplying power performance curves of VS4- methanol under different current densities
3 结 论
为了证明溶剂热法是制备VS4负极材料的一种简单有效方法,本文成功合成了VS4-甲醇和VS4-乙二醇负极材料.制备得到的VS4-甲醇负极材料为规则海胆状纳米微团,纳米分枝较长且数量较多、纳米微团均匀分布且不堆叠、表面粗糙,扩大了活性位点面积,减少了锂离子扩散距离,因而提供了更为开放的锂离子扩散通道.VS4-甲醇电极具有良好的循环持久性,倍率性能也很突出,促使VS4有望成为电化学性能更为突出的锂离子电池电极材料.
