鸦胆子油乳联合阿帕替尼及替莫唑胺治疗复发性恶性脑胶质瘤
2021-05-21李梦依马青青杨玉丹
高 明,李梦依,马青青,史 昊,杨玉丹
(郑州大学第一附属医院肿瘤科,河南 郑州 450052)
脑胶质瘤临床常见,治疗难度大,手术难以切除干净,即使接受了术后标准放、化疗,仍然有大多数患者会出现复发,复发后疗效差,无标准治疗策略[1-3]。替莫唑胺作为抗肿瘤化疗药物,由于其穿透血脑屏障能力强,目前广泛应用于颅内肿瘤[4]。然而,替莫唑胺用于复发性胶质瘤的总体缓解率不甚理想。脑胶质瘤富含血管内皮生长因子(vascular endothelial growth factor,VEGF),并且过表达与高度恶性和预后不良相关[5-7]。因此,抗VEGF抗体如贝伐单抗,及抗血管内皮生长因子(vascular endothelial growth factor receptor,VEGFR)小分子抑制剂如阿帕替尼等已用于治疗神经胶质瘤患者[8]。替莫唑胺联用阿帕替尼对于复发性胶质瘤具有较好的临床疗效[9-10]。但是该联合疗法增加了不良反应,一定程度上影响了患者的生活质量。如何进一步提高复发性恶性脑胶质瘤的临床疗效,改善患者的生活质量,是亟待解决的问题。
鸦胆子油乳是从中药鸦胆子中提取的,其可以通过血脑屏障,目前已被应用于全身多种肿瘤的治疗[11-12]。本文主要分析鸦胆子油乳联合阿帕替尼及替莫唑胺治疗复发性恶性脑胶质瘤的临床疗效及对患者免疫功能的影响,并探讨其安全性,期待为复发性恶性胶质瘤患者提供更广阔的治疗空间。
1 资料与方法
1.1 临床资料入组2016年6月至2018年12月郑州大学第一附属医院经组织学确认为复发性恶性脑胶质瘤(WHO评定的Ⅲ级或Ⅳ级)患者52例,男32例,女20例,年龄20~66岁,平均年龄43岁。所有患者曾接受过手术及术后标准STUPP方案化疗同步放疗,术后平均复发时间8.5个月。所有患者通过磁共振成像(magnetic resonance imaging,MRI)证实存在可测量病灶。52例患者随机平分为2组,A组26例给予为替莫唑胺(北京双鹭药业)及阿帕替尼治疗,B组26例给予鸦胆子油乳联合替莫唑胺及阿帕替尼治疗。2组患者基线资料比较差异无统计学意义(P>0.05),具有可比性。该项研究已获批于本院伦理委员会,且所有患者均签署了知情同意文书。见表1。

表1 2组患者基线资料比较
1.2 治疗方法A组、B组患者均给予护胃、护肝、减轻水肿、止吐等治疗。A组治疗方案:替莫唑胺起始用量150 mg/(m2·d),连用5 d,28 d为1个周期;同时口服甲磺酸阿帕替尼500 mg/d进行治疗。B组治疗方案:在A组治疗方案基础上,服药当天联合应用鸦胆子油乳30 mL/d静脉滴注,定期监测血压,并每周复查血常规、尿常规、肝功能、肾功能。根据不良反应情况调整替莫唑胺及阿帕替尼用量。所有入组患者至少连续治疗2个周期后评价疗效。
1.3 纳入及排除标准纳入标准:既往已接受过手术、放疗和替莫唑胺化疗失败的患者;无严重的脏器功能损害;生存期预计>3个月。排除标准: 新诊断未接受标准治疗的胶质瘤; 近期出血史或脑卒中病史;患有严重系统性疾病;使用其他免疫制剂者。
1.4 评价标准根据WHO标准评价近期疗效:完全缓解(CR)、部分缓解(PR)、稳定(SD)、进展(PD)以及客观缓解率(以CR+PR计算)。生存评估应用疾病无进展生存期和总生存期,疾病无进展生存期和总生存期计算从胶质瘤复发后治疗开始。采用KPS评分评价患者的生活质量。不良反应参照WHO(1998年)抗肿瘤药物不良反应评价标准分为0~Ⅳ度。
1.5 免疫功能监测治疗前后分别抽取静脉血3 mL,利用流式细胞仪来进行分析T细胞总数(CD3+)、CD4+ T细胞数及CD4+/CD8+值。

2 结果
2.1 2组患者近期疗效比较治疗后,B组客观缓解率为69.23%,高于A组的38.46%,差异有统计学意义 (P=0.026)。见表2。
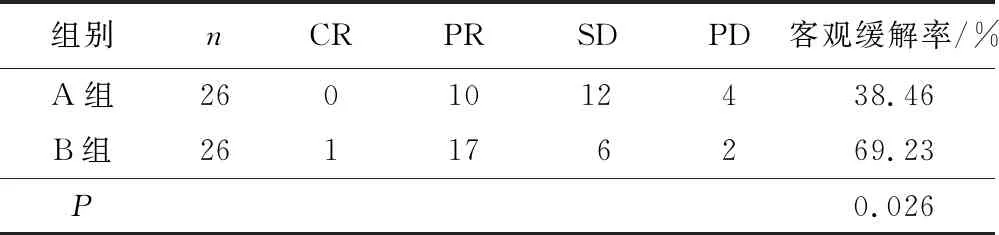
表2 2组患者近期疗效比较
2.2 2组患者治疗前后T细胞亚群变化比较治疗后,A组CD3+ T细胞、CD4+辅助性T细胞、CD4+/CD8+较治疗前显著降低(P均<0.05),而B组上述指标较治疗前显著升高(P均<0.05),且均显著高于A组(P<0.05)。见表3。

表3 2组患者治疗前后T细胞亚群变化比较
2.3 2组患者治疗前后KPS评分比较治疗后,B组KPS评分高于治疗前,且高于A组(P均<0.05)。见表4。

表4 2组患者治疗前后KPS评分比较
2.4 2组患者不良反应比较B组不良反应发生率低于A组,但差异无统计学意义(P>0.05),且不良反应轻微可耐受,对症处理后消失。见表5。

表5 2组患者不良反应比较
2.5 2组疾病无进展生存期和总生存期比较B组6个月疾病无进展生存率65.4%、中位疾病无进展生存期7.56个月(95%CI:5.72~9.40个月)、中位总生存期10.14个月(95%CI:8.59~11.70个月),均明显高于A组的46.2%、5.78个月( 95%CI:4.64~6.92个月)、8.73个月(95%CI:8.22~9.25个月)(P均<0.05)。见图1、2。

图1 2组患者疾病无进展生存曲线比较

图2 2组患者总生存曲线比较
3 讨论
胶质瘤是原发性中枢系统的恶性肿瘤,其复发率及死亡率极高。尽管术后常规进行放、化疗,但复发率仍然居高不下。替莫唑胺为新型烷化剂,易透过血脑屏障,口服吸收充分,是一种广谱抗肿瘤药物。替莫唑胺目前应用较为广泛,但由于肿瘤耐药性的产生,疗效令人不甚满意。迄今为止,复发性恶性脑胶质瘤尚无标准治疗方案。治疗策略的选择通常是在对患者的总体状况、复发性肿瘤的位置和先前治疗的有效性等进行全面评估后决定的。
VEGF、VEGFR在各种肿瘤细胞的表面过度表达,是影响血管生成的重要配体和受体。抗血管生成治疗能够改善肿瘤微环境,促使肿瘤血管正常化。这种作用可能是联合抗血管生成和细胞毒性疗法治疗获益的基础[13-14]。阿帕替尼和贝伐单抗均为抗血管生成剂,但前者比贝伐单抗具有某些优势。阿帕替尼是口服小分子酪氨酸激酶抑制剂,其靶标是VEGFR-2的细胞内结构域。与贝伐单抗不同,阿帕替尼可通过细胞内自分泌VEGF信号促进肿瘤细胞凋亡[15-16]。此外,阿帕替尼还可以抑制c-Kit、c-SRC、血小板衍生生长因子受体-β和MET,直接发挥抗肿瘤作用[17-18]。近年来,阿帕替尼联合化疗在复发性恶性脑胶质瘤患者中取得了一定疗效。Wang等[9]研究发现,阿帕替尼联合替莫唑胺组客观缓解率为45%(9/20),疾病控制率为90%(18/20),中位总生存期为9个月,显著优于单药阿帕替尼或者替莫唑胺组。我们课题组前期研究[10]发现,替莫唑胺密集方案联合阿帕替尼治疗复发性恶性胶质瘤,患者KPS评分等在短期内得到明显改善,瘤周水肿明显减轻,且较单纯应用替莫唑胺密集方案,疾病无进展生存期得到延长,总体生存期亦有所延长。
如何进一步提高复发性恶性脑胶质瘤的临床疗效,改善患者的生活质量,是亟待解决的问题。近年来,随着中医中药的不断发展,中药制剂在胶质瘤治疗的应用中越来越广泛,并取得了一定效果。鸦胆子油乳是从草本植物鸦胆子中提取的水包油剂,可完全通过血脑屏障并在颅内达到较高浓度。大量研究[19-20]发现,鸦胆子油乳注射液与放疗或化疗药物联用有减毒增效、提高机体免疫力的作用。胶质瘤的侵袭性来自恶性胶质瘤细胞的增殖和侵袭能力。研究[21]表明,鸦胆子油乳注射液可降低胶质瘤的侵袭性,发挥作用主要是通过PI3K/AKT信号通路影响增殖。鸦胆子油乳与替莫唑胺两药联用治疗胶质瘤能提高疗效及改善胶质瘤患者的生活质量[22]。
基于这些研究结果,我们认为患有复发性恶性脑胶质瘤可能受益于鸦胆子油乳联合阿帕替尼及替莫唑胺方案。据报道,三种药物最常见的不良事件为骨髓抑制、高血压、消化道反应、蛋白尿、手足皮肤反应,且安全性良好。这些与我们的研究结果相似。T细胞是免疫系统重要成分,可以将肿瘤相关抗原识别为“非自身”抗原或外来抗原,通过一系列的免疫激活反应,从而清除肿瘤细胞。其中CD3+、CD4+、CD4+/CD8+的动态平衡是维持正常机体免疫应答的基础。脑胶质瘤患者预后与自身免疫功能有着密切联系,CD3+ T细胞主要参与细胞免疫,CD4+ T细胞正向调节细胞免疫,CD4+/CD8+能反映细胞免疫功能状态。本研究结果显示,治疗后,三药联合患者CD3+ T细胞、CD4+ T细胞、CD4+ /CD8+均显著高于两药联合患者。并且,与治疗前相比,2种方案治疗后KPS评分均明显升高,三药联合者显著高于两药联合者。这说明鸦胆子油乳联合阿帕替尼及替莫唑胺治疗脑胶质瘤患者,可调节患者免疫功能,改善其生活质量。
总之,鸦胆子油乳联合阿帕替尼及替莫唑胺治疗复发性恶性脑胶质瘤患者,不仅可以显著提高客观缓解率,改善机体生活质量和免疫功能,还能明显提高疾病无进展生存期、总生存期,并且不良反应轻微。由于本研究的样本量较小,因此鸦胆子油乳联合阿帕替尼及替莫唑胺对复发性恶性脑胶质瘤患者的疗效和安全性也需要在更大样本人群中进行进一步研究。对于复发性恶性脑胶质瘤患者,鸦胆子油乳联合阿帕替尼及替莫唑胺可能成为一种安全有效的治疗策略。
