利用CLARITY技术实现珊瑚组织透明化的初步探索
2021-05-20赖庆娜林雪琳
赖庆娜,林雪琳,王 路
(闽江学院海洋研究院,福建 福州 350108)
组织透明技术(tissue optical clearing technique)是应用水溶性有机溶剂或亲水性试剂,通过浸泡、电泳、灌注等方式处理部分或者完整组织,利用高折射率介质匹配组织折射率,降低光散射,使组织达到光学透明的技术[1]。一般常用的组织透明技术包括CLARITY(clear lipid-exchanged acrylamide-hybridized rigid imaging tissue-hydrogel)/PACT、BABB、3DISCO、iDISCO、SeeDB、CUBIC、PARS等(表1)[2-3]。其中CLARITY技术于2013年被评为十大科学突破之一,引起了学术界对组织透明技术的广泛关注[4]。CLARITY技术是基于洗涤剂的脱脂作用,利用水凝胶包埋为组织提供物理框架支持,与蛋白质、核酸等生物分子形成共价连接,达到使细胞结构和分子信息得到有效保存的目的[5]。常规的CLARITY技术主要包括:1)制备以丙烯酰胺为主要成分的水凝胶;2)制备组织脂质清除液;3)通过器官组织脉管系统灌注水凝胶;4)组织标本水凝胶固定,避免气泡的形成;5)电泳主动清除或被动浸泡清除组织脂质,实现组织标本的透明化[6]。其设计思路清晰,实验步骤简便,应用样品多样,从小鼠神经组织到整体器官、斑马鱼[7]、死后人脑组织[8]等均有涉及。近年来,CLARITY技术被广泛应用到组织的深部成像。由于组织的深部微观结构对于一般的激光共聚焦显微镜来说是一个较难达到的深度,传统上要通过连续组织切片,并进行三维重构才能达到观察的目的。但是CLARITY技术却可以在“无损伤”的前提下实现深部微观观察,甚至已经有科学家利用CLARITY技术将整个小鼠做了透明化处理,包括脑,肝,肾,小肠等,得到了清晰的组织成像[9]。因此,CLARITY技术使大尺度的深度成像及自然状态下直接分析活体结构成为可能[10]。
珊瑚作为珊瑚礁生态系统的重要组成部分,由于其多样性和脆弱性而在全球环境变化的大背景下受到人们越来越多的关注。珊瑚属于腔肠动物门珊瑚虫纲,是腔肠动物门中最大的一个纲,有7 000余种,分为八放珊瑚亚纲及六放珊瑚亚纲[11]。目前珊瑚生态学研究的重点多集中在“共生”和“钙化”,对珊瑚显微结构的观察尤为重要,但是由于珊瑚外形多样、颜色鲜艳,大大加深了研究其内部结构的难度。传统方法通常采用解剖或者切片技术研究珊瑚的内部生理结构,但是这些方法常会破坏研究对象的完整性或细胞显微结构的连续性,不利于对整体形态结构的研究。而透明化技术可以在保持组织完整性的基础上达到显微成像效果,从而为珊瑚共生和钙化过程的理解提供新的研究思路。目前,组织透明技术在珊瑚研究领域逐步得到应用,主要是通过组织脱水对珊瑚进行透明成像并获得了珊瑚全生物体三维成像图[12],然而CLARITY技术在珊瑚研究领域中的尝试与应用目前尚未检索到相关报道。
本研究以软珊瑚中亲缘关系较近的两个种Xeniaumbellata和Xeniaelongata为实验对象,通过梯度调整CLARITY实验步骤中主要试剂的浓度,成功摸索出透明化珊瑚的最佳试剂浓度。透明化后的珊瑚组织可被清晰观察到珊瑚虫完整的水螅体及消化腔的组织结构,成功弥补了传统组织学研究方法中的一些不足,避免了切片间的信息丢失,为珊瑚在神经发育、胚胎发育、骨骼发育、共生关系等方面的研究提供了有效的技术支持。
1 材料与方法
1.1 珊瑚培养与鉴定
1.1.1 水族箱培养
将Xeniaumbellata和Xeniaelongata培养于循环海水水族箱中,设置水族箱中海水温度为(25±2)℃,盐度32%~35%,pH=8.1。珊瑚养殖使用hqi-10000K金属卤化物灯(BLV-Nepturion)提供有效光辐射强度(PAR)180 μmol-2·s-1,光暗周期为12 h∶12 h。
1.1.2 DNA提取、PCR与测序
取3~5个完整的珊瑚水螅体,使用液氮速冻后在研砵中将组织研磨均匀,研磨后的粉末加入DNA裂解液(10 mmol·L-1Tris pH 8.0;100 mmol·L-1EDTA pH8.0;0.5%SDS;100 μg·ml-1蛋白酶K),56 ℃下孵育48 h。用CTAB法提取DNA,并用DNA纯化富集柱(Zymo Research;Orange;CA;USA)进行核酸纯化。最后将纯化后的DNA溶解在10 mmol·L-1Tris-HCl缓冲液(pH8.0)中,使用NanoDrop(Thermo Fisher Scientific;Inc.;Wilmington;DE;USA)检测核酸浓度,置于-20 ℃储藏。
采用珊瑚特异型引物对大核糖体亚基(28S rRNA)进行扩增,正向引物为28S-Far(5’-CACGAGACCGATAGCGAACAAGTA-3’),反向引物为28S-Rar(5’-TCATTTCGACCCTAAGACCTC-3’)[13]。PCR扩增体系包括15μl带GE缓冲液的PCR Phusion Master Mix,2 μmol·L-1正向和反向引物,以及10ng DNA模板。反应流程为:94 ℃预变性1 min;34个循环(95 ℃变性30 s;56 ℃退火30 s;72 ℃延伸1 min);72 ℃延伸7 min。PCR结束后,进行2%浓度的琼脂糖凝胶电泳,检测产物长度。之后采用凝胶回收试剂盒进行产物纯化,并进行后续的测序。
1.1.3 分子鉴定与进化分析
将测序结果在NCBI中进行序列比对,得到与已知rDNA相似性较高的基因序列后下载。28S rDNA基因序列的选择基于Catherine[14]报道的系统发育树。使用CLUSTAL X进行序列比对并调整校准参数[15]进行手动编辑。使用GTR模型在PhyM服务器上进行了最大似然法系统发育分析(http://www.atgc-montpellier.fr/phyml/)。
1.2 方法
1.2.1 组织固定
取珊瑚组织样品,25 ℃下在7%氯化镁中孵育10 min[16],转移至4%多聚甲醛中4 ℃过夜,PBS溶液清洗3遍后,放入配置好的水凝胶缓冲液中,4 ℃低温孵育3 d。水凝胶缓冲液配比如下:4%多聚甲醛,浓度梯度分别为1%和4%的丙烯酰胺,0.05%双丙烯酰胺(丙烯酰胺:双丙烯酰胺比例为20∶1),0.25%VA-044(温度依赖型引发剂)溶于1xPBS中。
1.2.2 水凝胶形成
在水凝胶缓冲液上滴入矿物油以隔绝空气,然后将样品37 ℃水浴孵化3 h。
1.2.3 脂质的清除
温育后将组织浸没于含有SDS的硼酸缓冲液(0.2 mmol·L-1,pH 8.5)中,其中SDS浓度梯度分别为4%和8%,37℃恒温摇床孵育5 d,每天更换缓冲液。TPBS(1xPBS;0.1%Triton X-100)37 ℃恒温摇床孵育2 d,每天更换缓冲液[6]。
1.2.4 样品的保存
RIMS缓冲液保存样品,RIMS缓冲液配方[8]:20 mmol·L-1PBS缓冲液(pH7.5)15 mL ,碘海醇20 g,10%叠氮钠缓冲液250 μL。
1.2.5 组织观察与拍照
应用莱卡体视显微镜(Leica M165FC)观察并拍摄透明化前后的珊瑚水螅体。
2 结果与讨论
2.1 两种珊瑚的系统分类
以Catherine[14]报道的28S rDNA系统发育树为框架,获知本研究涉及的两种珊瑚分别属于不同的进化分枝(图1)。Xeniaelongata属于Clade X3进化分枝,Xeniaumbellata属于Clade X1进化分枝。
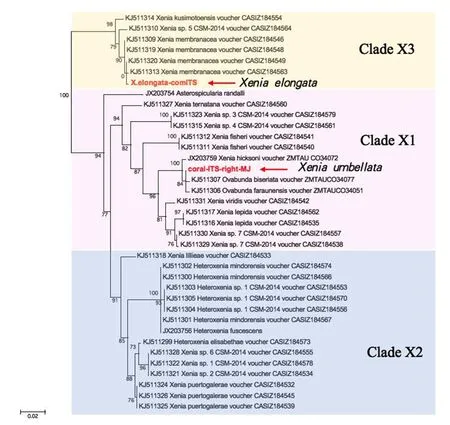
图1 Xeniidae-28srDNA家族的进化树Fig.1 The evolutionary tree of Xeniidae-28srDNA family
2.2 不同浓度的丙烯酰胺和SDS处理后珊瑚的透明化程度
组织透明化过程中,丙烯酰胺作为水凝胶主要成分,用以替代细胞骨架架构,保持样品的结构形状;SDS作为脂质清除液主要成分,用以去除细胞上影响大分子物质渗透和光线透过的脂质成分[17]。根据实验处理所需的两个关键溶液的不同溶度,设置了4个实验组,分别为1%丙烯酰胺与4%SDS、1%丙烯酰胺与8%SDS、4%丙烯酰胺与4%SDS、4%丙烯酰胺与8%SDS,再结合一组空白对照,摸索出透明化珊瑚的最佳试剂浓度。实验结果发现,不同处理组的珊瑚组织均出现了明显的透明化现象,其中Xeniaelongata的透明化效果比Xeniaumbellata的更为明显。透明化处理后,可以清晰地看到Xeniaumbellata单个透明化的触手以及排列清晰的刺细胞。对比空白组,可以发现CLARITY技术在透明化过程中可以较好地保持组织原有的形状,与空白对照相比,触手更加明显清晰,可以更清晰地观察到触手纹路甚至是表面的刺细胞结构。这两种珊瑚的透明化结果都表明,4%丙烯酰胺和4%SDS处理后的珊瑚外形保持和透明化程度最佳(图2)。

图2 不同比例透明液组织透明化效果Fig.2 Transparency effect of different proportions of transparent fluid
2.3 CLARITY处理后珊瑚的组织结构观察
水体中正常培养的Xeniaumbellata和Xeniaelongata在颜色形态上差距较大,Xeniaumbellata珊瑚体呈紫红色,形态上呈平铺的表覆形,近似于肥厚肉质珊瑚,触手较不明显。Xeniaelongata呈明黄色,水螅体呈树枝状分枝,触手明显。透明化后,虽然外形上二者仍存在较大的差异,但是可以发现其触手具有形似的刺细胞排列纹路,通常情况下这种微观结构需要通过组织切片后才能在共聚焦显微镜上观察到,但是组织切片会破坏组织完整性,即使进行三维图像重构,也可能造成空间信息丢失。
3 结论
CLARITY技术的核心是通过组织脱脂提高组织渗透性和透明效率,尤其是对脂质等高折射率介质的去除,所以第一步和第二步中水凝胶和脂质清除液的配制尤为关键。本次珊瑚组织透明化实验主要以被动浸泡的形式通过设置不同浓度的丙烯酰胺和脂质清除液SDS摸索最佳的组织透明化效果。成功透明化珊瑚Xeniaumbellata和Xeniaelongata后,可以较清晰地观察到珊瑚水螅体及消化腔的结构。同时,透明化后的两种珊瑚褪去了原有的颜色,可以更容易被观察到形态上接近的触手结构。CLARITY透明化技术能够弥补传统组织切片和图像重构的缺陷,在避免结构信息丢失的同时成功达到微观结构观察的目的,这或许可以为珊瑚甚至腔肠动物在三维重构、神经发育、骨骼生长、组织进化、共生关系等方面的研究提供一定的技术支持及研究思路。
