基于HPLC指纹图谱及多成分含量测定的薄荷 与留兰香药材非挥发性成分比较研究
2021-05-20田伟范帅帅甄亚钦高乐王梦牛丽颖
田伟,范帅帅,甄亚钦,高乐,王梦,牛丽颖
1.河北中医学院,河北 石家庄 050091;2.河北省中药配方颗粒技术创新中心,河北 石家庄 050091; 3.河北省中药材品质评价与标准化工程研究中心,河北 石家庄 050091
薄荷为唇形科植物薄荷Mentha haplocalyxBriq.的干燥地上部分,夏、秋二季茎叶茂盛或花开至三轮时采割[1]。薄荷属植物既是药食两用、历史悠久的清凉药草,又是重要的芳香油原料,在中医临床及中药制剂生产中应用广泛。全球薄荷属植物约有30个种,140多个变种,我国共有12种。薄荷属植物在世界各地广泛栽培,栽培种主要有两大类,一类是富含薄荷脑(menthol)的薄荷类[2],另一类为富含香芹酮(carvone)的留兰香类[3]。薄荷属中药的挥发性成分具有多种药理作用,2015年版《中华人民共和国药典》“薄荷”项下以挥发油为含量测定指标。但薄荷的传统入药形式以水煎、后下为主,鲜薄荷、鲜留兰香亦可直接食用,因此非挥发性成分的作用不容忽视。薄荷的非挥发性化学成分主要有黄酮类和有机酸类等,表现出良好的抗氧化能力[4-5]。对非挥发性成分进行控制,可更全面评价薄荷属中药的质量。
目前,指纹图谱与多指标含量测定的结合化学计量学方法已广泛用于中药材质量控制和相近品种区分与鉴别等方面[6-10],但关于薄荷与留兰香非挥发性成分的系统比较尚未见文献报道。本研究采用HPLC分析薄荷和留兰香的非挥发性化学成分,建立其HPLC指纹图谱。在此基础上,建立薄荷和留兰香药材中隐绿原酸、咖啡酸、橙皮苷、迷迭香酸、香叶木苷、香蜂草苷、蒙花苷和香叶木素8种成分的含量测定方法,并对16批薄荷药材和11批留兰香药材进行含量测定,进一步结合主成分分析和聚类分析,对薄荷和留兰香进行比较,以期为薄荷和留兰香药材的质量控制提供方法和数据支撑。
1 仪器与试药
LC-20A型高效液相色谱仪,日本岛津公司;Poroshell 120 EC-C18色谱柱(4.6 mm×250 mm,4 μm),美国安捷伦公司;TB-215D电子天平(十万分之一),BSA224S-CW电子天平(万分之一),德国赛多利斯;KQ-250型超声波清洗器(功率250 W,频率40 kHz),昆山市超声仪器有限公司。
对照品隐绿原酸(批号PY20170224,纯度99.8%),南京普怡生物科技有限公司;咖啡酸(批号110885-200102,纯度100.0%)、橙皮苷(批号110721-201818,纯度96.2%),中国食品药品检定研究院;迷迭香酸(批号111820-201404,纯度98.0%)、蒙花苷(批号111528-201509,纯度98.0%),成都曼斯特生物技术有限公司;香叶木苷(批号PS020083,纯度98.0%)、香叶木素(批号PS010395,纯度98.0%)、香蜂草苷(批号PS14081801,纯度98.0%),成都普思生物科技股份有限公司。甲醇、乙腈、乙酸为色谱纯,水为超纯水,其他试剂均为分析纯。16批薄荷药材(Y1~Y16)和11批留兰香药材(L1~L11)购自河北安国药材市场和安徽亳州药材市场,其中Y16、L9、L10、L11采收期为4月,产地见表1。经河北省药品检验研究院孙宝惠主任中药师鉴定,分别为唇形科植物薄荷Mentha haplocalyxBriq.的干燥地上部分和唇形科植物留兰香Mentha spicataL.的干燥地上部分,药材标本保存于河北省中药材品质评价与标准化工程研究中心。

表1 16批薄荷和11批留兰香药材来源信息
2 方法与结果
2.1 色谱条件
采用Poroshell 120 EC-C18色谱柱(4.6 mm×250 mm,4 μm),以甲醇(A)-乙腈(B)-5%冰醋酸(C)为流动相,梯度洗脱(0~15 min,8%→28%A,2%B;15~40 min,28%A,2%→15%B;40~65 min,28%A,15%→30%B;65~70 min,28%→8%A,30%→2%B),流速0.6 mL/min,柱温35 ℃,指纹图谱检测波长为305 nm,含量测定时隐绿原酸、咖啡酸、迷迭香酸、香叶木苷、蒙花苷、香叶木素检测波长为330 nm,橙皮苷、香蜂草苷为284 nm。
2.2 混合对照品溶液制备
精密称取隐绿原酸、咖啡酸、迷迭香酸、香蜂草苷、香叶木素对照品适量,分别加甲醇溶解并稀释,制备各自对照品贮备液;精密称取橙皮苷、香叶木苷、蒙花苷对照品适量,分别加DMSO溶解并稀释,制备各自对照品贮备液。分别精密吸取各对照品贮备液适量,置同一50 mL量瓶中,加甲醇稀释至刻度,摇匀,即得每1 mL含隐绿原酸2.95 μg、咖啡酸1.92 μg、迷迭香酸33.28 μg、香叶木苷259.41 μg、蒙花苷125.03 μg、香叶木素0.84 μg、橙皮苷24.72 μg、香蜂草苷7.06 μg的混合对照品贮备液。
2.3 供试品溶液制备
取药材粉末(过4号筛)约0.2 g,精密称定,置具塞锥形瓶中,加入含0.5%甲酸、30%DMSO的甲醇溶液25 mL,密塞,称定质量,超声处理(功率250 W,频率40 kHz)45 min,放冷,再次称定质量,用含0.5%甲酸、30%DMSO的甲醇溶液补足减失的质量,摇匀,过滤,取续滤液,即得。
2.4 指纹图谱建立与评价
2.4.1 精密度试验
取薄荷药材(Y1)粉末,按“2.3”项下方法制备供试品溶液,按“2.1”项下色谱条件,连续进样6次,记录色谱图,以香叶木苷峰(7号峰)为参照峰,计算各共有峰的相对保留时间和相对峰面积,结果各共有峰的相对保留时间RSD≤0.5%,各共有峰的相对峰面积RSD≤2.0%,表明仪器精密度良好。
2.4.2 稳定性试验
取薄荷药材(Y1)粉末,按“2.3”项下方法制备供试品溶液,按“2.1”项下色谱条件,分别于制备后0、3、6、12、20、36 h进样分析,记录色谱图,以香叶木苷峰(7号峰)为参照峰,计算各共有峰的相对保留时间和相对峰面积,结果各共有峰的相对保留时间RSD≤0.5%,各共有峰的相对峰面积RSD≤2.0%,表明供试品溶液在36 h内稳定性良好。
2.4.3 重复性试验
精密称取薄荷药材(Y1)粉末,分别取低(0.1 g)、中(0.2 g)、高(0.3 g)水平样品量,每个样品量3份,按“2.3”项下方法平行制备供试品溶液,按“2.1”项下色谱条件进样分析,记录色谱图,以香叶木苷峰(7号峰)为参照峰,计算低、中、高水平样品量指纹图谱中各共有峰的相对保留时间和相对峰面积,结果各共有峰的相对保留时间RSD≤0.5%,各共有峰的相对峰面积RSD≤3.0%,表明该方法重复性良好。
2.4.4 指纹图谱相似度评价
取16批薄荷和11批留兰香药材粉末,分别按“2.3”项下方法制备供试品溶液,按“2.1”项下色谱条件进行测定,记录色谱图。将所得薄荷HPLC图谱导入国家药典委员会《中药色谱指纹图谱相似度评价系统》(2012版)软件,以样品Y1图谱作为参照图谱,采用中位数法建立薄荷HPLC指纹图谱,经多点校正后,进行色谱峰匹配,生成薄荷对照指纹图谱。由于香叶木苷色谱峰(7号峰)分离情况较好、峰面积最大且保留时间居中,故以其为参照峰(S)。最终确定14个共有峰,通过与混合对照品溶液的色谱图比对,指认7个成分,分别为隐绿原酸(2号峰)、咖啡酸(4号峰)、橙皮苷(5号峰)、迷迭香酸(6号峰)、香叶木苷(7号峰)、香蜂草苷(9号峰)、蒙花苷(10号峰)。以薄荷对照图谱为参照图谱,导入11批留兰香药材的HPLC指纹图谱,经多点校正后,进行色谱峰匹配,计算相似度。16批薄荷和11批留兰香样品指纹图谱与薄荷对照图谱的相似度见表2。所有批次薄荷与对照图谱相似度均大于0.9,表明薄荷药材的质量较稳定;8批夏、秋两季采收的留兰香与薄荷对照图谱的相似度为0.890~0.996,表明留兰香药材与薄荷药材整体相似,个别批次存在较小差异;4月采收的留兰香与薄荷对照图谱的相似度较差,表明采收期对药材质量影响较大。16批薄荷药材和11批留兰香药材指纹图谱见图1、图2。

表2 16批薄荷与11批留兰香药材指纹图谱相似度分析结果

图1 16批薄荷药材HPLC指纹图谱叠加图及对照图谱

图2 11批留兰香药材HPLC指纹图谱叠加图及薄荷对照图谱
2.5 含量测定
2.5.1 线性关系考察
精密量取“2.2”项下混合对照品贮备液0.5、1、2、4、6 mL,分别置10 mL量瓶中,用甲醇稀释至刻度,摇匀,得到8种成分的系列浓度混合对照品溶液。分别精密吸取上述溶液及混合对照品贮备液10 µL,按“2.1”项下色谱条件测定,以对照品浓度为横坐标,峰面积为纵坐标,绘制标准曲线,计算回归方程和线性范围,结果见表3。隐绿原酸、咖啡酸、橙皮苷、迷迭香酸、香叶木苷、香蜂草苷、蒙花苷和香叶木素在各自的范围内呈良好线性关系。

表3 8种成分线性关系考察结果
2.5.2 精密度试验
精密吸取“2.2”项下混合对照品溶液10 µL,连续进样6次,计算隐绿原酸、咖啡酸、橙皮苷、迷迭香酸、香叶木苷、香蜂草苷、蒙花苷和香叶木素的峰面积RSD分别为0.61%、0.62%、0.24%、0.21%、0.22%、0.20%、0.24%、0.28%,表明仪器精密度良好。
2.5.3 稳定性试验
取同一份供试品溶液,分别于制备后0、3、6、12、20、36 h进样10 µL,测得隐绿原酸、咖啡酸、橙皮苷、迷迭香酸、香叶木苷、香蜂草苷、蒙花苷和香叶木素的峰面积RSD分别为1.06%、1.27%、0.53%、0.52%、0.54%、0.79%、0.50%、1.12%,表明供试品溶液在36 h内稳定。
2.5.4 重复性试验
称取同一份药材粉末,分别取低(0.1 g)、中(0.2 g)、高(0.3 g)样品量,每个样品量3份,按“2.3”项下方法平行制备供试品溶液,按“2.1”项下色谱条件进样,分别测定隐绿原酸、咖啡酸、橙皮苷、迷迭香酸、香叶木苷、香蜂草苷、蒙花苷和香叶木素的峰面积,计算其含量RSD分别为1.85%、2.23%、1.09%、2.59%、2.02%、1.85%、1.14%、1.80%,表明本方法重复性良好。
2.5.5 加样回收试验
取同一批已知含量的样品粉末,每3份为一组,每组精密加入对照品隐绿原酸、咖啡酸、橙皮苷、迷迭香酸、香叶木苷、香蜂草苷、蒙花苷和香叶木素的量相当于样品中各对照品含量的50%、100%、150%,按“2.3”项下方法制备供试品溶液,按“2.1”项下色谱条件测定,计算加样回收率及RSD。结果隐绿原酸、咖啡酸、橙皮苷、迷迭香酸、香叶木苷、香蜂草苷、蒙花苷和香叶木素的加样回收率分别为101.0%、100.9%、100.7%、100.7%、99.9%、102.0%、99.1%、99.4%,RSD分别为1.95%、1.90%、1.90%、2.19%、1.84%、2.34%、1.98%、2.15%,表明本方法准确度良好。
2.5.6 样品含量测定
取16批薄荷和11批留兰香药材粉末,分别按“2.3”项下方法制备供试品溶液,按“2.1”项下色谱条件进行测定,记录色谱图,计算样品中隐绿原酸、咖啡酸、橙皮苷、迷迭香酸、香叶木苷、香蜂草苷、蒙花苷和香叶木素的含量,结果见图3、表4。

图3 薄荷和留兰香药材中8种成分HPLC图

表4 薄荷和留兰香药材中8种成分含量测定结果(mg/g,n=2)
2.6 化学计量学分析
2.6.1 聚类分析
将16批薄荷和11批留兰香药材中8种成分的含量导入SPSS26.0软件进行分析,采用组间连接法,以欧氏距离平方为量度,进行聚类分析,结果见图4。4月采收的薄荷和留兰香药材与正常采收期样品差异较大,根据采收期可分为两类。
2.6.2 主成分分析
进一步采用主成分分析对薄荷和留兰香药材进行比较。前3个主成分累积贡献率>80%,三维散点图见图5。不同采收期的药材在图中分布离散,与聚类分析结果一致。

图4 薄荷和留兰香药材聚类分析图
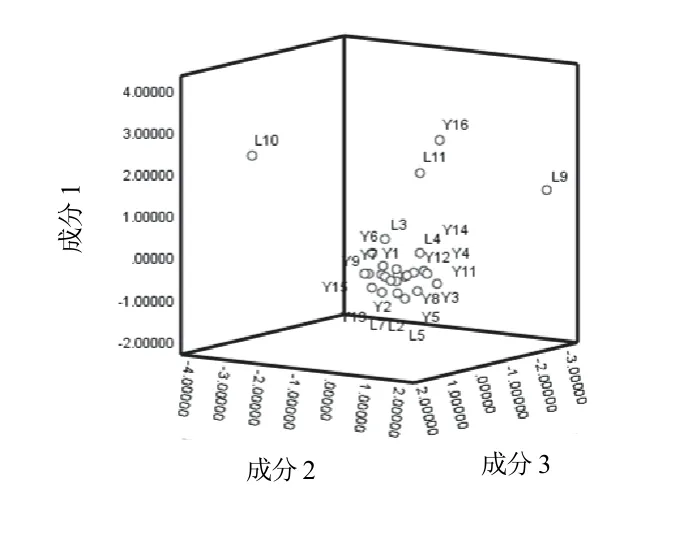
图5 薄荷与留兰香药材主成分分析
3 讨论
薄荷含有多种化学成分,非挥发性成分主要为黄酮类和有机酸类等。迷迭香酸等有机酸类及香叶木苷、蒙花苷等黄酮类在波长330 nm处有较大吸收,橙皮苷、香蜂草苷等二氢黄酮在波长284 nm处有最大吸收,而在波长330 nm处紫外吸收很弱,因此含量测定时选择波长284、330 nm同时监测。采用二极管阵列检测器对供试品溶液进行200~400 nm全波长扫描,结果在波长305 nm处色谱峰数目较多且分离度良好,因此选择305 nm作为指纹图谱的检测波长。
香叶木苷不溶于甲醇,橙皮苷和蒙花苷在甲醇中溶解度较低,故配制香叶木苷、橙皮苷和蒙花苷对照品贮备液时使用DMSO溶解稀释。供试品溶液制备时考察含不同浓度DMSO和不同浓度甲酸的甲醇溶液对有效成分提取率的影响,加入DMSO可显著提高橙皮苷、蒙花苷、香叶木苷和香蜂草苷的提取率,加入甲酸可提高隐绿原酸、咖啡酸和迷迭香酸的提取率,但甲酸浓度过高会降低橙皮苷、蒙花苷、香叶木苷和香蜂草苷的提取率。结果显示,含0.5%甲酸、30%DMSO的甲醇溶液提取效果最优。
目前,薄荷的市场需求量越来越大,留兰香是常见的薄荷伪品之一。关于薄荷和留兰香挥发性成分的区别已有较多文献报道[11-13]:薄荷挥发油的主要成分为薄荷脑,不含香芹酮;留兰香挥发油的主要成分为香芹酮,少含薄荷脑。此外,薄荷和留兰香还含有大量非挥发性成分。本研究建立薄荷和留兰香药材的HPLC指纹图谱,并比较了薄荷和留兰香中8种指标成分的含量。综合指纹图谱、多成分含量测定和化学计量学研究结果表明,薄荷和留兰香所含非挥发性成分大体相似,薄荷中黄酮类成分的含量略高于留兰香,而留兰香中有机酸类成分的含量略高于薄荷,但差异并不显著。
现代药理学研究表明,薄荷黄酮类成分具有良好的抗病毒、抗氧化、抗炎等作用,与其临床疗效关系密切[4-5]。此前研究认为薄荷中蒙花苷、橙皮苷含量较高,为主要的黄酮物质[14-15]。考虑薄荷药材的提取溶剂多为甲醇或甲醇水溶液,香叶木苷在甲醇和水中均不溶解,因此提取效率较低。本研究在提取溶剂中加入30%DMSO,与甲醇作为提取溶剂相比,对香叶木苷的提取效率提高近8倍,对橙皮苷和蒙花苷的提取效率提高3倍左右。薄荷药材中香叶木苷的平均含量高达12 mg/g,高于蒙花苷和橙皮苷含量之和。香叶木苷能增加静脉张力、改善静脉通透性、改善微循环、抗炎、抗肿瘤等,目前已被开发为化学药地奥司明[16]。“植物留兰香作为制备治痔疮病药的应用”已获得国家专利[17]。香叶木苷作为薄荷和留兰香中含量最高的黄酮类化合物,应与蒙花苷、橙皮苷共同作为重要的含量控制指标。
本研究采用HPLC建立薄荷、留兰香药材的HPLC指纹图谱,同时测定了薄荷和留兰香药材中隐绿原酸、咖啡酸、橙皮苷、迷迭香酸、香叶木苷、香蜂草苷、蒙花苷和香叶木素8种化学成分的含量。所建立的方法简便、准确,可为薄荷和留兰香药材非挥发性成分的控制提供方法参考和数据支撑。
有研究报道,部位、采收期、产地的不同均对薄荷药材中黄酮类成分含量有不同程度的影响[18]。本研究基于指纹图谱和多指标含量测定数据,综合聚类分析和主成分分析结果,表明薄荷与留兰香药材中非挥发性成分无明显差异,但采收期可能对薄荷和留兰香的质量产生较大的影响。不同采收期薄荷和留兰香中迷迭香酸的含量差异最大,4月采收的样品中迷迭香酸含量较夏秋采收者高近10倍。但本研究样本量较小,今后将对不同采收期薄荷和留兰香的非挥发性成分含量进一步研究。
