神经性毒剂诺维乔克类(Novichoks)化合物研究进展
2021-05-15肖静淞但国蓉赵远鹏邹仲敏
赛 燕,程 晋,肖静淞,叶 枫,但国蓉,赵远鹏,唐 禾,邹仲敏
(陆军军医大学军事预防医学系毒理学研究所,重庆 400038)
2018年,《化学与工程新闻》的一篇报道介绍了一个由3种诺维乔克类(Novichoks)化合物组成的神经性毒剂家族成员(图1),其中包括一种命名为A-234的化合物,该家族中其他结构相关的类似物被分别命名为A-230和A-232。至此,Novichoks化合物进入大众的视野。它们也被称为A类化合物(包括A-230,A-232和A-234等),是20世纪70年代至90年代研制的有争议的一类化学毒剂,大多数学者将之称为第三代神经性毒剂,前两代神经性毒剂分别为G类和V类化合物[1-3],也有部分学者称之为第四代神经性毒剂(第三代神经性毒剂为二元化学武器)[3]。
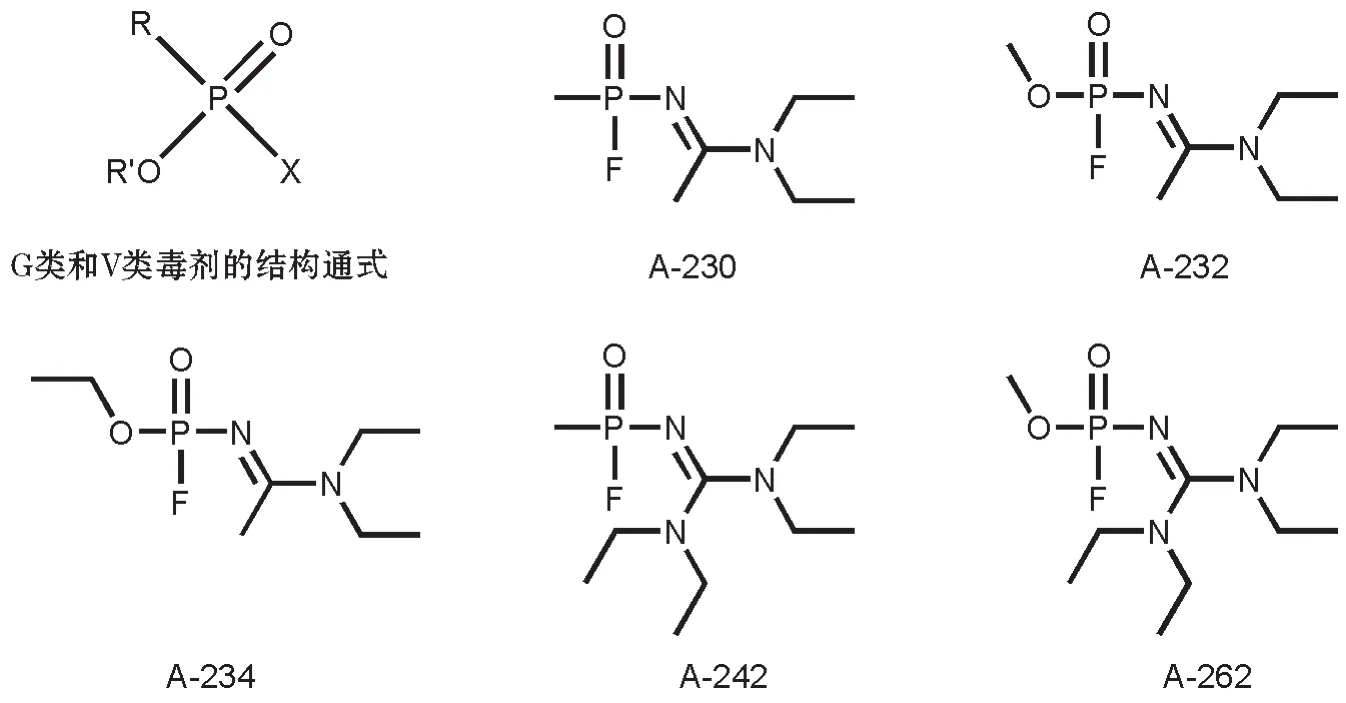
图1 Novichoks化合物可能的框架结构:磷氮原子直接相连[2,4].
1 Novichoks化合物的结构
由于前苏联FOLIANT计划的高度保密性,目前对Novichoks化合物的真实结构知之甚少,已有的文献中报道了许多推测性结构。据Mirzayanov[4]报道,前苏联国家有机化学和技术科学研究所(GOSNIIOKhT)合成的这类化合物是从G类和V类毒剂衍生出来的新一代神经性毒剂,其化学结构见图2。通过结构比对,其结构框架与《化学与工程新闻》中报道的基本一致。Harvey等[2]也报道了类似的Novichoks化合物的结构。上述报道的这类化合物在结构上与G类和V类神经性毒剂具有一定相似性,分子中都含有磷氧(P=O)双键,并且磷原子与氮原子直接相连(图1)。该系列合成并测试的第一个化合物代号为A-230(GOSNIIOKhT的内部报告中称之为84号物质),其本质上是一种沙林衍生物,其中的邻异丙基被乙酰基戊基取代[4]。A-230的毒性是RVX(俄罗斯VX,简称33号物质)的5~8倍。然而人们发现,A-230在-10℃时易形成结晶状态,在其液态时中加入N,N-二甲基甲酰胺可解决该问题。在化合物A-230之后,又陆续合成并测试了其衍生物 A-232,A-234,A-242和 A-262,其中A-232和A-234分别为A-230甲氧基和乙氧基的类似物,具有类似于RVX的毒性,且A-232和A-234具有易挥发和不易水解的特性。A-242和A-262分别是A-230和A-232的胍基类似物,可能是目前第一类合成的固态神经性毒剂。
与 Mirzayanov研究结果[4]不同,Hoenig[5]推测化合物A-230,A-232和A-234是氟膦酸盐(图2),除含有P=O双键外,其中氮原子不直接与磷原子结合,而是通过氧原子进而与磷原子相连接,并且它们在结构中含有若干卤素。目前也有学者基于FOLIANT计划部分数据推测,认为Novichoks化合物是含有二卤甲醛肟结构单元的有机磷酸盐,在结构上以具有P=O,P=S或P=Se键的有机磷为核心,以氟为离开基团,并含有其他有机基团,如光气肟基团等,以增强其毒性[1,6]。Ellison[7]和 Patocka[8]也报道了Novichoks化合物的类似结构,与Hoenig报道的这类化合物的框架结构基本一致。Chai等[9]报道,Novichoks化合物中的A-230和A-232的框架结构为磷原子与氮原子直接相连,与Mirzayanov报道基本框架结构一致;但A-234的结构框架为磷原子与氮原子之间通过氧原子相连,与Hoenig报道的框架结构基本一致。

图2 Novichoks化合物可能存在的框架结构:磷氮原子通过氧原子相连[1,5-6,8].虚线圈表示G类、V类和A类毒剂的结构通式.
虽已合成数以百计的Novichoks化合物,但可能只有33号物质、A-230、A-232、A-234、Novichok-5和Novichok-7已武器化[4,10]。目前认为最可能武器化的Novichoks化合物被认为是二元的,如A-234,据报道其二元毒物分别为氰甲烷和低效有机磷[7]。
2 Novichoks化合物的理化性质
关于这类化合物的理化性质,目前公开报道的信息不多。但G类和V类毒剂的一个显著缺点是其持久性和挥发度之间的不平衡性。首先,G类毒剂具有高挥发性和低持久性的特点。其次,V类毒剂挥发性虽和G类毒剂相比有所降低,但通过蒸气的直接作用降低了活性消除的效率[11-12]。因此,军事化学家的目标是研究在空气和水介质中挥发性、密度和稳定性等理化性质相对均衡的新一代化合物。Nepovimova等[1]和Kloske等[13]认为,这类化合物已基本消除了G类和V类化合物的几个显著的缺点。另外,A-230,A-232和A-234和其他神经性毒剂一样是液体,而A-242和A-262是目前已知的在室温条件下为固态的一类神经性毒剂[4]。表1总结了G类、V类和Novichoks化合物的部分结构和理化性质参数,并列出了使用chemicalize服务器计算的对数P值[14-15]。G类、V类和Novichoks化合物蒸气压值都比较低,表明它们在环境中适度持久,而对数P的估计值表明,这类化合物具有相当高的亲脂性,A-230,A-232和A-234的对数P值分别为2.14,2.55和2.97,提示其被身体吸收的能力较强。目前关于A-230,A-232和A-234理化性质存在争议比较大的是其沸点,多数学者认为其沸点高于G类和V类毒剂,但也有少数学者认为其沸点低于G类和V类毒剂。

表1 Novichoks化合物及G类和V类化合物的理化性质[1-2,4,14-15]
神经性毒剂水解酶又被称为有机磷酸脱水酶(organophophorus acid anhydrolase,OPAA),已被证明可催化G类毒剂的水解,在较小程度上催化V类毒剂的水解[16-17]。OPAA对这类化合物的催化活性大约比其对G类毒剂的活性低2~3个数量级,比其对V类毒剂的活性高2个数量级[16-18]。Harvey等[2]报道,OPAA对这类化合物的催化效率在1×104~1×105mol-1·min-1之间,其Kcat/Km值 A-230>A-232>A-234。表2显示了以Novichoks化合物为底物的OPAA酶动力学常数[2]。另外,Harvey等[2]用氟电极测定了G类化合物及这类化合物中的A-230,A-232和A-234在50 mmol·L-1双(2-羟乙基)氨基(三羟甲基)丙烷缓冲液、pH值为7.2、温度为25℃下的水解速率(结果见表2)。该类化合物水解速率较低,尤其是A-234可使水源长期染毒。Novichoks化合物在25℃下的水解速率比G类毒剂低2~3个数量级,比V类毒剂低0~2个数量级。A-230是最不稳定的Novichoks化合物,其次是A-232,然后是 A-234[19]。而根据 Ellison[7]的报道,这类化合物可水解产生HF、HCl、HCN和剧毒肟类化合物[7]。
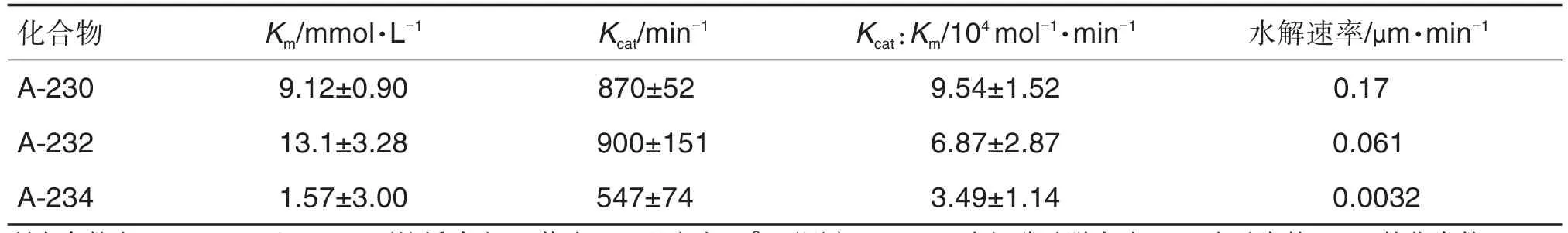
表2 以3种Novichoks化合物为底物的OPAA动力学常数和水解速率[2]
Jeong等[18]通过量子力学计算了这类化合物和已知部分神经性毒剂自然布局分析电荷,结果显示Novichoks化合物中的磷原子的正电荷均大于已知的G类和V类神经性毒剂,因此在化学性质上可能更活泼,更易在体内对一些酶活性中心的丝氨酸羟基进行亲核性攻击,发生酰化反应。Novichoks不同化合物之间的自然电荷布局分析(natural charge population analysis,NPA)电荷差别不是很明显,目前通过不同的分析方法显示,A-230的自然布局分析电荷最大,具有较高的反应活性。同时,A-230也是所有这类化合物中P=O键距离最短的一个化合物,进一步提示,A-230具有较高反应活性的结构基础。
3 Novichoks化合物的毒性
目前关于这类化合物的毒性尚无可靠数据,但一致认为其毒性远远大于V类毒剂,可能是V类毒剂毒性的几倍,而且既可用于一元化学武器也可用于二元化学武器。它们为致死性毒剂,接触这类化合物是致命的,除非进行有效的防治。根据Mirzayanov[4]和其他一些文献[6-7]报道(表3),A-230毒性是RVX的5~8倍,RVX的毒性与VX相似,而A-232的毒性比梭曼高10倍,而且A-242和A-262是A-230和A-232的“超高”毒性衍生物,但目前尚无相关的进一步解释。根据相关信息,Kuca等[20]估算了这些化合物的人吸入半数致死浓时积(LCt50)和皮下注射半数致死剂量(LD50)值(表3),Novichoks类化合物的毒性要远远高于已知的G类和V类神经性毒剂。Mirzayanov[4]虽然未报告A-234的毒性,但考虑到A-234的结构与A-232具有一定的相似性,推测A-234和A-232应具有类似的毒性,而且他认为A-242和A-262具有“超高毒性”,比A-230和A-232毒性更大,可能是这类化合物当中毒性最强的神经性毒剂。然而,由于A-242和A-262是固态,这一物理性质使得它们很难武器化,大大削弱了其军事意义。但A-242和A-262作为胍类似物的衍生物,很可能在水中具有良好的溶解性,非常适合污染水源,造成水源的长期染毒[2]。
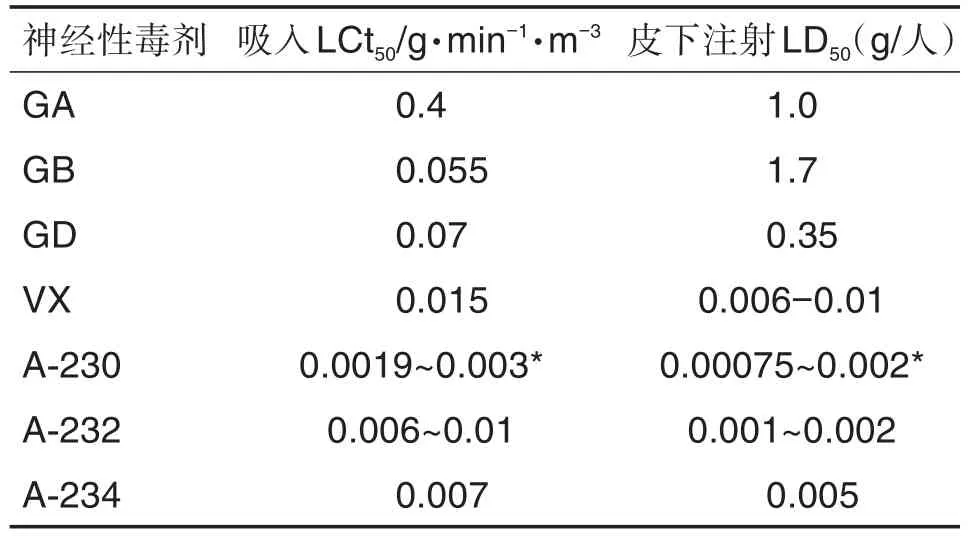
表3 Novichoks、G类和V类化合物对人吸入半数致死浓时积(LCt50)和皮下注射半数致死剂量(LD50)[5-7,20]
4 Novichoks化合物的中毒机制
在生理条件下,乙酰胆碱酯酶(acetylcholines⁃terase,AChE)的活性部位丝氨酸-组氨酸-谷氨酸三联体水解神经递质乙酰胆碱(acetylcholine,ACh),从而降低ACh在神经元突触间隙和神经肌肉连接处的浓度[21]。G类和V类神经性毒剂是通过与ACh相同的方式共价结合AChE,G类和V类神经性毒剂中的带有正电荷的磷原子攻击AChE的酯解部位带负电荷的丝氨酸羟基,丝氨酸残基发生膦酰化作用,膦酰化酶失去水解ACh的功能,大量的ACh在突触间隙蓄积,导致中毒。
Novichoks化合物的作用方式与G类和V类神经性毒剂的作用方式相似,也是对AChE的不可逆性抑制。首先,其分子结构中含有磷原子,在体内能对AChE活性中心的丝氨酸羟基进行亲核性攻击,导致AChE分子上导入酰基,发生酰化作用形成膦酰化酶,同时伴有离开基团的脱落,胆碱酯酶(cholinesterase,ChE)被膦酰化后,失去水解ACh的能力[1]。但由于这类化合物自身的构效关系的影响,磷原子与AChE丝氨酸之间形成的共价键较为稳定,膦酰化酶的自发水解速度极为缓慢,从数小时到数天不等[22]。
Jeong等[18]认为,由于Novichoks化合物中磷原子的正电荷数超过其他已知神经性毒剂的磷原子,这意味着这类化合物更容易对位于AChE催化位点的丝氨酸残基进行亲核性攻击而发生酰化反应,进而导致它们的毒性较G类和V类毒剂更强。尽管这类化合物之间的电荷数差别不大,但不同的计算方法都显示A-230的电荷数是最多的,且其P=O键的距离[18]在这类化合物之中最短,因此A-230的动力学反应性最高。
神经性毒剂抑制ChE的重活化剂是肟类化合物。ChE活性被重活化后,会形成磷酸化肟(POX)进而重新抑制ChE,其抑制作用可能比神经性毒剂更强,只是磷酸化肟相对不稳定[23]。有学者认为,磷酸化肟与Hoenig[5]报道的Novichoks化合物在结构上存在相似性(图3),因此,Novichoks化合物-AChE加合物内的=N-O-键的快速水解可能导致所谓的酶的老化形式,其中磷氧阴离子与质子化组氨酸形成盐桥,从而形成稳定的共轭物,加速中毒酶的老化,而且一旦老化发生,乙酰化酶就永久失活,无任何药物可再次恢复其活性[20,24-25]。实验研究也显示,Novichoks化合物抑制ChE后迅速出现老化现象,A-230的老化半衰期与梭曼接近,为2~4 min[26],该实验结果进一步证明了上述理论假设。

图3 A-230,A-232和A-234与磷酸化肟(POX)结构比较.虚线图环绕区域所示POX和Novichoks化合物结构上的相似部分:均含有磷氧双键,磷原子与氮原子通过氧原子相连.
另外,Novichoks化合物结构上含有的特异性肟基中的碳带有正电荷,这种带有高正电荷的碳原子使Novichoks化合物更易受到AChE空间周围的一系列亲核性物质〔水和(或)氨基酸残基〕的攻击,从而加速酶的老化和变性[26]。因此,使用肟类化合物(如解磷定)作为解毒剂对抗这类化合物中毒可能不会有效,反而导致其毒性增加[18]。Jeong等[18]根据水、羧酸盐或胺(赖氨酸残基)是否会发生亲核性作用,提出Novichoks化合物几种可能的老化或酶变性机制。具体来说,它们与水分子的反应产生氨基磷酸盐和二氧化碳,而在与丝氨酸、苏氨酸或酪氨酸的反应中,其活性部位连接氨基酸进而抑制酶的活性。而有水存在的情况下,这类化合物与天冬氨酸和谷氨酸的反应产生氨基酸磷酸盐和CO2,而与赖氨酸的反应导致交联和氨基磷酸盐的形成。由于这类化合物与AChE结构中的丝氨酸结合后形成的类光气肟结构的高反应活性,因此,所有上述这些反应代表的新型老化机制被认为是非常迅速的[18]。
虽然,Novichoks化合物主要的中毒机制是抑制AChE,导致该酶失活,引起胆碱能神经功能紊乱的临床表现,与G类和V类毒剂具有一致性。但Jeong等[18]通过计算出的NPA电荷和静电势进一步揭示了其高毒性的最可能原因,即这类化合物与AChE丝氨酸残基结合后,在其第二亲电部分可再次发生亲核反应(即其与AChE存在着二次反应),这一反应被称为Novichoks化合物新型老化机制,区别于G类和V类神经性毒剂。
5 Novichoks化合物中毒的临床表现
Novichoks化合物抑制AChE,导致蓄积的ACh持续作用于ACh受体并产生胆碱能症状。症状的严重程度主要取决于进入体内的毒物的量和类别。一般可分为毒蕈碱样症状、烟碱样症状和中枢神经系统症状。毒蕈碱样症状主要表现为瞳孔收缩、腺体大量分泌、排尿、排便、发汗和呕吐等。烟碱样症状包括骨骼肌肌束震颤、肌力减退、肌痉挛、松弛型肌麻痹(包括呼吸肌麻痹)等。中枢神经系统症状主要表现为易怒、头晕、疲劳、嗜睡、癫痫、昏迷,严重的出现呼吸抑制[22,27]。不过,Novichoks 化合物的中毒症状与G类和V类毒剂中毒也有一些不同之处。除了直接的胆碱能作用外,Novichoks化合物还可作用于周围感觉神经元,长时间或高剂量地接触会导致周围神经中毒症状。这类化合物对外周神经的毒性作用是其与常见的有机磷酸酯类化合物临床表现的主要差异[9-10]。在一份报告[28]中认为,Novichoks化合物中毒的症状实际上是无法治愈的,接触这种毒剂的人基本上最终可能会致残。报告描述了Novichoks化合物中毒后出现的所谓的迟发性神经毒性,其特征是神经系统严重破坏,表现为中毒后1~3周内出现瘫痪[28],甚至在中毒若干年后,出现肝硬化、三叉神经炎和癫痫。
6 Novichoks化合物中毒的救治
Novichoks化合物中毒的一般治疗方案包括药理学方法和非药理学方法。非药理学方法包括供氧、复苏和洗消。目前尚无关于这类化合物特异性的防护和洗消策略的报道,而已有的防护服可直接用于防护这类化合物。除个人防护外,与任何接触神经性毒剂的情况一样,对中毒人员以及应急人员直接快速洗消对于防止继续中毒非常重要[7]。为达到洗消的目的,不同的国家在国家标准的基础上采用了不同的洗消剂和不同的洗消方法。其中,最为重要的应是个人和现场洗消。染毒后立即进行皮肤洗消可提高伤员的生存率,防止与中毒相关的有害影响的继续发展,而现场洗消可防止医务人员等急救人员中毒。尽管大多数神经性毒剂在水中水解缓慢,但提高洗消溶液的pH值可能会加快水解速度。有学者认为,Novichoks化合物水解可产生氢氟酸、盐酸、氰化氢和下游肟类化合物,这些肟类化合物还可继续对暴露的个体产生胆碱能效应,导致中毒[7],因此也需要慎重。常用的活性皮肤去污乳液含有Dekon139和少量2,3-丁二酮单肟[14],可能会具有一定的效果。关于去污洗消,根据其与其他神经性毒剂的结构相似性,Novichoks化合物可被碱液(按NaOH或NaCO3质量计>10%)破坏。
目前尚无关于这类化合物专一性解毒剂的报道。部分学者认为,由于其中毒机制与G类和V类神经性毒剂存在相同之处,都可通过抑制AChE引发胆碱能综合征[1,22,27]。因此,可采用多种药物联用的方法进行优先防治,包括:①应用抗胆碱能药物(主要是阿托品)拮抗ACh受体,阻止突触间隙内ACh对ACh受体的持续激动作用,减轻中毒症状。因此,与其他神经性毒剂一样,接触Novichoks化合物后临床医生应立即静脉注射阿托品,直到心动过缓、支气管漏和支气管痉挛(如毒蕈碱症状)等症状消失。②应用抗惊厥药(通常是地西泮或其前体药物),对抗胆碱能综合征的影响;地西泮可同时预防和治疗神经性毒剂中毒引起的癫痫发作。③使用以肟类化合物为代表的重活化剂活化ChE[26],这一方案虽存在争议,但仍有部分学者认为如1-甲基-2-吡啶甲醛肟盐(2-PAM)和HI-6能在一定程度上对抗Novichoks化合物中毒[29]。静脉注射2-PAM或双氧嘧啶的抗毒药物治疗可恢复AChE的活性,但肟类化合物解毒剂(如2-PAM或其他肟)必须在中毒酶老化过程发生前使用[28]。
上述3种治疗方案用于Novichoks化合物的治疗目前也存在一定的争议。虽然其中毒症状类似于G类和V类神经性毒剂[13],但其中毒机制除了抑制AChE之外,可能会引起不可逆性的神经病变。因此,用于对抗麻痹和神经递质的抗毒剂治疗Novichoks化合物中毒的效果可能较差或无效[1]。而且有学者认为,其毒性似乎主要并不依赖于AChE的抑制作用。因此,一些学者认为反应性肟如2,3-丁二酮单肟酸钾(仅在欧洲可用)目前可能是Novichoks化合物抗毒治疗的首选药物[29]。然而,部分研究者认为,肟类药物可能对Novichoks化合物中毒救治无效,因为重活化剂难以对其和ACh活性位点相互作用形成的中间产物发动亲核性攻击,发生重活化作用[30]。此外,由于其与AChE形成的中毒酶更易发生老化作用,以及磷原子上部分正电荷的衰变作用。因此,目前可用的重活化剂(如解磷定、双复磷和HI-6)为代表的亲核性试剂几乎不会攻击这些磷原子。从治疗的角度来看,重活化Novichoks化合物与AChE作用后形成中毒酶的抗毒策略可能无效[13]。部分研究者认为,针对这类化合物中毒,目前唯一有效的治疗方法可能是对症治疗或服用所谓的生物清除剂,如丁酰胆碱酯酶。丁酰胆碱酯酶作为一种外源性的分子或酶,可非选择性地结合进入患者血液中的游离Novichoks化合物,使后者无法达到组织与其靶点AChE作用产生中毒的临床症状[31]。一般来说,生物清除剂属于预防策略之一,预防效果好于治疗用药。但如果在病因治疗无效的情况下,Novichoks化合物中毒后可考虑使用生物清除剂。此外,因为判定中毒毒剂的种类并选择适当的治疗方法需要一定的时间[31],且丁酰胆碱酯酶作为一种能对所有类型的神经性毒剂进行解毒的候选药物。因此,丁酰胆碱酯酶可作为一种广谱的抗毒治疗药物用于Novichoks化合物中毒[1]。
7 结语
Novichoks化合物作为第三代神经性毒剂,不应被视为一个独立的化学战剂类别。在讨论神经性毒剂化学武器公约时,Novichoks化合物应以与G类和V类等其他神经性毒剂相同的方式对待。将其一并列入《化学武器公约》的毒性物质清单,这一点可能尤为重要。由于其毒性较大,也有必要研究其抗毒药物和快速的检测方法。
