天青石锶废渣氯化钡浸出及其动力学研究
2021-05-15何宇刘作华栾进华崔志伟张雄毛玲玲陶长元
何宇,刘作华,栾进华,崔志伟,张雄,毛玲玲,陶长元
(1 重庆大学化学化工学院,重庆400044; 2 煤矿灾害动力学与控制国家重点实验室(重庆大学),重庆400044;3 重庆地质矿产研究院,重庆400044)
引 言
天青石的主要成分为SrSO4,主要用来制备生产碳酸锶[1]。天青石采用碳化法[2-5]制备生产碳酸锶的工艺过程中会产生大量的废渣,废渣中锶主要存在形式为硫酸锶、碳酸锶、硅酸锶等水不溶锶[6]。大量堆存的锶废渣不仅会占用大量土地,还会造成水质污染[7]、空气污染[8]等环境问题。目前锶废渣的主要利用途径有铺路[9]、水泥配料[10-11]。将锶废渣用于铺路和水泥配料,虽然解决了锶废渣的堆存问题,但锶废渣中高达20%的锶资源并没有得到有效利用[12],造成了锶资源的浪费[6]。
Carrillo 等[13]、Castillejos 等[14]研 究 了 溶 液 中Na2CO3将天青石中的SrSO4直接转化为SrCO3过程的动力学,发现以CO32-通过碳酸锶产物层空隙的扩散过程为限速阶段,能很好地描述转化过程的动力学,证明了该过程符合未反应核缩模型。碳酸铵[15]也能将天青石中的SrSO4直接转化为SrCO3。转化生成的SrCO3可用来制备SrCl2[16]、Sr(NO3)2[17]等水溶性锶盐,SrCl2经除杂[18-19]后可用来制备高纯碳酸锶、锶铁氧体[20-21]等,也能用于细胞克隆[22]、鱼生存环境影响模拟[23]、生物活性复合配合物制备[24]等方面,浸出后的二次锶渣还可用于去除废水中的铬[25]、磷[26]等,以实现天青石锶废渣的资源综合利用。
鉴于利用天青石锶废渣制备水溶性锶盐SrCl2需先经过碳酸盐转化为SrCO3,再盐酸浸出得到SrCl2,要经过两步反应,工艺过程复杂。又Ksp(SrSO4)/Ksp(BaSO4)=2.909×103,使SrSO4与BaCl2反应能生成BaSO4和SrCl2,理论上具备可行性,故本文考虑先用盐酸预处理天青石锶废渣,再以BaCl2作为浸出剂,通过一步浸出来制备SrCl2,并探究浸出过程动力学。
1 实验材料与方法
1.1 材料
天青石锶废渣,重庆大足某锶盐企业提供,天青石制备生产碳酸锶后余下的废渣。将其在80℃烘箱中烘焙48 h 去除水分,冷却后经球磨机处理,过筛,得粒径为0.074 mm 锶废渣。实验采用分析纯试剂及去离子水。
1.2 实验与方法
1.2.1 预处理及BaCl2浸出实验 往0.074 mm 锶渣中加入适量稀盐酸,搅拌反应后,过滤,往滤渣上滴加稀盐酸,无气泡产生即可,洗涤后烘干,研磨后得酸处理后锶废渣。
取适量酸洗后锶废渣,在搅拌下反应,分别探究浸出时间、浸出温度、BaCl2/SrSO4摩尔比、初始液固比对锶浸出率的影响。
1.2.2 分析仪器 X 射线衍射仪,XRD-6000 型号,日本岛津制作所;X 射线荧光光谱仪,ARL Perform’X,美国赛默飞世尔科技;场发射扫描电镜,FEI Insperct F50,日本电子株式会社;X射线光电子能谱仪,ESCALAB250Xi,美国赛默飞世尔科技;电感耦合等离子体发射光谱仪,iCAP 6300 Duo,美国赛默飞世尔科技。
1.2.3 锶浸出率的计算方法 用ICP-AES 测定锶的含量[27]。浸出率的计算公式:

式中,X 为锶浸出率,%;m 为浸出液中锶的质量,g;M 为天青石锶废渣的质量,g;W 为酸处理后天青石锶废渣中锶的含量,%。
2 结果与讨论
2.1 酸处理前后锶废渣的XRD表征
酸处理前锶废渣中锶的主要存在形式为SrSO4,还存在SrCO3、SrTiO3等形式,锶废渣中还含有SiO2、Ca(OH)2、Ca(Fe,Mg)(CO3)2等物质;酸处理后,锶废渣中的Ca(OH)2、Ca(Fe,Mg)(CO3)2被除去,残留固体中主要存在物质为SrSO4、SiO2(图1)。Ca(Fe,Mg)(CO3)2的去除,可减少浸出剂BaCl2的用量,也能避免生成的BaCO3覆盖在SrSO4表面,阻碍反应的进一步进行[14]。

图1 锶废渣酸处理前后的XRD谱图Fig.1 XRD patterns of strontium waste residue before and after acid treatment
2.2 酸处理前后锶废渣的XRF表征
酸处理前锶废渣中的锶含量为19.04%,钙、硅、硫、镁的含量分别为13.56%、9.38%、6.61%、4.29%,酸处理后锶废渣中的锶含量为17.88%,钙、硅、硫、镁的含量分别为2.80%、17.30%、6.12%、1.43%(表1)。酸处理前后,锶废渣中的Sr、Ca、Mg、S 等元素含量都有所下降,锶含量降低是酸处理过程中SrCO3等被浸出,Ca、Mg 含量的下降,有利于后续锶的浸出。

表1 酸处理前后锶废渣组成Table 1 Composition of strontium waste residue before and after acid treatment
2.3 酸处理前后尾渣的SEM表征
通过扫描电镜观察酸处理前后锶废渣的表面形态(图2),可以发现酸处理前锶废渣容易结块,团聚现象明显,但酸处理后锶废渣无结块,且团聚现象有所改善。酸处理后锶废渣比表面积增大,与浸出剂BaCl2的接触面积越大,使反应更加充分。
2.4 酸处理后锶废渣的EDS表征
锶废渣的EDS 表征表明尾渣颗粒表面含有O、Si、Mg、Mo、S、Fe 等元素(图3),说明尾渣颗粒表面包裹着一层SiO2,SrSO4在颗粒内部,BaCl2必须通过锶废渣颗粒表面空隙进入到颗粒内部才能与SrSO4发生反应。
2.5 不同浸出条件对锶浸出率的影响
2.5.1 浸出时间、浸出温度对锶浸出率的影响 不同浸出温度、浸出时间对锶浸出率的影响如图4 所示。总体来看,在相同浸出温度下,延长浸出时间,锶浸出率增大。延长浸出时间到120 min 时,再延长浸出时间,锶浸出率稍有增大,但能耗增加,经济可行性降低。故选取的浸出时间为120 min。
由图4可知,相同浸出时间下,锶浸出率随着浸出温度的升高而增大。在浸出温度低于40℃下,锶浸出率较低,且随着时间的延长增大缓慢;浸出温度从40℃增大到80℃,锶浸出率迅速增大;浸出温度高于80℃,锶浸出率增大速率减缓。浸出温度100℃、浸出时间180 min的条件下,锶浸出率最大为70.52%。

图2 酸处理前后锶废渣的SEM图Fig.2 SEM images of strontium waste residue before and after acid treatment

图3 酸处理后锶废渣的EDS表征Fig.3 EDS characterization of strontium waste residue after acid treatment
在碱性水热条件下,CO32-会取代SrSO4中的部分或全部SO42-[28-29],同理Ba2+会取代SrSO4中部分或全部的锶[30]。在浸出温度较低时,Ba2+会取代SrSO4中部分的锶,导致锶部分被浸出,随着浸出温度的升高,反应体系活化分子数量增加,体系中的Ba2+运动加剧,反应进行得更迅速更彻底[31-32],此时Ba2+取代SrSO4中锶的比例增加,提高了锶的浸出率。又100℃下水会沸腾,能耗太大,故选取的浸出温度为90℃。
2.5.2 BaCl2/SrSO4摩尔比对锶浸出率的影响 不同BaCl2/SrSO4摩尔比对锶浸出率的影响如图5 所示。由图5 可知,BaCl2/SrSO4摩尔比增大,锶浸出率随之增大。当BaCl2/SrSO4摩尔比为2.0 时锶浸出率最大为68.79%,是因为随着BaCl2/SrSO4摩尔比的增大,反应体系中的Ba2+浓度更高,Ba2+更容易扩散进入到废渣颗粒内部,扩散进入固体颗粒内部的Ba2+增多,Ba2+取代SrSO4中部分的锶的取代量增大,锶浸出率增大。BaCl2/SrSO4摩尔比由1.8 增大到2.0,锶浸出率缓慢增大,是因为Ba2+取代SrSO4中部分的锶后生成了BaSO4,BaSO4会覆盖在SrSO4表面,在一定程度上阻碍了Ba2+与SrSO4的进一步反应,导致残余的锶很难被浸出,从而降低了锶浸出率的增大速率。选取的BaCl2/SrSO4摩尔比为2.0。

图4 浸出时间、浸出温度对锶浸出率的影响Fig.4 Effects of leaching time and leaching temperature on strontium leaching ratio
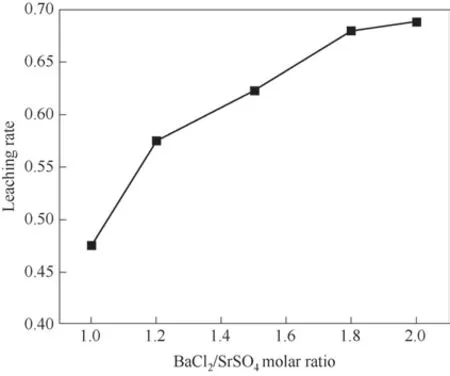
图5 BaCl2/SrSO4摩尔比对锶浸出率的影响Fig.5 Effect of BaCl2/SrSO4 molar ratio on strontium leaching rate
2.5.3 液固比对锶浸出率的影响 不同液固比对锶浸出率的影响如图6 所示。由图6 可知,随着液固比的增大,锶浸出率也增大。增大液固比等同于增大液相主体和反应界面之间浸出产物浓度差(即增大传质推动力),有利于锶的浸出[33]。液固比从4 ml/g 增加到10 ml/g,锶浸出率由17.53%增加到68.79%;但液固比由10 ml/g 再增大到15 ml/g,锶浸出率仅仅由68.79%增加到70.36%,稍有增大,这是因为随着液固比的进一步增大,Ba2+与锶废渣中的SrSO4反应速率过快,在SrSO4表面形成了一层BaSO4产物层,阻碍了Ba2+与SrSO4的进一步反应。为增加经济可行性,选取液固比为10 ml/g。
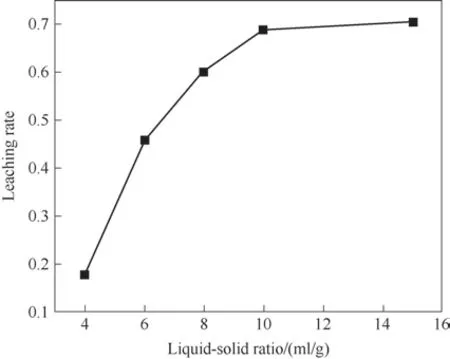
图6 初始液固比对锶浸出率的影响Fig.6 Effect of initial liquid-solid ratio on strontium leaching rate
2.5.4 浸出动力学 BaCl2浸出过程属于固液非均相反应,常用缩核模型描述[34]。根据核缩模型,反应过程发生在惰性物料层和未反应核之间的界面上,总的反应过程由液体反应物在固体外的扩散、惰性物料层扩散的过程及界面上发生的化学反应这三个步骤所构成,整个反应过程受某个关键步骤的控制。
浸出反应可用式(2)表示:
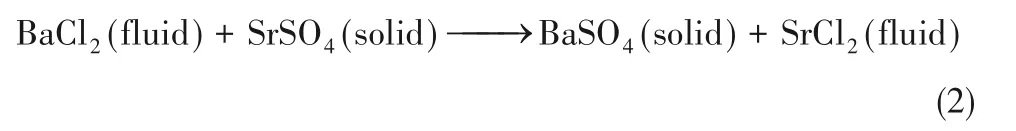
对于液膜扩散传质控制、界面化学反应控制和产物层扩散传质控制,其反应动力学表达式分别为:

其中,X 为锶浸出率,k1为液膜扩散表观速率常数,kr为界面化学反应表观速率常数,km为产物层扩散表观速率常数,t为浸出时间。
为确定锶浸出动力学参数及控制步骤,将浸出温度为20、40、60、80 及100℃得到的锶浸出率数据代入到式(3)~式(5)中,结果如图7 所示。发现式(5)拟合R2值均在0.92 以上,且都能通过原点,说明式(5)用来描述BaCl2浸出过程更为合适。
以lnkm对T-1作图,得到图8 所示BaCl2浸出过程中的Arrhenius 拟合曲线,根据拟合斜率,通过Arrhenius 公式求出其表观活化能为38.75 kJ/mol,液膜扩散控制过程的活化能通常为4~12 kJ/mol,化学反应控制过程的活化能大于41.80 kJ/mol[35-36],天青石锶废渣BaCl2浸出过程的表观活化能处于12~41.80 kJ/mol,属于产物层扩散控制。这与图7 中采用产物层扩散模型进行数据拟合得出的结论一致。

图7 浸出过程动力学模型Fig.7 Kinetic model of leaching process
2.5.5 浸出渣表征 浸出渣(最佳浸出条件下)XRD(图9)表明固体中主要成分为BaSO4,还伴有SiO2、Ba0.75Sr0.25SO4、SrSiO3等物质,说明酸处理后锶渣中的SrSO4与加入的BaCl2反应生成了BaSO4和SrCl2。Ba0.75Sr0.25SO4、SrSiO3的存在,也表明浸出渣中还含有一定量的锶。Ba0.75Sr0.25SO4的存在,表明Ba2+在取代SrSO4中锶的过程中,首先会部分取代,再到全部取代,取代过程中会形成SrxBa1-xSO4介稳结构,使得锶废渣中的锶以SrCl2的形式被浸出。

图8 BaCl2浸出过程中的Arrhenius 拟合曲线Fig.8 Arrhenius fitting curve during BaCl2 leaching process

图9 浸出渣XRD谱图Fig.9 XRD pattern of leaching residue
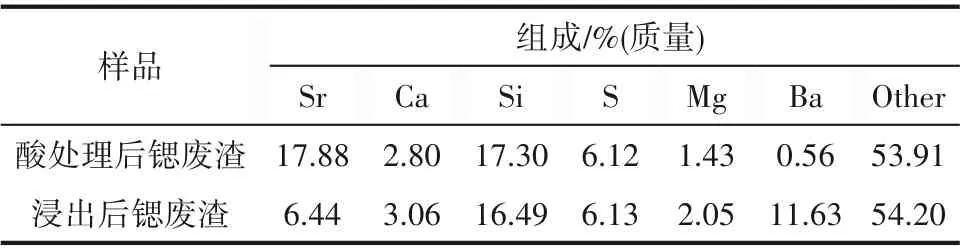
表2 浸出后锶废渣组成Table 2 Composition of strontium waste residue after leaching
浸出渣XRF(表2)表明锶含量由浸出前17.88%降低到6.44%,而钡含量由0.56%增大到11.63%,算得锶浸出率为63.98%,与测得的锶浸出率68.79%接近,说明在误差范围内数据可靠。
在酸性条件下,CaF2与SiO2反应生成SiF62-,从而剥离矿物表面的硅氧层,能够显著提高钒的浸出效率,加快钒的浸出速率[37]。预处理后的天青石锶废渣表面也覆盖着一层硅氧层,在酸性条件下,可利用CaF2来剥离表面硅氧层,强化浸出过程,进一步提高锶浸出率。
3 结 论
(1)采用氯化钡为浸出剂,从天青石锶废渣中回收锶,Ba2+部分或全部取代SrSO4中的锶,使得锶废渣中的锶以SrCl2的形式被浸出;
(2)浸出过程符合未反应核缩模型,且主要受BaSO4产物层扩散控制,其表观活化能为38.75 kJ/mol;
(3)浸出条件为浸出温度90℃、浸出时间120 min、BaCl2/SrSO4摩尔比2.0、初始液固比10 ml/g时的锶浸出率可达到68.79%。
