人血浆脂蛋白相关磷脂酶A2 在急性冠脉综合症患者中的变化及对预后的影响
2021-05-15于宗良王俊峰
赵 波,于宗良,王俊峰
(江苏大学附属昆山医院 江苏 苏州 215300)
动脉粥样硬化性疾病在全球仍然是一种非常常见的疾病,并且有学者提出“泛血管疾病”的概念[1]。泛血管疾病以动脉粥样硬化为共同的病理基础,发生发展进而危害心、脑、肾、四肢等重要器官,其中动脉粥样硬化致心血管疾病危害尤为严重,致死率、再住院率及医疗负担均较高。冠状动脉粥样硬化性心脏病是引起心脏性死亡的主要原因,其中急性冠状动脉综合征(acute coronary syndrome,ACS)是冠心病尤为严重一种类型。血管内皮损伤、斑块破裂、血小板聚集等多种因素共同导致ACS 的病理生理发生,并发展为ACS 的不同类型阶段。动脉粥样硬化这一病理进展过程发挥重要的作用,除血脂异常外,动脉粥样斑块的发生和发展中血管内皮炎症反应及其氧化应激承担至关重要的作用,其参与了整个过程动脉粥样斑块的形成和发展,甚至最终斑块破裂,而出现不同的临床结局[2]。而人血浆脂蛋白相关磷脂酶A2(Lp-PLA2)作为一种新型血管特异性炎症标记物,且生物活性较为稳定而被临床广泛应用[3]。研究也发现Lp-PLA2 可以作为冠心病和缺血性脑卒中的独立危险因素,其在一定程度上反应血管内皮损失炎症反应为病理基础的疾病状态,并参与动脉粥样硬化发生、发展及斑块破裂过程。鉴于此,本文对不同临床类型冠心病患者以及非冠心病患者对比,以探讨Lp-PLA2 在急性冠脉综合症患者中的变化及其与近期预后的关系,也为临床医生合理使用Lp-PLA2 作为临床应用价值的生物标志物提供资料。
1.资料与方法
1.1 一般资料
选择2018 年6 月—2019 年5 月在我院心内科住院并接受冠脉造影的患者共258 例,根据中国经皮冠状动脉介入治疗指南2016 年诊断治疗标准将其分为ACS 组86 例,其中不稳定心绞痛(unstable angina pectoris,UAP)组50 例,男28 例,女22 例,年龄56.2±6.2 岁,急性心肌梗死(acute myocardial infarction,AMI)组36 例,男20 例,女16 例,年龄59.8±6.8 岁;稳定型心绞痛(stable angina pectoris,SAP)组90 例,男51 例,女39 例,年龄59.4±8.1 岁;对照组冠脉造影阴性82 例,男46 例,女36 例,年龄52.6±3.8 岁,为胸痛待查而冠脉造影阴性的患者。有以下情况之一者排除:(1)严重的肝、肾功能不全及急性心力衰竭者;(2)合并严重感染、肿瘤或免疫系统疾病者;(3)各种凝血功能异常性疾病;(4)急性脑梗死或精神疾病。(5)长期服用他汀类药物。已签署知情同意书且通过医院伦理委员会审批。各组基线资料比较,包括年龄、性别、高血压病、糖尿病、吸烟因素差异无统计学意义(均为P>0.05),见表1。
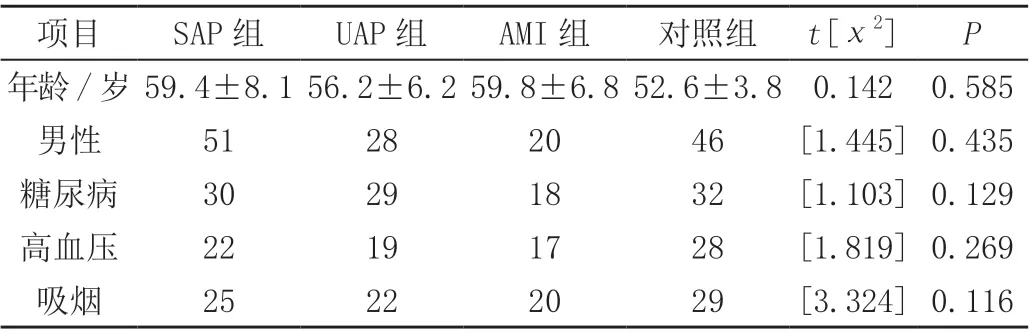
表1 各组一般资料比较
1.2 方法
1.2.1 标本的采集及测定 所有入选患者于清晨空腹取前臂静脉血5ml,Lp-PLA2 由我院检验科采用酶联免疫反应测定[4],国内研究[4]提示Lp-PLA2 <175 ng/mL为正常,Lp-PLA2 ≥175 ng/mL 提示心血管事件风险增加。根据Lp-PLA2 ≥175 ng/mL 和Lp-PLA2 <175 ng/mL 将冠心病患者分成两组,两组患者年龄、高血压、糖尿病、吸烟率及基础用药方面相比差异无统计学意义(P>0.05)。
1.2.2 诊疗情况 冠状动脉造影结果由两位经验丰富的心导管医师判定冠状动脉狭窄程度,严格根据中国经皮冠状动脉介入治疗指南2016 年诊疗指南给予相应病变血管行经皮冠状动脉内成形术、支架置入术及冠心病常规药物治疗。观察住院期间及出院后6 个月内新出现心肌梗死、心脏性死亡等不良心血管事件作为短期预后评价指标。
1.3 统计学处理
2.结果
2.1 ACS 组、SAP 组、对照组之间Lp-PLA2 比较
AMI 组、UAP 组和SAP 组中的Lp-PLA2 水平均较对照组明显升高并有统计学差异(P<0.05);AMI 组、UAP组中的LP-PLA2 水平均较SAP 组升高,差异有统计学意义(P<0.05);AMI 组和UAP 组组间Lp-PLA2 水平比较,差异无统计学意义(P>0.05),见表2。
表2 对照组与冠心病各组Lp-PLA2 的比较(±s,ng/mL)

表2 对照组与冠心病各组Lp-PLA2 的比较(±s,ng/mL)
注:与对照组比较,*P <0.05;与SAP 组比较,ΔP <0.05;与UAP 组比较,▲P >0.05。
分组 例数 Lp-PLA2 SAP 组 90 180.31±79.17*UAP 组 50 218.78±62.59*Δ AMI 组 36 256.61±80.29*Δ▲对照组 82 136.58±30.16
2.2 两组不良心血管事件发生情况比较
将入选冠心病患者按Lp-PLA2 ≥175 ng/mL 和Lp-PLA2 <175 ng/mL 分两组,比较两组间于住院期间及出院后6 个月内不良心血管事件发生情况,见表3。其中Lp-PLA2 ≥175 ng/mL 组共106 例,再发心肌梗死7 例(6.6%),心源性死亡3 例(2.8%);Lp-PLA2 <175 ng/mL 组共70 例,再发心肌梗死2 例(2.6%),心源性死亡1 例(1.3%);两组间再发心肌梗死事件发生率、心源性死亡事件发生率差异均无统计学意义(P>0.05)。
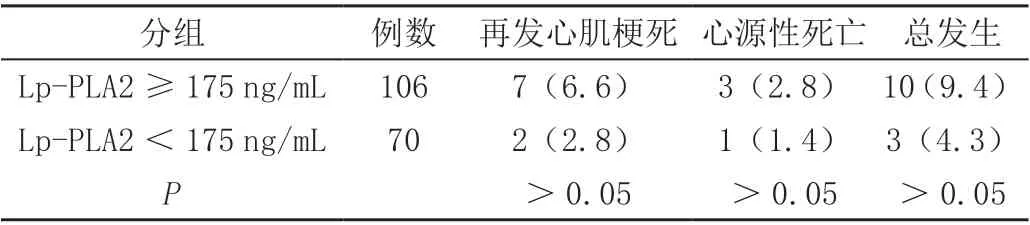
表3 两组不良心血管事件发生情况比较[n(%)]
3.讨论
既往研究证实炎症反应和氧化应激等在动脉粥样硬化发生、发展中扮演着重要角色,其中动脉粥样硬化血栓形成过程也涉及多种炎症标志物。L p-P L A2 作为磷脂酶超家族中的亚型之一,是一种钙离子依赖的磷脂酶,能够催化细胞膜中脂蛋白和甘油磷脂第二酰基酯键水解,从而产生赖氨酸磷脂酶和非酯化脂肪酸的酶。L p-P L A2 由血管内皮中的肥大细胞、巨噬细胞等炎性细胞分泌合成,在人体血液循环中,L p-P L A2与血脂中的脂蛋白颗粒相结合,其中有80% 与低密度脂蛋白结合,有15% ~20% 与高低度脂蛋白结合,其余皆与极低密度脂蛋白结合[3]。L p-P L A2 其活性产物可以诱导氧化应激和免疫反应,导致内皮功能受损,从而促进血小板聚集、中性粒细胞和单核细胞趋化,促使动脉粥样硬化斑块形成和进展。冠心病的发生发展是多种因素共同作用的结果,且既往研究及meta 分析发现L p-P L A2 是一种致动脉粥样硬化的危险因子及冠心病的独立危险因素[5]。本文中冠心病组患者L p-P L A2 水平明显高于对照组,且由S A P 组、U A P 组到AMI 组,随病变发展Lp-PLA2 呈逐渐增高趋势,且ACS组的患者L p-P L A2 水平高于S A P 组,同样提示L p-P L A2 升高可作为冠状动脉粥样硬化病变严重程度的独立预测因子。同时亦发现L p-P L A2 提示动脉粥样硬化斑块是否为易损斑块。另外,本文结果显示,冠心病患者血运重建或药物保守治疗后6 个月内再发心肌梗死事件发生率、心源性死亡率L p-P L A2 ≥175 n g/m L组高于Lp-PLA2 <175 ng/mL 组,但两组间差异均无统计学意义。Kolodgie 等[6]学者通过对心源性猝死患者尸检,采用免疫定位分析发现在冠状动脉硬化斑块中,L p-P L A2 于坏死核心区域呈高表达,尤其集中在易损斑块中,以破裂斑块表达尤为突出,L p-P L A2 可进一步水解氧化低密度脂蛋白(ox-LDL)中的氧化磷脂,生成如溶血卵磷脂和氧化游离脂肪酸等脂类促炎物质,从而会促使多种致动脉粥样硬化发生,包括内皮功能异常及内皮细胞死亡,且可以刺激粘附因子和细胞因子的产生,恰恰这些物质可进一步通过趋化炎症细胞产生自我强化的恶性循环,产生更多促炎物质[7], 由此研究可以推测L p-P L A2 可能促进斑块的不稳定性,从而形成易损斑块、破裂斑块。同时,既往研究发现冠心病急性期后30 天测定的Lp-PLA2 是独立于低密度脂蛋白和C 反应蛋白的预后指标[8]。且既往一项社区急性心肌梗死患者临床研究[9]提示心肌梗死急性期测定的L p-P L A2 水平与1 年内死亡率具有相关性,也进一步提示L p-P L A2 可能不受急性炎症事件的影响,而恰是反应血管炎症的特异性指标之一。同样,本文亦能提示ACS 患者高水平的Lp-PLA2 增加了心血管不良事件发生的危险。
综上所述,Lp-PLA2 在冠状动脉粥样硬化斑块形成及发展中有着密切相关性,对冠状动脉粥样硬化评估、疾病严重程度及预后有重要的临床参考价值。而且,既往研究Lp-PLA2 在不稳定斑块及破裂斑块中呈现高度表达,使其可能作为心血管事件的独立预测因子[10]。因此,检测及分析Lp-PLA2 有助于评估冠心病风险、冠状动脉血管病变严重程度及斑块稳定性,同时提示对冠心病的可疑人群作到早期干预,从而减少冠心病相关心脏事件的发生率。本文也存在一定局限性,临床病例数较少且观察时间较短等,可能会导致结果分析不全面,进而需要进一步增加样本量及随访时间。
