一氧化氮供体型心脑血管药物研究的实践与思考
2021-05-08吴建兵黄张建张奕华
吴建兵,黄张建,张奕华
(中国药科大学新药研究中心,南京210009)
自20世纪80年代发现内皮衍生的血管舒张因子(EDRF)的化学本质为一氧化氮(NO•,简写为NO)以来,人们对这一双原子的自由基气体小分子产生了浓厚的兴趣,有关NO的生物学和化学研究不断深入。1992年,NO被美国Science杂志评为“明星分子”。1998年,美国学者Furchgott、Ignarro和Murad因各自在NO生物学研究中的重大发现而分享当年诺贝尔生理或医学奖。大量的研究表明,NO作为信使物质和/或效应分子在心血管、神经、免疫等系统发挥极其重要的作用,体内NO生成不足或信号传导异常与多种疾病的形成和发展密切相关。NO在医药方面所显示出的巨大潜力吸引了全世界许多著名大学和科研单位,直接或间接调控体内NO水平及其相关代谢途径的研究已成为生物医学和药学领域研究的重大课题。
NO最初以气体吸入方式用于治疗新生儿持续性肺动脉高压,其后的研究主要集中在NO供体方面。NO供体一般是指在体内经酶或非酶作用释放NO的化合物,它可作为一种NO体内运输形式,又可作为一种贮存形式,延长NO半衰期,克服吸入NO所引起的诸多不便及难以控制的缺点。现已发现多种结构类型的NO供体,较重要的有硝酸酯、亚硝基硫醇、呋咱N-氧化物、偶氮鎓二醇盐等[1]。NO供体型药物主要指NO供体与活性化合物或药物以共价键或离子键结合,在体内经酶或非酶作用释放NO和活性化合物或药物的前药。
在已知的NO供体型药物中,硝酸甘油的临床应用已超过一个世纪,挽救了无数心绞痛患者的生命;硝普钠、单硝酸异山梨酯以及尼可地尔等也在20世纪广泛用于心力衰竭、心绞痛、高血压危象等重大疾病的治疗。21世纪以来,NO供体型药物研究方兴未艾。2005年抗心力衰竭药BiDil应用于临床,2017年治疗青光眼/眼高压的拉坦前列腺素硝酸酯(Latanoprostene bunod)及其滴眼剂(Vyzulta)被FDA批准上市,另有10多个各类NO供体型药物处于临床前和临床研究阶段,如抗肿瘤的RRx-001正在美国进行Ⅱ期临床研究[2]。
NO虽然在体内具有多种重要生理功能,但具有“双刃剑”作用的特点。通常低浓度的NO(pmol/L级至nmol/L级)通过经典的NO-sGC-cGMP[3]或非经典的S-亚硝化[4]途径发挥舒张血管、保护细胞等有益作用;而高浓度的NO(µmol/L级至mmol/L级)则可与某些活性氧(ROS)反应生成活性氮(RNS),对蛋白、脂质以及DNA进行硝化或亚硝化,产生细胞毒性,诱导细胞凋亡[5]。由此人们设想:(1)能否扬“长”避“短”,通过外源性提供适量的NO来治疗因NO生成不足而引起的某些疾病呢?(2)既然正常组织、细胞内NO生成过量会导致肌体损伤,能否将这种破坏作用选择性地发生在癌变的组织或细胞内呢?也就是说,让NO在正常细胞做“好事”,但在肿瘤细胞做“坏事”。本课题组正是基于上述设想来设计、合成NO供体型药物的。如何释放适量NO到特定组织而不影响其他组织,即如何“定位”和“定量”释放NO,以发挥其治疗作用,抑制或减少其不良反应,是研究面临的挑战。围绕这一科学问题,本课题组系统制备了多种结构类型的NO供体化合物,其中一些可选择性地在肿瘤细胞释放高浓度的NO,与特定靶分子作用,发挥抗肿瘤、抗肿瘤耐药和/或抗肿瘤转移的活性;另一些可在循环系统或病变部位缓慢释放低浓度的NO,治疗心脑血管疾病或降低其他药物所产生的心血管不良反应。两方面的研究均取得了一些重要进展。在NO供体型抗肿瘤药物研究方面,本课题组研发的化合物ZCVI4-2曾被遴选为“‘十一五’重大新药创制”的候选药物,进行过较深入的研究。此外,本课题组还应邀在JMed Chem杂志上发表了一篇与NO供体型抗肿瘤药物研究相关的综述文章[5]。因篇幅有限,本文仅简要介绍体内NO的产生及其在心脑血管系统的生理、病理作用,重点综述本课题组在NO供体型心脑血管药物研究方面所开展的工作,并对今后的发展方向提出一些自己的见解。
1 体内NO的产生及其在心脑血管系统的生理、病理作用
体内NO由NO合酶(NOS)在辅因子还原型烟碱酰胺-腺嘌呤-二核苷酸磷酸盐(NADPH)、黄素腺嘌呤二核苷酸(FAD)、黄素单核苷酸(FMN)和(6R-)5,6,7,8-四氢生物蝶呤(BH4)存在下,催化L-精氨酸和氧分子反应产生[6]。哺乳动物细胞内NOS有3种亚型,即内皮型NOS(eNOS)、神经元型NOS(nNOS)和诱生型NOS(iNOS),其中eNOS和nNOS又统称为原生型或组成型NOS(cNOS)。
eNOS主要在内皮细胞中表达,但在成纤维细胞、骨骼肌、骨、运动神经元和星形胶质细胞中也有表达。在正常的心脑血管系统中,由eNOS催化产生的NO具有血管舒张作用,其机制为激活平滑肌细胞中可溶性鸟苷酸环化酶(sGC),使胞内的环鸟苷酸(cGMP)水平增加,激活cGMP依赖性的激酶PKG1(eNOS-NO-cGMP-PKG1通路),从而舒张血管、调节血压[3,6-7];其他机制,如NO直接激活钾离子通道,引起血管舒张,也见报道[8]。除舒张血管外,NO还可通过抑制单核细胞、血小板黏附和血小板聚集以及抑制平滑肌细胞增生,产生抗血栓、抗动脉粥样硬化作用,从而保护心脑血管[7]。
在生理情况下,由eNOS衍生的NO与超氧阴离子(O2•-)反应速度比超氧化物岐化酶(SOD)清除O2•-的速度快3倍,但由于体内NO浓度(10~100 nmol/L)约为SOD浓度的90%,此时产生的NO很难与SOD竞争O2•-,主要作为信使分子行使其正常的生理功能[9]。在某些病理条件下,如氧化应激、eNOS解偶联和血管内皮功能障碍等可导致NO生成不足,介导多种心血管病变,包括高血压、冠状动脉硬化、心力衰竭等[6]。
nNOS主要在中枢和外周神经元表达,经nNOS-NO-cGMP-PKG1信号通路,行使正常生理功能,包括中枢神经系统的突触可塑性、血压的中枢调节、平滑肌松驰和外周氧化氮能神经(peripheral nitrergic nerves)介导的血管舒张等[6,10]。nNOS有4种不同的亚型(α,β,γ,µ),其中nNOSα和nNOSµ固定在神经元的PDZ结构域,nNOSβ和nNOSγ存在于胞质内。nNOSα通过突触后密度-95蛋白(PSD-95)与NMDA受体结合并相互作用。在外周神经系统,NO于氧化氮能神经突触前末梢释放,作为顺行神经递质行使功能;在大脑的大部分区域,NO产生于神经元突触后,作为逆行神经递质发挥作用[10]。
iNOS主要由炎症因子、氧化应激、缺氧、各种内毒性等产生,可在巨噬细胞等多种细胞中表达,产生大量的NO,抑制寄生的靶细胞,参与炎症性疾病和感染性休克等病理、生理过程[6,10]。在大脑中,iNOS主要在小胶质细胞、星形胶质细胞、浸润淋巴细胞经诱导产生,释放NO的时间可长达数小时甚至几天[10]。
必须指出的是,早期的研究系根据NOS亚型在细胞中分布及生成方式不同对其加以命名的。后来的研究提示这种分类过于简单,因为3种亚型除在原先所述的细胞内产生外,也出现在其他一些细胞内,而且cNOS可诱导产生,iNOS亦有少量原生型表达。cNOS和iNOS真正的区别在于前者活性依赖Ca2+,催化生成的NO较少,一般在pmol/L(1×10-12mol/L)水平,后者由于与Ca2+/钙调素(CaM)具有高度亲和力,其活性不依赖Ca2+,可催化生成高达µmol/L(1×10-6mol/L)浓度以上的NO[6,10-11]。
脑缺血后,NO在缺血性脑组织中所起的有益或有害作用取决于NOS的亚型、细胞种类、NO浓度和缺血微环境等[12]。研究表明,由内皮细胞eNOS衍生的NO具有保护血脑屏障(BBB)、减少氧化应激以及保护神经的功能,而神经细胞、小胶质细胞、星形胶质细胞内nNOS/iNOS衍生的NO则发挥损伤神经的作用,究其原因,主要是在缺血早期,兴奋性谷氨酸过度释放,激活NMDA受体的亚型GluN2B,使Ca2+经离子通道内进入胞浆,与钙调蛋白结合,从而激活GluN2B-PSD95-nNOS信号通路,产生过量NO及其他自由基,导致神经损伤;在缺血后期,炎性细胞因子等诱导了iNOS表达,生成大量NO,触发神经细胞凋亡或坏死[9-10,12-16]。
脑缺血后NO的不同作用可能与其本身的氧化还原状态有关。NO可失去一个电子或获得一个电子,形成3种互变形式:NO自由基(NO•)、亚硝基阳离子(NO+)和亚硝基阴离子(NO-)。NO+能使NMDA亚型受体的巯基亚硝化,发挥神经保护作用;而NO•可与O2•-反应,生成过氧亚硝酸阴离子(ONOO-),引起细胞毒性[9,17-18]。
2 NO供体型心脑血管药物及相关药物的研究
鉴于NO在维持血管张力、血压及血流动力学方面起着十分重要的作用,外源性补充NO己成为治疗心脑血管疾病的有效策略之一。本课题组将各种NO供体通过连接基团与已知的心脑血管药物或活性化合物杂合,设计、合成了一系列NO供体型药物。不同的NO供体和连接基团可调节NO的释放部位、释放量和释放时间,使NO以持续、可控的方式释放到特定组织和/或血液中,这样不仅可改善原药或活性化合物的心脑血管活性,还能减少其不良反应。
2.1 抗缺血性脑卒中药物
缺血性脑卒中严重危害人类的健康和生命,已成为我国第一致残和致死的重大疾病,目前临床缺乏高效、安全的治疗药物,研究和发现新型抗缺血性脑卒中药物具有重要意义。
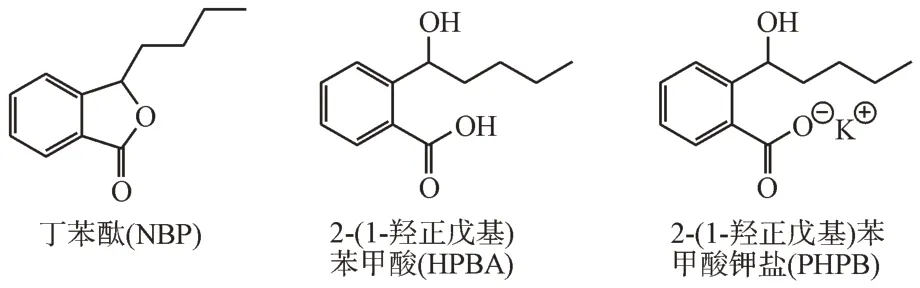
2.1.1 NO供体型丁苯酞开环衍生物 丁苯酞(NBP)是我国自主研发并于2004年上市的治疗轻、中度缺血性脑卒中药物。NBP虽有确切的抗血小板聚集、抗血栓、减少脑梗死体积、保护线粒体功能、改善脑微循环等多种生物活性,但常与其他药物联用以增强其疗效[19]。此外,NBP水溶性极差,对其制剂的制备及其疗效产生不良影响。为改善NBP的水溶性和/或活性,本课题组以其为先导物进行了结构修饰和改造。
已知NBP的内酯开环物2-(1-羟正戊基)苯甲酸(HPBA)的钾盐2-(1-羟正戊基)苯甲酸钾盐(PHPB),具有较高的水溶性,且在体内可转变为NBP,发挥与NBP相当的抗脑缺血活性,其口服生物利用度优于NBP[20-21],这为本课题组设计HPBA衍生物提供了依据。
此外,众所周知,阿魏酸(ferulic acid,FA)等桂皮酸类化合物是当归、川芎、阿魏等中草药的主要活性成分,具有抑制活性氧、抗氧化、抗炎、抗血小板聚集等药理活性。近年来的研究表明,FA在小鼠急性血栓模型通过下调αIIbβ3/FIB/AKT表达,抑制血小板聚集,发挥抗血栓活性[22];FA抑制大鼠中脑动脉闭塞(MCAO)诱导的eNOS下调以及nNOS和iNOS的上调,产生抗脑缺血作用[23]。FA可以单独使用,也可以作为两个活性分子之间的连接基,增强心脑血管疾病的治疗效果。
本课题组以FA等作为连接基团将HPBA的羧基与硝酸酯类NO供体杂合,并在HPBA侧链戊基的羟基上引入亲水性基团(二甲胺、吗啉、哌啶盐酸盐等)取代的烷(芳)酰基,设计、合成了NO供体型NBP的开环衍生物,以改善分子理化性质、增强其化学稳定性和生物活性。大部分衍生物的水溶性及血小板聚集抑制活性均优于NBP[24-26],其中ZJM-289尤为特出,故对其重点研究。结果表明,ZJM-289可在体内释放出HPBA,继而环合成NBP,同时释放出NO及阿魏酸片段,发挥协同作用[27]。ZJM-289对缺氧缺糖及过氧化氢诱导的PC12细胞神经损伤及凋亡具有明显的保护作用,体内抗血栓活性优于等摩尔量的NBP或阿司匹林。
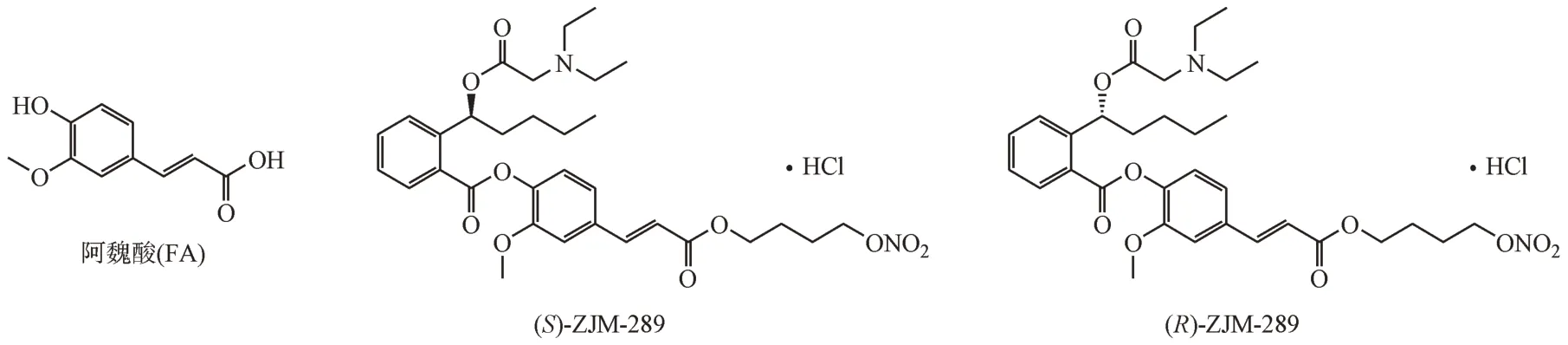
此外,ZJM-289具有良好的BBB通透性,对大鼠局灶性脑缺血/再灌注(I/R)损伤的抑制作用显著强于等摩尔量的NBP,其分子机制主要为增加脑内eNOS的表达,激活eNOS-NO-cGMP途径,发挥脑神经元保护效应[28]。该化合物安全性较好,小鼠经口给药的LD50大于5 g/kg,Ames试验无明显的致突变作用。ZJM-289在大鼠和Beagle犬体内具有良好的药代动力学性质[27,29]。基于以上优良特性,ZJM-289曾被遴选为“十一五”重大新药创制的候选药物,进行过较深入的研究。
NBP分子中含有一个手性碳原子,故存在(S)-和(R)-对映体。已知(S)-NBP在抑制血小板聚集、抗血栓、抗脑缺血以及神经保护作用等方面略优于(R)-NBP[30-32]。因此,本课题组合成了(S)-和(R)-ZJM-289,并对其生物活性进行了比较,发现(S)-ZJM-289在抑制血小板聚集、抗血栓和神经保护方面的作用与ZJM-289和(R)-ZJM-289并无显著差异[33]。研究表明,(S)-ZJM-289可通过抑制线粒体功能障碍等机制,减少短暂性脑缺血及缺氧-缺糖诱导的神经损伤[34-35]。
2.1.2 NO/H2S双供体型NBP开环衍生物 硫化氢(H2S)是继NO和一氧化碳(CO)之后发现的第3种气体信号分子,与NO类似,具有舒张血管、增加脑血流量、抗氧化应激、减少自由基、保护神经细胞等作用。近年来研究表明,H2S对脑卒中和神经退行性疾病等具有潜在治疗价值[36-37],NO/H2S双供体型药物比单一供体型药物具有更好的生物活性[38]。
本课题组将HPBA的羧基和侧链羟基分别与NO供体和H2S供体杂合,设计、合成了NO/H2S双供体型NBP开环衍生物,并对其生物活性及作用机制进行了研究[39-40]。结果表明,所有目标化合物对二磷酸腺苷(ADP)诱导的家兔血小板聚集的抑制活性均优于NBP,其中化合物1最佳:(1)对ADP诱导的家兔血小板聚集的抑制活性是NBP的5.2倍;(2)释放适量浓度的NO和H2S,NO清除剂PTIO和H2S清除剂均可显著降低其抗血小板聚集活性,提示NO和H2S对它的抗血小板聚集活性至关重要;(3)血小板聚集抑制活性优于相应的H2S供体型NBP开环衍生物和/或NO供体型NBP开环衍生物,提示化合物1的两个供体片段协同作用,发挥比NBP更强的活性;(4)显著降低I/R大鼠的梗死体积及脑含水量,效果优于等摩尔的NBP;(5)改善神经行为功能;(6)抑制神经元死亡和缺血引起的BBB功能障碍。
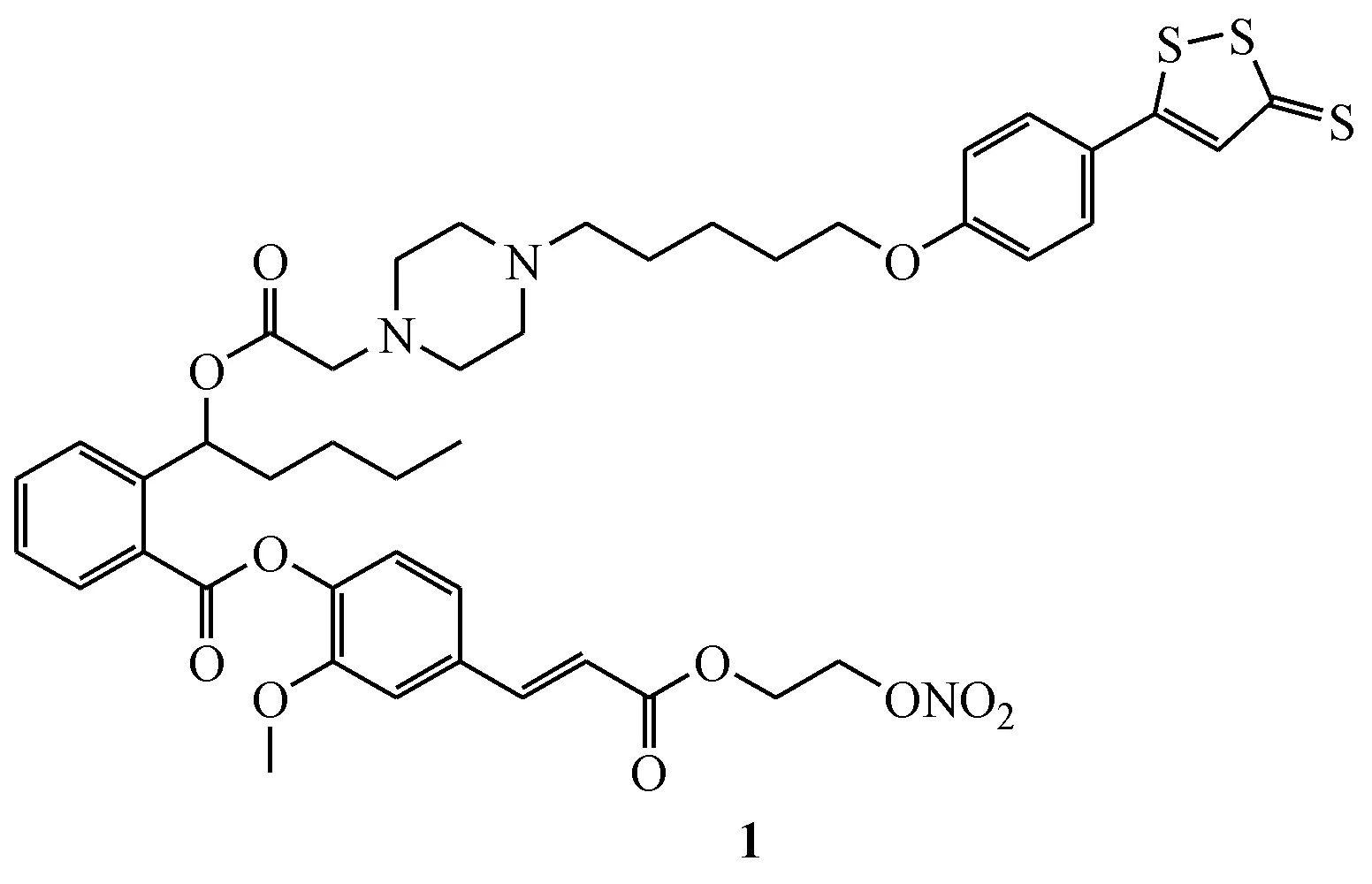
作用机制研究表明,化合物1可通过升高I/R大鼠脑内GSH、SOD及GSH-Px的含量,降低MDA的水平,发挥其抗氧化作用。此外,化合物1通过抑制TLR4/MyD88/NF-κB通路和NLRP3炎性小体,抑制M1样小胶质细胞活化,并增强PPAR核易位,促进M2样小胶质细胞活化,使小胶质细胞/巨噬细胞从炎症M1表型向保护性M2表型转变,从而对缺血性脑神经产生保护作用。
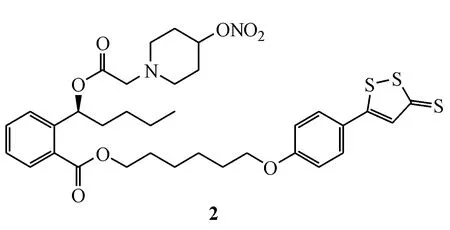
在上述基础上,本课题组以(S)-HPBA为先导物,将其羧基和侧链上的羟基通过不同的连接基团分别与H2S供体和NO供体杂合,设计、合成了光学活性的NO/H2S双供体型NBP开环衍生物,发现所有化合物在体外均能释放一定水平的NO和H2S,对ADP或AA诱导的血小板聚集具有明显的抑制作用,其中化合物2活性最强,优于(S)-NBP、阿司匹林(ASA)和噻氯匹定(ticlid)。此外,化合物2结构中的3个片段抑制ADP诱导的血小板聚集活性均低于整体分子,提示三者可能协同作用,对化合物2的活性具有重要贡献[41]。
2.1.3 HPBA衍生物与L-精氨酸的成盐产物 L-精氨酸在体内可被NOS代谢为对心血管有益的NO,亦可被非酶途径氧化成NO。膳食补充L-精氨酸可降低高胆固醇患者的血小板反应活性、阻止动脉粥样硬化形成。L-精氨酸可通过血-脑脊液屏障上的阳离子氨基酸转运体(CAT1)从外周血液进入脑内,对大脑发育十分重要[42]。此外,梅拉斯(MELAS)型线粒体脑病患者静脉滴注或口服L-精氨酸可增加脑血流微循环,减少局灶性脑缺血急性损伤,明显降低脑卒中症状的频率和严重程度[43];直接向AD大鼠脑室注射L-精氨酸可产生显著的神经保护和抗凋亡活性[44]。对缺血再灌注大鼠的脑室注射L-精氨酸可降低其神经元的死亡,促进其功能恢复[45]。此外,L-精氨酸能有效地保护肝脏,对肝脏的氨中毒具有解毒作用,还能预防肝硬化形成等。事实上,L-精氨酸的多种剂型已被中国药典收录[46],是多年来用于临床治疗血氨增高所致精神症状的有效药物。
考虑到已在动物脑卒中模型显示优良神经保护活性但改善血流活性较弱的一些化合物如neri⁃netide(NA-1)未能获得理想的临床疗效[47-48],还考虑到仅能改善血流而无神保护活性的药物如rt-PA的治疗局限性,本课题组基于神经血管单元(NVU)理念[49],运用多靶点作用策略,设计、合成了L-精氨酸与HPBA衍生物(S-APB)形成的新型盐类化合物(AAPB)[50]。AAPB具有前药及孪药双重作用的特点。作为前药,S-APB在体内可经离解、去乙酰化、成环3步反应转化为S-NBP;作为孪药,AAPB体内可产生两个已知的药物(S-NBP和L-精氨酸),协同发挥抗脑缺血作用。
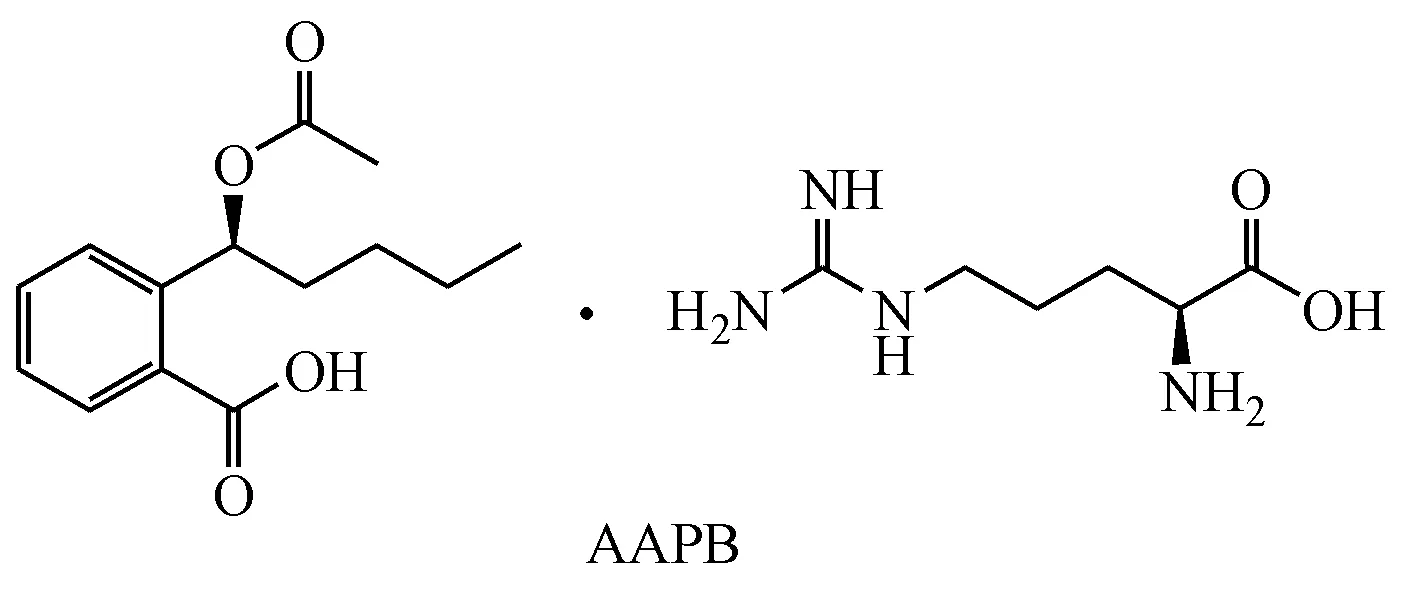
体外以及啮齿/灵长目类动物的体内研究表明,AAPB既改善了S-NBP的水溶性,又延长了其表观半衰期。与一般为增加某化合物水溶性而将其成盐的方法相比,AAPB的设计策略显示了多样性效果,不仅药效(特别是改善脑血循环和保护神经的活性)而且安全性均优于对照的临床用药或正在研究的药物。
AAPB除具有NBP作用机制外,还具有L-精氨酸介导的作用特点:(1)释放适量NO、保护细胞免受OGD/R诱导的神经元损伤;(2)亚硝化磷酸酶及张力蛋白同源体(PTEN),激活PI3k/Akt通路,增加Akt磷酸化;(3)亚硝化Bcl-2,抗细胞凋亡;(4)亚硝化Keap1,抗氧化应激;(5)促进缺血脑组织中血管和神经生成。
如果说NBP是抗缺血性脑卒中的一把“利剑”,那么AAPB则可能是“双剑合璧”(S-NBP和L-精氨酸)的更强大武器。
2.1.4 NO2–供体化合物 近年来不少文献报道,NaNO2对一些心脑血管缺血性疾病具有很好的治疗保护作用。I/R大鼠静脉注NaNO2可降低其梗死体积,增加局部血流,改善神经功能[51]。在颈动脉闭塞前或闭塞后腹腔注射NaNO2,对缺血性脑卒中大鼠具有显著的神经保护作用,可降低其死亡率[52]。
研究发现,NO清除剂可以抑制NaNO2抗I/R活性,提示NaNO2的治疗效果具有NO依赖性[51]。此外,Pluta等[53]在人体试验时也发现,静脉滴注NaNO2后血浆中亚硝基硫醇量显著增加,提示NaNO2可能被还原成NO后,再与硫醇进行亚硝化反应,生成亚硝基硫醇。进一步研究发现,在缺血导致的低氧、低pH环境,亚硝酸阴离子(NO2–)可被脱氧血红蛋白、黄嘌呤氧化还原酶或eNOS等还原为NO,产生舒张血管、增加血流,清除自由基、抗氧化,促进缺血部位的血管新生等多种治疗作用;在正常的含氧组织中,NO2–被氧化为无害的NO3–排出体外[54]。因此,NO2–可被视为缺血组织中NO的前药。
虽然NaNO2治疗多种动物缺血性疾病已显示出很好的效果,但它进入体内可被快速代谢。此外,NaNO2大剂量给药,并未产生缺血保护作用。究其原因,可能是高浓度的NaNO2在短时间内产生大量的NO,与O2•-反应,生成氧化能力更强的ONOO-,导致蛋白硝化和DNA损伤等不良反应[55]。再者,若频繁给予NaNO2,有可能造成过多Na+摄入,对心血管产生不良影响。故此,研究和发现有机小分子化合物,使其持续释放少量NO2–,不仅具有重要的理论意义,而且具有潜在的临床应用价值。
本课题组设计、合成了2-硝甲基-1,3-二苯基丙烯酮类NO2–供体(ND1~ND5),并对其生物活性进行了初步评价[56]。体外研究发现,化合物ND1可在含巯基的小分子如谷胱甘肽或半胱胺酸存在下,通过加成、消除反应释放NO2–。体内研究表明,ND1明显降低I/R大鼠的神经损伤,减少梗死体积,改善脑水肿。更重要的是,ND1可刺激脑缺血半暗带血管内皮细胞增殖,促进血管新生。
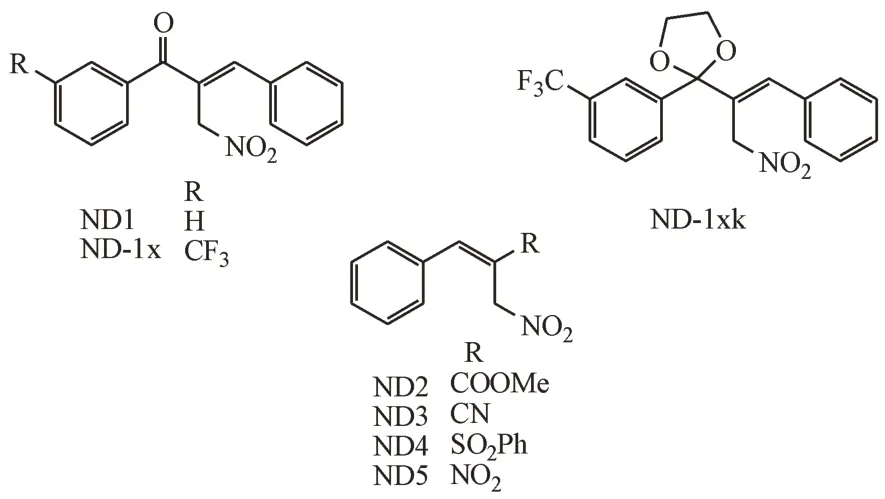
以ND1为先导化合物,设计、合成了三氟甲基取代的化合物ND-1x及其缩酮前药ND-1xk。ND-1xk在血浆和GSH、N-Ac-L-Cys等亲核试剂中都具有较好的稳定性,显著优于ND-1x。ND-1xk在偏酸性的PBS缓冲溶液中可快速降解,释放出亚硝酸阴离子,可剂量依赖性提高OGD/R模型原代神经元细胞的生存率,还可降低MCAO大鼠脑梗死体积、降低脑含水量及改善神经功能评分,显著优于NaNO2、ND1及ND-1x组。重要的是,ND-1xk具有较好的脑选择性作用,其作用机制仍在深入研究中,结果将另文报道。
2.2 抗血小板聚集、抗血栓药物
血栓主要因动脉粥样硬化或其他原因使动脉管腔狭窄或完全闭塞所致。脑血栓可使脑组织缺血、缺氧、坏死,引起局限性神经功能障碍,是急性缺血性脑卒中形成的重要因素。血小板黏附、聚集、释放各种因子与局部血栓形成密切相关。因此,研究抗血小板聚集、抗血栓药物具有重要意义。
2.2.1 NO供体型ASA衍生物 阿司匹林(acetyl⁃salicylic acid,ASA)不可逆地乙酰化血小板中环氧化酶-1(COX-1)530位丝氨酸的羟基,抑制COX-1催化花生四烯酸(AA)转化为血栓烷A2(TXA2),对AA激活的血小板聚集及其血栓形成有较强的抑制作用[57]。但是激活血小板有多种途径,ASA仅阻断了其中的一种,故其作用仍有一定的局限性。此外,ASA还可导致胃肠道溃疡、出血等不良反应。因此,研发优于ASA的抗血小板聚集、抗血栓药物是药学研究中的热点之一。
NO通过激活sGC,抑制血小板的激活,使GTP转化为cGMP,增加了ATP酶依赖性的内皮钙库的贮存,其结果是阻断胞内钙外流,减少了P-选择素的表达以及与纤维蛋白酶原结合的糖蛋白Ⅱb/Ⅱa(GPIIb/IIIa)活性构象,产生抗血小板聚集作用[58]。此外,NO在胃肠道中还发挥着与前列腺素相同的黏膜保护作用[11]。
桂皮酸类化合物FA等能清除自由基、调节机体免疫、抗血小板聚集、抑制动静脉旁路血栓形成[22-23]。它们与ASA联合用药,不仅能明显抑制TXA2生成,而且在抑制血小板功能上有协同作用。
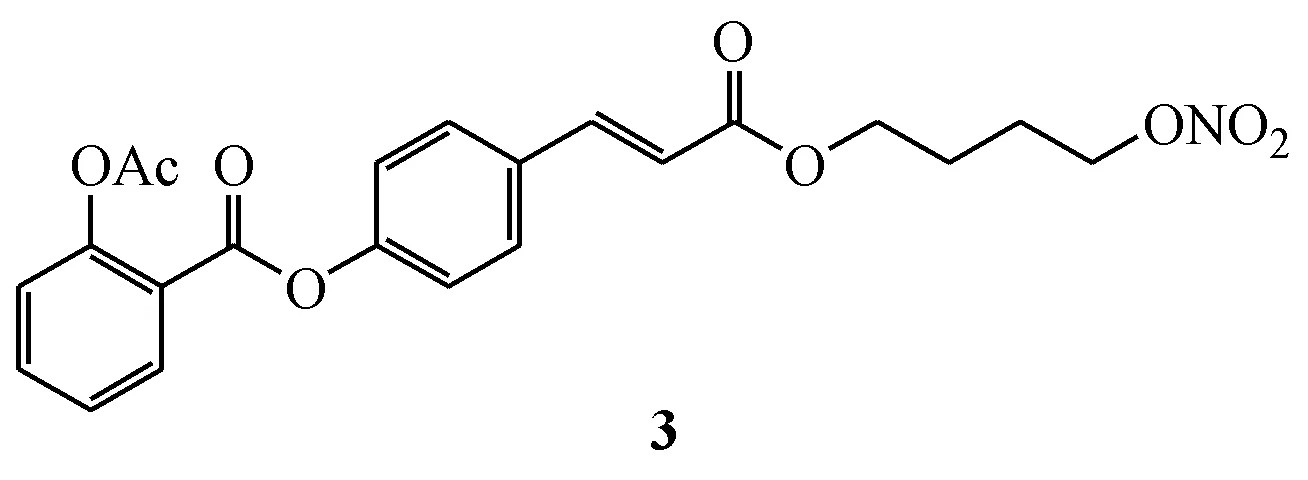
基于上述背景,本课题组分别以对羟基桂皮酸和阿魏酸为连接基团,将ASA与不同类型的NO供体连接,合成了两个系列化合物,并进行了抗血小板聚集试验、动静脉旁路血栓试验、肺血栓试验[59-62]。结果表明,多数化合物的活性与阴性对照组相比具有显著差异,其中化合物3最优。化合物3显著抑制大鼠体内血小板的聚集,抑制率优于ASA及阳性对照药NCX-4016。此外,化合物3能明显抑制大鼠下腔静脉血栓和肺血栓形成,降低大鼠血浆中血栓素B2(TXB2)和6-酮-前列腺素F1α(6-Keto-PGF1α)水平,其活性与NCX-4016相当。
此外,本课题组还将ASA与NO供体3-芳基-1,2,3,4-三唑-5-亚胺以酰胺键偶联,合成了未见文献报道的新型ASA衍生物。其中化合物4活性最好,体外可强效抑制ADP、AA或胶原蛋白3种诱导剂诱导的血小板聚集,活性优于ASA。大鼠经口给予化合物4后,血浆中NO及cAMP浓度明显升高。化合物4能显著抑制大鼠动-静脉旁路模型血栓的形成。此外,化合物4对由胶原蛋白和肾上腺素引发的小鼠肺血栓形成也具有较好的抑制作用,明显提高小鼠存活率[63-64]。
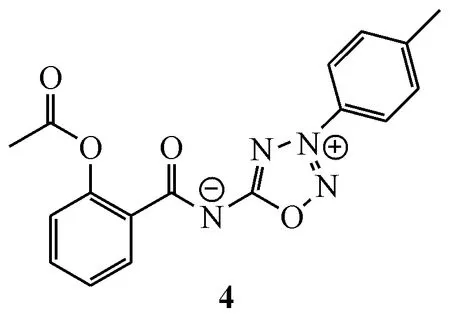
2.2.2 NO供体型6-氨基NBP衍生物 据报道,6-氨基NBP能显著抑制血小板聚集,减少脑梗死面积,改善线粒体功能,减少氧化损伤和神经元凋亡[65]。本课题组以6-氨基NBP为先导化合物设计、合成了一系列NO供体型6-氨基丁苯酞衍生物,其中化合物5水溶性优于NBP,抗血小板聚集活性是NBP的2倍。

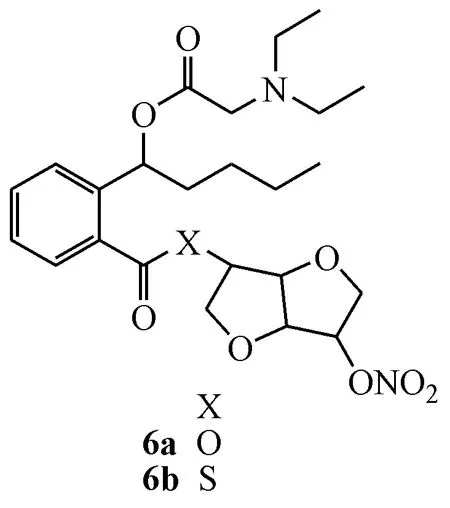
2.2.3 NO供体型HPBA/异山梨醇杂合物 双硝酸异山梨醇酯(ISDN)及单硝酸异山梨醇酯(5-IS⁃MN)是一类经典的NO供体型药物,具有抑制血小板聚集和黏附作用,临床上用于心绞痛的预防和治疗。另据报道,硫代单硝酸异山梨醇酯类化合物LA-419具有良好的抗血小板聚集和抗血栓活性,并且能够减少硝酸酯药物的耐受性,曾进入Ⅱ期临床试验阶段,用于缺血性心血管疾病的治疗[66]。本课题组将HPBA与5-ISMN或其硫代类似物杂合,并在HPBA侧链羟基上引入二甲胺、二乙胺、吗啉、吡咯、哌啶盐酸盐取代的乙酰基,以增加目标化合物的水溶性及其活性,设计、合成了HP⁃BA/5-ISMN杂合物。其中化合物6a和6b比NBP或ASA具有更强的抗血小板活性,且释放适量NO,有利于改善心脑循环[67]。
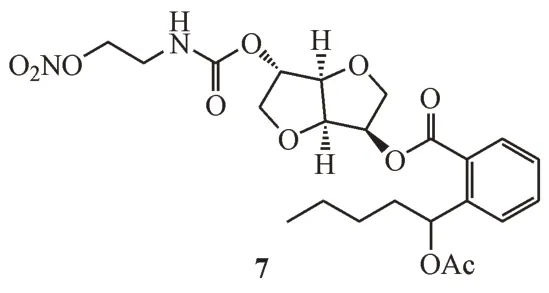
考虑到氨基甲酸酯结构有助于异山梨醇与体内丁酰胆碱酯酶结合,加快前药酯键断裂成原药的速度,同时考虑到氨基甲酸酯具有较好的水溶性,本课题组合成了含硝酸酯基团的氨基甲酸-异山梨醇-HPBA三联体。体外活性筛选结果表明,化合物7的水溶性及对ADP诱导的血小板聚集抑制活性均显著优于NBP[68]。
2.3 抗高血压药物
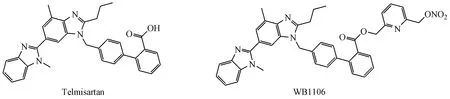
2.3.1 NO供体型替米沙坦衍生物 血管紧张素转化酶(ACE)抑制剂作用于肾素-血管紧张素系统(RAS),阻止血管紧张素Ⅰ被ACE转化为血管紧张素Ⅱ(AII),是高血压和充血性心衰治疗的一线选择药,但有干咳、血管水肿等不良反应。AII受体拮抗剂沙坦类药物无ACE抑制剂的不良反应,且阻断AII的作用更全面。然而,沙坦类药物在减轻或避免缓激肽诱发干咳症状的同时却缺少了ACE抑制剂调节NO的作用。为了增强这类药物的抗高血压活性并获得NO介导的心血管活性,本课题组以AII受体拮抗剂替米沙坦为先导化合物,应用生物电子等排原理、杂合原理及同系原理等药物设计方法,设计、合成了NO供体型替米沙坦衍生物,并进行了生物活性评价[69-70]。其中化合物WB1106的活性最高,对低钾和高钾引起的动脉条收缩均有较强的抑制作用。WB1106能剂量依赖性地增加cGMP的生成,而相同条件下,替米沙坦对cGMP的生成无显著影响。体内降压实验结果表明,WB1106对大鼠具有较好的降血压作用。重要的是,与等摩尔量的替米沙坦相比,WB1106明显减轻高脂、高碳化合物喂养的大鼠体重增加,改善糖耐量,体现了NO与替米沙坦的协同作用。
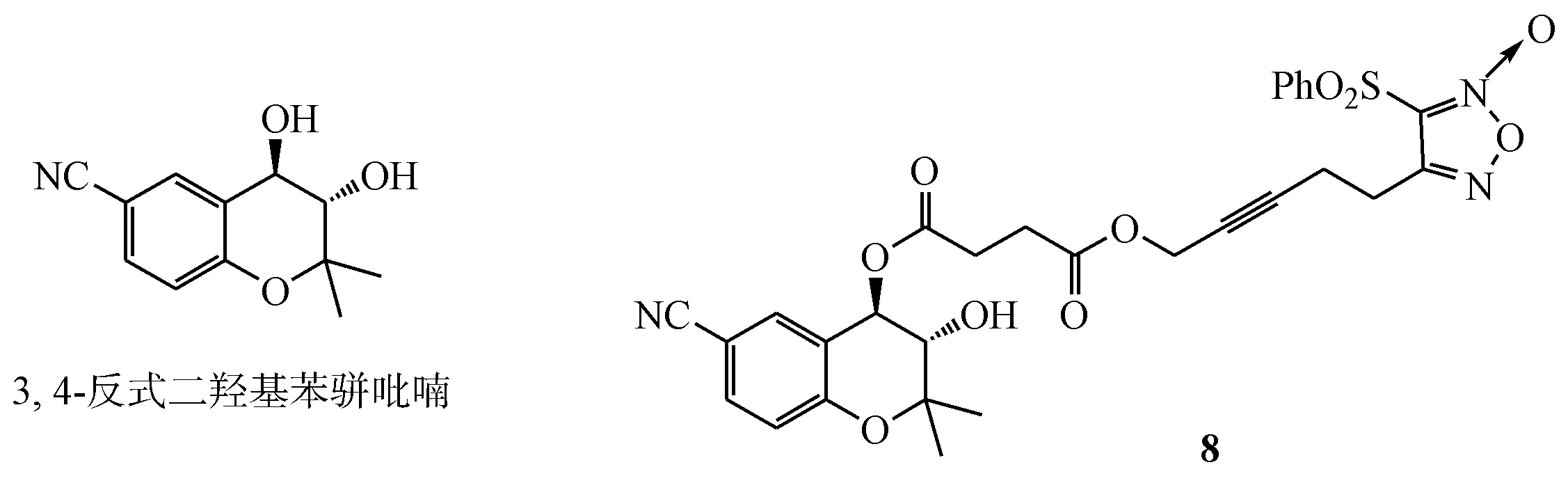
2.3.2 NO供体型苯骈吡喃衍生物 苯骈吡喃为多种心血管药物的基本结构,对心脏有直接保护作用的K+ATP-启开剂——cromakalim是苯骈吡喃的衍生物。本课题组以3,4位反式苯骈吡喃为基本骨架,分别在其3位和4位羟基上连接硝酸酯和呋咱氮氧化物类NO供体,合成了NO供体型苯骈吡喃衍生物,其中化合物8释放适量的NO,对大鼠胸主动脉条收缩具有较强的抑制作用,活性与阳性药吡那地尔(PIN)相当。化合物8对原发性高血压大鼠(SHR)尾动脉收缩压和舒张压的抑制幅度及降压持续时间与PIN相当[71-72]。
2.4 抗阿尔茨海默病药物
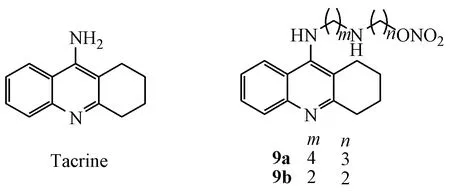
阿尔茨海默病(AD)等痴呆性疾病死亡率仅次于心血管病、肿瘤而位居第3,已成为严重威胁老年人健康和生命的重大疾病之一。研究发现,NO水平下降引起的脑部微循环萎缩及供血不足是诱发AD的重要因素,适量补充外源性NO,可以有效地恢复神经系统NO功能,阻断痴呆症的演变进程[73]。基于此,本课题组以抗AD药物他克林(tacrine)为先导物,在其母核9位引入一个烷基二胺侧链,然后将有机硝酸酯及偶氮鎓二醇盐两类NO供体分别与之连接,设计、合成了NO供体型他克林衍生物,并进行了生物活性评价[74-75]。
目标物显示了与他克林相当或更高(6~8倍)的乙酰胆碱酯酶(AChE)抑制活性,对丁酰胆碱酯酶(BChE)的抑制活性与他克林相当。其中化合物9a能温和地舒张血管,提示其可能具有改善痴呆患者脑部供血的潜在疗效。进一步研究发现,化合物9a的同系物9b在神经元细胞(SH-SY5Y)中能够有效释放低浓度的NO。有趣的是,SH-SY5Y细胞经Aβ损伤后,iNOS被激活,细胞中NO浓度明显高于正常细胞,但加入化合物9b后,NO浓度降低,且呈剂量依赖性,提示它可能通过抑制iNOS的表达,保护神经元细胞免受高浓度NO的毒性损伤,其作用机制类似于NO-NSAIDs[76]。
采用射线形八臂迷宫(radial arm 8-maze)法测试化合物9a改善动物智力的活性。结果表明,化合物9a能够显著地改善东莨菪碱诱导的智力损伤,活性与他克林相当。为考察目标物分子中硝酸酯基团的影响,测定了化合物9a类似物(分子中无硝酸酯片段,其余与化合物9a相同)的体内胆碱酯酶抑制活性。结果显示,类似物的活性较化合物9a明显下降,提示硝酸酯对化合物9a活性发挥重要作用。此外,将类似物与NO供体1-丙基硝酸酯联合用药,体内胆碱酯酶抑制活性并无显著提高;单独应用1-丙基硝酸酯亦未明显改善智力,提示化合物9a的活性优于他克林和NO供体单独给药或联合用药。
研究发现,高剂量的他克林可引起大鼠天冬氨酸转氨酶和乳酸脱氢酶水平显著上升,白蛋白浓度和肝组织蛋白质含量明显下降,但大鼠经口给予等摩尔量的化合物9a后,各项生化指标与空白对照组相比无明显差异。此外,服用他克林的大鼠肝组织出现明显坏死及脂肪性变性,而化合物9a给药后肝组织形态与正常肝组织比较无明显变化。上述结果提示,化合物9a肝脏安全性较好。
2.5 抗肺动脉高压药物
肺动脉高压(PAH)是一类肺血管阻力增大,肺动脉压力升高,最终导致右心衰竭甚至死亡的恶性进展性疾病,素有“心血管系统的恶性肿瘤”之称[77]。目前抗PAH药物主要为血管舒张剂,吸入NO气体也用于PAH的治疗,但频繁吸入、剂量窗口狭窄以及需要特殊装置等限制了其广泛应用[78]。
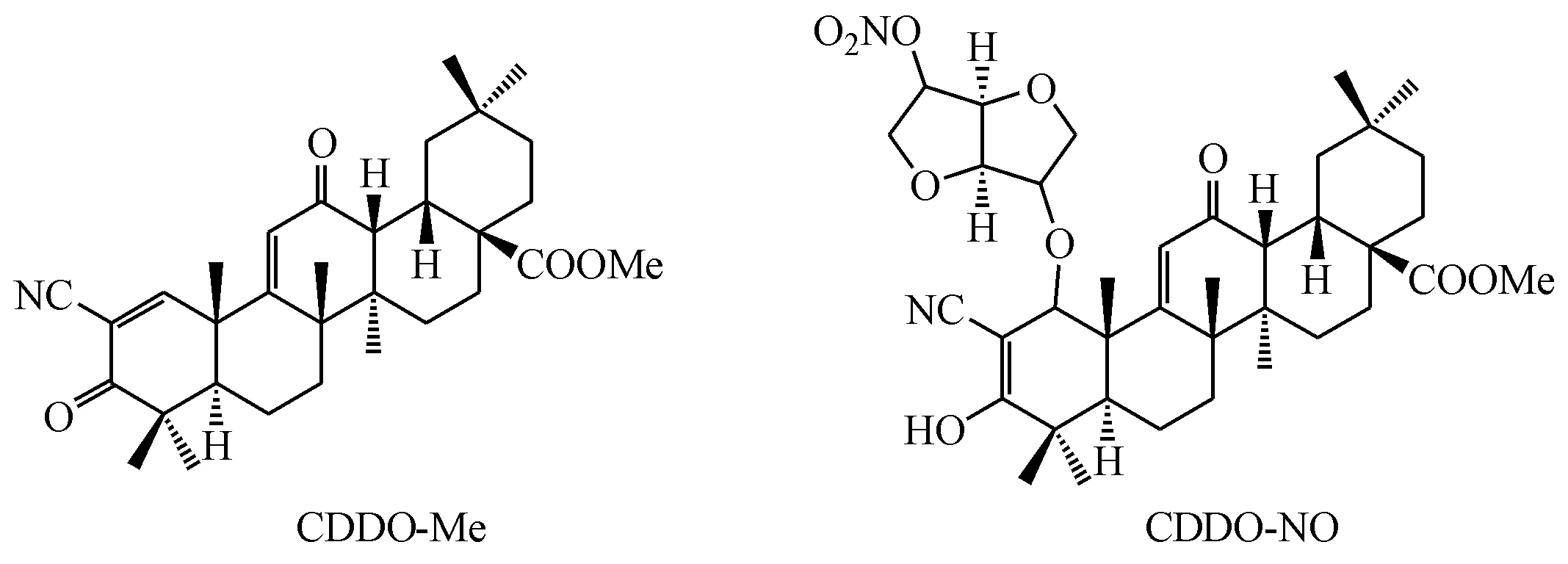
CDDO-Me是一个半合成的齐墩果酸衍生物,它通过抑制NF-κB通路、降低ET-1的分泌、减少ETA的表达而舒张血管。更重要的是,CDDO-Me是Nrf2的诱导剂,具有强效的抗炎、抗氧化作用,改善代谢紊乱,抑制血管增生,防止肺动脉血管重构[79-80]。
本课题组设想,舒张肺动脉血管同时抑制其重构的NO供体型CDDO-Me衍生物可能对PAH具有更好的治疗作用。因此,将CDDO-Me与ISMN进行杂合,得到化合物CDDO-NO。在野百合碱(MCT)诱导的PAH大鼠中,CDDO-NO显著降低平均肺动脉压(mPAP)、右心室收缩压(RVSP)和右心肥厚指数,活性优于CDDO-Me和ISMN单独或联合用药。CDDO-NO明显减少MCT诱导的TGFβ和胶原蛋白的增加,改善了非肌层血管的肺动脉内侧厚度(PAMT)和肌纤维化,减少了肺纤维化形成和血管周围炎性细胞的浸润,抑制了肺动脉血管重构。此外,CDDO-NO可减少PAH大鼠血管周围NOX4阳性细胞以及NOX4的表达,抑制过量的氧化应激,并降低了PAH大鼠右心心肌细胞横断面积和纤维化。这些结果表明,CDDO-NO具有NO和CDDO介导的舒张肺动脉血管和抑制肺动脉血管重构的双重活性,因此发挥了强效的抗PAH作用[81]。目前,课题组正在开展CDDO-NO相关成药性研究,将CDDO-NO固体微粉化后制备混悬吸入制剂,研究其有效剂量范围及其吸入的代谢动力学性质。
2.6 降低其他药物心血管不良反应的药物
2.6.1 NO供体型非甾体抗炎药 传统的非甾体抗炎药(NSAIDs)和环氧化酶-2(COX-2)选择性抑制剂临床应用极为广泛,是仅次于抗感染药的第2大类药物,但严重的胃肠道(GI)不良反应和心血管不良反应限制了它们进一步的应用。NO供体型NSAIDs(NO-NSAIDs)的问世是抗炎药物研究的重大进展,此类药物既抑制COX,产生抗炎、镇痛作用,又具有NO介导的GI和心血管保护作用[76]。本课题组开展了NO-双氯芬酸、NO-氟罗布芬等NO-NSAIDs的研究工作[82-87],本文不再赘述。
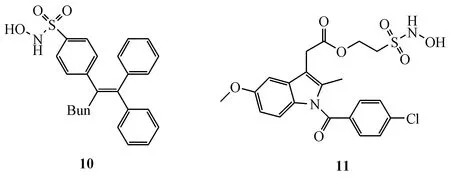
2.6.2 NO/HNO双供体型抗炎药物研究 HNO作为NO-的质子化形式,既具有和NO类似的生物活性,又具有独特的活性,如正性心肌作用,保护心脏免遭缺血再灌注损伤等。本课题组以芳基硫代羟肟酸片段作为潜在的HNO/NO的双供体,与COX-2选择性抑制剂杂合,得到的化合物10可以释放一定量的HNO,体内显示中等抗炎活性[88]。进一步将烷基硫代羟肟酸片段与传统的非甾体抗炎药吲哚美辛杂合得到化合物11,它除能释放适量的NO和HNO,还具有的COX-2选择性抑制活性和强效的体内抗炎活性,无胃肠道等不良反应[89]。
2.6.3 NO供体型甾体类抗炎药 糖皮质激素类甾体药物应用十分广泛,然而药源性的高血压、骨质疏松、胃肠道不良反应等在很大程度上限制了其进一步应用。因此,降低不良反应成为研究新型糖皮质激素类药物的一个挑战性课题。
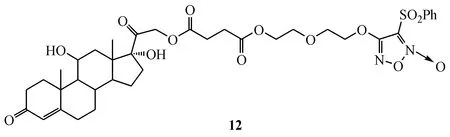
NO具有舒张血管、调节骨代谢以及保护胃肠道等生理活性[90]。有鉴于此,本课题组通过不同连接基团将氢化可的松分别与有机硝酸酯及呋咱氮氧化物两类NO供体杂合,设计、合成了NO供体型氢化可的松衍生物,并对其进行了生物活性评价[91-92]。结果发现,化合物12对角叉菜胶诱导大鼠足跖肿胀的急性炎症、棉球肉芽肿胀诱导的大鼠亚急性炎症以及大鼠佐剂性关节炎类免疫性炎症均具有强效抑制作用,优于等摩尔量的氢化可的松。
研究发现,大鼠连续服用氢化可的松三周后产生明显高血压反应,但服用等摩尔量化合物12的大鼠血压却无显著变化。进一步研究发现,化合物12给药后,大鼠血清中NO含量明显高于氢化可的松组,并呈剂量依赖性,提示NO抑制了高血压的产生。此外,化合物12可促进骨形成及抑制骨吸收,阻止骨流失,提示其能防止氢化可的松所诱导的骨质疏松。
2.6.4 NO供体型抗糖尿病药 2型糖尿病(T2DM)的特征是胰岛素抵抗和胰岛β细胞功能受损,机体对血糖的调控能力下降,最终导致持续性的高血糖和由之引起的多种病理进程,如氧化应激、慢性炎症效应、微血管及大血管并发症等。近年来,多种T2DM治疗药物如罗格列酮(ROG)等已上市,其疗效虽然确切,但具有心血管不良反应。
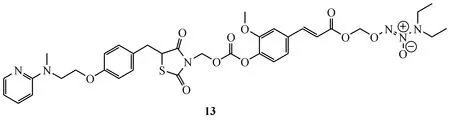
已知NO供体与抗T2DM药物杂合后,可保留降糖活性,同时增加抗血小板聚集和抗高血压等心血管保护作用[93-94]。本课题组以ROG为先导化合物,将ROG通过具有抗炎、抗氧化和心肌保护作用的阿魏酸等与NO供体连接,合成NO供体型ROG衍生物,发现目标物13体内外的降糖活性指标与ROG相当或优于ROG,且在稳定性方面具有优良的前药特性[95]。更重要的是,与等摩尔量的ROG相比,化合物13显著降低心血管不良反应,具体表现为:(1)持续给药18 d后,化合物13引起的db/db小鼠体重增加量比ROG降低了31%;(2))化合物13显著抑制大鼠内髓集合管(IMCD)细胞水通道蛋白2(AQP2)由细胞胞浆迁移至细胞膜表面,提示化合物13引起水钠潴留的可能性低于ROG;(3)对ADP或AA诱导的血小板聚集抑制作用显著优于ROG;(4)化合物13给药组的小鼠血清TNF-α和cTnI水平均显著降低,提示化合物13对心肌细胞具有保护作用;(5)对hERG通道的抑制作用小于ROG,提示化合物13产生心律失常的可能性较小;(6)小鼠经口给予化合物13的急性毒性小于ROG[95]。
3 结语与展望
虽然在NO供体型心脑血管药物及相关药物研究方面本课题组取得了一些进展,但仍面临一些科学难题,正在思考和解决中。
3.1 NO供体与药物作用的强度相当
NO供体型心脑血管药物中NO供体应释放少量、生理需要量的NO,且与药物的作用相当,才能发挥二者最大的药代动力学和药效学优势。选择和应用合适的NO供体和连接基团以及了解它们在体内可能的代谢方式是非常重要的[96]。
3.2 靶向转运、选择性释放NO并与特定分子作用的药物
选择体内能够被特定酶识别或对特定组织具有高度亲和力的载体或连接基团制备NO供体型药物,使其在体内靶向转运至病变部位,然后选择性地在某些组织、细胞内释放药物和NO,并与特定分子作用,以发挥高效、低毒的优点。
3.3 新型NO供体或促进体内NO生成的药物
除了应用直接释放NO或经酶促释放NO的已知NO供体外,可研究释放NO的新型化合物,如NO2–供体、L-精氨酸衍生物等,发挥其缓释NO的优势和特点。还可研究选择性高的eNOS激动剂或eNOS解偶联抑制剂,促进体内NO的生成。
3.4 局部释放NO以减少NO全身不良反应的药物制剂
除口服和注射剂外,可考虑开发局部释放NO的药物制剂,如降低眼内压的滴眼剂、治疗肺动脉高压的气道雾化剂等,以最大限度地减少NO的全身不良反应。
3.5 具有iNOS抑制活性的NO供体型药物
虽然NO供体型药物对一些重大疾病如缺血性脑卒中、类风湿性关节炎、2型糖尿病等具有良好的治疗作用,但考虑到这些疾病发病过程中特别是中后期,iNOS被诱导表达,产生大量的NO,而且已有iNOS抑制剂和NO供体分子杂合或联合用药的报道[97-98],故有必要研究和探索具有iNOS选择性抑制活性的NO供体型药物,并从细胞和分子水平上阐明其作用机制。
3.6 基于NO对蛋白亚硝化修饰的NO供体型药物
蛋白S-亚硝基化(S-NO)是一种NO介导的可逆性蛋白修饰,是NO信号传导以及生物活性的主要机制之一,可引起靶蛋白活性和功能的改变,与磷酰化、乙酰化等蛋白翻译后修饰一样,具有重要的生理、病理作用[99-100]。近年来蛋白-蛋白转亚硝基化反应(transnitrosylation)的发现揭示了NO调节特定信号通路的机制。已知细胞内S-亚硝化的谷胱甘肽(GSNO)是转亚硝基化的重要介质,由NO/SNO信号的调控因子GSNO还原酶(GSNOR)等调控。研究表明,适当抑制GSNOR可增加GSNO水平,对一些疾病具有治疗作用[101-102]。因此,以GSNOR为靶点,研发GSNOR选择性抑制剂,可能具有重要的科学意义和应用价值。
另一方面,可以设计和研究新型NO供体型心脑血管药物,使其选择性地亚硝化体内可引起病变的某些蛋白,如前述的PTEN等,抑制其不良作用,产生抗脑缺血及神经保护等优良活性,也可能具有潜在的应用价值。
总之,有理由相信,随着生命科学和信息科学等学科的发展,药物化学家与分子生物学家、分子药理学家等密切配合,在研究双重或多重作用的NO供体型药物以及探讨其分子作用机制方面,必将取得更大的进展。
致谢:感谢参与本文研究工作的各位老师及博(硕)士研究生。
