稀土铁酸盐的制备及光催化性能*
2021-05-07林永乐蒋琪英李文进邓洪权
林永乐,蒋琪英,李文进,周 熙,邓洪权
(1.西南科技大学 材料科学与工程学院 ,四川 绵阳 621010;2.西南科技大学 工程训练中心 ,四川 绵阳 621010)
0 引 言
随着中国工业化的迅速发展和人们生活水平的提高,大气污染和室内环境污染对人体健康形成严重威胁。因此,工业有机废气的催化治理技术,以及室内空气净化是近年来稀土催化研究最为活跃的领域之一。目前利用稀土催化技术治理工业废气和人居环境净化的工作,主要集中在挥发性有机废气治理、烟气脱硫脱氮、光催化空气净化和焦化污水催化净化等方面[1-4]。ABO3型复合氧化物(A-稀土,碱土金属或碱金属,B-过渡金属)是由两种金属氧化物复合而成,具有钙钛矿层状结构,由于结构的多变性、优异表面性能、同时拥有电、磁性、导电性以及热性能等,在物质检测、环境处理、能源等方面的研究受到广泛关注[5-10]。稀土铁酸盐(ReFeO3)中稀土离子的4f和铁离子的3d间相互作用,使得稀土铁酸盐的结构和磁性呈现多变性,出现大量有关稀土铁酸盐在气敏性、催化性、铁电性、铁磁性等方面的研究[11-17]。目前,ReFeO3的制备方法较多,如微波辅助热分解法、水热法、溶胶凝胶法,固相沉淀法等[18-22]。本文选择了电子结构具有较大差异的5种稀土离子-Y3+、La3+、Sm3+、Gd3+和Ho3+,以分解多胺羧酸为配体的前驱体来制备稀土铁酸盐,并分析各稀土铁酸盐组成、结构和性质的差异。
1 实 验
1.1 实验试剂及仪器
美国TA公司SDT Q 600热重分析仪;日本日立公司TM 3000型扫描电镜;日本Rigaku公司DMAX 1400的X-射线粉末衍射仪(λ=0.15406 nm、扫描范围3~80°、扫描速率4°/min);日本岛津日立Solid Spec 37000紫外可见近红外分光光度计带球积分(BaSO4参比,200~900 nm);日本岛津日立FL 4600荧光光谱仪;美国VARIAN公司UV041型紫外可见分光光度计;自制列管式光催化反应器。
Bi(NO3)3·5H2O(AR),Fe(NO3)3·9H2O,HNO3(AR),二乙三胺五乙酸(H5DTPA)(AR),Y2O3,La2O3,Sm2O3,Ho2O3, Gd2O3,NaAc-HAc缓冲溶液(pH=3.8),甲基橙(MO)。
1.2 稀土铁酸盐的制备
将3.15 g(0.008 mol)H5DTPA加入装有200 mL,80 ℃ 蒸馏水的烧杯中,加热搅拌使H5DTPA全部溶解,接着将硝酸铁(0.008 mol)加入,继续加热并搅拌约30 min,最后将制备好的硝酸钇溶液(0.008 mol)加入,继续恒温搅拌60 min,最后得浅黄色透明溶液。反应完毕后,将烧杯置于80 ℃的烘箱中,保温5天左右,得干凝胶。将干凝胶研磨后置于坩锅中,先在电炉上小火碳化,然后再置于马弗炉中于一定温度下灼烧1 h,待样品自然冷却至室温,取出,研磨,得到砖红色粉末YFeO3。LaFeO3,SmFeO3,GdFeO3和HoFO3的制备与上相同。各稀土铁酸盐的颜色都为深浅不同的棕色。根据稀土,分别命名:YFO,LFO,SFO,GFO和HFO。
1.3 光催化实验
将100 mL浓度为20 mg/L的MO水溶液加入自制的石英管,然后再加入HAc-NaAc缓冲溶液1mL,此时溶液pH=4左右,最后将制备的光催化剂0.1000 g加入上述石英管中。用泵曝气1 h,甲基橙在催化剂表面吸附达到平衡。然后用功率为100 W 的卤素灯(中心波长365 nm)作为光源照射石英管中溶液(光源距离石英管10 cm),使甲基橙进行光降解反应,每隔一定时间从石英管下取样口取样并离心,然后取上层清液进行分析吸光度测定。曝气过程和降解过程反应体系都处于流化状态。根据溶液吸光度数值计算浓度,应用式(1)计算甲基橙溶液的脱色率(R),最后根据甲基橙的褪色率来判断催化剂的催化性。
R(%)=(c0-ct)/c0×100%=(A0-At)/A0×100%
(1)
式中,c0,A0为光照前溶液的浓度(mg/L)和吸光度,ct,At光照时间t后溶液浓度(mg/L)和吸光度。
2 结果与讨论
2.1 前驱体的热稳定性
为了确定前驱体的灼烧温度,将前驱体在动态N2环境中进行热分解测试,热分解曲线见图1(内插图为DSC曲线)。从图1的TG曲线看,所有前驱体大约在500 ℃时灼烧残余物已达到稳定,因此可选择前驱体在600 ℃进行灼烧来制备稀土铁酸盐。对比各TG曲线发现,HFO和SFO这两个铁酸盐的前驱体在200 ℃附近分解剧烈,短时间内失重迅速,DSC曲线反映放热剧烈,而YFO和LFO这两个稀土铁酸盐的前驱体前期热分解较缓慢,在后期(360 ℃)放热量大。SFOHE HFO前驱体的热分解过程、剧烈性以及每个阶段分解温度范围与以甘氨酸为配体制备HFO类似[19],即大致经历4个过程,每个过程形成的中间产物都不稳定,而GFO的前驱体热分解过程激烈程度间于上述两者之间,即200 ℃前失水和硝酸盐分解,300 ℃前配体裂解形成碳酸盐以及碱式碳酸盐等,最后于400 ℃附近开始盐的分解,于500 ℃时分解完全,最终形成稳定的稀土铁酸盐。
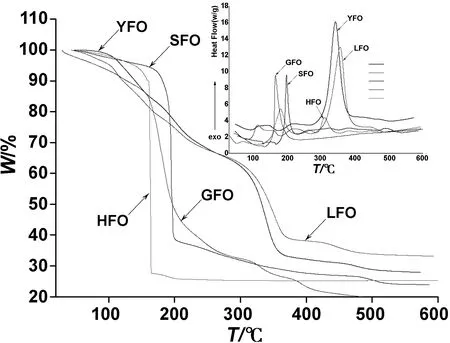
图1 前驱体的TG曲线(内插图为DSC曲线)
2.2 XRD分析
图2为各前驱体在600 ℃下灼烧1 h所得产物的X射线粉末衍射图。从图2各产物的衍射峰相对强度以及数量看,YFO存在两个宽而弱的衍射峰,说明其结晶度很低,为非晶态物质。HFO和GFO衍射峰尖锐且很强,说明产物结晶度高,缺陷少。LFO的衍射峰数量少、尖且较强,说明其结晶度较高,晶体结构对称性高。通常,颗粒的晶化程度越高,晶体的缺陷越少,在进行光催化过程中,光生电子从颗粒内部转移到颗粒表面的路径少且较短,从而降低光生电子和空穴对在体内复合的几率。对于非晶态产物,比表面大,表面不饱和的原子多,同时内部缺陷也较多,有利于对物质的吸附。将各产物的衍射图与标准谱图比较发现,YFeO3为六方晶系(PCPDF No:48-0529),LaFeO3(PCPDF No:82-1958)、SmFeO3(PCPDF No:88-1330)、GdFeO3(PCPDF No:78-0451)和HoFeO3(PCPDF No:74-1479)则为正交晶系。另外,SFO和HFO两者在2θ=29°附近还存在微弱的衍射峰,分别归属于立方晶系的Sm2O3(PCPDF No:86-2479)和Ho2O3(PCPDF No:86-1329)。从上面结果看,含Sm3+和Ho3+的前驱体灼烧后所得产物由两相组成(主相稀土正铁酸盐ReFeO3和微量稀土氧化物Re2O3)的复合物,而其他前驱体灼烧后所得产物均为单相稀土正铁酸盐ReFeO3。这可能与前驱体热裂解相关。TG曲线中,含Sm3+和Ho3+的前驱体在200 ℃附近急剧失重,在电炉上碳化过程中当达到分解点观察到瞬间火花飞溅,释放大量的热,瞬间温度很高,使得少量的稀土氧化物偏析出。选取各自衍射图中最强衍射峰,按谢乐公式d=kλ/Bcosθ(k=0.92,λ=0.154 nm,B对应最强衍射角的半峰宽)对粉末颗粒的粒径进行粗略估算,YFeO3的粒径在10 nm左右,LaFeO3和SmFeO3的粒径在40 nm左右,而GdFeO3和HoFeO3的粒径则大大超过100 nm。另外,从X粉末衍射图还发现,稀土铁酸盐的衍射角则随原子序数增加向高角度方向有轻微的移动,与以燃烧法制备的YFO和LFO一致[24]。这与稀土离子半径相关[25]。在5种稀土离子中,随着稀土离子半径的减小[La3+(0.106 nm)>Sm3+(0.0964 nm)>Gd3+(0.0934 nm)>Ho3+(0.0894 nm)≈Y3+(0.0893 pm)],Re-O键长缩短,Fe-O键受到挤压,Fe-O键长相应缩短,Fe-O-Fe键角缩小,相应晶胞体积缩小,衍射峰向高角度移动。该现象与Cr3+、Tm3+分别对SmFeO3的掺杂以及Na+和Mn2+对LaFeO3[17]的共掺杂后晶体改变一致[16-18]。
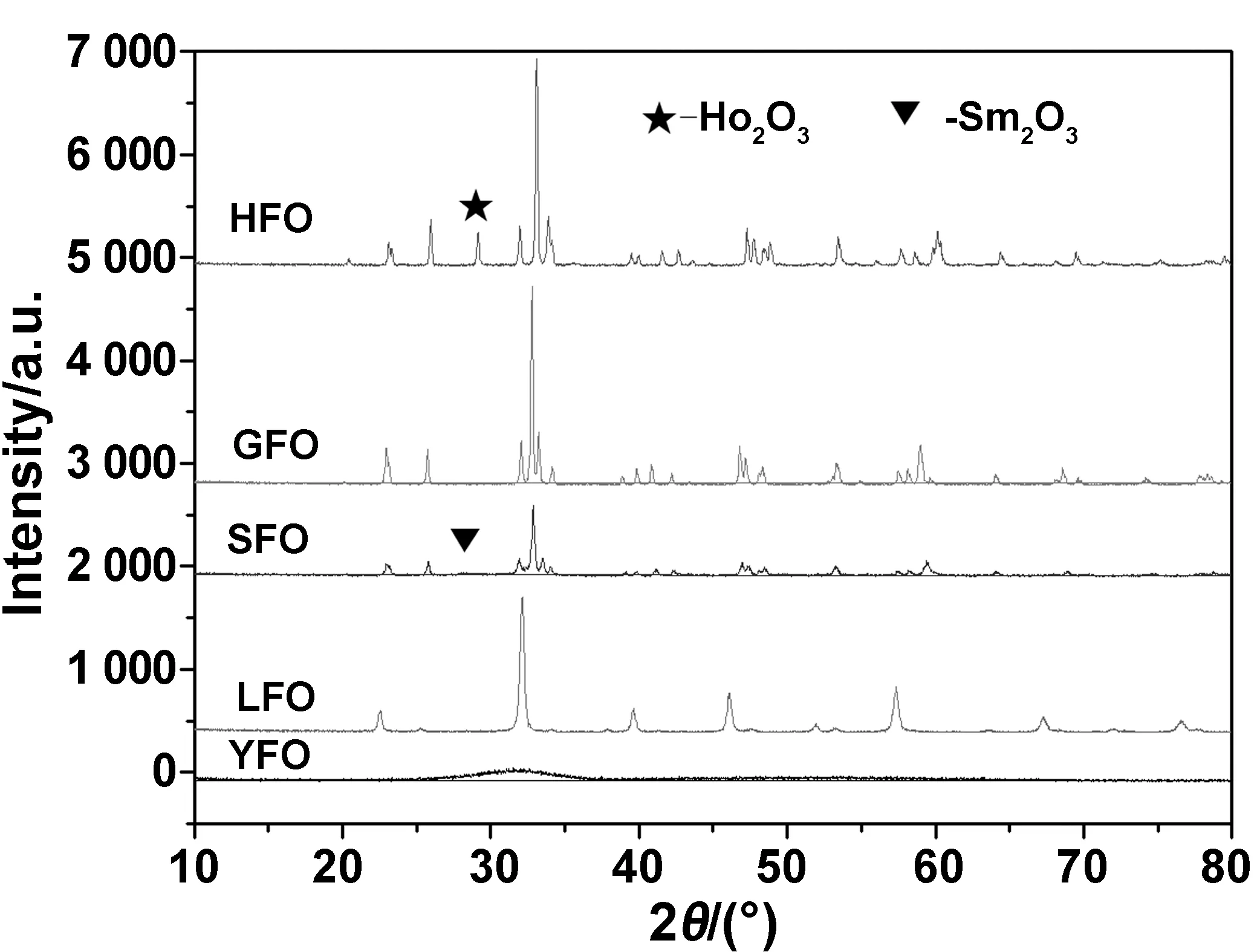
图2 图2稀土铁酸盐的XRD
2.3 表面形貌(SEM)
图3是所有灼烧产物的SEM图。从图中可以看出,YFeO3颗粒很小,均匀,表面粗糙,LaFeO3和SmFeO3呈絮状,表面有大量的空洞、无规则,颗粒间无明显界限,GdFeO3和HoFeO3颗粒不均匀,颗粒粒径很大,颗粒间界面明显,颗粒表面光滑,其中GdFeO3颗粒达5 μm,而HoFeO3颗粒大小不等,超过10 μm,同时表面还有少量无规则的颗粒存在。引起GdFeO3和HoFeO3颗粒大、表面光滑是因为前驱体在配体裂解过程中反应太快,放热量大,导致体系瞬间温度过高,从而GdFeO3和HoFeO3出现烧结状态。

图3 不同铁酸稀土的SEM图
2.4 光谱分析
所有产物的紫外-可见漫反射光谱如图4所示,内插图为其(αhv)2-hv曲线。从图4可以看出,所有产物在200~500 nm范围具有强吸收,归属于O2-与Fe3+和Re3+电荷跃迁,在500~700 nm范围也存在弱吸收,归属于Fe3+的d-d以及Re3+的f-f电子跃迁。产物对光响应范围宽,为充分利用太阳光提供有利条件。同时,相对于GFO和HFO陡峭的吸收边,YFO、LFO和SFO的吸收边比较平慢,这可能是结晶度低使得缺陷较多造成的。另外,在(αhv)2-hv图中,可对每条曲线作切线,切线与x轴相交点即为各铁酸盐的带隙宽度Eg,结果见表1。利用公式(2)和(3)[23]得出各产物的能带结构,结果见表1。

图4 稀土铁酸盐的紫外-可见漫反射光谱图
ECB=x-Ec-0.5Eg
(2)
EVB=ECB+Eg
(3)
上式中x为物质电负性,Ec为4.5 eV(vs NHE),ECB为导带,EVB为价带。
从表1看出,YFeO3的带隙最窄(1.93 eV),价带位置最高,达3.074 eV,和文献值相差较大[18,20]。高价带使得光生空穴(h+)具有更高的氧化性,利于生成高活性自由基·OH[E(·OH/H2O=2.54 V],但导带位置过高,不能通过光生电子使O2形成·O2-[E(O2/·O2-)=-0.137 V][25]。SmFeO3的带隙最大(2.48 eV),与文献一致[25],而导带位置较低(-0.267 eV),为·O2-的生成提供了有利条件[24]。LaFeO3的带隙小于文献中的2.48 eV[24],与由抗坏血酸作辅助溶胶凝胶制备的产物一致[26]。GFO和HFO的带隙及能带结构相差不大。能带结构的差异由带隙以及稀土元素的电负性共同作用引起的。
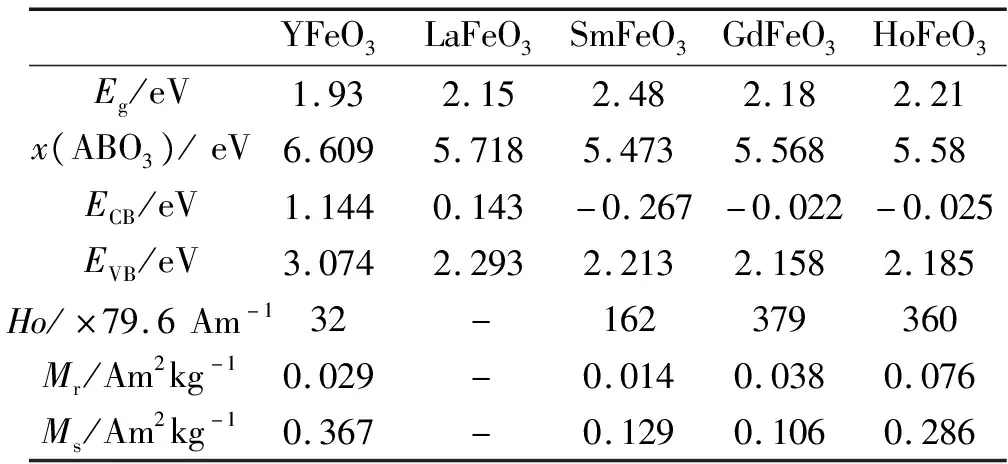
表1 产物的能带结构及磁参数
荧光光谱常用来评价光催化剂在催化过程中光生载流子对的复合情况,荧光强度越强则其光生载流子复合的几率越大。图5反映了各产物在254 nm激发下荧光情况。对比图5中各产物中最强峰的荧光强度发现存在:GFO≈LFO>SFO>HFO>YFO。说明光照时光生载流子复合几率最小的是YFO,而复合几率较大的是GFO和LFO。
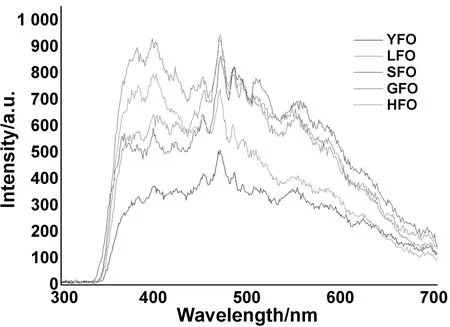
图5 稀土铁酸盐的荧光光谱(λex=254 nm)
2.5 磁性分析
图6是所有产物在室温下的磁滞回线,反映了这些铁酸盐磁性对外磁场的敏感性。从图中可以看出,YFeO3的磁化程度对外磁场强度较敏感,磁滞回线很窄,呈细长的S型,矫顽力较大,表现出弱铁磁性,与文献类似[18,24]。LFO的磁化程度对外磁场强度不敏感,磁滞回线呈线性,表现为反磁性或顺磁性,而其他方法制备的LFO则表现为弱铁磁性[16,24]。SFO、GFO和HFO的磁滞回线较宽,属于典型的弱铁磁性,且磁滞回线宽度随原子序数增加而不断变宽。各产物相关磁参数见表1。从表1可见,所有产物的剩磁都很低,其中HFO的剩磁强度最大(0.076 Am2/kg),YFO的矫顽力最大,同时随着稀土原子序数的增加,铁酸盐的铁磁性增强。产物磁性的差异与稀土铁酸盐的磁性来源有关。稀土铁酸盐的磁性来源于各种离子的固有磁矩以及晶体内部各种离子间的超级交换(Fe3+-Fe3+、Re3+-Re3+以及Re3+-Fe3+)[14-17,19,22-23,25-26]。YFO中Y3+离子无单电子,Fe3+-Fe3+间超级交换引起电子自旋不完全反平行,从而表现为弱铁磁性,其剩磁为0.029 Am2/kg。LFO中La3+(4f06s0)无单电子,因此不存在Re3+-Re3+和Re3+-Fe3+间的超级交换作用,仅存在Fe3+-Fe3+通过O2-离子发生超级交换,由于晶体结构的对称性使得Fe3+的3d层电子自旋方向完全反向平行,因此表现为反铁磁性或顺磁性。Sm3+(4f56s0)、Gd3+(4f76s0)和Ho3+(4f106s0)的4f轨道均存在未成对的单电子,固有磁矩不断增加Sm3+(1.54 B.M.)、Gd3+(8.2 B.M.)和Ho3+(10.5 B.M.),同时离子半径不断降低,使得Fe-O-Fe 键角缩小,FeO6八面体倾斜加大,这样Fe3+电子自旋不完全反平行增加,从而铁磁性增强[15,17,24-25]。
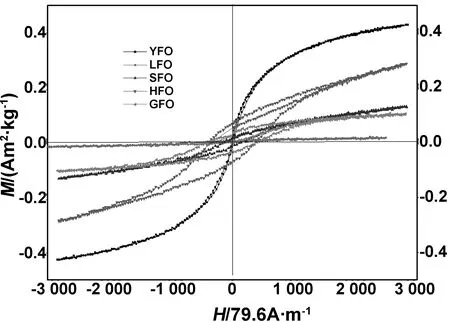
图6 产物的磁滞回线
2.6 光催化性能分析
图7反映了MO在所得产物催化下随光照时间延长的降解情况。从图中可以看出,当光照4 h后,MO在无催化剂作用下的降解率仅为15%,而有催化剂作用下的降解率超过75%。由此说明,这些灼烧产物对MO的光降解具有明显的催化作用。对比各稀土铁酸盐对MO降解的催化效果发现,YFO的催化能力更强,其次是SFO和HFO,而LFO稍微弱一些。对MO光降解催化的差异性由多种因素造成的。从避光曝气1h后MO在催化剂的吸附来看,YFO和SFO对MO的吸附量最大,而HFO对MO的吸附量最小。催化反应在颗粒内表面上进行,底物在催化剂表面吸附越多,底物降解也就越快。而吸附量多少与比表面有关。从XRD和SEM结果可知,YFO为非晶态物质,SFO结晶度也很低且存在大量的空洞,因此它们的比表面很大,使得MO在其内表面吸附量大。HFO结晶度很高,颗粒大,这样比表面积小,所以对MO的吸附量小。同时,YFO和SFO的低晶化度有利于产生大量捕获光生电子的氧空位缺陷,可降低光生载流子间的复合,从而提高光催化。FL表征结果也反映了这一结果。FL表明,YFO的FL相对强度最低,具有最小的光生载流子复合几率,而GFO和LFO两者的FL相对强度较高,光催化过程光生载流子复合几率较大,这样催化效果较低,因此MO的降解率也就较低。另外,能带结构表明,YFO的高价带使光生空穴h+具有更高的氧化性,而SFO的低导带使光生电子e-具有更高的还原性,光生电子(e-)和空穴(h+)是使MO光降解过程必要的各种高化学活性自由基(·OH和·O2-)的关键因素。从荧光结果看,SFO和HFO的荧光强度相对较高,但对MO降解的催化作用却比较强,这可能与形成的产物组成有关。SFO和HFO体系均由大量稀土正铁酸盐和微量的稀土氧化物组成复合物,两相间可形成有利于光生载流子的分离的异质结,从而提高其光催化性。HFO的高催化性还可能与形成高晶化程度的晶体有关。通常结晶度越高,晶体内部的缺陷就越少,底物从内表面到外表面的迁移路径简单且缩短,这也可降低光生载流子对间的复合几率,提高催化性。
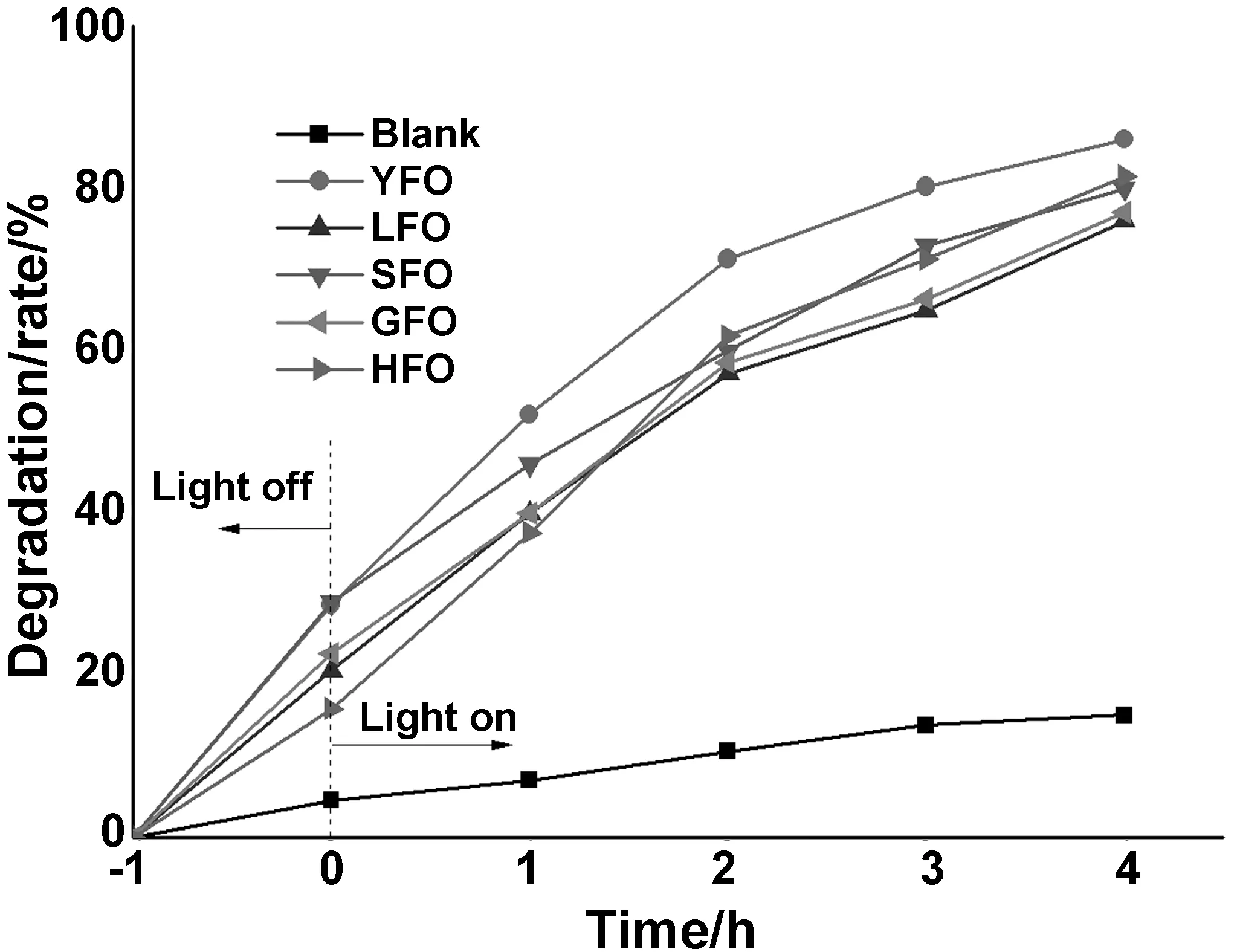
图7 MO在催化剂存在随光照的降解曲线
3 结 论
(1)600 ℃下灼烧配位前驱体干凝胶,可得到粒径大小、晶化程度以及组成、结构不同的稀土铁酸盐,其中含Y3+、Gd3+和La3+的灼烧产物为单相ReFeO3,而含Sm3+和Ho3+的灼烧产物则是由稀土正铁酸盐(ReFeO3)和微量稀土氧化物(Re2O3)构成的复合物。这些铁酸盐中,YFeO3为畸变六方钙钛矿结构,而其他稀土的铁酸盐均为畸变正交钙钛矿结构;
(2)所有灼烧产物对光从紫外区到可见区都有较强的响应,带隙大小顺序为YFO (3)室温下YFO对外磁场很敏感,而LFO则呈现顺磁性或反铁磁性,而其他稀土铁酸盐则表现出强度不同的弱铁磁性。灼烧产物的铁磁性随稀土离子半径的减小以及4f轨道上电子数的增加而增强; (4)所有灼烧产物对MO溶液光降解均具有较强的催化性,光照4h能使MO溶液中MO降解75%。催化性强弱为:YFO>HFO>SFO>GFO>LFO。从灼烧产物的晶化程度,颗粒的比表面积、能带结构以及产物组成等多方面分析了引起MO降解差异性的原因。当灼烧产物具有较大的比表面积、适度的晶化程度和氧空位数、较高的价带和较低的导带以及异质结构的形成,则有利于催化剂催化性的提高。
