离子色谱法测定阿仑膦酸钠片含量的不确定度评定
2021-05-07叶红兵
叶红兵
(合肥市食品药品检验中心,合肥 236000)
阿仑膦酸钠片主要成分是阿仑膦酸钠,为氨基二膦酸盐骨代谢调节剂[1–2]。该调节剂与骨内羟磷灰石有很强的亲和力,能进入骨基质羟磷灰石晶体中。当破骨细胞溶解晶体,药物被释放,能抑制破骨细胞活性,并通过成骨细胞间接起到抑制骨吸收效应,防止骨质的丢失[3–5]。准确测定阿仑膦酸钠片的含量可以有效控制药品质量,《中国药典》2015 年版中阿仑膦酸钠片含量的测定采用离子色谱法[6–7]。利用不确定度评定,可以定量评价测量结果的质量和可信度。目前离子色谱法测定阿仑膦酸钠片含量的不确定度评定未见报道[9–14]。为了提高阿仑膦酸钠片含量检测方法的准确度,笔者对离子色谱法测定阿伦膦酸钠含量不确定度进行评定,依据《中国药典》和JJF 1059.1–012 《测量不确定度评定与表示》[15],分析影响不确定度的因素,并对各个不确定度分量进行评估,最终给出测量结果的置信区间和置信水平。建立适用于离子色谱法测定阿伦膦酸钠含量不确定度的评定方法,有助于在药品检验过程中,严格按照标准操作,从而提高检验水平,也为测定结果的科学评估提供依据。
1 实验部分
1.1 主要仪器与试剂
离子色谱仪:ICS–1600 型,美国赛默飞世尔科技公司。
超声波清洗器:S120H 型,德国ELMA 公司。
电子天平:Mettler–Toledo XP205 型,十万分之一,瑞士梅特勒公司。
超纯水仪:Cascada I 型,颇尔(中国)有限公司。
离心机:Centrifuge5430R 型,德国艾本德公司。
草酸:分析纯,国药集团化学试剂有限公司。
阿仑膦酸钠对照品:含量为83.0%,编号为100901–201302,中国食品药品检定研究院。
阿仑膦酸钠片:批号为20190401,万特制药(海南)有限公司。
实验用水为超纯水。
1.2 对照品溶液的配制
精密称取2 份阿仑膦酸钠对照品适量,分别置于2 只25 mL 容量瓶中,加水溶解并稀释至标线,摇匀,过滤,分别为对照品溶液1、对照品溶液2。
1.3 供试品溶液的制备
取20 片阿仑膦酸钠样品,精密称定,研细,过孔径为1.8 mm 的筛,精密称取10 份阿仑膦酸钠细粉各20 mg 于10 只50 mL 容量瓶中,加水适量,超声溶解,用水稀释至标线,摇匀,以3 000 r/min 转速离心3 min,取上清液,过滤,作为供试品溶液。
1.4 色谱条件
保护柱:Dionex Ion-PacTMAG23 阴离子交换色谱柱(250 mm×4 mm,美国赛默飞世尔科技公司);检测器:电导检测器;检测方式:非抑制电导检测;柱温:30 ℃;流动相:6 mmol/L 的草酸溶液,流量为1.0 mL/min。
1.5 测量值与输入量的数学模型
样品中阿仑膦酸钠含量按式(1)、式(2)计算:

式中:X——样品中阿仑膦酸钠的标示值,%;
ft——供试品溶液制备时的稀释倍数;
249.08——阿仑膦酸的相对分子质量;
271.06——阿仑膦酸钠的相对分子质量;
mt——样品质量,g;
B——标示量,mg;
F——对照品溶液响应因子;
As——对照品色谱峰面积;
fs——对照品溶液制备时的稀释倍数;
ms——对照品质量,g;
P——对照品纯度,%。
2 不确定度来源
参考《中国药典》[1–2]和JJF 1059.1–012 《测量不确定度评定与表示》[3],根据1.5 数学模型,确定阿仑膦酸钠含量的不确定度来源:
(1)A 类不确定度。重复性测定引入的相对标准不确定度。
(2)B 类不确定度。a.天平称量,包括样品的称量和对照品的称量;b.稀释定容,包括样品的稀释定容和对照品的稀释定容;c.离子色谱仪引入的相对标准不确定度。
3 不确定度评定
3.1 重复性测定引入的相对标准不确定度
对10 份供试品进行测定,数据结果见表1。

表1 10 份供试品测定结果 %
重复性测定引入的标准不确定度:
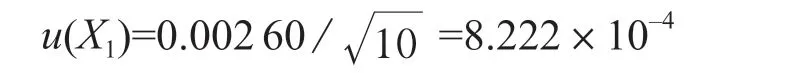
重复性测定引入的相对标准不确定度:

3.2 天平称量引入的相对标准不确定度
天平称量引入的不确定度主要包括重复性标准偏差引入的不确定度u1和示值最大误差引入的不确定度u2。实验室环境相对独立,称量迅速且及时,环境温度、湿度在短时间内变化甚微,对称量结果的影响可忽略不计。
3.2.1 供试品称样量(mt)引入的不确定度分量
20 片阿仑膦酸钠的质量为4.379 2 g。计算得每片平均质量为0.219 0 g,标示量为70 mg/片,平行称取10 份样品,称量结果见表2。

表2 平行10 份样品称量结果 mg


天平称量允许的最大误差为±0.03 mg,样品需称取10 次,按均匀分布考虑,K= 3,天平称量示值最大误差引入的标准不确定:

称取64.35 mg 供试品的标准不确定度:
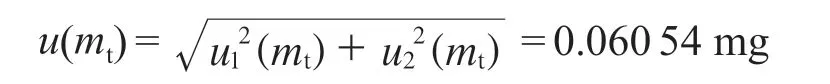
64.35 mg 供试品称样量引入的相对标准不确定度:urel(mt) = u(mt)/64.35=9.408×10–4。
3.2.2 对照品称样量(ms)引入的不确定度分量
平行称取对照品2 份,测得量分别为10.97、11.52 mg,平均值为11.24 mg。由天平检定证书提供,天平称量重复性的标准偏差为0.01 mg ,按均匀分布考虑,K= 3,天平称量的重复性引入的不确定度:u1(ms) = 0.005 77 mg。
天平称量允许的最大误差为±0.03 mg,对照品称取2 次,按均匀分布考虑,K= 3,天平称量的准确性引入的不确定度:u2(ms)=0.072 08 mg。称取11.24 mg 对照品的标准不确定度:

称取11.24 mg 对照品引入的相对标准不确定度:urel(ms) = u(ms)/11.24 = 6.433×10–4。
3.3 定容体积引入的相对标准不确定度
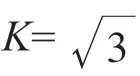
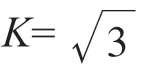
定容至50 mL 容量瓶引入的相对标准不确定度:urel(Vs50) = 8.166×10–4。
3.4 离子色谱仪测量引入的相对标准不确定度
取对照品溶液1 连续进样6 次,测得色谱峰面积分别为8.789、8.803、8.823、8.823、8.862、8.862,计算标准偏差为0.025 7,测定结果的相对标准偏差为2.92×10–3,则离子色谱仪测量引入的标准不确定度:u(X2) = 0.025 7/ 6 =10.49×10–3。离子色谱仪测量引入的相对标准不确定度:
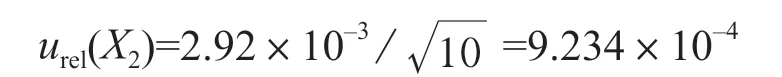
3.5 合成相对标准不确定度
各分量的不确定度来源彼此独立不相关,合成各相对标准不确定度分量,采用离子色谱法测定阿仑膦酸钠片含量的相对标准不确定度:
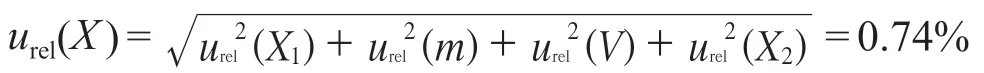
3.6 扩展不确定度
在95%置信概率下,k=2,相对扩展不确定度:

4 结语
阿仑膦酸钠片含量测定的不确定度主要来源于样品制备的定容体积和天平称量引入的不确定度。因此,分析人员要熟练掌握测定的各个操作技术,严格按照规定进行测定。
