PD-L1 在非小细胞肺癌中表达的检测方法
2021-05-06钟国方综述袁霞审校广东省惠州市中心人民医院肿瘤内科广东惠州516000
钟国方(综述),袁霞(审校)(广东省惠州市中心人民医院肿瘤内科,广东惠州516000)
肺癌是全球发病率和致死率最高的恶性肿瘤。2018 年全球肿瘤统计分析报告显示,全球肺癌的男女发病率分别为:年龄标化率(age standardized rate,ASR)1.5/10 万和14.6/10 万;病死率为ASR 27.1/10 万和11.2/10 万[1]。按病理组织学分类,肺癌可分为小细胞肺癌和非小细胞肺癌(non-small cell lung cancer,NSCLC)两大类,其中NSCLC 作为最常见的肺癌组织学类型,占所有肺癌的85%,其5 a 生存率仅为16%[2]。免疫治疗,特别是免疫检查点抑制剂(immune checkpoint inhibitors,ICIs)自问世以来,已在多个肿瘤包括肺癌在内的治疗领域取得了突破性的进展,相继批准以程序性死亡受体-1(programmed death-1,PD-1)/程序性死亡配体-1(programmed deathligand 1,PD-L1)为靶点的ICIs 用于肺癌治疗,免疫治疗为晚期NSCLC 的治疗带来了新希望。因此,筛选合适人群以期在免疫治疗中获得更好的疗效尤为重要。现今,越来越多的研究证实,肿瘤细胞上PD-L1的表达可预测肺癌患者对ICIs 的反应性,PD-L1 已作为免疫治疗的预测生物标志物。因此,本文旨对NSCLC 患者PD-L1 表达的相关检测进行综述。
1 PD-L1 的表达与检测方法
PD-L1 是属于B7 配体家族的1 型跨膜蛋白(B7H1),可在造血细胞(树突状细胞、巨噬细胞、肥大细胞、T 细胞和B 淋巴细胞)和非造血细胞(包括内皮细胞、上皮细胞和肿瘤细胞)上表达。肿瘤细胞上PDL1 的表达通过与调节性T 细胞受体PD-1 结合抑制T 细胞炎性活动,促进免疫系统对肿瘤的抑制和自我耐受。在B7 家族的配体中,PD-L1 是NSCLC 的主要膜抑制配体,也是目前研究最多的配体[3]。
PD-L1 表达的检测对PD-1/PD-L1 抑制剂的应用有重要价值。PD-L1 的检测是基于细胞蛋白水平的检测,因此临床试验中以免疫组织化学(IHC) 方法为主。免疫组织化学是检测蛋白表达的经典手法,通过抗体着色后由病理医师镜下观察着色深浅和阳性细胞比例。在诊断病理学中,重要的是用一个有效IHC 计数,它能可靠地检测PD-L1 阳性病例。
2 PD-L1 的临床意义
用PD-L1/PD-1 抗体进行的免疫治疗在晚期NSCLC 患者中显示出令人鼓舞的结果。KEYNOTE-001 的研究结果发现[4],晚期初治NSCLC 患者应用帕博利珠单抗治疗的5 a 总体生存(overall survival,OS)率为23.2%,中位OS 为22.3 个月,而对于初治PD-L1高表达的NSCLC 患者从帕博利珠单抗中获益最大,特别是PD-L1 肿瘤细胞阳性比例分数(tumor proportion score,TPS) ≥50%的患者5 a 的OS 率为29.6%,中位OS 为35.4 个月。对KEYNOTE024 研究结果显示帕博利珠单抗在PD-L1 表达≥50%的驱动基因阴性晚期NSCLC 人群中,与标准的含铂化疗相比,使用帕博利珠单抗的患者其OS 得到了显著的改善,中位OS 为26.3 个月,而化疗组中位OS 为14.2个月(Hr=0.65,95%CI:0.50~0.86,P=0.001),3 a 的OS率,两组分别为43.7%和24.9%[5]。基于KEYNOTE-024 研究,2016 年美国食品药品监管局(FDA)批准帕博利珠单抗用于PD-L1≥50%的驱动基因阴性晚期NSCLC 的一线治疗。在此研究基础之上,KEYNOTE-042 研究进一步探索了在PD-L1 表达≥50%、≥20%和≥1%的NSCLC 患者帕博利珠单抗单药一线治疗的效果,结果提示对所有评估PD-L1 TPS 状态(TPS≥50%、≥20% 和≥1%)且无EGFR/ALK 改变的未经治疗的局部进展或转移性NSCLC的中国患者而言,帕博利珠单抗较含铂方案化疗可以明显改善OS,其中PD-L1≥50%人群的疗效最为显著[6]。基于KEYNOTE-042 的研究结果,2019 年FDA和中国国家药品监督管理局(NMPA)批准了帕博利珠单抗作为单一疗法,用于一线治疗PD-L1≥1%、人表皮生长因子受体EGFR/ALK 阴性晚期NSCLC 患者。
IMpower 110 研究是一项3 期、开放标签的随机对照研究,比较阿特珠单抗单药对比铂类(顺铂或卡铂)联合培美曲塞或吉西他滨用于治疗经PD-L1 筛选的初治Ⅳ期NSCLC 患者,其中期OS 分析结果显示,对于高表达的TC3/IC3(PD-L1≥50%)患者,阿特珠单抗单药一线治疗较标准化疗有显著的OS 获益[7]。除了在一线单药上的相关研究,在联合化疗及二线治疗上也取得了进展。
3 PD-L1 检测试剂与平台
PD-L1 表达检测目前主要是2 家公司的4 种检测技术:美国安捷伦公司(Agilent)的Dako PD-L1 IHC 22C3 pharmDx 和Dako PD-L1 IHC 28-8 pharmDx ;瑞士罗氏公司(Roche)的VENTANA PD-L1 (SP142)Assay 和VENTANA PD-L1(SP263) Assay(表1)。
3.1 PD-L1 IHC 22C3 pharmDx
Dako 22C3 pharmDx 是首个获得监管部门批准的PD-L1 IHC 试剂盒之一,也是迄今为止唯一一个获得美国食品和药物管理局(FDA)监管地位的“伴随”诊断试剂盒,用于治疗经治和初治的晚期NSCLC患者。用小鼠单抗22C3,在Dako Autostainer Link 48染色平台上检测来评价福尔马林固定石蜡包埋(FFPE)组织中的肿瘤细胞,至少需要100 个肿瘤细胞,当观察到肿瘤细胞的膜染色(部分或完全)≥1%时,定义为PD-L1 表达阳性。
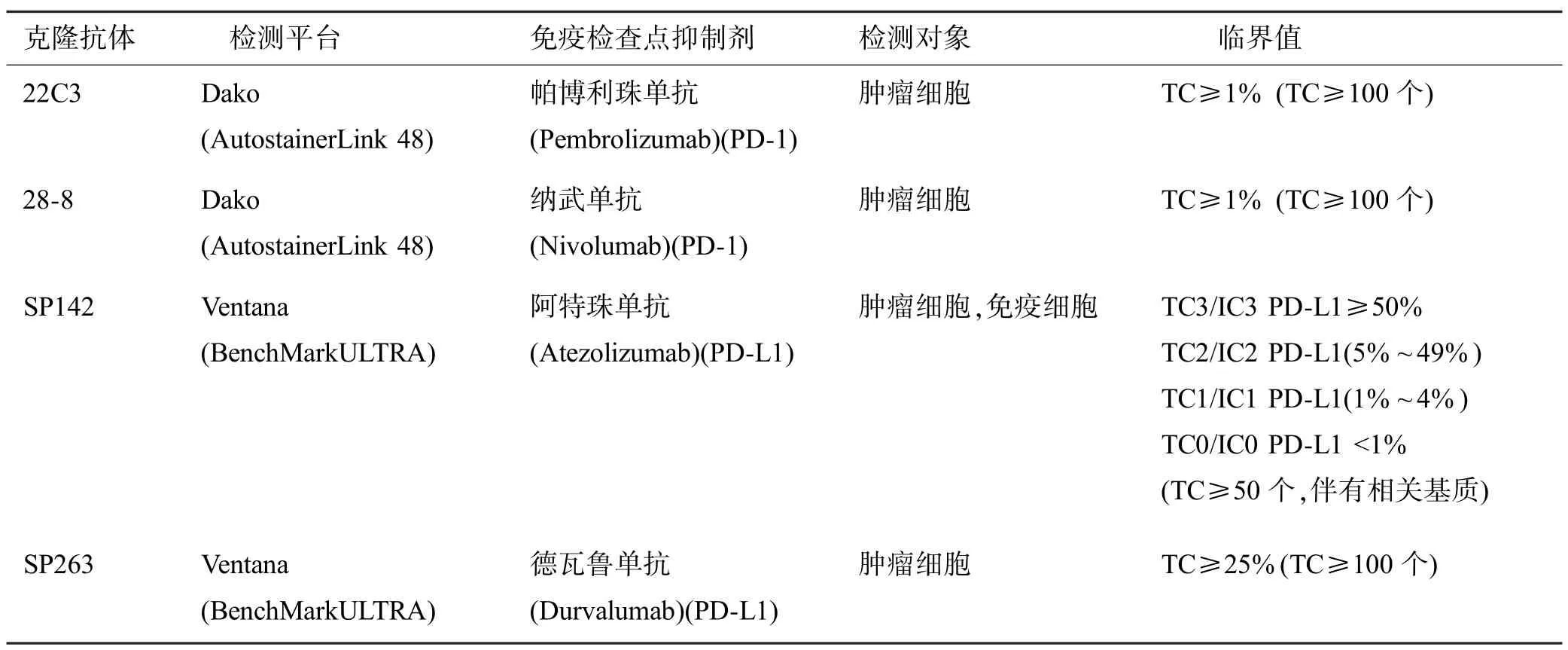
表1 NSCLC PD-L1 IHC 检测抗体及平台的比较
3.2 PD-L1 IHC 28-8 pharmDx
Dako 28-8 pharmDx 是一种定性的PD-L1 免疫组化检测抗体,作为一种“补充”诊断试验获得美国FDA 的批准。用兔单抗28-8 在Dako Autostainer Link 48 染色平台上检测来评价FFPE 组织样本中的肿瘤细胞,至少需要100 个肿瘤细胞来定位PD-L1,并且阳性定义为TPS ≥1%。
3.3 PD-L1 IHC SP142 Assay
Ventana SP142 Assay 使用与蛋白的细胞内结构域结合的兔单克隆抗体,其已被美国FDA 批准为治疗在含铂化疗期间或之后进展的转移性NSCLC 患者以及晚期尿路上皮癌患者使用阿特珠单抗(atezolizumab)治疗的“补充”诊断工具。用SP142 在VENTANA BenchMark ULTRA 染色平台同时评估PD-L1 在肿瘤细胞(NSCLC,≥50%的肿瘤细胞染色,任何强度)和肿瘤浸润免疫细胞(NSCLC≥10%免疫细胞染色和尿路上皮癌≥5%免疫细胞染色为阳性)的表达,FFPE 样品中的评估至少需要50 个肿瘤细胞。肿瘤细胞评分不需要与肿瘤相关的基质,但对肿瘤浸润免疫细胞(IC)评分是必不可少的。
3.4 PD-L1 IHC SP263Assay
PD-L1 SP263 Assay 是兔单克隆抗体,可与跨膜糖蛋白结合。用Ventana SP263 在VENTANA BenchMark ULTRA 染色平台来评估FFPE 中PD-L1 的表达组织,用于鉴定最有可能受益于德瓦鲁单抗(durvalumab)的局部晚期或转移性尿路上皮癌患者。对于德瓦鲁单抗治疗,当在至少25%的肿瘤细胞中观察到任何强度的质膜蛋白染色时,认为PD-L1 细胞呈阳性。确定TPS 至少需要100 个肿瘤细胞。
4 PD-L1 表达检测的实践
4.1 检测抗体的选择
PD-L1 表达时存在两个问题:首先,同一抗体克隆在不同肿瘤中显示出不同的染色能力,而不同抗体克隆在同一肿瘤中,尤其是在免疫/基质细胞中显示出不同的染色能力(表2);第二,不同抗体检测平台及结果临界值设定不一致[8]。Hirsch 等[9]旨在提供有关临床试验中使用的四种PD-L1 IHC 检测抗体的分析和临床可比性的信息。通过四种PD-L1 IHC 抗体(22C3、28-8,SP142 和SP263)对39 例NSCLC 肿瘤进行了染色。3 位专家进行了独立评估,分析比较表明,当使用22C3、28-8 和SP263 抗体时,PD-L1 染色的肿瘤细胞的百分比是可比的,而SP142 显示总体上染色的肿瘤细胞较少。所有的抗体都证明了可对免疫细胞染色,但是比肿瘤细胞染色具有更大的变异性。通过比较抗体和临界值,研究表明,尽管在三种抗体中PD-L1 表达的分析性能相似,但互换抗体和临界值将导致某些患者的PD-L1 状态“分类错误”。Chan 等[10]使用4 种PD-L1 IHC 检测抗体(即22C3、28-8,SP142 和SP263)评估了713 个连续的NSCLC中PD-L1 的表达。在这4 种抗体中,22C3、28-8 和SP263 的肿瘤细胞评分高度一致,当临界值设为≥50%时,一致性>97%。
美国的一项研究中,使用28-8 和22C3 抗体对1930 例患者(包括412 例确诊为肺癌)进行了PD-L1 IHC 检测,结果显示,PD-L1 IHC 28-8 和22C3 在所有样本中以及在经确诊为肺癌诊断的样本中均显示出强相关性,所有样本整体一致性(OPA)达到97%~98%[11]。Fujimoto 等[12]使用22C3 和SP263 抗体在不同临界值(≥50%和≥1%)下对NSCLC 标本进行PD-L1 IHC 检测,结果表明22C3 和SP263 数据之间的总体一致性为80%~99%,这两种抗体可互换选择使用。但Munari 等[13]却得出相反的结论,当临界值设为50%时,两位病理学家将SP263 阳性的病例中大约一半定义为22C3 阴性,因此认为PD-L1 检测22C3 和SP263在NSCLC 中是不可互换的。Xu 等[14]探究SP142 和22C3 抗体是否可以互换,用22C3 和SP142 抗体检测了135 个肿瘤样品的组织学切片。与SP142 相比,22C3 通常会低估肿瘤细胞和免疫细胞中PD-L1 的表达,因此两种抗体不能互换。
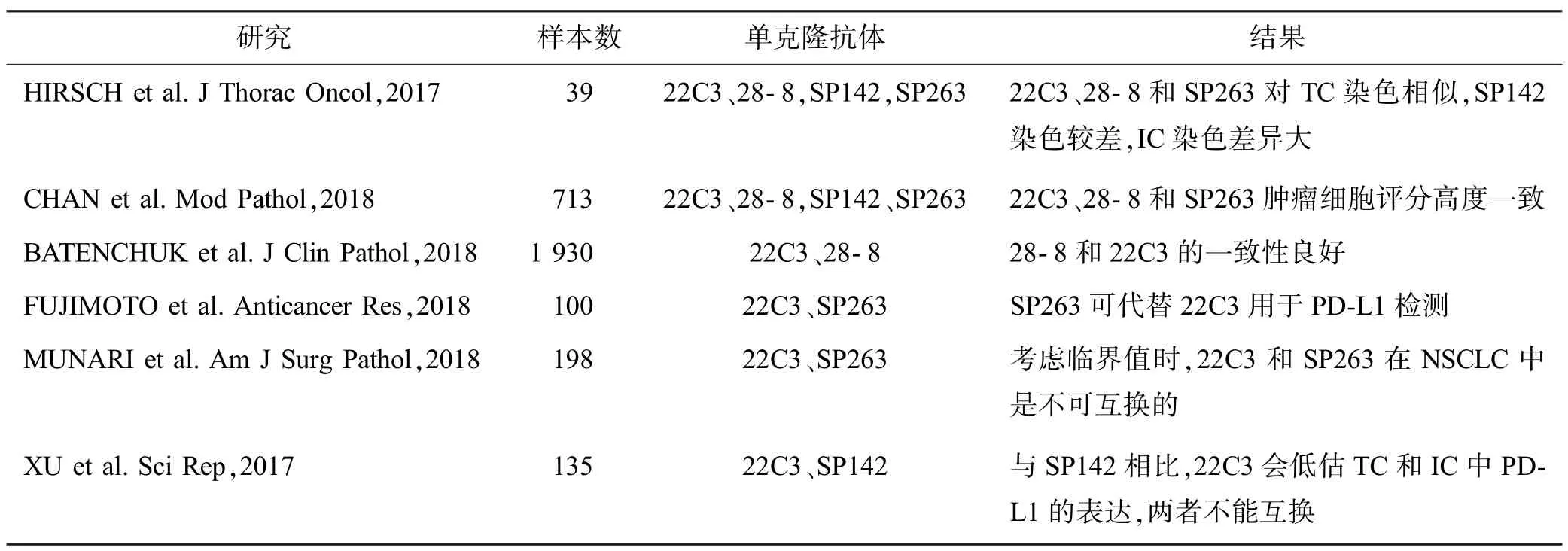
表2 NSCLC 中PD-L1 表达IHC 检测不同抗体比较
4.2 检测样本的选择
在临床上,部分晚期非小细胞肺癌患者诊断的唯一材料来源是细胞学,因此,对不同组织类别PD-L1 IHC 表达情况值得进一步研究(表3)。Wang 等[15]比较了细胞学、小活检、手术标本细胞块PD-L1 IHC 分析的可行性。结果表明,当TPS≥50%用作终点时,PD-L1 IHC 在细胞学细胞块中表现良好,在42%的细胞学细胞块中观察到,而小活检样本为36%(P=0.04)和手术切除样本29%(P=0.001)。Torous 等[16]测试了232 例患者肿瘤标本(细胞学和手术病理标本)的PDL1 表达。在细胞学和手术病理学组之间未观察到PD-L1 肿瘤比例评分(TPS)的显著差异,两个患者队列中约35%的肿瘤显示TPS≥50%。虽然数量很少,但接受细胞学和手术病理学检查的PD-L1 TPS ≥50%的患者接受了派姆单抗的治疗显示出相似的反应和疾病控制率。在活检样本和手术样本的比较上,Kim 等[17]使用3 种PD-L1 IHC 检测(22C3、SP142 和SP263)对46 名NSCLC 小活检样本和手术样本进行PD-L1 检测。PD-L1 IHC 分析结果的临界值分别为1%、5%、10%和50%。以手术标本的PD-L1 IHC 结果为参考值,22C3、SP142 和SP263 PD-L1 检测的符合率分别为73%~96%、65%~80%和72%~91%,证实使用小型活检样本是可靠的。Smith 等[18]为研究支气管内超声引导下经支气管针吸(EBUS-TBNA)标本对评估PD-L1 状态的适用性。对比发现用于诊断和分期NSCLC 的大多数EBUS-TBNA 样品中是可行的,其结果与组织学样本的比较显示中等一致,没有假阴性结果。
虽然细胞学标本已在多数研究中证实与活检和手术标本在PD-L1 表达的检测上一致性良好,但多数类型的检测标本的要求是≥100 个肿瘤细胞。Hernandez 等[19]应用22C3 抗体对52 个经手术病理证实的PD-L1 IHC 细胞学标本进行染色,比较肿瘤细胞数<100 和≥100 细胞的标本PD-L1 表达情况。以肿瘤细胞染色百分率(<1%,1%~49%,≥50%)对PDL1 IHC 进行评分,并与对照组进行比较。结果表明,肿瘤细胞≥100 的细胞学标本与手术标本的kappa 值基本一致,而肿瘤细胞<100 的细胞学标本与手术标本的kappa 值轻微一致。
对于NSCLC 晚期患者,当临床上无法获取原发病灶的标本时,远处转移病灶PD-L1 的表达情况值得进一步研究探讨。Sakakibara 等[20]报道了NSCLC 患者PD-L1 IHC 在原发肿瘤和淋巴结转移之间的良好一致性(r=0.93,P=0.02),但是,该研究样本较小(n=5),在他们的研究中使用了非临床使用的抗体(兔单克隆抗体EPR1161)。Wan 等[21]评估了NSCLC 中来自不同远处转移部位(大脑、骨骼、远端淋巴结、浆膜和胸外实体器官和皮肤/软组织)的PD-L1 表达,对580 份NSCLC 远处转移标本进行研究,其中包括来自两个不同转移部位的35 对配对标本。结果表明,PD-L1 TPS 评分在不同的转移部位相似,任何活检部位都将为指导临床治疗提供必要的信息。在临床上,从原发性肿瘤和任何其他转移性组织中获得足够的标本进行PD-L1 IHC 检测是相对困难的,因此需要多中心、更大样本量的研究可能会阐明肿瘤间异质性问题。
PD-L1 的表达具有动态变化的特点,随时间和治疗应答而波动、上调或下调,并且关于存档标本与新鲜标本的价值也是争论的焦点。Takeda 等[22]对比了存档标本与新鲜标本之间PD-L1 表达的差异性。与近期标本相比,存档标本中PD-L1 的表达量明显降低,使用包埋时间4 年以上的石蜡块无表达病例的比例明显增加。然而,KEYNOTE-010 试验表明,与使用多西紫杉醇相比,帕博利珠单抗(pembrolizumab)与多西他赛相比均具有益处,而无论是否使用存档或新鲜肿瘤标本评估PD-L1 的表达(HR 分别为0.81 和0.86)[23]。同样,在使用阿特珠单抗(atezolizumab)的FIR 研究中,在所有PD-L1 表达临界值中,在配对的存档和新鲜肿瘤样本之间观察到PD-L1 表达高度一致,NSCLC 肿瘤组织中PD-L1 表达的患者内异质性相对较低,这意味着新鲜或存档标本可以通过IHC 可靠地评估PD-L1 的状态[24]。
4.3 PD-L1 IHC 检测平台的选择
由于Dako 和Ventana IHC 平台并非在所有实验室都可用,而且由于标准化、即用的PD-L1 检测成本高,且NSCLC 样本体积小,无法对每种特定药物使用不同的检测,因此越来越多的病理学家实施了PD-L1实验室开发的检测(表4)。这些试验更经常使用浓缩抗体(主要是22C3、28-8、E1L3N 和QR1),很少使用从PDL1 分析中提取的预稀释抗体用于非专用平台[25]。
Skov 等[26]在Dako ASL48 和Dako Omnis 平台上,用22C3 抗体评估了NSCLC 细胞学和组织学144个标本,结果表明,在ASL48 和Dako Omnis 平台上运行的22C3 抗体的PD-L1 评分高度吻合,无论是应用于组织学还是细胞学细胞块,总体一致性OPA 为99%,阳性一致性PPA 和阴性一致性NPA 为95%。Koppel 等[27]在多种组织学(肺癌、黑色素瘤、头颈癌)上运用28-8 抗体在4 个IHC 平台(Dako ASL48,Dako Omnis,Leica Bond-III 和Ventana BenchMark ULTRA)上对PD-L1 表达水平分析进行了比较。所有肿瘤类型(肺癌、黑色素瘤、头颈癌)和所有染色方案的平均总体一致性好(>0.85)。Ilie 等[28]使用22C3 抗体浓缩物在3 种主要的市售自动染色剂 Dako ASL48,BenchMark ULTRA(Ventana Medical Systems,Inc.)和Bond-III(Leica Biosystems)中评估了PD-L1 的表达。与Dako ASL48 平台上的22C3 pharmDx 试剂盒相比,使用 Dako ASL48 和 VENTANA BenchMark ULTRA 平台上的22C3 抗体浓缩物在TPS 评分之间观察到的TPS 一致率几乎100%。Savic 等[29]旨在对Benchmark Ultra(VBMU)和Leica Bond(LBO)免疫染色剂上的22C3 抗PD-L1 抗体进行交叉验证。使用Dako ASL48 平台上的22C3 pharmDx 检测结果作为参考,结果表明,ASL48 的22C3 pharmDx 和LBO 的22C3 的一致性很好。

表3 NSCLC 中PD-L1 表达IHC 检测不同样本比较

表4 NSCLC 中PD-L1 表达IHC 检测不同平台比较
5 结语
免疫疗法已经在NSCLC 治疗领域确立了坚实的立足点,通过IHC 分析检测到的PD-L1 表达已成为探索抗PD-1/PD-L1 免疫疗法反应的主要预测生物标志物。PD-L1 检测方法、抗体的选择和检测样本的要求等研究对优化PD-L1 在临床工作中的检测显得至关重要。当前国内外推出的免疫检查点抑制剂相关药物的临床试验日益增多,部分药物已被批准NSCLC 一线治疗,但确定哪些患者将从这些药物中获得最大收益仍然是一个需要继续探讨的问题。其他检测PD-L1 表达的方法,例如检测mRNA 表达以及其他免疫检查点相关的方法检测PD-L1 表达,可能有助于更深入地了解PD-L1 生物标志物。将来,可在其他信息(例如其他免疫检查点或突变负荷TMB)的背景下评估PD-L1 蛋白的表达,以更准确地指导免疫疗法的临床应用。
