肾综合征出血热继发噬血细胞综合征一例
2021-05-06黄丽华鲍振中
黄丽华 顾 伟 罗 娇 鲍振中
1 临床资料患者女,48岁,因“发热10 d”于2019年11月28日收入大理大学第一附属医院。入院时体温峰值达40 ℃。入院前,患者曾在当地诊所接受治疗1周(具体不详),无好转,遂转至本院进一步诊治。患者自诉发病前进食了疑似被鼠类啃食过的污染食物。入院体格检查:体温38.2 ℃,脉搏111次/min,呼吸频率23次/min,血压101/65 mmHg(1 mmHg=0.133 kPa)。神志清楚,精神差,双侧颈前和颈后可扪及数枚肿大的淋巴结,最大者约为2.0 cm×1.0 cm,质韧,边缘规则,与周围组织无粘连,无压痛。全身皮肤无瘀点、瘀斑。双肺呼吸音粗,可闻及散在分布的湿啰音,余体格检查未见显著异常。血常规示:白细胞计数1.7×109/L,红细胞计数 3.57×1012/L,血红蛋白82 g/L,血小板计数 20×109/L;尿常规示:尿蛋白(++),白细胞0~2/高倍视野,红细胞0~1/高倍视野,上皮细胞0~2/高倍视野,管型 0/低倍视野。外周血实验室检查示:总胆红素33.3 μmol/L,直接胆红素23.1 μmol/L,ALT 84 U/L,AST 192 U/L,尿素氮 4.75 mmol/L,血肌酐63 μmol/L,血钾3.48 mmol/L;CRP 36.28 mg/L,降钙素原0.902 mg/L,IL-6 153.8 ng/L;TG 2.88 mmol/L,TC 1.74 mmol/L,PT 16.8 s,APTT 60.6 s,纤维蛋白原1.3 g/L;铁蛋白1 564 μg/L;肾综合征出血热(hemorrhagic fever with renal syndrome, HFRS)相关免疫球蛋白抗体IgM为1∶20,IgG为1∶40,均呈阳性;血清可溶性CD25(sCD25)为35 195 ng/L;自然杀伤细胞比例为0.162 3。骨髓穿刺血涂片:增生性贫血骨髓象(骨髓细胞内外铁消失,幼红细胞呈缺铁样改变,提示缺铁性贫血骨髓象);全片见散在噬血组织细胞、吞噬粒细胞、幼红细胞、成熟红细胞和血小板(图1)。浅表淋巴结彩色多普勒超声检查示:双侧颈部多发淋巴结肿大,余未见异常。肺部CT提示双肺散在炎性渗出。综合上述症状、体征、实验室检查和影像学检查结果,诊断为HFRS继发噬血细胞综合征。诊断明确后,予地塞米松磷酸钠注射液[第1~2周10 mg/(m2·d)、第3~4周5 mg/(m2·d)]治疗;第1~4周更昔洛韦0.25 g(2次/d)抗病毒治疗,第1~2周比阿培南0.6 g(1次/12 h)抗菌治疗,第1~4周利可君片20 mg(3次/d)升白细胞,第1~4周升血小板胶囊1.8 g(3次/d )升血小板,第1~4周还原型谷胱甘肽冻干粉 3 g(1次/d)护肝等对症治疗,患者好转出院。继续口服地塞米松2.5 mg/(m2·d)第5~6周,1.55 mg/(m2·d)第7周,第8周减量至停用。出院后1个月复查血常规,三系血细胞计数均恢复至正常水平,肝功能检测提示氨基转移酶、凝血功能均在正常范围内;TG、TC、铁蛋白水平均较前显著下降。2个月后电话随访,患者未诉不适。
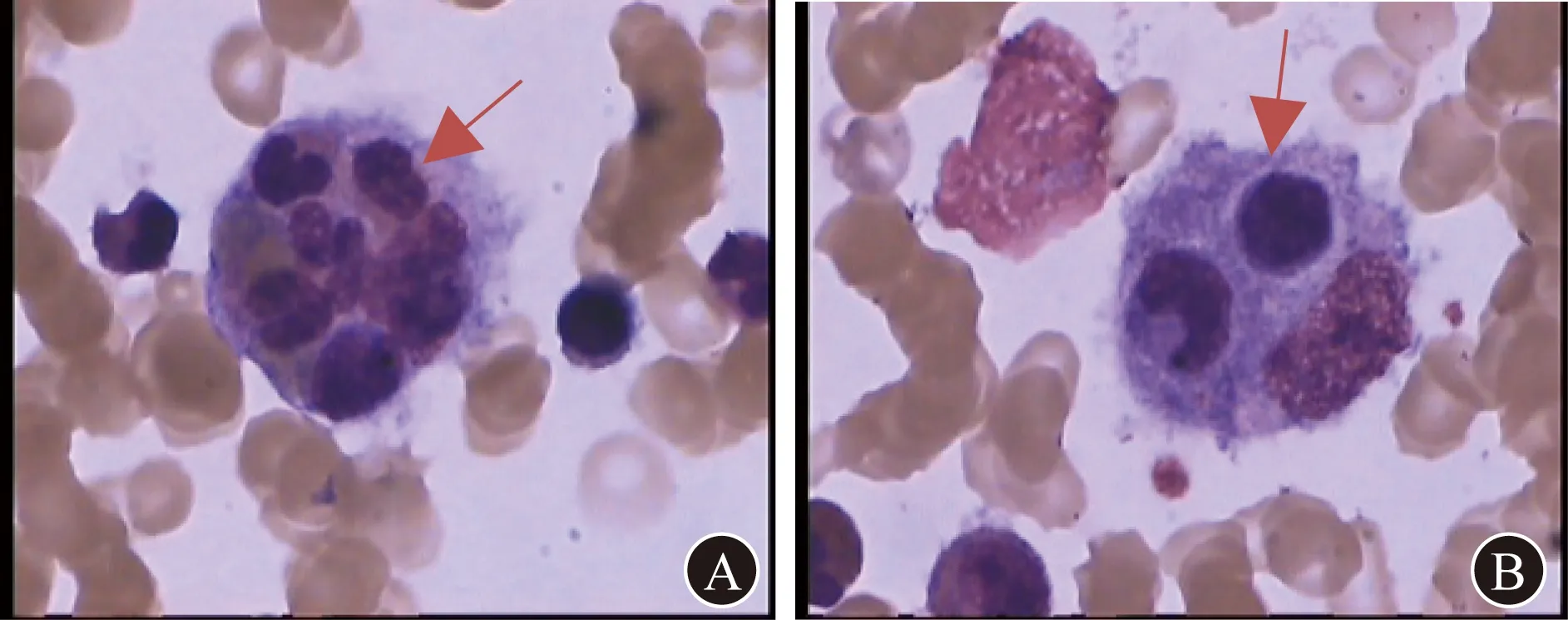
A 红色箭头所指处见噬血组织细胞、吞噬粒细胞、幼红细胞、成熟红细胞和血小板 B 红色箭头所指处为噬血组织细胞图1 患者骨髓穿刺血涂片(瑞特染色,×100)
2 讨 论HFRS是由汉坦病毒感染啮齿类动物诱发的人畜共患性疾病,其病理生理学特征以全身小血管和毛细血管的广泛损害为主[1]。目前,HFRS的发病机制尚不明确。有研究[2]认为,汉坦病毒感染血管内皮细胞,引起血管内皮生长因子(VEGF)分泌增多,造成血管通透性增加,诱发的机体低血压休克,是该疾病的病理生理学基础。也有研究[3]认为,由汉坦病毒感染诱发的机体免疫反应是主要的致病机制。本例患者发病前,疑似进食被鼠类啃食过的污染食物,同时,实验室检查结果显示 IgM和IgG抗体滴度升高,呈阳性。故HFRS的诊断明确。
噬血细胞综合征又称噬血细胞性淋巴组织细胞增多症(hemophagocytic lymphohistiocytosis,HLH),是一种罕见,但潜在致命的免疫过度激活综合征,预后较差,病死率高达50%[4-6]。根据病因可将HLH分为原发性和继发性两种:原发性HLH与基因缺陷有关;继发性HLH多见于肿瘤、免疫异常相关性疾病,或由各种病原微生物感染而诱发。 该疾病的诊断主要依据2004年制订的噬血细胞综合征诊断和治疗指南中的标准[7]。原发性HLH主要依据分子诊断结果,包括编码穿孔素的基因突变、基因UNC13D突变,以及STX11和RAB27a等基因的突变。继发性HLH患者常有明确的恶性肿瘤、免疫异常相关性疾病,或各种病原微生物感染等病史。此外,患者的症状、体征和实验室检查结果符合下列8项中的5项,即可诊断为继发性HLH:①发热;②肝脾肿大;③血常规中两系或三系血细胞计数减少;④血脂升高和(或)纤维蛋白原降低;⑤骨髓、肝脏或淋巴结中发现噬血细胞;⑥血清铁蛋白水平升高;⑦自然杀伤细胞活性降低(指自然杀伤细胞杀伤靶细胞的功能降低,而不能以自然杀伤细胞的数量或比例为标准)或缺陷;⑧可溶性IL-2受体(sCD25)水平升高。本例患者发病前曾进食鼠类啃食过的食物,HFRS抗体IgM、IgG均阳性,有发热、外周血三系血细胞计数减少,血脂水平升高,纤维蛋白原水平降低,骨髓穿刺血涂片出现噬血现象,血清铁蛋白水平升高,sCD25水平升高,故考虑HFRS继发HLH。目前HLH的治疗主要有HLH-94方案、HLH-04方案,以及单药或联合化学治疗、免疫治疗或生物制剂治疗等。对于继发性HLH病例而言,治疗原发疾病尤为重要;对于难治性或复发性HLH患者,进行造血干细胞移植是有效的治疗方案[8]。特别是对继发于致死率较高疾病的HLH患者,早期诊断、早期治疗尤为重要,可显著改善患者预后[9]。本例患者使用注射地塞米松磷酸钠抑制免疫反应,更昔洛韦抗病毒感染,比阿培南抗细菌感染,还原型谷胱甘肽护肝,利可君片和升血小板胶囊升白细胞、血小板等,经上述对症治疗后,好转出院。与Yang等[4]报道的HFRS继发HLH中的治疗方案不同的是本例患者使用了糖皮质激素,因患者入院后持续高热,白细胞和血小板计数较于当地住院时下降,考虑病情进展,故加用了糖皮质激素。上述结果提示,HFRS继发HLH时若出现病情进展,应及时加用糖皮质激素或免疫抑制剂,这对挽救患者生命至关重要;此外,本例患者病程中24 h尿量均正常,血肌酐值在正常范围内,无并发急性肺水肿,无电解质代谢紊乱,故未行血液透析治疗,提示HFRS继发HLH的患者若能早期诊断,积极治疗原发疾病,可降低多器官功能衰竭的发生风险。HFRS继发HLH的机制可能与汉坦病毒感染机体后产生大量的辅助性T淋巴细胞亚群1(Th1)细胞因子,从而引起机体严重的炎症反应有关[10]。本病在临床中较罕见,且相关报道鲜见[11-12],其致病机制目前尚不明确,有待更多的研究来探索与确证。
因此,医师应提高对HFRS继发HLH的认识,在临床工作中做到早诊断、早治疗,可改善患者预后。
