盐酸生产过程中的游离氯控制与分析
2021-05-06韩玲
韩 玲
(江苏泰洁检测技术股份有限公司 安全事业部, 江苏 南通 226010)
在离子膜制碱工业中,盐酸既是主要产品又作为辅助原料,被送往电解、纯水站、成品罐区,用于氯化钠电解槽阳极液和盐水精制过程中脱氯淡盐水的pH 值调节、螯合树脂塔酸再生、盐水反渗透膜组件的酸洗等。盐酸的制备方法是:采用氯气、氢气燃烧合成氯化氢,再用纯水吸收气相氯化氢制得质量分数为31 %的合格盐酸。由于氯气为主要制备原料,故盐酸产品中往往含有少量的游离氯。盐酸中的游离氯又称游离有效氯或游离有效余氯,以溶解的单质氯或次氯酸、次氯酸根离子的形式存在,具有强氧化性。若游离氯含量超标,易损坏树脂,同时会导致盐酸炉内压力升高,造成盐酸合成炉尾气排放不达标,成为安全生产隐患,影响整个氯碱工业的生产[1]。为提高盐酸的质量,开展其生产过程中游离氯控制与分析十分必要。
1 游离氯超标原因与控制
(1)氯氢压力波动的影响
游离氯超标最直接的原因是进炉氯气压力波动造成合成炉过氯[2],同时氢气输送管道内有积水或进炉氢气压力波动[3]也会造成合成炉过氯。所以,实时监控并及时调节控制氯气、氢气压力的平稳至关重要[4]。
(2)氯氢配比的影响
在操作控制四合一盐酸合成炉时,炉内火焰颜色若发黄,则氯气过量;火焰若发白,则氢气过量。所以应精准调节氯氢阀门,随时监视合成炉内火焰的颜色,密切关注氯气、氢气压力的变化,及时调节进入合成炉的氯气、氢气量,精确控制氯氢的配比[3]。氯氢最佳配比控制在 1 ∶1.05~1 ∶1.20。
(3)喷射泵抽力不稳[5]
若氯化氢吸收水喷射泵系统发生泄露,系统内压力就会剧烈波动,造成氯化氢吸收不正常,导致盐酸游离氯超标。因此,要严格控制系统内的压力波动,发现问题,立即检查喷射泵及循环系统,及时发现漏点,根据实际情况,迅速正确处理。
2 游离氯的测定
由于游离氯的超标会带来极大危害,必须准确分析测定游离氯的含量,以便采取有效措施加以控制。为提升游离氯含量测定方法的准确性和重现性,本文针对碘量法进行方法选择论证,并分析测定方法的影响因素。
2.1 测定原理
在酸性条件下,游离氯能将碘化钾中的碘离子氧化生成碘,故可用标准溶液硫代硫酸钠滴定碘离子氧化生成碘,反应过程如下:

2.2 试剂与溶液
碘化钾(KI),100 g/L 溶液,贮于褐色瓶中;盐酸(HCl),1+1;指示剂淀粉,10 g/L 溶液;标准溶液硫代硫酸钠,0.02 mol/L Na2S2O3。
2.3 测定步骤
取2 mL 碘化钾溶液和50 mL 新煮沸的水,置于250 mL 的锥形瓶中,加入一定体积的试样,在避光处静置5 min。
若静置后试样呈淡黄色,直接加几滴淀粉指示剂,用标准溶液硫代硫酸钠滴定至蓝色消失为止。若静置后试样呈黄色或深黄色,需先用标准溶液硫代硫酸钠滴定至淡黄色,再加几滴淀粉指示剂,继续滴定至蓝色消失为止。
2.4 计算

其中,c 为标准溶液硫代硫酸钠物质的量浓度,V为滴定消耗硫代硫酸钠的体积,V样为试样体积。
3 结果与讨论
3.1 溶液的准备
以5 g/L 次氯酸钠和新煮沸的水为原料,按一定配比(见表1),分别配置5 组不同浓度的次氯酸钠溶液,溶液中氯含量近似盐酸中游离氯含量。

表1 不同浓度次氯酸钠溶液配制
3.2 方法的准确度测定
按照2.3 的步骤(根据pH 值调节酸度),分别测定表1 中5 组样品的游离氯含量,结果见表2。

表2 游离氯测定方法的准确度
由表2 可知,测定结果的绝对误差和相对误差均在标准范围内,游离氯的测量值与真实值接近,方法的准确度符合要求。
3.3 方法的精密度测定[6]
分别称取5 份E 组的样品,按照2.3 的步骤测定游离氯的含量,结果见表3。
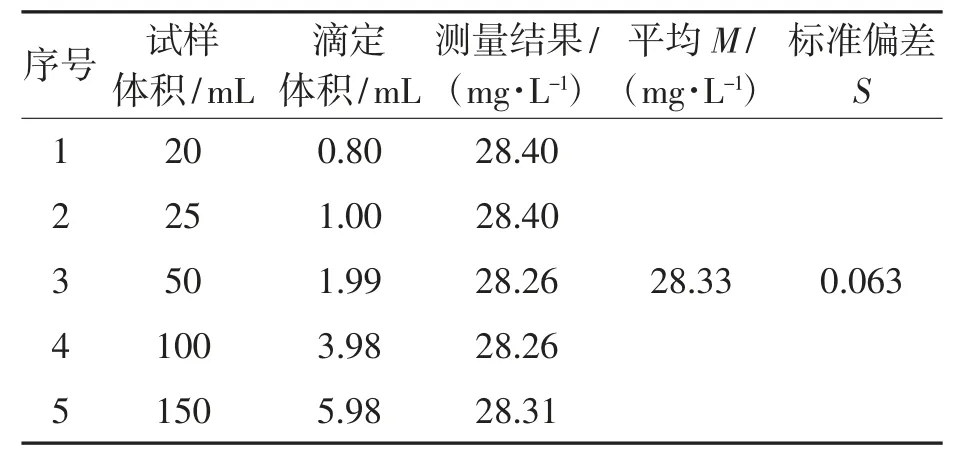
表3 游离氯测定方法的精密度
由表3 可知,测定结果的标准偏差在规定范围内,分析方法的精密度比较好。
综上可见,游离氯的测定方法简便快速,能够准确定量测定,重现性较好。方法的准确度、精密度能为工艺控制提供准确的参考依据。
4 测定方法的影响因素分析
4.1 酸碱度影响
碱性溶液调节下,I2和Na2S2O3氧化还原过程复杂化,故使用本方法测定游离氯时,应严格控制反应溶液为弱酸性或中性[6]。
若特殊情况需要在碱性溶液中滴定被氧化的I2,则不可用Na2S2O3标准溶液,而应该用NaAsO2标准溶液替代。若在较强酸性溶液中,因Na2S2O3易分解,故滴定时,应均匀搅拌,以减少Na2S2O3分解所造成的分析误差;同时在酸性溶液中,碘离子易被空气中的氧所氧化,随着氢离子浓度增加,其被氧化程度加快,若受阳光直射,氧化速度则更快。因此,碘量法一般在低温下的中性或弱酸性溶液中完成。I2溶液应用密闭的棕色容器保存。此外,为减少碘离子与空气的接触,滴定时不应过度摇荡[7]。
4.2 温度影响
在常温及少量碘离子存在的条件下,该反应的灵敏度[8]为(1~2)×10-5N;无碘离子时,反应的灵敏度降低;随着试样溶液温度升高,反应灵敏度有所下降(50 ℃时反应灵敏度仅为25 ℃时的1/10)[9]。同时I2具有挥发性,温度过高更容易挥发损失,使结果误差增大。综上,反应温度一般控制在 25 ℃以下[8]。
4.3 指示剂影响
(1)本试验方法判断滴定终点的指示剂为淀粉,在少量I-存在条件下,指示剂与I2反应形成吸附络合物呈蓝色,根据蓝色的出现或消失来判断终点。I-浓度太大,终点变色不灵敏[8]。
(2)淀粉指示剂应现配现用,若放置过久,淀粉指示剂与I2形成的络合物呈紫色或红色。这种紫色或红色的吸附络合物再用标准溶液Na2S2O3进行滴定时褪色慢,终点不敏锐[9]。
5 结 语
在离子膜制碱工业中,采用四合一副产蒸汽盐酸合成炉生产盐酸时,合理控制氯氢压力波动、氯氢配比、喷射泵抽力等,可有效控制盐酸中游离氯的含量。碘量法测定盐酸中游离氯含量,准确度、精密度能满足需要,可为盐酸生产工艺控制提供准确的参考值。
