357 例儿童死亡后器官捐献供肾移植血栓性并发症回顾性分析
2021-05-06胡善彪代贺龙余少杰郭勇蓝恭斌彭风华谢续标彭龙开中南大学湘雅二医院肾脏移植科湖南长沙410011
胡善彪,代贺龙,余少杰,郭勇,蓝恭斌,彭风华,谢续标,彭龙开(中南大学湘雅二医院肾脏移植科,湖南 长沙 410011)
在器官供需矛盾日益突出的形势下,儿童供肾已成为国内外器官来源的一个重要组成部分。儿童供肾移植具有其自身的特殊性,其移植手术相对复杂,围术期管理难度大,术后并发症发生率高:如移植肾动静脉血栓形成、出血、移植肾尿漏、移植肾功能恢复延迟、高灌注损伤等,而移植肾动静脉血栓形成是术后最严重的并发症之一,直接导致移植物失功。本文回顾性分析了2012 年1 月—2018 年12 月在中南大学湘雅二医院完成的357 例儿童死亡后器官捐献(deceased donor, DD)供肾移植血栓性并发症的发生率,分析供体年龄、供肾大小以及手术方式的选择与术后血栓性并发症的关系。
1 资料与方法
1.1 供者资料:供者209 例,其中男性115 例,女 性94 例, 中 位 年 龄7.1 岁(2 d ~17 岁),中位体重26.5 kg(1.9 ~63 kg),供肾纵轴中位长度7.3 cm(3.7 ~10.2 cm),供体原发病包括颅内肿瘤、脑外伤、缺血缺氧性脑病、溺水、手足口病等。
1.2 受者资料:受者357 例,其中男性233 例,女性124 例,中位年龄32.4(10 ~54)岁,中位体重43.5(21 ~58)kg,原发病包括慢性肾小球肾炎105 例,IgA 肾病51 例,多囊肾22 例,梗阻性肾病18 例,其余患者发现即为终末期肾病,病因不明。术前接受血液透析者250 例,腹膜透析者82 例,25 例未行透析即行肾移植手术。所有受者中2 例为2 次移植,其术前群体反应抗体(panel reactive antibody,PRA)Ⅰ类为弱阳,Ⅱ类阴性,但用Luminex 检测供体特异性抗体(donor specific antibody,DSA)为阴性。人类白细胞抗原(human leucocyte antigen,HLA)抗原错配数平均为3.1 个,补体依赖细胞毒试验均为阴性。
1.3 手术方式及围术期管理:357 例儿童供肾移植中,单肾移植297 例,双肾移植60 例。将357 例肾移植分为3 组,297 例单肾移植为组一,其中2 例供体年龄为5 个月,其余供体年龄均大于14 个月,供肾长径有6 例为5.2 ~ 6 cm,其余均>6 cm;60 例双肾移植中,32 例供体满足三“5”原则(供体年龄>5 个月,供体体重>5 kg,供肾长径>5 cm), 设 为 组 二;28 例不满足三“5”原则,设为组三。组二中,13 例受体接受分离式双肾移植,19 例受体接受双肾整块移植;组三中,10 例受体接受分离式双肾移植,18 例受体接受“利用主动脉远端建立流出道的双肾整块移植术”。
手术方式:单肾移植术式与常规成人肾移植相同。双肾移植术式包括分离式双肾移植和整块移植。分离式双肾移植是将左、右肾分开,在同侧髂窝,分别将左、右肾血管与髂血管进行吻合。整块移植术式分为3 种:① 端侧吻合供肾下腔静脉(inferior vena cava, IVC)近心端和髂外静脉,端侧吻合供肾主动脉(aorta, AO)近心端和髂总/髂外动脉,AO/IVC 远心端关闭;② 在整块移植的基础上,将供体AO 远心端的髂总动脉与受体髂外动脉端侧吻合(图1A)或与受体腹壁下动脉远心端端端吻合(图1B)建立流出道。移植肾常规留置双J管,5 个月以内供体留置F3 号双J 管,5 个月 ~ 1 岁供体留置F4 号双J 管,1 岁以上供体留置F4.7 号双J 管,术后血压控制在120/80 mmHg(1 mmHg =0.133 kPa)以下。对于分离式双肾移植或整块移植术式1 的受者,围术期给予普通肝素抗凝治疗,24 h 持续静脉泵入肝素的用量为5 ~10 U/(kg·h),维持3 ~5 d,序贯口服拜阿司匹林50 mg Qd 至1 个月,而对于建立了流出道的双肾整块移植术式受者,均未使用抗凝治疗。
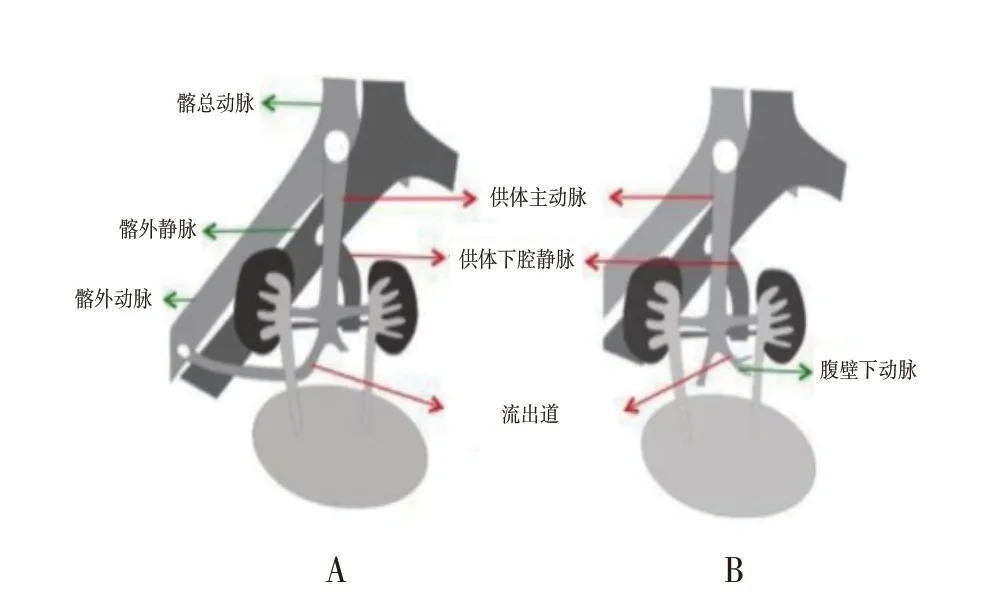
图1 利用供体AO 远心端的髂总动脉建立流出道的双肾整块移植
免疫抑制方案:所有受者均采用减量抗胸腺细胞球蛋白(ATG)/巴利昔单抗+ 甲强龙进行术前诱导,术后采用Tac+MMF+Pred 三联免疫抑制方案,起始剂量为0.1 mg/kg,根据Tac 谷浓度调整剂量:术后前3 个月 Tac 谷浓度维持在 6 ~8 ng/ml,术后3 个月~1 年谷浓度维持在5 ~7 ng/ml;MMF口 服 剂 量 为0.75 g,2 次/d,MMF AUC 维 持 在30 ~ 60 mg·h/L之间;甲泼尼龙从64 mg/d 开始服用,逐步递减至8 ~16 mg/d 维持剂量。
2 结 果
血管并发症:组一297 例单肾移植受体有2 例发生移植肾栓塞,发生率为0.67%,经分析为外科操作失误所致;组二32 例双肾移植受体未出现血栓并发症,血栓发生率为0,肾动脉狭窄1 例,介入球囊扩张治疗后好转;组三28 例受体有5 例发生移植肾栓塞,其中3 例单肾动脉栓塞,1 例双肾动脉栓塞,1 例单肾静脉栓塞,其均为采用分离式双肾移植术式的受体,而接受“利用主动脉远端建立流出道的双肾移植”术式的18 例受体无1 例发生栓塞。栓塞发生率为17.8%。
人、肾存活及移植肾功能情况(见表1):随访24 ~90 个月,随访截止时,单肾移植组(组一)中2 例患者因肺部感染死亡,1 例因移植肾血管栓塞而切除移植肾,恢复透析,1 例术后 5 个月因原发病复发,导致移植肾失功,恢复透析,其余受者移植肾功能恢复良好,人和肾存活率分别为99.3% 和 98.7%,末次随访时血肌酐为(69.8±22.5)μmol/L(41 ~154 μmol/L)。 双 肾 移 植 组中组二至随访截止时1 例患者因肺部感染死亡,2 例因排斥反应导致移植肾失功。人和肾存活率分别为 97% 和90.7 %,末次随访血肌酐为(81.4±24.5)μmol/L(42.2 ~115.4 μmol/L)。组三中1 例因双侧移植肾血管栓塞而切除移植肾恢复透析,另有4 例分别由于单侧血管栓塞导致一侧移植肾丢失,但对侧移植肾存活,人和肾存活率分别为 100% 和89.3 %,末次随访血肌酐为(53.4±21.3) μmol/L(32.5 ~105.5 μmol/L)。然而组三中18 例带流出道术式受者人、肾存活率均为100%。
3 讨 论
移植肾血管栓塞是围术期影响移植肾存活的主要原因,一旦发生则极难逆转,常导致移植肾失功。随着移植技术的发展,由于肾血管栓塞导致的移植肾失功的发生率在逐年降低[1],但是对于低龄的婴幼儿供体栓塞发生率仍较高。有研究报道,小儿(15 ~ 20 kg 或<2 岁)供肾肾移植栓塞发生率为2.5% ~ 12.5%[2-3]。汪笑宇等[4]报道了13 例婴幼儿供肾双肾移植给儿童受者,供体年龄为4 ~ 60 d,体重为2.5 ~ 5.3 kg,4 例患儿于术后1 周内出现移植肾血管栓塞,栓塞发生率达30.8%,其中3 例为双侧移植肾血管栓塞导致移植肾失功,切除移植肾,1 例为单侧移植肾血管栓塞导致一侧移植肾失功。
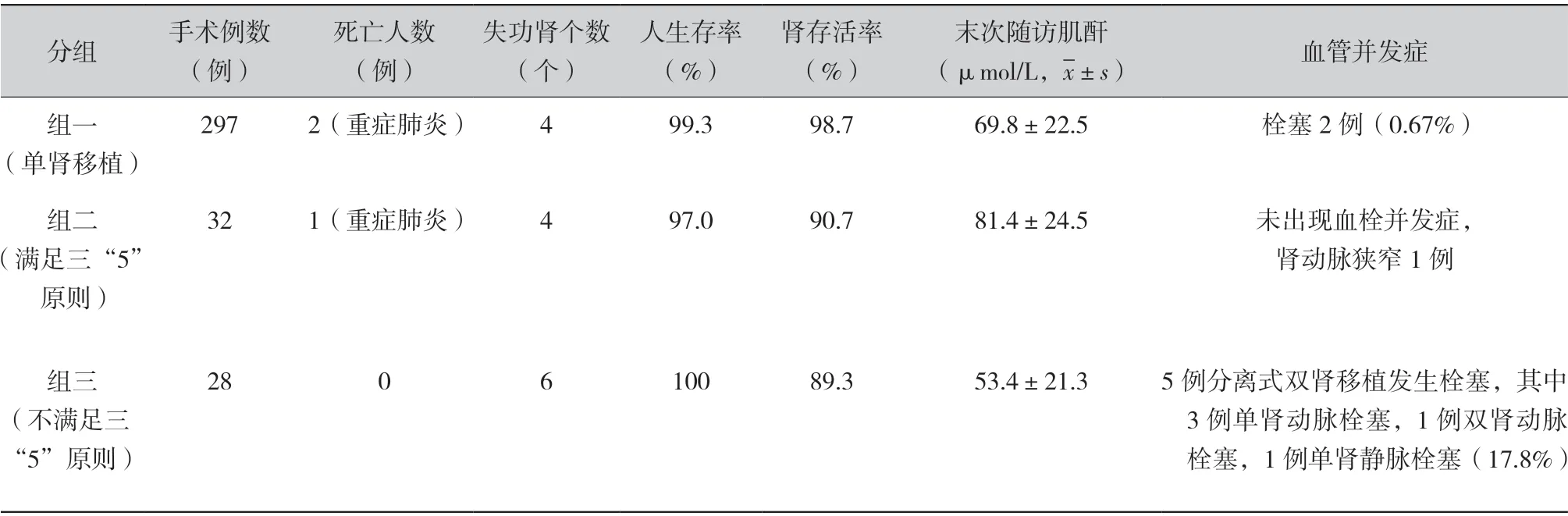
表1 人/肾存活及移植肾功能情况
移植肾血管栓塞的危险因素包括:血管过细、血管扭曲、血管骨骼化导致血管痉挛和血管壁缺血挛缩、低血压、经典整块移植中供者腹主动脉或下腔静脉盲端血栓形成,高凝状态和急性排斥反应,外科技术,手术方式选择等。婴幼儿供体年龄、体重越小,供肾也越小,肾血管越细,更容易形成血栓且容易扭曲而导致移植肾栓塞。
本研究显示,不满足“三5 原则”(供体年龄<5 个月,供体体重<5 kg,供肾长径<5 cm)的组三比满足“三5 原则”组二移植肾血管栓塞率明显升高。同为分离式双肾移植,满足“三5 原则”的组二中13 例无1 例栓塞,而不满足“三5 原则”的组三中10 例分离式双肾移植中3 例单肾动脉栓塞,1 例双肾动脉栓塞,1 例单肾静脉栓塞,二者栓塞发生率差异巨大,说明对于不满足“三5 原则”的供肾移植术后血管栓塞的发生风险显著增加,可以将“三5 原则”作为肾移植术式选择的判断标准。因此本中心提出婴幼儿供肾利用的安全边界:供体年龄>5 月,供体体重>5 kg,供肾长径>5 cm(三“5”原则)[5]。三“5”原则不是划分手术禁区的红线,而是一个量化标准,利用这一原则,可以帮助外科医生更好地选择手术方式和进行术后管理。符合三“5”原则的供体,可选择任意手术方式,术后无需常规抗凝;不符合三“5”原则的供体,尽量避免做分离式移植,且需根据手术方式决定是否抗凝。
由于不满足“三5 原则”的供肾行分离式双肾移植术式在使用抗凝药的情况下血管栓塞率仍非常高,面对这一挑战,我们对栓塞的原因进行分析,认为与以下因素有关:① 修肾时将血管骨骼化容易导致肾动脉痉挛和动脉管壁缺血、挛缩;② 肾血管极其细小,肾脏极小范围的滑动均可能导致肾血管扭曲、狭窄,从而导致栓塞;③ 应尽量保持肾血管在供者体内时的走行方向;④ 建立一个可能的通道使小的血栓能不进入肾血管内。针对这些原因我们对传统整块移植术式进行改良,保留供者较长的胸腹主动脉近端,与受者髂外或者髂总动脉吻合,利用供体腹主动脉远端的髂总动脉与受体髂外动脉端侧吻合或与受体腹壁下动脉远心端端端吻合建立流出道的术式,专门应对不满足“三5 原则”的供肾的血栓高发问题。该术式有三个要点:① 建立流出道;② 保护肾血管鞘及周围组织;③ 左、右肾位置对调,3 个要点的优点分别如下:① 建立流出道,血液在主动脉内快速流动,避免淤积形成血栓,即便有小的血栓形成,也很可能被从流出道内冲出,降低了肾动脉栓塞的风险;避免了传统整块移植主动脉盲端涡流形成,容易形成血栓的缺点;流出道可能有调节肾动脉内流量和压力的作用,有助于减轻婴儿肾的高灌注损伤,减少尿蛋白;② 保留肾门周围结缔组织,维持供肾在供体体内的原有状态,为肾蒂血管提供结构和组织支撑,可防止肾血管扭曲;保护血管鞘,也是最大限度地保护肾动脉壁的血供,能有效避免肾动脉痉挛和动脉管壁缺血、挛缩,我们认为这是避免血栓形成的关键环节;③ 将左右肾位置对调,顺应肾蒂血管的自然走行方向,可避免血管过度伸展、成角或扭转。另外较长的胸腹主动脉一方面可做大与受体髂外动脉和髂总动脉的吻合口,利于术后肾脏的生长,另一方面可使移植肾脏位置摆放在较低水平,输尿管与膀胱吻合后无张力,可减少术后输尿管并发症。我们将移植肾周脂肪囊保留,可以使移植肾很快和周围形成粘连而固定,加上术后3 d 内嘱受者不下床活动,可减少移植肾移动。
我们应用该改良术式明显降低了不满足“三5 原则”的供肾的血管栓塞并发症,完成的18 例受体无1 例发生栓塞,其中最轻的供体体重仅为1.9 kg,安全有效,且术后无需抗凝治疗[6],成为本中心解决该类型供体的常规术式。这说明外科技术是影响移植肾血管栓塞的一个非常重要因素。然而对于不满足三“5”原则的供体,手术难度大,栓塞发生率高,无相关经验的移植医生尽量避免这类手术。
手术方式的选择是儿童供肾移植术后肾功能恢复正常的一个重要因素。对于双肾整块移植还是单肾移植的实施标准目前尚不统一,儿童供者的年龄、体重、移植肾的大小均可作为判断标准。各移植中心根据供肾的实际情况(如供肾大小、血管条件等)结合受者的情况(年龄、身高、体重等),并根据自身的手术技术和经验选择合适的手术方法。本中心认为选择单/双肾移植术式决定性的标准是肾脏的长径:① 肾脏长径≤5 cm,选择双肾移植;② 5 cm <肾脏长径<7 cm,可选择单肾移植或双肾移植,若选择单肾移植则需选择体重较轻受体(体重≤60 kg 的受体;③ 肾脏长径≥7 cm,可选择单肾移植,且受体体重不受限制[5]。
组一297 例单肾移植中仅有6 例供肾长径为5.2 ~6.0 cm,其余均>6 cm,该6 例供肾均选择体重较轻的女性受者,体重介于32 ~50 kg,2 例患者术后出现移植移植肾功能延迟恢复(delayed graft function,DGF),供肾长径分别为5.2 cm 和5.4 cm,受体体重分别为49 kg 和50 kg,肌酐分别于术后32 d、36 d 恢复正常。这说明婴幼儿供肾肾脏功能尚不能满足较大体重受者的需要,但随着供肾的增大、储备功能的增加,可逐渐满足受者的需要。术后2 例受者出现血管栓塞,分析其原因与早期行儿童供肾移植的外科技术不成熟有关,其余295 例受者肾功能均恢复正常。
婴幼儿供肾移植术后血栓并发症远高于成人供肾移植,围术期管理尤为重要。早期血压控制在收缩压110 ~ 130 mmHg 为宜,血压过低容易出现移植肾灌注不足、血栓形成,血压过高可能会导致移植肾破裂。对于婴幼儿供肾移植患者,建议术后卧床休息3 d 后再下床活动,减少移植肾移动导致肾脏血管扭曲的风险。术后预防性的抗凝治疗可以减少肾血管栓塞的风险,但应注意避免抗凝过度导致出血量增加,建议在监测患者血栓弹力图、凝血功能以及伤口引流液的情况下调整抗凝方案。国内上海长征医院对于小于5 kg 婴幼儿供体捐献给儿童受者,术后静脉以10 U/(kg·h)速度持续泵入肝素,监测活性部分凝血活酶时间(actived partial thromboplastin time,APTT)不超过正常值1.5 倍,使用1 周后改阿司匹林50 mg/d 口服抗凝[4]。
本中心术后抗凝方案:由于术后抗凝有出血的风险,我们一般不使用抗凝药。对于供体年龄小于5 个月、供肾长度小于5 cm、供体体重低于5 kg 时,可酌情选择抗凝方案:抗凝药物可选用前列地尔、小剂量普通肝素(1 mg/hr×5 ~ 7 d)等,对于建立流出道的双肾整块移植,若术中对移植肾血管鞘进行了严密的保护,可不使用抗凝药物。
总之,儿童供体是一个重要的供体来源,而婴幼儿供体手术难度大,栓塞发生率高,手术风险大,应根据供体年龄、体重、供肾大小来慎重选择手术方式。利用主动脉远端建立流出道的双肾整块移植术式用于新生儿供肾移植短期效果良好,但仍需进一步积累样本量及进行长期随访观察。
