国产CalliSpheres 载药微球经导管肝动脉化疗栓塞治疗肝恶性肿瘤的临床分析
2021-05-01黄永东通讯作者陆双林蔡晓晴皇甫风华张振岳南通大学附属启东医院启东市人民医院介入科江苏启东226200
黄永东,毛 健(通讯作者),张 英,陆双林,蔡晓晴,皇甫风华,张振岳(南通大学附属启东医院<启东市人民医院>介入科 江苏 启东 226200)
早期肝癌由于症状隐匿因此一般确诊时已经发展到中晚期,不再适合手术切除治疗,并且合并糖尿病、高血压以及心脏病的患者也无法进行手术治疗,而对于中晚期肝癌而言,经导管肝动脉化疗栓塞治疗是一种首选的治疗方案[1]。本院将国产CalliSpheres 载药微球经导管肝动脉化疗栓塞治疗应用于2019 年5 月—2020 年9月期间收治的肝恶性肿瘤患者的治疗工作中,并与传统经导管肝动脉化疗栓塞治疗进行对照研究,现报道如下。
1 资料和方法
1.1 一般资料
选取2019 年5 月—2020 年9 月期间在我院治疗的符合纳入和排除标准的肝恶性肿瘤30 例,其中男性、女性分别为18 例、12 例;年龄33 ~78 岁,平均年龄(53.65±5.10)岁;肿瘤分期:Ⅲ期、Ⅳ期患者分别为21 例、9 例。将上述患者采用随机信封法分为参照组和治疗组各15 例,将两组的一般人口学资料做t检验或χ2检验,结果显示(P>0.05),差异无统计学意义,说明两组可比。
1.2 方法
1.2.1 参照组 本组患者采纳传统经导管肝动脉化疗栓塞治疗:麻醉方式为局部麻醉,对患者进行经皮股动脉穿刺以及肝动脉造影,对患者的肿瘤染色情况进行观察,将0.27F 微导管引入并于肝总动脉处放置,对患者的病变处情况进行造影查看,如果肿瘤分布较多则需对上述操作重复进行[2]。于肿瘤供血动脉处置导管超,并注入碘油混悬液以及吡柔比星、奥沙利铂等化疗药物的混合液,在此过程中需要结合患者的肿瘤血供情况来合理选择化疗药物的使用剂量,采用明胶海绵颗粒来对患者肿瘤供血动脉近端进行加强栓塞;治疗完成后对患者进行造影检查,确定病灶肿瘤染色情况是否完全消失[3]。
1.2.2 治疗组 本组患者采纳国产CalliSpheres 载药微球经导管肝动脉化疗栓塞治疗:前期操作与上述相同,将3 mL 的5%葡萄糖注射液+40 mg 的吡柔比星+1 瓶蓝色型1 g 聚乙烯醇栓塞微球(100 ~300μm)混合均匀[4],针对肠癌转移患者则需要使用120 mg 的伊立替康来替代吡柔比星,直到微球达到悬浮状态,抽取一定量(约1/3 ~2/3 瓶)的微球混悬液并缓慢注入,直到患者肿瘤血管的血流变缓,一般也就到达了栓塞终点,则需要暂停注射,如果注入所有的目标剂量后未到达栓塞终点,则需要注入空白微球;对患者行肝动脉造影,对肿瘤染色情况进行观察,确定病灶肿瘤染色情况是否完全消失。这种治疗方法一般需要治疗2 ~3 次,每次治疗需要4周的间隔时间。
1.3 观察指标
(1)对两组的治疗效果采用美国肝病学会改良实体瘤疗效评价标准(mRECIST)来进行评价并对比,如果治疗后病灶动脉期显影消失,则判定为CR(完全缓解);如果治疗后存活病灶直径缩小程度在30%以上,则判定为PR(部分缓解);如果治疗后存活病灶直径没有显著变化,则判定为SD(疾病稳定);如果治疗后存活病灶直径增加程度在20%以上,则判定为PD(疾病进展)[5];疾病控制率以CR、PR、SD 总和所占比重计算;疾病缓解率以CR、PR 总和所占比重计算。(2)对两组患者治疗后的不良反应发生情况进行统计并对比。(3)对治疗前以及治疗后2 个月对患者的血清PLGF、PIVKA-Ⅱ水平进行检测并对比。
1.4 统计学分析
采用SPSS 22.0 软件来数据进行处理,组与组之间的计量资料采用(±s)表示,用t来进行检验;组与组之间的临床效果(%)用χ2来进行检验;同时按照P<0.05 的标准,来衡量统计学意义。
2 结果
2.1 临床疗效对比
就疾病缓解率以及疾病控制率而言,治疗组患者分别为73.33%、93.33%,均显著高于参照组的40%以及80%,χ2=8.565,7.774;P<0.05,有统计学意义,见表1。
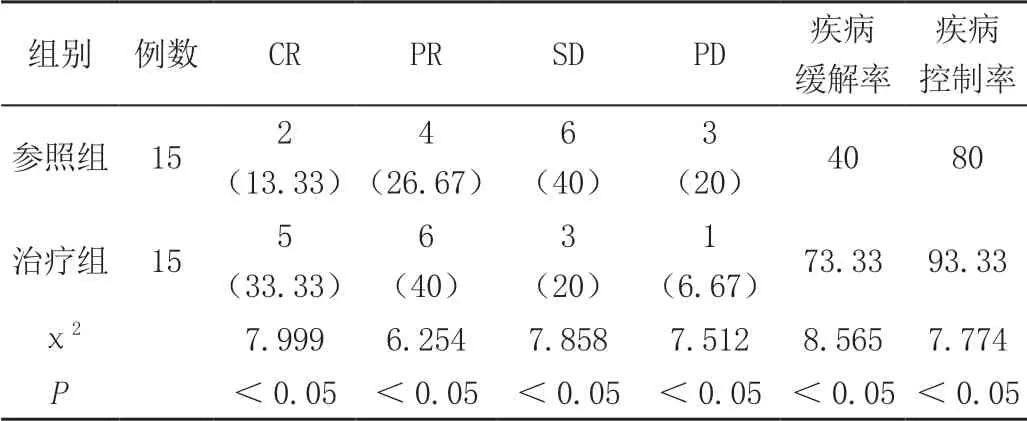
表1 两组患者的临床疗效对比[n(%)]
2.2 不良反应发生情况对比
参照组患者的不良反应发生率为73.33%(11/15),其中消化道反应、乏力、肝功能不全、肝区疼痛患者分别为5 例、3 例、1 例及2 例;治疗组患者的不良反应发生率为46.67%(7/15),其中消化道反应、乏力、肝功能不全、肝区疼痛患者分别为3 例、2 例、1 例及1 例;差异有统计学意义(χ2=10.256;P<0.01);两组患者在出现不良反应后均给予积极的对症治疗,未出现严重并发症(肝破裂出血、肝功能衰竭等)。
2.3 血清PLGF、PIVKA-Ⅱ水平对比 就治疗前的血清PLGF、PIVKA-Ⅱ水平而言,两组无统计学差异(P>0.05);接受不同方式的治疗后,两组患者的血清PLGF、PIVKA-Ⅱ水平均显著降低(P<0.05),但是治疗组均明显低于参照组,P<0.01,有统计学意义,见表2。
表2 治疗前后两组患者的血清PLGF、PIVKA-Ⅱ水平对比(±s)
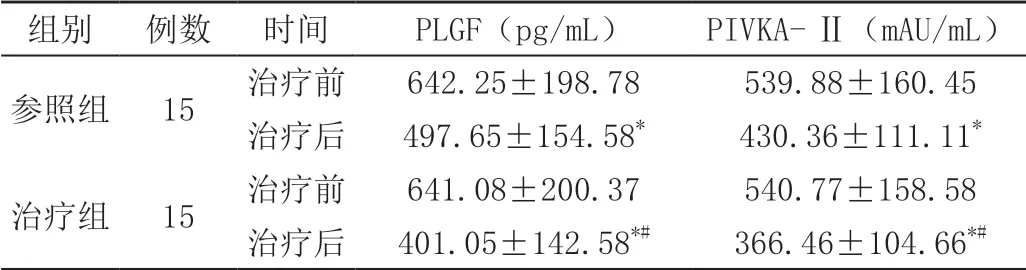
表2 治疗前后两组患者的血清PLGF、PIVKA-Ⅱ水平对比(±s)
注:与治疗前比较,*P <0.05;与参照组比较,#P <0.01。
组别 例数 时间 PLGF(pg/mL) PIVKA-Ⅱ(mAU/mL)参照组 15 治疗前 642.25±198.78 539.88±160.45治疗后 497.65±154.58* 430.36±111.11*治疗组 15 治疗前 641.08±200.37 540.77±158.58治疗后 401.05±142.58*# 366.46±104.66*#
3 讨论
肝动脉化疗栓塞术是目前临床上针对失去手术机会的肝癌患者首选的治疗方案[6],载药微球作为一种新的给药方式,其载体为某种高分子材料,通过对化疗药物制成球形来进行吸附或者包裹,有利于对药物进行保护,还能够使外周循环的药物浓度得到一定程度的减弱,从而有利于不良反应发生率的降低。本次研究结果显示:就疾病缓解率以及疾病控制率而言,治疗组患者分别为73.33%、93.33%,均显著高于参照组的40%以及80%,χ2=8.565,7.774;P<0.05,有统计学意义;就不良反应发生率而言,治疗组患者为46.67%,显著低于参照组的73.33%,有统计学意义(χ2=10.256;P<0.01);接受不同方式的治疗后,两组患者的血清PLGF、PIVKA-Ⅱ水平均显著降低(P<0.05),但是治疗组均明显低于参照组,P<0.01,有统计学意义。综上所述,肝恶性肿瘤患者应用国产CalliSpheres 载药微球经导管肝动脉化疗栓塞治疗的临床效果确切,有助于降低不良反应,患者耐受性更好,对提高治疗效果以及改善血清水平均具有重要作用,值得推广。
