奥贝胆酸关键双键杂质的合成研究
2021-04-30张尚师郑滔谢晓玲邓南翔舒兵
张尚师,郑滔,谢晓玲,邓南翔,舒兵
(广东药科大学1.新药研究中心;2.药学院,广东广州510006)
关键字:奥贝胆酸;杂质;合成
奥贝胆酸(obeticholic acid,OCA,结构式见图1)通过激动法尼醇X 受体(farnesoid X receptor,FXR)间接抑制细胞色素7A1(CYP7A1)的基因表达,从而抑制胆酸的合成,用以治疗对熊去氧胆酸应答补加或者无法耐受的原发性胆汁性胆管炎,具有较高的安全性[1-4]。但是,在工业化生产奥贝胆酸的过程中,氢化条件较为苛刻,且催化剂随着反应时间的延长催化性能逐渐下降,导致起始物料中的碳碳双键难以彻底被还原,起始物料中羰基被还原后会引入奥贝胆酸的关键双键杂质——(Z)-3α,7α-二羟基-6-亚乙基-5β-胆烷酸(A-1,结构式见图1),严重影响奥贝胆酸的纯度[5-6]。为了建立奥贝胆酸的质量标准,必须对其中的关键杂质进行研究,建立该杂质的质量标准。因此,合成该杂质作为对照品,用于后续的分析和研究,显得很有必要。

图1 奥贝胆酸(OCA)和奥贝胆酸双键杂质(A-1)的结构Figure 1 The structure of Obeticholic acid(OCA)and double bond impurity(A-1)
本研究以鹅去氧胆酸甲酯为起始原料,通过二异丙基氨基锂(LDA)拔氢后上TMS 保护剂、三氟化硼(BF3)催化的羟醛缩合反应、对羧酸进行水解和对酮羰基进行还原等步骤得到奥贝胆酸双键杂质A-1,合成路线见图2。

图2 奥贝胆酸双键杂质(A-1)的合成路线Figure 2 The synthesis route of Obeticholic acid double bond impurity(A-1)
1 仪器与试剂
1.1 仪器
DF-101S 集热式恒温加热磁力搅拌器(河南巩义予华有限公司);ZF-7A 手提式紫外分析仪(杭州齐威仪器有限公司);N-1300V-W 旋转蒸发仪(上海艾朗仪器有限公司);ME104电子天平、SHB-III循环水式多用真空泵(巩义市科瑞仪器有限公司);Advance Bruker 400M 超导核磁共振波谱仪(瑞士BRUKER 公司);Thermo 超高效液相色谱串联质谱仪(赛默飞世尔科技公司)。
1.2 试剂
鹅去氧胆酸甲酯(分析纯,萨恩化学技术有限公司);三甲基氯硅烷(分析纯,萨恩化学技术有限公司);乙醛溶液(分析纯,上海毕得医药有限公司);三氟化硼乙醚溶液(分析纯,上海毕得医药有限公司),其余所有溶剂如甲苯、DMF、DCM、EA 等均为化学纯。
2 方法与结果
2.1 3α,7-双[(三甲基硅烷基)氧基]-6-烯-5β-胆烷酸甲酯(2)的合成
称取鹅去氧胆酸甲酯(1,10.0 g,24.75 mmol)于500 mL 三口瓶中,加入无水四氢呋喃200 mL,换N2保护,换气5 次,将反应液置于-40 ℃环境中,搅拌20 min 后,滴加27.2 mL 二异丙基氨基锂(LDA,54.45 mmol,2.0 mol/L in THF),搅拌1 h 后,滴加三甲基氯硅烷(5.92 g,54.45 mmol)。搅拌2 h 后,停止反应,将反应液倒入500 mL 饱和氯化铵溶液中,加入100 mL 乙酸乙酯,搅拌20 min 后分液,水层加50 mL 乙酸乙酯萃取3 次,合并有机层,饱和食盐水洗3次,无水硫酸钠干燥,彻底旋干,直接投下一步。
2.2 (Z)-3α-羟基-6-亚乙基-7-氧代-5β-胆烷酸甲酯(3)的合成
将得到的粗品溶于300 mL无水二氯甲烷中,加入5.9 mL 乙醛四氢呋喃溶液(1.2 eq,5.0 mol/L in THF,以原料1 计算),将反应体系降温至0 ℃,滴加5 mL 三氟化硼乙醚溶液,搅拌3 h 后反应完全,将反应液倒入500 mL 稀盐酸溶液中,分液,水层加100 mL 二氯甲烷萃取3 次,合并有机层,饱和食盐水洗3 次,无水硫酸钠干燥,旋干,硅胶柱层析(PE/EA:64/1-8/1)得到中间体2,6.3 g,两步反应产率59%。1H NMR(400 MHz,MeOD)δ:6.03(q,J=7.1 Hz,1H),3.64(s,3H),3.62-3.45(m,1H),2.63(dd,J=13.0,4.2 Hz,1H),2.29 (tdd,J=12.3,7.6,2.8 Hz,3H),2.22-2.09 (m, 1H), 2.02 (dd,J=9.6, 3.2 Hz, 1H), 1.98-1.82(m, 3H), 1.81-1.71 (m, 1H), 1.66 (d,J=7.1 Hz, 4H),1.57-1.45 (m, 3H), 1.45-1.35 (m, 2H), 1.33-1.23 (m,3H),1.23-1.04(m,5H),0.99(s,3H),0.92(d,J=6.5 Hz,3H),0.64(s,3H)。ESI-MS(m/z):431.4[M+H]+。
2.3 (Z)-3α-羟基-6-亚乙基-7-氧代-5β-胆烷酸(4)的合成
称取中间体3(4.0 g,9.3 mmol)于250 mL 反应瓶中,加入50 mL 甲醇,搅拌使之溶解,加入10%NaOH 溶液10.0 mL,50 ℃搅拌1 h。反应结束后,放冷,旋干甲醇,加入20 mL 水,冰浴下搅拌10 min,滴加5%稀盐酸调pH=4~5,过滤,滤饼用水洗2~3 次,干燥后乙醇重结晶得到中间体4,无需纯化,直接投下一步反应。
2.4 (Z)-3α,7α-二羟基-6-亚乙基-5β-胆烷酸(A-1)的合成
称取中间体4(2.0 g,4.81 mmol)于250 mL 反应瓶中,加30 mL水搅拌,加入50%NaOH溶液2.0 mL,搅拌使之溶解。滴加由NaBH4(363 mg,9.56 mmol)、1.5 mL 水和0.3 mL 50%NaOH 溶液组成的混合溶液(参照文献[7-8]方法)。加毕,90 ℃下反应5 h。反应结束后将反应液倒入100 mL 冰饱和NH4Cl 溶液中,搅拌,加饱和柠檬酸溶液调pH=4~5。加30 mL乙酸乙酯萃取3次,合并萃取液,饱和食盐水洗后无水硫酸钠干燥,室温旋干,硅胶柱分离(DCM∶MeOH=120∶1~30∶1,0.5% HAc),得到奥贝胆酸双键杂质A-1,白色固体,1.34 g,产率67%,纯度97.2%(示差检测器),mp 221.3~224.5 ℃。1H NMR (400 MHz,CDCl3)δ:5.77-5.54 (m, 1H),4.04-4.01 (m,1H),3.75-3.52(m,1H),2.58-2.36(m,2H),2.34-2.20(m,1H),2.06-1.98(m,1H),1.97-1.78(m,4H),1.76-1.58(m,7H),1.53-1.19 (m,11H),1.18-1.00 (m,2H),0.96 (d,J=6.2 Hz,3H),0.80(s,3H),0.67(s,2H)。13C NMR(101 MHz,CDCl3)δ:178.43,140.65,113.55,72.39,70.37,55.19,54.08,44.52,43.77,43.11,39.13,38.69,35.17,34.44,34.36,33.79,30.13,29.94,29.15,27.69,26.21,21.91,20.32,17.51,11.51,11.29。ESI-MS(m/z):417.1[M-H]+。以上数据与文献[7-8]报道的一致,详见图3。
3 讨论
在本合成路线中,使用还原试剂将7-羰基还原为7-α羟基是研究的关键。常见的还原剂有氢化铝锂、硼氢化钠、硼氢化钾、氢气钯碳体系等。由于氢化铝锂能够还原羧酸、氢气钯碳体系可以还原6-烯基,均不能得到目标杂质A-1。本研究参照奥贝胆酸的合成方法,使用硼氢化钠进行还原。从立体结构方面来看,7 位的羰基突出于胆烷酸骨架外侧,H负离子从位阻较小的环下侧进攻羰基,得到动力学稳定的7β-羟基,而在较高温度下,由于β位空间位阻较大,因此,7β-羟基会转变为热力学稳定的7α-羟基。
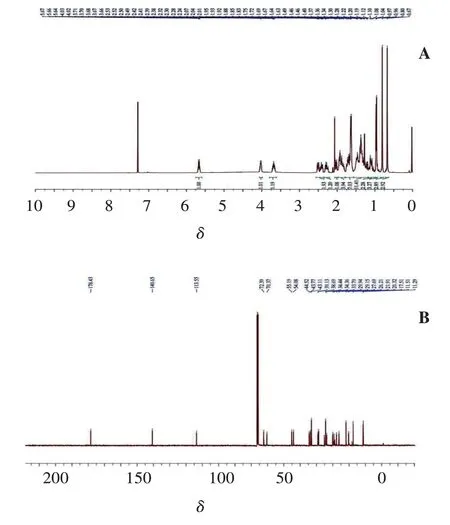
图3 奥贝胆酸双键杂质(A-1)的氢谱(A)和碳谱(B)Figure 3 The1H NMR(A)and 13C NMR(B)spectra of Obeticholic acid double bond impurity(A-1)
本研究以鹅去氧胆酸甲酯为起始原料,在LDA作用下,使3α,7 位接上了TMS 保护基,然后在三氟化硼乙醚的催化下,与乙醛发生羟醛缩合反应得到乙烯基鹅去氧胆酸甲酯,最后经碱水解、硼氢化钠还原羰基后得到奥贝胆酸关键杂质A-1。本方法制备的杂质A-1 纯度高,可直接用于建立奥贝胆酸原料药的质量标准和相关杂质分析。
