腰椎间盘突出症术后椎间隙感染病原菌分布及影响因素分析 *
2021-04-30黄海锋尹振宇羊刚毅宋晋刚
赵 兵, 黄海锋, 尹振宇, 羊刚毅, 宋晋刚
(四川省绵阳市中心医院脊柱外科, 四川 绵阳 621000)
腰椎键盘突出症(Lumbar disc herniation ,LDH)为腰椎退行性疾病,在临床中较为常见,多发于男性[1]。临床上LDH患者多采用非手术治疗,多数可经保守治疗得到有效缓解或是治愈,保守治疗无效或情况较为严重者需行手术治疗,以确保减压效果[2]。临床研究表明,少数LDH患者术后可并发椎间隙感染,会对患者预后造成不良影响[3]。且现阶段,与腰椎间盘突出症术后并发椎间隙感染相关研究较为鲜见。基于此,本研究回顾2013年3月至2020年3月我院收治且行手术治疗的895例LDH患者临床资料,统计LDH术后椎间隙感染发生及病原菌分析情况,分析其影响因素。现作如下报道。
1 资料与方法
1.1入选标准:诊断标准:符合《外科学》[4](第3版)中LDH相关诊断标准。LDH术后椎间隙感染判定:①出现切口持续红肿疼痛、自发或经叩击腰部有痛感等临床表现,或可伴体温升高等全身症状;②MRI影像学检查提示椎间盘及终板出现损伤甚至破坏,相临近的椎体界限模糊,髓核裂隙发生改变甚至消失,椎间隙发生变化,明显变窄;③实验室检查显示血沉超过45mm/h,C-反应蛋白(CRP)超过25mg/L;④椎间隙组织标本培养显示结果为阳性。纳入标准:①符合诊断标准;②符合手术治疗指征;③首次接受腰椎手术治疗;④未出现椎弓峡部裂状况;⑤凝血及造血功能正常;⑥肝肾等重要脏器功能均正常。排除标准:①临床资料不甚详尽或不完整;②合并恶性肿瘤;③合并严重消耗性疾病;④术前合并急性或慢性感染疾病;⑤骨质疏松较严重者;⑥合并免疫系统疾病。
1.2一般资料:基于上述入选标准,从2013年3月至2020年3月我院收治且行手术治疗的LDH患者中筛选出895例,其中,男531例,女364例;年龄36~78岁,平均年龄(58.24±5.69)岁;在手术方面,行开窗减压术治疗有466例,行内固定术治疗有429例;在腰椎间盘突出部位方面,38例L3~4患病,396例L4~5患病,347例L5~S1患病,31例L3~4合并L4~5,71例L4~5合并L5~S1,10例三项合并。895例LDH患者中并发术后椎间隙感染有38例,均为单间隙感染,L2~3、L3~4、L4~5、L5~S1分别有2例、3例、18例、15例。
1.3研究方法
1.3.1病原学检查:经皮椎间盘进行穿刺,对疑诊为椎间隙感染患者进行病变节段组织标本取样,而后基于《全国临床检验操作规程》,按照其中相关要求进行细菌培养,筛选出结果为阳性标本,应用法国梅里埃VITEK全自动微生物分析系统予以检定,以明确感染病原菌种类。
1.3.2组别划分:以是否术后并发椎间隙感染为依据,划分为观察组(并发感染者,38例)与对照组(未并发感染者,857例)。收集两组患者一般资料(性别、年龄),习惯或基础病史(吸烟史、糖尿病史、高血压史),身体状况(体质指数BMI、营养情况);同时,观察并记录两组围手术期指标(术式、手术时间)以及术后合并其他系统感染情况。
1.4统计学处理:应用SPSS26.0分析数据。并发椎间隙感染患者的病原菌分布情况,用例数与构成比形式统计;计数资料用n(%)表示,应用χ2检验进行单因素分析,影响因素检验采用多因素Logistic回归分析。P<0.05示差异具有统计学意义。
2 结 果
2.1椎间隙感染结果与病原菌分布情况:895例LDH患者中,术后并发椎间隙感染有38例,发生率为4.25%。8例未能检测出病原菌,另外30例患者,病变节段组织样本于有氧条件下培养,检测出病原菌33株,其中出现3例混合感染,分别为2例金黄色葡萄球菌与大肠埃希菌混合感染、1例金黄色葡萄球菌与表皮葡萄球菌混合感染。就病原菌分布情况而言,金黄色葡萄球菌构成比最高(30.30%),其次分别为表皮葡萄球菌(21.21%)与大肠埃希菌(15.15%),详见表1。
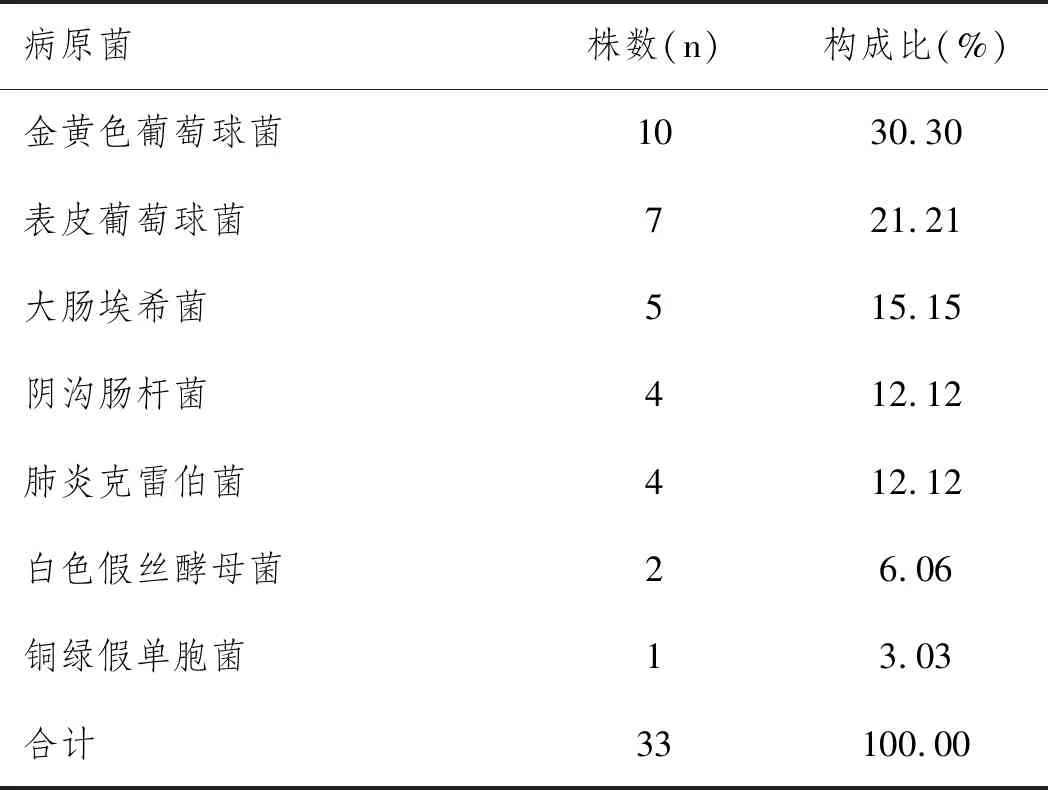
表1 LDH患者术后并发椎间隙感染的病原菌分布情况
2.2LDH术后并发椎间隙感染的单因素分析:针对LDH术后并发椎间隙感染相关影响因素,进行变量定义并对各变量项目赋值,详见表2。将X1~10变量数据录入SPSS软件,行单因素分析,结果显示:两组X1、X3、X5、X8情况比较无显著差异(P>0.05),两组X2、X4、X6、X7、X9、X10情况比较均存在显著差异(P<0.05),提示年龄、糖尿病史、BMI、营养不良、手术时间、术后合并其他系统感染为LDH术后并发椎间隙感染的影响因素,详见表3。

表2 LDH术后并发椎间隙感染相关因素赋值
2.3LDH术后并发椎间隙感染的多因素分析:将单因素分析显示有统计学意义的因素X2、X4、X6、X7、X9、X10设为自变量,组别设为因变量(1=观察组,2=对照组),纳入多因素Logistic回归模型,分析显示:年龄≥55岁(X2=2.00)、有糖尿病史(X4=1.00)、BMI≥27kg/m2(X6=2.00)、营养不良(X7=1.00)、手术时间≥3h(X9=2.00)、术后合并其他感染(X10=1.00)为LDH术后并发椎间隙感染的独立危险因素(P<0.05),详见表4。
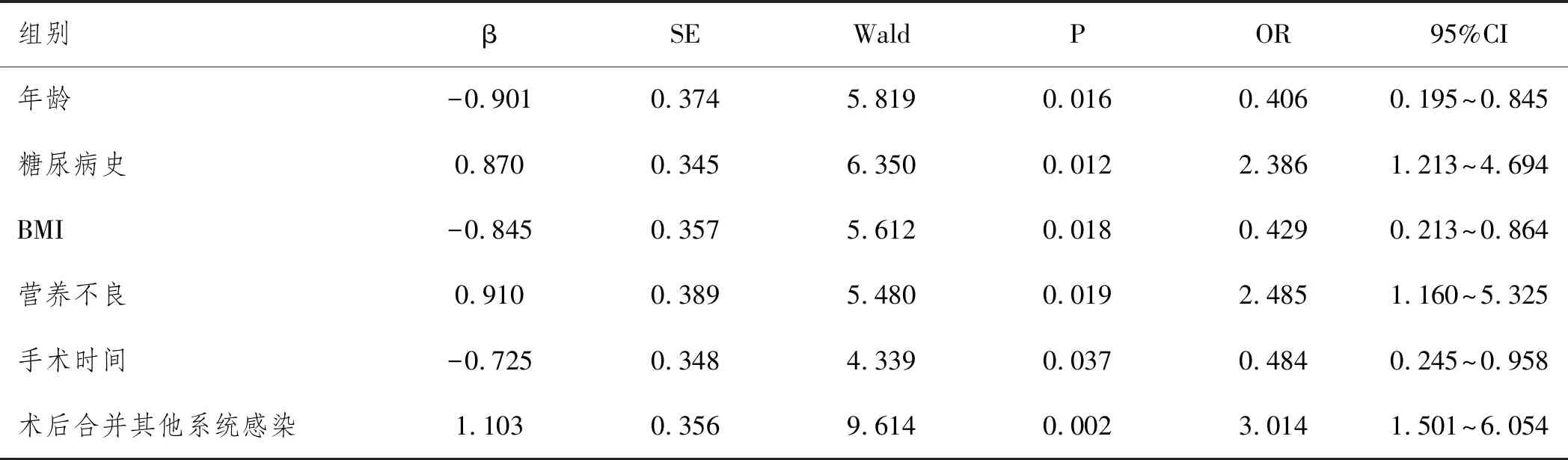
表4 LDH术后并发椎间隙感染的多因素Logistic回归分析
3 讨 论
LDH术后椎间隙感染近年来发生率,在临床脊柱手术持续改进不断发展、以及临床手术愈发重视无菌要求情况下,而呈现逐年降低态势,并且随内窥镜下脊柱微创手术逐渐广泛应用于临床,LDH术后并发椎间隙感染处于低水平状态[5,6]。然而,LDH患者术后一旦并发椎间隙感染,若未得到及时处理或处理方式不当,极易致使患者预后不良,从而对患者日常生活质量造成严重影响[7]。因此,分析并明确LDH术后椎间隙感染病原菌分布情况及其危险因素,在椎间隙感染预防及发生感染后及时治疗方面至关重要。
LDH术后并发椎间感染原因探究,为近年来骨科医师正欲解决的重点与难点,相关临床研究虽较多,但就目前来看,其具体发病原因及机制仍未有明确定论[8]。有研究报道,5例行手术治疗的LDH患者椎间隙穿刺物,经培养结果未检出细菌[9]。本研究结果显示,895例LDH患者中,术后并发椎间隙感染有38例(4.25%),8例未能检测出病原菌,分析其原因或为椎间盘损伤引发椎体血运障碍,进而出现坏死反应,或为人体自身免疫性反应所引发;另外30例患者检测出病原菌33株,提示LDH术后并发椎间隙感染以细菌感染为主;并且本研究发现,金黄色葡萄球菌检出率最高,所占比例为30.30%,其次分别为表皮葡萄球菌(21.21%)与大肠埃希菌(15.15%),提示临床可根据常见病原菌种类及分布情况,对LDH患者进行预防性用药治疗。此外,本研究中多因素Logistic回归分析发现,≥55岁、有糖尿病史、BMI≥27kg/m2、营养不良、手术时间≥3h、术后合并其他系统感染为LDH术后并发椎间隙感染的独立危险因素。究其缘由,①更高龄LDH患者机能及免疫力多具有进行性下降表表现,手术治疗后更易发生病原菌感染;②对于有糖尿病史的LDH患者,手术所致的急性应激反应能够加快肌糖原分解,从而大量渗入血液,使糖异生作用降低,并且可诱导机体胰岛素抵抗,机体高水平血糖为细菌生长繁殖提供有利的高糖环境,使得感染风险明显上升;③LDH患者BMI更高,其脂肪组织供血较差,会对手术切口愈合造成一定影响,且术中电刀应用可致脂肪液化,从而增加感染风险;④营养不良可致患者机体免疫功能减弱,机体对病原菌抵御能力降低;⑤手术进行过程中,LDH患者机体免疫力处于抑制状态,手术部位暴露时间过长,可明显增加感染风险;⑥术后合并其他系统感染能够使炎症因子增加,刺激机体应激,发生感染位置病原菌能够经血液转移至损伤的椎间隙,进而引发感染[10]。
综上所述,临床上LDH术后不易并发椎间隙感染,发生率在低水平,但在术后康复过程中仍需对并发椎间隙感染的独立危险因素给予重点关注,并且可基于病原菌分布情况合理应用抗生素加以预防,规范操作从而减少或避免术后椎间隙感染情况。
