沉积盆地地下水无机氮来源示踪及其演化模式
2021-04-29王晓光何海洋王长琪
李 霄,王晓光, 柴 璐,朱 巍,何海洋,王长琪
沉积盆地地下水无机氮来源示踪及其演化模式
李 霄*,王晓光, 柴 璐,朱 巍,何海洋,王长琪
(中国地质调查局沈阳地质调查中心,辽宁 沈阳 110034)
以我国沉积型盆地三江平原的典型农业区抚远地区为例,采用水化学法和GIS技术分析区域水化学成因作用及无机氮素的污染特征,利用氮氧双稳定同位素分布特征及稳定同位素解析模型(SIAR)确定氮素来源及各污染源贡献比,基于对影响氮素浓度变化的多项因素的认识,建立区域氮素的水化学演化模式.结果表明:研究区地下水中氨氮超标率为56.52%,毫克当量百分数平均值占无机氮总量的55.50%,是地下水无机氮素中污染影响程度最大的指标;土壤有机氮、厩肥污水和氨态化肥是径流补给区氮素的主要污染来源,各污染端元贡献比由大到小依次为40.49%、30.24%和29.27%.地下水补给区是氨氮污染最重的区域,排泄区是硝酸盐氮污染相对严重的区域,氧化还原条件是影响氮素浓度的关键因素;在氮素的时空演化过程中,除二级阶地仍保持天然水化学状态外,一级阶地和漫滩区的氮素浓度均有不同程度的升高.
无机氮浓度;来源示踪;影响因素;水化学演化模式;三江平原
三江平原是我国大型沉积型盆地之一,其丰富的水土资源为农作物种植创造了得天独厚的自然条件,因而也成为国家重要的商品粮基地之一.农业生产的快速发展,带动了地区GDP的增长,但也对区域地下水环境产生了一系列负面效应,最为突出的是因过度施用含氮化肥导致地下水中氮素含量升高,从而造成地下水呈面源污染,对人类生活生产用水安全构成严重威胁[1-2].此外,生物粪便排放、垃圾的非正规填埋和废水的排放等都能产生氮污染物.科学防治氮素对地下水化学环境产生的不良影响,不仅可以为居民安全饮水提供保障,也是生态水文地质研究领域长期以来的关注热点.而有效识别水体中氮素来源及其演化特征,是合理建立氮素污染防治对策的基础和关键.
氨氮、硝酸盐氮和亚硝酸盐氮是无机氮素的主要形态,通常称为"三氮",是地下水中普遍存在的氧化还原敏感性污染物,也是土壤圈、水圈等全球关键带中生物地球化学作用非常活跃的污染物之一[3].已有研究表明,当地下水处于弱氧化或还原环境下,氮素主要的存在形态为氨氮;当地下水趋于氧化环境时,硝酸盐氮为氮素的主要存在形态,亚硝酸盐氮为过渡形态[4-5].水体中氮素的主要存在形态一般可通过氮元素毫克当量百分比或相关系数法等方法确定[1].利用氮素与其他离子浓度特征关系或氮素浓度空间分布等传统水化学方法,可以定性追溯氮素的来源[6-7].目前应用氮、氧稳定同位素技术分析氮素来源与成因得到广泛推广,不同氮源具有独特的氮、氧同位素特征,δ15N可以识别氮素的来源[8-9].但是不同来源的δ15N分布特征有重叠现象,利用δ15N和δ18O双稳定同位素示踪能够更准确的判定氮素来源[10-11].基于氮、氧稳定同位素对氮源的定性分析,进一步利用稳定同位素分析模型定量判别各污染端元的贡献比,对于加强污染源源头控制更具针对性[12].综合运用水化学分析、离子浓度空间分析、氮氧同位素示踪等技术方法,能够更加准确获取氮素来源,便于分析水体中氮素的迁移特征及其影响因素[13-14].三江平原抚远地区是我国东北地区重要的生态保护屏障,但该区域有关地下水氮素污染方面的研究尚未开展,氮素来源及其影响因素尚不明晰.因此,本文以抚远地区为例,采用水化学方法和GIS技术分析地下水无机氮素主体形态和浓度特征,利用氮氧稳定同位素技术定性判断氮素来源并定量识别各氮源贡献比,结合区域水文地质条件和地下水氧化还原组分对氮素浓度的影响分析,建立研究区无机氮素水化学演化模式,为地方开展氮素污染源头治理,缓解和防治氮源污染提供科学参考.
1 材料与方法
1.1 研究区概况
抚远地区位于三江平原东北部,北、东两面与俄罗斯隔黑龙江、乌苏里江相望,南邻饶河县,西接同江市,坐标133°40′08"~135°05′20"E,47°25′30"~ 48°27′40"N,总面积6262.48km2(图1).研究区属中温带大陆性季风气候,多年平均气温2.9℃,年均降水量532.7mm,年均蒸发量580~730mm.地表水系发育,主要包括黑龙江、乌苏里江等大中型河流和浓江、别拉洪河、鸭绿河等小型支流,均属黑龙江水系.
全区广泛分布冲洪积、冲湖积平原,海拔高度多为40~60m,地形由西南向东北微倾斜,坡度1/5000~ 1/10000.主体地貌为两级阶地和高、低河漫滩,一、二级阶地分布面积最广.北部分布丘陵,出露前第四纪基岩,局部边缘有断续残丘和冰碛台地,其基底埋藏较浅.区内地层主要包括古生界石炭二叠系,中生界三叠系、侏罗系、白垩系,新生界新近系、第四系,以及燕山-印支期花岗闪长岩和闪长玢岩等侵入岩.新生代以来以沉降运动为主,接续沉积了厚度较大的新近纪和第四纪地层,属于典型的沉积型盆地.

图1 抚远地区水文地质条件及采样点分布
依据地下水的赋存条件、含水岩组特征和开采价值等因素,本区地下水可分为基岩裂隙水、碎屑岩类裂隙孔隙水和松散岩类孔隙水(图1).北部丘陵区发育有深浅不同的网状风化裂隙带,赋存有基岩风化裂隙水,多为潜水,埋深主要受地形的影响,区域径流模数一般小于1L/(s·km2).与北部基岩丘陵区交接部位发育有三叠系-侏罗系硅质岩、板岩、砂岩,赋存有少量碎屑岩类裂隙孔隙水,单井涌水量一般为10~200m3/d.新近系裂隙孔隙含水岩组埋藏于第四系含水岩组之下,埋藏深度40~300m,裂隙、孔隙发育,单井涌水量为300~800m3/d.松散岩类孔隙水在平原区广泛分布,地表覆有3~10m厚黏性土层,孔隙水具有微承压-承压性.含水层岩性主要为砂和砂砾石,厚度50~200m,单井涌水量一般大于5000m3/d,局部1000~5000m3/d.松散岩类孔隙水含水层是本区最具农业供水价值的开采层.
区域地下水流向依地形走势,为西南-东北流向,补给来源是径流补给和大气降水,地表水侧向入渗及灌溉水回渗对松散岩类孔隙水有一定的补给作用.人工开采是本区地下水最主要的排泄方式,其次为径流排泄和蒸发排泄.
1.2 数据来源
2017年7月,课题组在研究区采集了92组地下水水样(图1),进行理化指标现场测定和水质全分析测试,采样密度为1.5个/100km2.采用HQ40D和HI93703-11型便携式多参数测定仪现场测试理化指标,测试项目包括pH值、溶解氧(DO)、氧化还原电位(h)、电导率(EC)、浊度、气温、水温共7项.样品采集与封存按照相应标准[15]执行.水质全分析样品由自然资源部东北矿产资源监督检测中心检测,依据相应检验标准[16-17]测试Na+等16项化学指标.其中,采用电感耦合等离子体发射光谱法(ICP- AES)测试Na+、K+、Ca2+、Mg2+、TMn、TFe,采用离子色谱法(IC)测试Cl-、SO42-、NO3-,采用紫外可见分光光度法(UV)测试NH4+、NO2-、Fe2+、Fe3+,采用容量法(VOL)测试HCO3-、COD,采用重量法(GR)测试TDS.试验时室温25℃,空气湿度45%.通过12次加标回收测定降低测试误差,加标回收率90%~110%,相对标准偏差RSD%£15%,分析精度0.5%.课题组同期在区域地下水流场上游(图1),沿地下水径流路径设计3条采样剖面、10个采样点位,采集同一点位相邻的20和40m深度水井中地下水样品各1组,共采集20组水样测试氢氧及氮同位素特征值.氢氧同位素和氮同位素水样分别委托中国地质调查局岩溶地质研究所与核工业北京地质研究院分析检测.氢氧同位素和氮同位素分别依据相应分析方法[18]进行检测采用MAT253型稳定同位素质谱仪测试δ18O、δD和δ15N,分析精度0.5%.
1.3 方法
采用Excel 2003数据分析模块对主要水化学指标进行相关性分析.应用Gibbs图、离子比值法、氯碱指数法和氢氧同位素分布特征进一步分析地下水化学成因作用.以Mapgis 67的DTM模块为平台,采用克里金插值法分析地下水中氮素浓度的空间分布特征.基于水文地球化学理论,结合区域地貌、包气带岩性和厚度、氧化还原条件等影响因素,建立无机氮素的水化学时空演化模式.
为了定量识别氮素的主要来源,采用SIAR模型计算不同氮源对δ15N组成的贡献率.SIAR模型是Parnell等[19]开发的一种基于贝叶斯框架下构建的逻辑先验分布,通过马尔科夫链蒙特卡罗拟合模型,估算混合物中各来源贡献比例的概率分布.与传统的基于质量平衡模型来评估不同来源贡献率的IsoSoure模型[20]相比,SIAR模型能够反映多种潜在来源的混合作用,并且能够综合同位素分馏作用的影响[21].SIAR可以表示为:


式中:X是混合物同位素的值(=1,2,3,…,,=1, 2,3,…,);P是来源的贡献比例,需要由模型估算;S是来源同位素的值,服从均值为μ,方差为ω的正态分布;C是来源同位素的分馏系数,服从均值为λ,方差为τ的正态分布;ε是残余误差,表示其它各混合物间无法量化的方差,其均值为0,标准差为σ.
2 结果与分析
2.1 区域水化学特征

表1 地下水水化学成分含量特征
地下水水化学成分测试分析结果(表1)显示,水中pH值的平均值为7.23,属中性-弱碱性水,TDS和总硬度平均值分别为222.33, 142.93mg/L,属低矿化度的软水.经主要化学成分毫克当量百分比计算,地下水中主要阴离子为HCO3-,其次为SO42-、Cl-,其毫克当量百分数平均值依次为76.07%、11.73%和6.54%;阳离子以Ca2+、Mg2+为主,其次为Na+、K+,其毫克当量百分数平均值依次为43.02%、30.43%、22.83%和15.57%.地下水化学类型的舒卡列夫分类结果表明,水化学类型以HCO3-Ca·Mg型和HCO3-Ca·Na型水为主,其次为HCO3·SO4-Ca·Mg型水.
2.2 水化学成因作用 主要水化学成分的相关性分析可以初步推断各离子之间的关系和来源.表2显示:TDS与阳离子浓度均呈正相关关系,且与(Ca2+)、(Mg2+)、(Na+)正相关性更为显著.TDS与阴离子(SO42-)、(Cl-)、(NO3-)、(NO2-)均呈正相关且相关性递减,与(HCO3-)相关性不明显,说明地下水中TDS浓度的增加与含水介质中铝硅酸盐、硫酸盐和岩盐等矿物溶解释放出的离子有关.阳离子中(Mg2+)、(Na+)、(K+)与(Ca2+)呈正相关,说明地下水径流过程中存在阳离子交换吸附.(Na+)与(Cl-)相关系数为0.745,两者浓度的增加与蒸发浓缩作用有关.(Cl-)和(NO3-)相关系数达到0.822,反映出Cl-和NO3-浓度的增加与人类生活排污以及农业活动施肥关系较密切.阳立平等[22]研究表明,(NH4+-N)的变化与地下水中氧化还原性物质和胶体性质等因素有关,Fe3+既是氧化还原敏感性组分,含铁矿物颗粒又是北方地区常见的胶体形态,故(NH4+)与(Fe3+)具有较明显的正相关性.
2.2.1 溶滤作用 是指水与岩土相互作用,岩土中一部分物质输入水中,增加了水中相应组分的含量,而岩土则失去了相应的可溶组分.Gibbs图可以定性判断大气降水、岩石风化和蒸发浓缩作用对地下水化学成分的影响[23].由图2可以看出本区水化学成因整体上受岩石风化作用控制.阴离子比阳离子质量摩尔浓度比值的数据点向右飘移幅度略大,反映了蒸发浓缩对区域水化学成因具有一定作用.区域流场下游属于冲积河漫滩地貌,潜水位埋深浅且含水介质导水性良好,故潜水蒸发浓缩体现的较明显.

表2 地下水主要水化学成分Pearson相关系数矩阵
注:“*”表示显著正相关.
离子比值法可以进一步明确水化学成分主要来源于哪类矿物的溶解[24].当Na++K+与Cl-的质量摩尔浓度比为1:1时,说明Na+、K+主要来源于岩盐的溶解,反之来源于铝硅酸盐矿物的溶解[25].图3(a)显示,仅有少数河漫滩和一级阶地水样位于1:1直线上,其他水样均位于1:1直线两侧,说明地下水中Na+、K+主要来源于铝硅酸盐矿物的溶解,少量来源于岩盐溶解.而Ca2+、Mg2+离子的来源可以通过2[(Ca2+)+(Mg2+)]/[(HCO3-)+2(SO42-)]质量摩尔浓度比值来判断.当比值大于1时,表明其来源于碳酸盐矿物溶解;等于1,源于碳酸盐与铝硅酸盐矿物溶解;小于1,则源于铝硅酸盐或硫酸盐矿物溶解[1].图3(b)所示,本区多数基岩裂隙水、少量孔隙水样品位于1:1线上方,基岩裂隙水主要分布于区域流场下游,由此推断排泄区地下水中的Ca2+、Mg2+离子主要源于碳酸盐矿物溶解.有少量的两级阶地微承压水位于1:1线上,表明其Ca2+、Mg2+离子来源于碳酸盐与铝硅酸盐矿物的溶解,反映出地下水径流区多种矿物混合溶滤作用的特点.大部分水样处于1:1线下方,说明地下水中Ca2+、Mg2+离子主要源于铝硅酸盐和硫酸盐矿物溶解.

(a)主要阳离子Gibbs图;(b)主要阴离子Gibbs图
2.2.2 阳离子交换吸附作用 黏土颗粒表面带有负电荷,其吸附地下水中的某些阳离子,而将原来吸附的部分离子转为地下水中组分的过程为阳离子交换吸附作用.在含水层中普遍存在Ca2+、Mg2+离子和Na+、K+离子的交换吸附,通常可以由交换指数即氯碱指数CAI(包括CAI1和CAI2)来确定交换吸附是Ca2+、Mg2+置换Na+、K+的正向反应,还是Na+、K+置换Ca2+、Mg2+的逆向反应.两项指数都为正值表明含水层中发生逆向交换吸附,都为负值表明发生正向交换吸附[1].氯碱指数计算公式为:
CAI1=[(Cl-)-(Na++K+)]/(Cl-)(3)
CAI2=[(Cl-)-(Na++K+)]/[2(SO42-)+(HCO3-)+
(NO3-)](4)
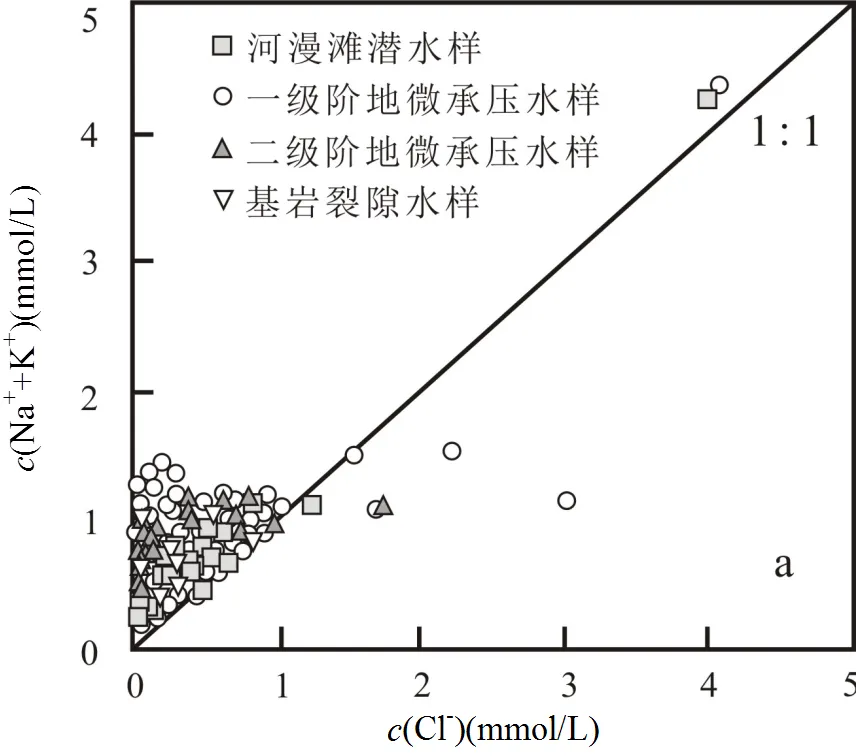
(a) (Na++K+)与Cl-的质量摩尔浓度比值关系图;(b) (Ca2++Mg2+)与(HCO3-+SO42-)的质量摩尔浓度比值关系图
经统计,92个水样中仅有流场下游的7个水样计算出两项CAI均为正值,说明排泄区地下水发生逆向交换吸附作用.其余85个水样两项CAI均为负值,表明本区含水层以正向交换吸附作用为主.
2.2.3 蒸发浓缩作用 通过分析不同水体的δD和δ18O稳定同位素关系,可以判断其来源和蒸发作用程度.δD和δ18O测试结果(表3)显示,区域流场上游20和40m两个深度的水样δ18O和δD值域接近,说明区域第四系孔隙水同源.已有研究表明,三江平原当地降水线斜率为7.4[26],略小于全球降水线斜率8.0,稍向右偏离于全球降水线,体现了内陆干旱半干旱区的地下水同位素补给环境的特点(图4) .本次测试的20和40m深度地下水样δ18O-δD特征值均分布在全球降水线的右下方,表明区域地下水同源于大气降水.当地降水线和40m地下水蒸发线斜率接近,两者斜率大于20m地下水蒸发线,且多数采样点分布于蒸发线和全球降水线之间,说明地下水存在蒸发排泄,20m地下水蒸发线明显向右偏移,说明20m地下水蒸发作用大于深部地下水.

表3 地下水流场上游δ18O和δD特征(‰)

图4 地下水流场上游δ18O-δD关系图
2.3 氮素浓度空间分布特征
地下水质量评价以检测数据为基础[27],为反映地下水中硝酸盐氮、亚硝酸盐氮和氨氮的浓度特征,开展单指标质量评价,按指标值所在的限值范围确定地下水质量类别,指标限值相同时,从优不从劣.以Ⅲ类质量标准(NH4+-N)£0.50mg/L、(NO3--N)£20.0mg/ L、(NO2--N)£1.0mg/L为标准值,单指标评价结果表明:研究区地下水中(NH4+-N)为0.015~1.84mg/L,平均浓度0.56mg/L,超标率达56.52%;(NO3--N)为0.0045~53.62mg/L,平均浓度3.79mg/L,超标率仅为5.43%;亚硝酸盐氮不超标.各组水样中氨氮、硝酸盐氮和亚硝酸盐氮毫克当量百分比平均值分别为55.50%、43.13%和1.37%.可见,氨氮是研究区地下水无机氮素中污染影响程度最大的指标.
基于MapGIS 67平台和克里金法得出的研究区地下水中氮素浓度空间分布特征表明:NH4+-N浓度超标区域主要分布于前哨农场-别拉洪乡-海青乡以南,地下水补给-径流区前锋农场一带的(NH4+-N)³1.5mg/L,超出V类水质标准(图5).而硝酸盐氮浓度仅在乌苏镇、海青乡、通江乡等地下水排泄区的局部超标(图6).氮素浓度的空间分布特征与水文地质条件、地貌类型、土地利用类型、包气带岩性和厚度等关系密切[2].地下水补给-径流区的地貌以两级阶地为主(图7),地面坡度小于1/5000,地表覆盖的黏性土厚度普遍大于6m,仅别拉洪河等小流域局部的地表黏性土厚度较薄(图8).该区域地下水埋深普遍为10~20m,厚度较大的黏性土覆盖在含水层上部,使地下水具有承压性,并处于贫氧或无氧的还原环境.两级阶地是当地水稻的主产区.化肥的持续施用为地下水提供了充足的氮源,无机氮在还原环境下的存在形态以氨氮为主,故而直接导致该区域地下水中氨氮浓度的升高.

图5 地下水氨氮浓度空间分布
图5~7显示,在地下水由阶地(补给区)向漫滩(排泄区)流动的过程中,(NH4+-N)逐渐下降,而(NO3--N)逐渐升高.至黑龙江、乌苏里江漫滩,地下水中(NO3--N)普遍为5~20mg/L,局部超出Ⅲ类水质标准30mg/L.结合水文地质条件分析,漫滩区地下水全部为潜水,含水层上覆黏性土厚度普遍小于1m(图8),潜水位埋藏深度2~5m,与地表环境接触密切,潜水整体处于氧化环境.抚远市及主要乡镇分布于此,人类生产、生活废物的无序排放都能对地下水输入额外的氮源,并在氧化环境下以硝酸盐氮为主要存在形态.同时,随着地下水由补给区向排泄区径流,水化学环境由还原态逐渐向氧化态过渡,硝化作用也在增加硝酸盐氮浓度上发挥了作用.硝化作用是指在有氧环境下,NH4+在硝化细菌的参与下被氧化成NO3-的过程[28]:NH4++2O2→NO3-+2H++H2O.因此,人类活动和水文地球化学作用共同促使了漫滩区潜水中硝酸盐氮浓度的升高.

图6 地下水硝酸盐氮浓度空间分布

图7 地貌类型分布

图8 包气带黏性土等厚度图
2.4 氮素来源识别
区域流场上游采集的20组孔隙水样品的δ15N值域为-4.2‰~10.6‰,均值为3.56‰.其中,20和40m深度水样的δ15N值域分别为-3.6‰~9.3‰和-4.2‰~10.6‰,均值分别为3.7‰和3.42‰.δ18O值域为-12.48‰~-10.26‰,均值为-11.778‰(表3).将20组数值绘制在δ15N/δ18O特征值分布图(图9)中可见,地下水中氮素主要来源于含铵化肥的施用,长期施肥过程中富集在土壤中的有机氮的分解,以及牲畜养殖和污灌等产生的废物.
SIAR模型估算不同物源贡献比例的关键是确定各物源的同位素的典型值域[12].张千千等[21]整理了国内外近60篇文献中不同污染源氮氧同位素的值域范围,氨态氮肥δ15N值域为-2.7‰~2.3‰,均值近于0‰;土壤氮δ15N值域为-3.5‰~9.0‰,均值近于2.2‰;厩肥和污水的δ15N值域接近,本次取厩肥δ15N值域5.9‰~22.0‰,均值为12.7‰.氮源的氧同位素主要来自硝酸盐中的氧,可分为大气沉降、硝化作用形成和硝酸盐氮肥3大类来源,图9显示研究区氮源中δ18O主要来源于氨态氮肥、土壤氮和厩肥污水等氮素经硝化作用形成的硝酸盐.张千千等[21]对36个样本统计后得到硝化作用产生的δ18O值域为3.5‰~16.8‰,均值为10.6‰,明显大于本次实测的δ18O值域.由于土壤一部分氧源于土壤氮的硝化作用,土壤水的δ18O通常为负,较大气源显著贫18O,因此将δ18O值的下限定为-10‰[29].由图9还可以看出,本区孔隙水样的δ15N/δ18O比值不在1:1和2:1反硝化作用范围内,说明含水层未发生明显的反硝化作用,故可以假设公式(4)中的分馏因子C=0,即本区孔隙水基本不发生微生物参与的反硝化作用.

图9 区域流场上游地下水δ15N/δ18O特征分布
SIAR模型输出结果显示(图10),地下水中氮素端元贡献中土壤氮所占比例最高,平均占比40.49%;氨态化肥和厩肥污水的贡献比例接近,平均占比分别为29.27%和30.24%.各氮源贡献率分配较均匀,与δ15N/δ18O特征值分布情况基本一致.
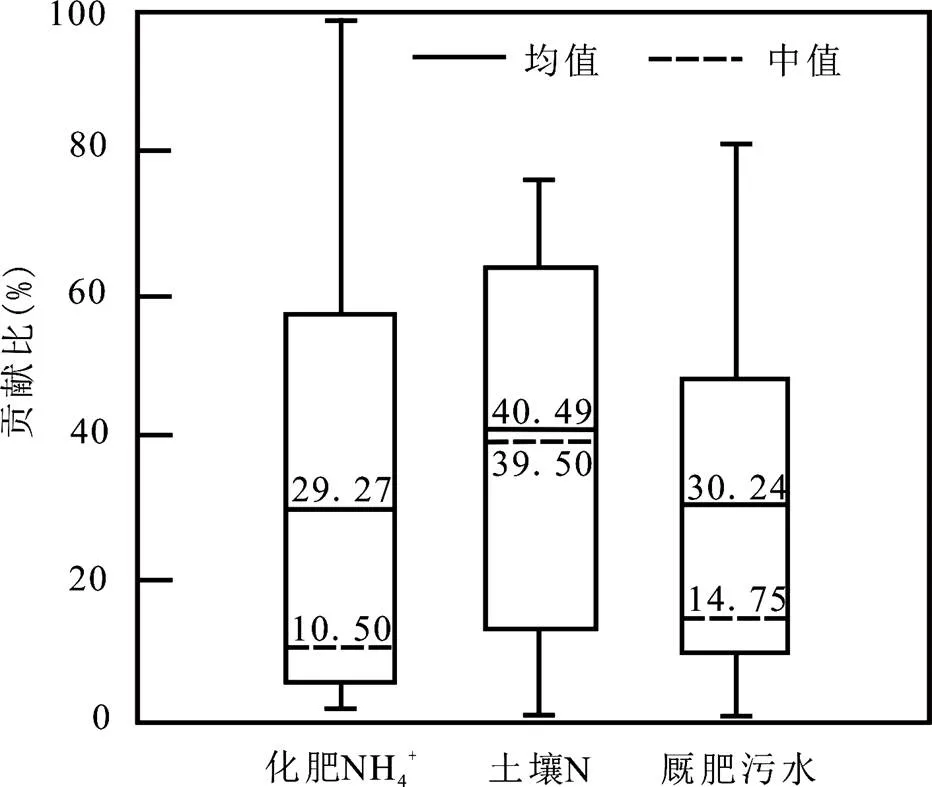
图10 地下水氮源贡献比箱式图
2.5 氮素浓度主要影响因素分析
氮素浓度的变化是由物理、化学、生物等综合作用的过程引起的[30].由于氮素是地下水中典型的氧化还原性污染物,因此,除了水文地质条件及人类活动等因素外,含水层中的氧化还原条件的变化对氮素浓度的改变将产生直接的影响.而氧化还原性组分DO、h、Fe2+、Fe3+、Mn2+、SO42-等是表征含水层氧化还原条件变化的重要指标.
图11表明,本区地下水中(NH4+-N)与(DO)、(NO3--N)、Eh值呈负相关.地下水中(DO)的高低,控制了氧化还原反应的方向[31].图11b、g显示,处于区域流场下游的河漫滩潜水(DO)较高,趋于氧化环境,有利于还原态的氨态氮向氧化态的硝酸盐氮转化,促使氨氮浓度下降而硝酸盐氮浓度升高.而两级阶地的(DO)普遍较低,以贫氧或还原环境为主,氨氮为水中无机氮的主要存在形态.此外,自然资源部东北矿产资源监督检测中心对本区土壤可溶盐测试结果显示:pH值为5.90~6.35,(NO3-)为0.2~ 1.28mg/L,(NO2-)为0.015~0.088mg/L.土壤与大气圈接触,处于开放的氧化环境,且富含有机质和腐殖质,这些物质的分解需要袭夺土壤中的溶解氧.土壤深度越大,受外界补给的氧越少,而好氧物质对溶解氧的消耗,使深部岩土介质趋于贫氧或还原环境,在水文地球化学作用下,土壤中的有机氮逐渐转化为还原态的氨氮,最终进入地下水中参与水循环.因此,本区两级阶地地下水中的(NH4+-N)普遍大于漫滩区或基岩区地下水的(NH4+-N).
h通常用于判断地下水的氧化还原状态.当Eh值为负值时,地下水通常处于还原环境;Eh值为正值时,则为氧化环境[31].本区地下水中h值为-61.4~ 69.6mV,平均值为11.71mV,92个水样中有20个水样的h值小于0mV,与之对应的(NH4+-N)为0.06~ 1.25mg/L,平均浓度为0.58mg/L;52个水样h值低于平均值,对应(NH4+-N)为0.06~1.84mg/L,平均浓度为0.62mg/L;Eh值高于平均值的40个水样对应的(NH4+-N)为0.05~1.78mg/L,平均浓度为0.49mg/L.由此可见,研究区地下水中h值低于平均值时,地下水处于弱氧化或还原环境,氨氮的平均浓度相对较高;而当h值升高后,地下水趋于氧化环境,有利于氨氮向硝酸盐氮转变,氨氮的质量浓度有所下降.
研究区地下水中(NH4+-N)与(Fe3+)、(Fe2+)、(Mn2+)呈显著正相关,与pH值和(SO42-)也呈正相关(图11) .铁、锰化合物是我国北方地区含水层中常见的胶体矿物,胶体表面多带有负电荷,它们可以充当阳离子交换剂,以正电荷形式存在的NH4+容易被吸附[32].而pH值对胶体的形成有较大的影响,含水介质表面存在零点电荷pHz,当水溶液的pH值大于pHz时,矿物表面带负电,可吸附阳离子.含水介质中常见的含铁、锰质胶体矿物按pHz值由小到大排序依次是-MnO2 图11 地下水中氨氮与氧化还原物质浓度关系 在区域氮素浓度特征、主要影响因素和水化学成因分析的基础上,结合水文地质条件,建立1条沿地下水流向的剖面A-A'(图1) ,利用2017年在该剖面上实测的7个水样S1~S7测试数据分析水化学演化特征,进而构建区域无机氮素的水化学演化模式(图12) .如图所示,剖面A-A'为西南-东北走向,地下水自流场上游向东北径流,最终汇入乌苏里江.流场上游以第四系上更新统别拉洪河组(Qp3b+l)粉质黏土、砂砾石构成的一级阶地为主,径流区以中更新统浓江组(Qp2n+fgl)砂砾石及冰水堆积物构成的二级阶地为主,两组地层的砂砾石为主要赋水层位.排泄区由别拉洪河组(Qp3b+l)一级阶地和全新统冲积层(Qh)构成的河漫滩组成. 图12 研究区无机氮素水化学演化模式 图12显示:流场中上游S1~S4点地下水化学类型为HCO3-Ca·Mg·Na型水;至二级阶地S5点处,水化学类型转化为Cl·HCO3-Ca·Mg·Na型水;至排泄区S7点处,水化学类型呈Cl·SO4-Na ·Mg·Ca型水.水化学成因作用表明,流场上游两级阶地水化学成分主要源于铝硅酸盐矿物的溶解以及阳离子正向交换吸附作用.因此,阴离子以铝硅酸盐发生溶解反应后通常形成的产物HCO3-为主,而阳离子以Ca2+、Mg2+为主.流场下游含水介质中的岩盐和硫酸盐矿物的溶解以及潜水蒸发,可以增加地下水中Cl-和SO42-的浓度;含水层中同时发生Na+、K+置换Ca2+、Mg2+的逆向交换吸附作用,从而增加了水中的Na+的浓度.因此,流场下游阴离子以Cl-和SO42-为主,阳离子以Na+为主,Ca2+、Mg2+次之. S1~S7水样的主要化学指标浓度随径流路径变化曲线(图12)显示:(NH4+-N)、(TFe)及pH值均随地下水径流而下降,以(NH4+-N)降幅最为明显.流场上游一级阶地S1~S2点的(NH4+-N)为1.03~ 1.44mg/L,经二级阶地至漫滩区的S3~S7点骤降至0.05~0.26mg/L.而(NO3--N)沿径流路径的变化特征与(NH4+-N)明显相反.流场中上游S1~S4点的(NO3--N)均小于0.2mg/L;由S5~S7点,(NO3--N)由22.42mg/L增至53.62mg/L.(NH4+-N)和(NO3-- N)沿径流路径的变化特征与区域地下水氮素浓度变化特征一致.(TDS)、(DO)及h具有由流场上游一级阶地至二级阶地先下降,再经二级阶地至漫滩区升高的变化趋势.S1~S4点Eh值为-1.9~10.9mV,小于区域h平均值,(DO)为2.41~4.94mg/L,说明流场中上游普遍处于弱氧化或还原环境,水中无机氮素以还原态的氨氮为主体.S5~S7点h、(DO)增幅明显,尤其是Eh值最大增至60.5mV,说明S5点下游的含水层明显趋于氧化环境,此时氧化态的硝酸盐氮取代氨氮,成为无机氮素的主体形态.二级阶地S3~ S4点范围内水化学类型以HCO3型水为主,(TDS)为109.43~161.31mg/L,(NH4+-N)为0.06~ 0.2mg/L,(NO3--N)<0.02mg/L,水中可溶盐含量较低,可以推断该范围内含水层中各项矿物指标基本处于饱和状态,地下水处于相对稳定的天然水化学环境. 对比分析2017年实测数据和2013年历史数据(图12)可知,主要指标浓度随径流路径的变化特征基本一致.但2017年水样的pH值明显低于2013年检测结果,而(NH4+-N)、(NO3--N)和(TDS)则普遍升高.天然水中pH值一般在7.2~8.5之间,当pH值过高或过低时,表示水体可能受到了污染[31].剖面A-A'地下水中,2013年pH值平均值为7.05,2017年pH值平均值降至6.55;2017年NH4+-N和TDS的最大质量浓度分别比2013年增加了0.92倍和1.31倍,(NO3--N)增加了7%,说明近5a来人类持续的农业活动和生活排污等行为,促进了氮素及可溶盐组分质量浓度的升高,加剧了地下水的受污染程度. 3.1 研究区地下水属中性-弱碱性、低矿化软水,水化学类型以HCO3型水为主,其次为HCO3·SO4型水.水化学成分主要源于铝硅酸盐矿物的溶解和阳离子交换吸附作用,少量来源于岩盐、硫酸盐等矿物的溶解.流场下游阳离子逆向交换吸附和蒸发浓缩作用促使该区域Na+、Cl-等离子质量浓度的增加. 3.2 地下水中氨氮、硝酸盐氮超标率分别为56.52%和5.43%,毫克当量百分比平均值分别为55.50%和43.13%,氨氮对区域地下水的污染影响程度最大.流场上游补给-径流区氨氮污染程度最为严重,同位素示踪得出土壤有机氮、厩肥污水和氨态化肥是氮素的主要污染来源,SIAR模型计算各端元贡献比分别为40.49%、30.24%和29.27%,土壤有机氮对地下水中氮素的富集贡献率最高. 3.3 氧化还原条件是影响氮素浓度变化和形态转化的关键因素.氮素空间演化特征表现为随地下水径流,水化学环境由还原态趋于氧化态,(NH4+-N)逐渐下降,(NO3--N)逐渐升高;时间演化特征表现为近5a持续的人类活动导致NH4+-N和TDS的最大浓度增加了0.92倍和1.31倍,pH值趋于酸性,地下水污染程度仍在加剧. 3.4 流场补给区的一级阶地和排泄区的河漫滩,分别是地下水受氨氮和硝酸盐氮污染较重的区域.补给区应控制含氮素化肥的使用量,提高折纯量;排泄区应做好垃圾分类处理,在人类可控范围内,降低氮素污染水体的风险.二级阶地水化学环境多年来基本处于天然状态,且地下水资源量丰富,可以保障城乡居民的正常生产生活供水. [1] 董维红,孟 莹,王雨山,等.三江平原富锦地区浅层地下水水化学特征及其形成作用[J]. 吉林大学学报(地球科学版), 2019,47(2):542− 553.Dong W H, Meng Y, Wang Y S, et al. Hydrochemical characteristics and formation of the shallow groundwater in Fujin, Sanjiang Plain [J]. Journal of Jilin University (Earth Science Edition), 2017,47(2):542− 553. [2] 方 敏.三江平原松花江-挠力河流域浅层地下水“三氮”污染形成过程研究[D]. 长春:吉林大学, 2019.Fang M. Formation process of inorganic nitrogen pollution in shallow groundwater of Songhua and Naoli River Basin, Sanjiang Plain [D]. Changchun: Jilin University, 2019. [3] Zhang W, Dennis P S, Bongghi H, et al. Influence of rapid rural-urban population migration on riverine nitrogen pollution: perspective from ammonia-nitrogen [J]. Environmental Science and Pollution Research, 2017,24(35):27201−27214. [4] Burke V, Greskowiak J, Asmub T, et al. Temperature dependent redox zonation and attenuation of wastewater-derived organic micropollutants in the hyporheic zone [J]. Science of the Total Environment, 2014,482−483,53−61. [5] 王晓玲,郑晓通,李松敏,等.农田排水沟渠底泥-间隙水-上覆水氮磷迁移转化规律研究[J]. 水利学报, 2017,48(12):1410−1418.Wang X L, Zheng X T, Li S M, et al. Study on the migration and transformation of nitrogen and phosphorus in sediment-interstitial water-overlying water in farmland drainage ditch [J]. Journal of Hydraulic Engineering, 2017,48(12):1410−1418. [6] Chandna P, Khurana M L, Ladha J K, et al. Spatial and seasonal distribution of nitrate-N in groundwater beneath the rice-wheat cropping system of India: a geospatial analysis [J]. Environmental Monitoring and Assessment, 2011,178(1):545−562. [7] Zhai Y, Zhao X, Teng Y, et al. Groundwater nitrate pollution and human health risk assessment by using HHRA model in an agricultural area, NE China [J]. Ecotoxicology and Environmental Safety, 2016, 137:130−142. [8] 徐志伟,张心昱,于贵瑞,等.中国水体硝酸盐氮氧双稳定同位素溯源研究进展[J]. 环境科学, 2014,35(8):3230−3238.Xu Z W, Zhang X Y, Yu G R, et al. Review of dual stable isotope technique for nitrate source identification in surface and groundwater in China [J]. Environmental Science, 2014,35(8):3230−3238. [9] Heaton T H E. Isotopic studies of nitrogen pollution in the hydrosphere and atmosphere: a review [J]. Chemical Geology: Isotope Geoscience Section, 1986,59(2):87−102. [10] Amberger A, Schmidt H L. Natural isotope contents of nitrate as indicators for its origin [J]. Geochim Cosmoch-im Acta, 1987,51(10): 2699−2705. [11] Meredith G, Hastings, Karen L, et al. Stable isotopes as tracers of anthropogenic nitrogen sources, deposition and impacts [J]. Elements, 2013,(9):339−344. [12] 李 严,曹明达,靳孟贵,等.湖北泉水河流域水化学特征和硝酸盐来源示踪[J]. 地球科学, 2020,45(3):1061−1070.Li Y, Cao M D, Jin M G, et al. Hydrochemical characteristics and tracing of nitrate sources in Quanshui River Catchment, Hubei Province [J]. Earth Science, 2020,45(3):1061−1070. [13] 傅雪梅,孙源媛,苏 婧,等.基于水化学和氮氧双同位素的地下水硝酸盐源解析[J]. 中国环境科学, 2019,39(9):3951−3958.Fu X M, Sun Y Y, Su J, et al. Source of nitrate in groundwater based on hydrochemical and dual stable isotopes [J]. China Environmental Science, 2019,39(9):3951−3958. [14] 彭 聪,潘晓东,焦友军,等.多种同位素手段的硝酸盐污染源解析:以会仙湿地为例[J]. 环境科学, 2018,39(12):5410−5417.Peng C, Pan X D, Jiao Y J, et al. Identification of nitrate pollution sources through various isotopic methods: a case study of the Huixian Wetland [J]. Environmental Science, 2018,39(12):5410−5417. [15] HJ493-2009 水质采样样品的保存和管理技术规定[S].HJ493-2009 Water quality sampling-technical regulation of the preservation and handling of samples [S]. [16] DZ/T 0064-1993 地下水质检验方法 [S].DZ/T 0064-1993 Groundwater quality inspection methods [S]. [17] GB 5749-2006 生活饮用水卫生标准 [S]. GB 5749-2006 Standards for drinking water quality [S]. [18] DZ/T 0184.1~0184.22-1997 同位素地质样品分析方法 [S]. DZ/T 0184.1~0184.22-1997 Analysis methods of isotopic geological samples [S]. [19] Parnell A C, Inger R, Bearhop S, et al.Source partitioning using stable isotopes: coping with too much variation [J]. PLOS ONE, 2010,5(3): e9672. [20] Phillips D L, Koch P L.Incorporating concentration dependence in stable isotope mixing models [J]. Oecologia, 2002,130:114−125. [21] 张千千,缪丽萍,孙继朝,等.稳定同位素识别水体硝酸盐污染来源的研究进展[J]. 长江流域资源与环境, 2015,24(5):742−749.Zhang Q Q, Miao L P, Sun J C, et al. Research advances in identifying nitrate pollution sources of water environment by using stable isotopes [J]. Resources and Environment in the Yangtze Basin, 2015,24(5): 742−749. [22] 阳立平,曾凡棠,黄海明,等.氮在环境介质中的迁移转化研究进展[J]. 水资源保护, 2014,30(5):1−8.Yang L P, Zeng F T, Huang H M, et al. Advances in research of migration and transformation of nitrogen in environmental media [J]. Water Resources Protection, 2014,30(5):1−8. [23] Gibbs R J. Mechanisms controlling world water chemistry [J]. Science, 1970,170(3962):1088−1090. [24] Xing L, Guo H, Zhan Y. Groundwater hydrochemical characteristics and processes along flow paths in the North China Plain [J]. Journal of Asian Earth Sciences, 2013,70-71(1):250−264. [25] Khairy H, Janardhana M R. Hydrogeochemistry and quality of groundwater of coastal unconfined aquifer in Amol-Ghaemshahr Plain, Mazandaran Province, Northern Iran [J]. Environmental Earth Sciences, 2014,71(11):4767−4782. [26] 张 兵,宋献方,张应华,等.三江平原地表水与地下水氢氧同位素和水化学特征[J]. 水文, 2014,34(2):38−43.Zhang B, Song X F, Zhang Y H, et al. Hydrogen and oxygen isotopic and hydrochemical characteristics of water in Sanjiang Plain [J]. Journal of China Hydrology, 2014,34(2):38−43. [27] GB/T 14848-2017 地下水质量标准 [S]. GB/T 14848-2017 Standard for groundwater quality [S]. [28] 李 霄,林学钰,都基众,等.齐齐哈尔市潜水水化学演化规律分析[J]. 水利学报, 2014,45(6):94−106.Li X, Lin X Y, Du J Z, et al. Analysis of hydrochemical evolution of phreatic water in Qiqihar City [J]. Journal of Hydraulic Engineering, 2014,45(6):94−106. [29] Hollocher T C.Source of the oxygen atoms of nitrate in the oxidation of nitrate by nitrocacter agilis and evidence against a P-O-N anhydride mechanism in oxidative phosphorylation [J]. Archives of Biochemistry and Biophysics, 1984,233(2):721−727. [30] Kumar A R, Riyazuddin P.Seasonal variation of redox species and redox potentials in shallow groundwater: a comparison of measured and calculated redox potentials [J]. Journal of Hydrology, 2012,444- 445(1):187−198. [31] 钱 会,马致远.水文地球化学[M]. 北京:地质出版社, 2005:42−64.Qian H, Ma Z Y. Hydrogeochemistry [M]. Beijing : Geological Publishing House, 2005:42−64. [32] 李 勇,汪莹莹,徐 纯,等.潜流带胶体特征及对生源要素迁移的影响机制[J]. 河海大学学报(自然科学版), 2019,47(4):296−303.Li Y, Wang Y Y, Xu C, et al. Colloid characteristic in hyporheic zone and its influencing mechanism on facilitated-transport of biogenic elements [J]. Journal of Hohai University (Natural Sciences), 2019,47 (4):296−303. [33] 王 博,李海明,贾晓玉,等.天然胶体对含水介质中氨氮迁移的影响[J]. 环境科学与技术, 2009,32(7):18−21.Wang B, Li H M, Jia X Y, et al. Effect of natural colloid on ammonia nitrogen transport in water-bearing media [J]. Environmental Science & Technology, 2009,32(7):18−21. Sources tracing and evolution model of inorganic nitrogen of groundwater in sedimentary basin. LI Xiao*, WANG Xiao-guang, CHAI Lu, ZHU Wei, HE Hai-yang, WANG Chang-qi (Shenyang Institute of Geology and Mineral Resources, CGS, Shenyang 110034, China)., 2021,41(4):1856~1867 Based on Fuyuan area in Sanjiang Plain, a typical agricultural area of a sedimentary basin, the study analyzed the regional hydrochemical effect and inorganic nitrogen pollution characteristics with the hydrochemical methods and GIS technology. The nitrogen source and contribution ratio of each pollution source were determined through the distribution characteristics of nitrogen, oxygen bistable isotopes and stable isotope analysis model (SIAR). With the understanding of affecting factors on the changes of nitrogen concentration, the regional hydrochemical evolution model of nitrogen were established. These results showed that 56.52% of groundwater had ammonia nitrogen concentration exceeding the standard rate in the study area and the average milligram equivalent percentage accounted for 55.50% of the total inorganic nitrogen, which was the most important index of groundwater inorganic nitrogen pollution. Soil organic nitrogen, manure sewage and ammonia fertilizer were the main sources of nitrogen pollution in the runoff recharge area, and the contribution ratios of each pollution source was 40.49%, 30.24% and 29.27% respectively in descending order. The groundwater recharge area was the most polluted area of ammonia nitrogen, while the discharge area was the relatively serious pollution area of nitrate nitrogen. The redox conditions were the key factor affected the nitrogen concentration. In the process of spatial and temporal evolution of nitrogen, the nitrogen concentration in the first terrace and floodplain area increased in varying degrees except the natural hydrochemical state in the second terrace. inorganic nitrogen concentration;sources tracing;influencing factors;hydrochemical evolution model;Sanjiang Plain X143,P641.3 A 1000-6923(2021)04-1856-12 李 霄(1983-),男,吉林通化人,高级工程师,博士,主要从事区域地下水形成演化规律研究.发表论文45篇. 2020-09-07 中国地质调查局地质调查项目(DD20190340,DD20160115) * 责任作者, 高级工程师, ZZLX19@163.com
2.6 区域无机氮素水化学演化模式

3 结论
