基于网络药理学探讨参地补肾胶囊抗肾间质纤维化的机制研究
2021-04-28吴宸广杨菲菲李淑菊
田 锋,吴宸广,陈 明,杨菲菲,李淑菊
(1黑龙江省中医药科学院·黑龙江 哈尔滨 150036;2黑龙江省老年病医院·黑龙江 哈尔滨 150036)
慢性肾衰竭(CRF)特征在于进行性的肾间质纤维化(RIF),最终导致终末期肾脏疾病,其发病率逐渐上升且呈现年轻化的趋势,严重威胁人们的健康,给国家造成严重的经济负担[1]。参地补肾胶囊是国医大师张琪教授根据多年治疗CRF的经验,铆定CRF脾肾两虚、湿浊内蕴的病机特点而拟定,临床上应用于治疗CRF,能够改善患者肾功能,调节脂代谢,提高肾小球滤过率,具有一定的抗RIF的作用[2]。
网络药理学是基于“药物-靶点-疾病”相互作用网络进行药物研究,适合于研究中药与疾病的复杂作用机制。故本文运用网络药理学方法对参地补肾胶囊活性成分及其抗RIF相关靶点进行体统研究,为参地补肾胶囊治疗CRF的临床应用供理论依据。
1 材料与方法
1.1 材料 TCMSP数据库(http://tcmspw.com/tcmsp.php)、Universal Protein数据库(https://www.uniprot.org/)、Gene Cards数据库(https://www.genecards.org/)、OMIN生物数据库(https://www.omim.org/)、Venny2.1在线软件作图工具平台(https://bioinfogp.cnb.csic.es/tools/venny/)、STRING数据库(https://string-db.org/)、Metascape数据库(https://www.metascape.org/)和 Cytoscape3.7.2软件、Origin Lab 2019绘图软件。
1.2 方法
1.2.1 药物化学成分及其作用靶点的收集 将参地补肾胶囊中涉及的中药成分(人参、白术、茯苓、大黄、黄连、半夏、草果仁、竹茹、熟地黄、菟丝子、淫羊藿、桃仁、红花、丹参、赤芍)逐一输进中药系统药理学数据库与分析平台(TCMSP)中进行检索,设定口服生物利用度(OB)≥30%及类药性(DL)≥0.18筛选得到所有中药的活性成分,并在TCMSP数据库检索活性成分对应的作用靶点。所获得的作用靶点名称(protein name)输入到Universal Protein数据库中进行检索,选定物种来源为“human”,找到各靶点对应的基因名(gene name),方便后续的分析。
1.2.2 疾病靶点获取 在Gene Cards生物数据库和OMIN生物数据库,输入“Renal interstitial fibrosis”,去掉重复项目获得RIF靶点集。
1.2.3 潜在作用靶点的获取 在Venny2.1在线作图工具平台上分别录入参地补肾胶囊作用靶点和RIF靶点,得到两者的交集,作为潜在作用靶点,并绘制韦恩图。
1.2.4 蛋白之间相互作用(Protein-Protein Interaction,PPI)网络构建及分析 将方法3中所得到潜在作用靶点导入STRING数据库中进行检索,设置蛋白种类为“Homo sapiens”,最低相互作用阈值设置为0.9,获取蛋白之间相互作用关系的数据信息,将其导入Cytoscape3.72软件,绘制PPI网络图。
1.2.5 网络模型的构建及分析 将药物的活性成分,以及“1.2.3”中所得的潜在作用靶点分别导入Cytoscape软件,使用Network Analyzer功能对药物中的主要活性成分进行分析,构建“药物-成分-靶点-疾病”相互作用网络关系图。
1.2.6 基因本体(Gene Ontology,GO)与京都基因与基因组百科全书(Kyoto Encyclopedia of Genes and Genomes,KEGG)通路富集分析 将潜在作用靶点导入metascape数据库,分别得到GO中的生物过程(biological process,BP)、分子功能(molecular function,MF)和细胞组成(cellular component,CC),和KEGG富集分析结果。并通过Origin Lab 2019绘图软件对之进行数据可视化。
2 结果
2.1 参地补肾胶囊活性成分及作用靶点信息 将参地补肾胶囊中涉及的中药成分(人参、白术、茯苓、大黄、黄连、半夏、草果仁、竹茹、熟地黄、菟丝子、淫羊藿、桃仁、红花、丹参、赤芍)逐一输进中药系统药理学数据库与分析平台(TCMSP)中进行检索,在TCMSP数据库中设定口服生物利用度(oral bioavailability,OB)≥30%,类药性(drug-likeness,DL)≥0.18筛选化合物靶点信息。其中未检索到中药竹茹的相关信息,经查询文献找寻中药竹茹的化学成分,在TCMSP中对其分子进行单项查询,结合(OB)及类药性结合既往研究结果,纳入相应成分及其作用靶点[3-4]。并结合已有化学成分、药理作用和临床应用文献报道,去掉多种中药含有相同的成分后得到163个有效化学成分和286个可能有效靶点。将所获得的作用靶点名称(protein name)输入到Universal Protein数据库中进行检索,选定物种来源为“human”,找到各靶点与之对应的基因名(gene name)。中药成分靶点信息概况见表1。
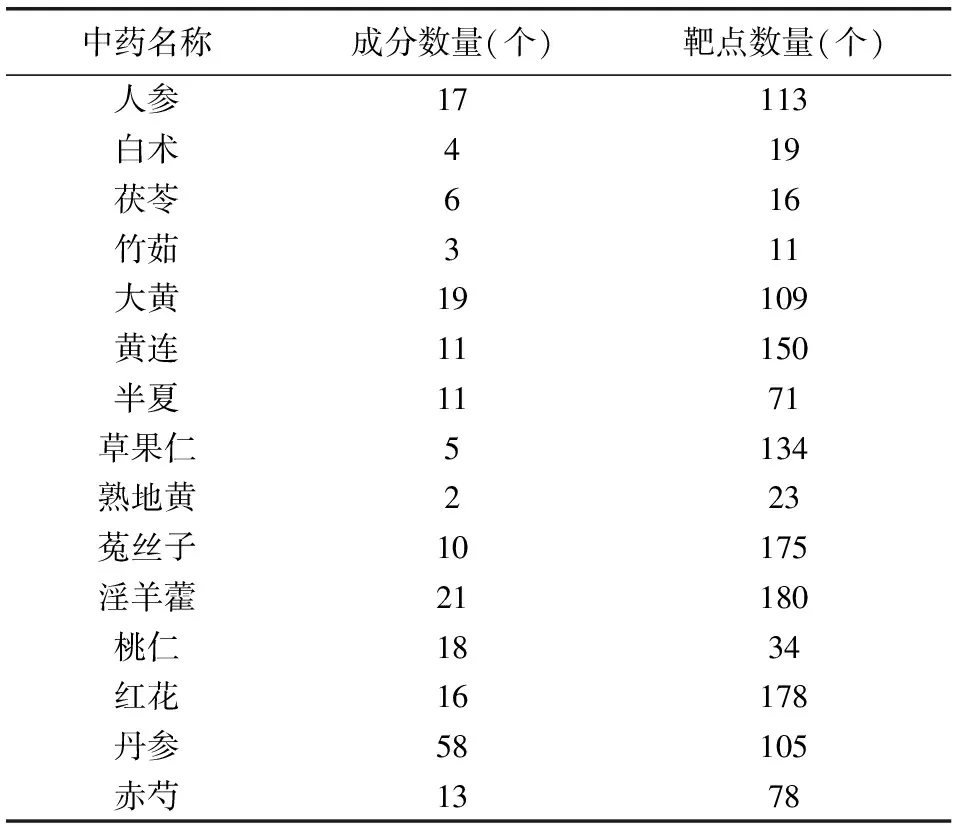
表1 参地补肾胶囊成分及靶点
2.2 疾病靶点和潜在靶点获取 在Gene Cards生物数据库,OMIN生物数据库,按疾病“Chronic renal failure”搜检索,去除重复项目后共获得关于RIF的靶点1 248个。将2.1中得到的286个药物活性成分作用的靶点与1 248个疾病靶点导入在Venny2.1在线做图工具平台上,两者取交集后获得共同靶点121个,即为参地补肾胶囊抗RIF的潜在作用靶点,并绘制韦恩图。见图1。
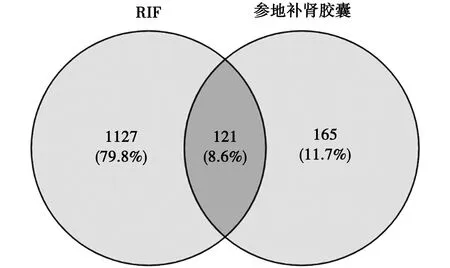
图1 疾病与药物靶点交集韦恩图
2.3 参地补肾胶囊治疗慢性肾衰竭潜在作用靶点的蛋白互作网络(PPI) 将“2.2”中得到的121个潜在作用靶点导入STRING数据库,物种选择为Homo sapiens,最低相互作用阈值设为最高等“Highest confidence(0.9)”,获得蛋白-蛋白相互作用关系,得到蛋白质相互作用网络图,剔除游离节点后获得114个节点,586条边。把获得的TSV数据导入到Cytoscape3.7.2软件进行分析,其中节点的大小、颜色的深浅变化代表度值(degree)的大小,边的粗细反映结合律评分(Combined Score)大小,并根据节点的度值筛选出核心靶点,见图2。其中Degree值≥20的有15个,从大到小分别是信号转导和转录激活因子3(Signal transducer and activator of transcription 3,STAT3)、细胞肿瘤抗原基因(TP53)、AP-1转录因子亚单位c-jun转录因子(JUN)、蛋白激酶B(protein kinase B,又名AKT,AKT1为AKT家族蛋白之一)、肿瘤坏死因子(tumor necrosis factor,TNF)、酪氨酸蛋白激酶(SRC)、丝裂原活化蛋白激酶-1(mitogen-activated protein kinase,MAPK1)、MAPK8、白介素6(interleukin6,IL-6)、MAPK14、RELA(核因子κB蛋白-p65)、血管内皮生长因子A(vascular endothelial growth factor A,VEGFA)、上皮生长因子受体(epidermal growth factor receptor,EGFR)、AP-1转录因子亚单位c-FOS转录因子(FOS)、雌激素受体1(Estrogen receptor 1,ESR1)。提示参地补肾胶囊治疗慢性肾衰竭的机制与上述核心靶点具有密切的联系,参地补肾胶囊很有可能通过作用于这些核心靶点而发挥其药理作用的。

图2 PPI网络图
2.4 构建参地补肾胶囊治疗慢性肾衰竭网络图(中药-潜在活性成分-潜在作用靶点-疾病网络图) 将参地补肾胶囊的163个活性化学成分与121个潜在作用靶点输入Cytoscape软件,筛除与靶点无交集的孤立成分,绘制网络图,见图3。使用Network Analyzer对网络进行分析显示,度值表示预测出该成分与作用靶点的关联个数,度值越大说明该成分越重要。图3中,左边圆形图标组成的外围环代表潜在作用靶点,环中八边形图标代表疾病;右边三角形图标组成的外围环代表中药活性成分,环中长方形图标代表中药名称。节点间的连线代表二者的对应关系,连线越多的成分或靶点,提示该成分或靶点在网络中发挥越关键的作用,该成分或靶点可能为参地补肾胶囊中抗RIF的关键成分或发挥作用的主要靶点。通过网络分析发现槲皮素、木犀草素、山奈酚、丹参酮IIA、β-谷甾醇、黄芩素、β-胡萝卜素、植物甾醇、芦荟大黄素、脱水淫羊藿素、隐丹参酮、鞣花酸、D-乳酸、异鼠李素、苦参碱、芝麻素、去甲脱水淫羊藿黄素等度值大于10,其与中药之间的关系见表2。
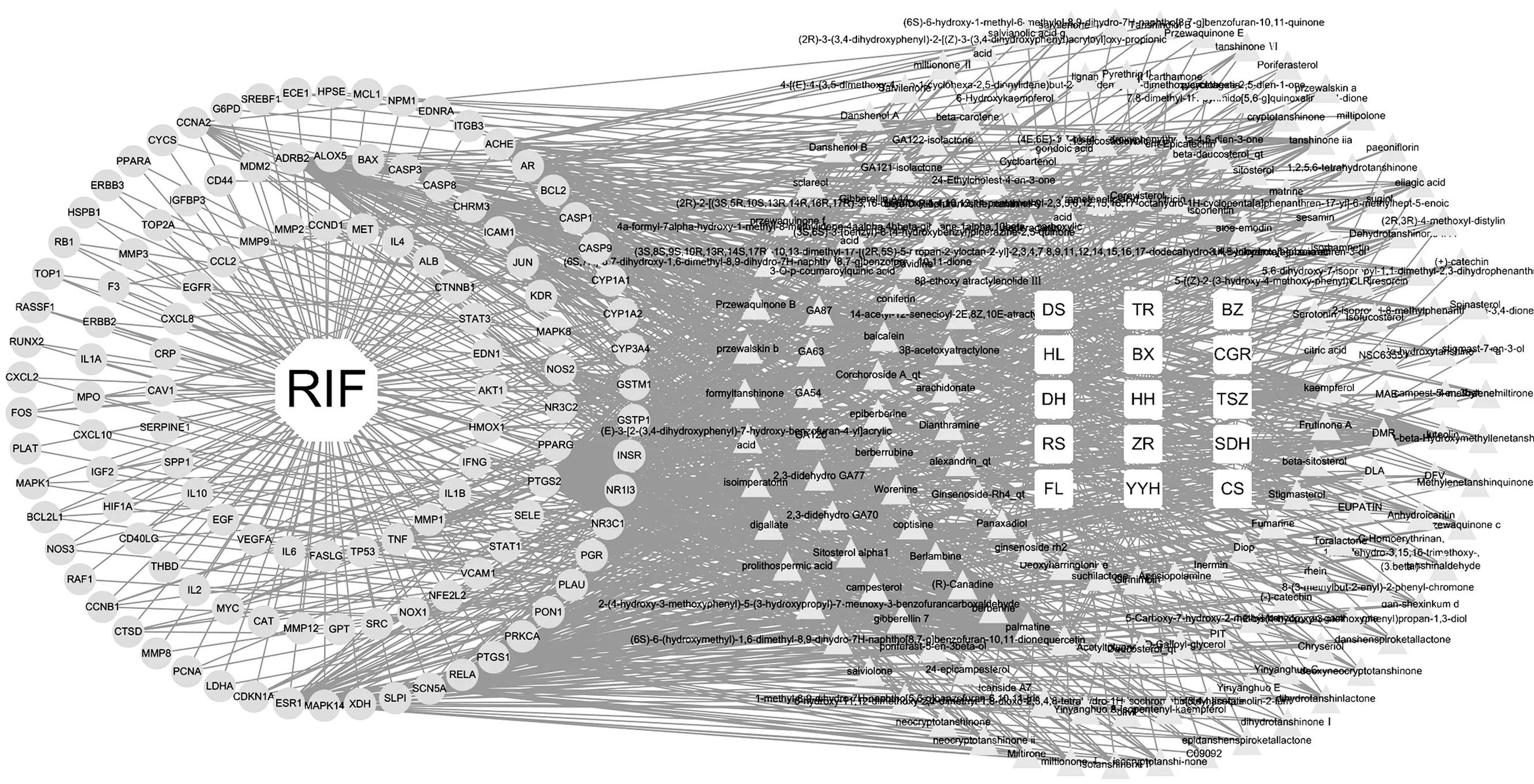
图3 药物-成分-靶点-疾病图
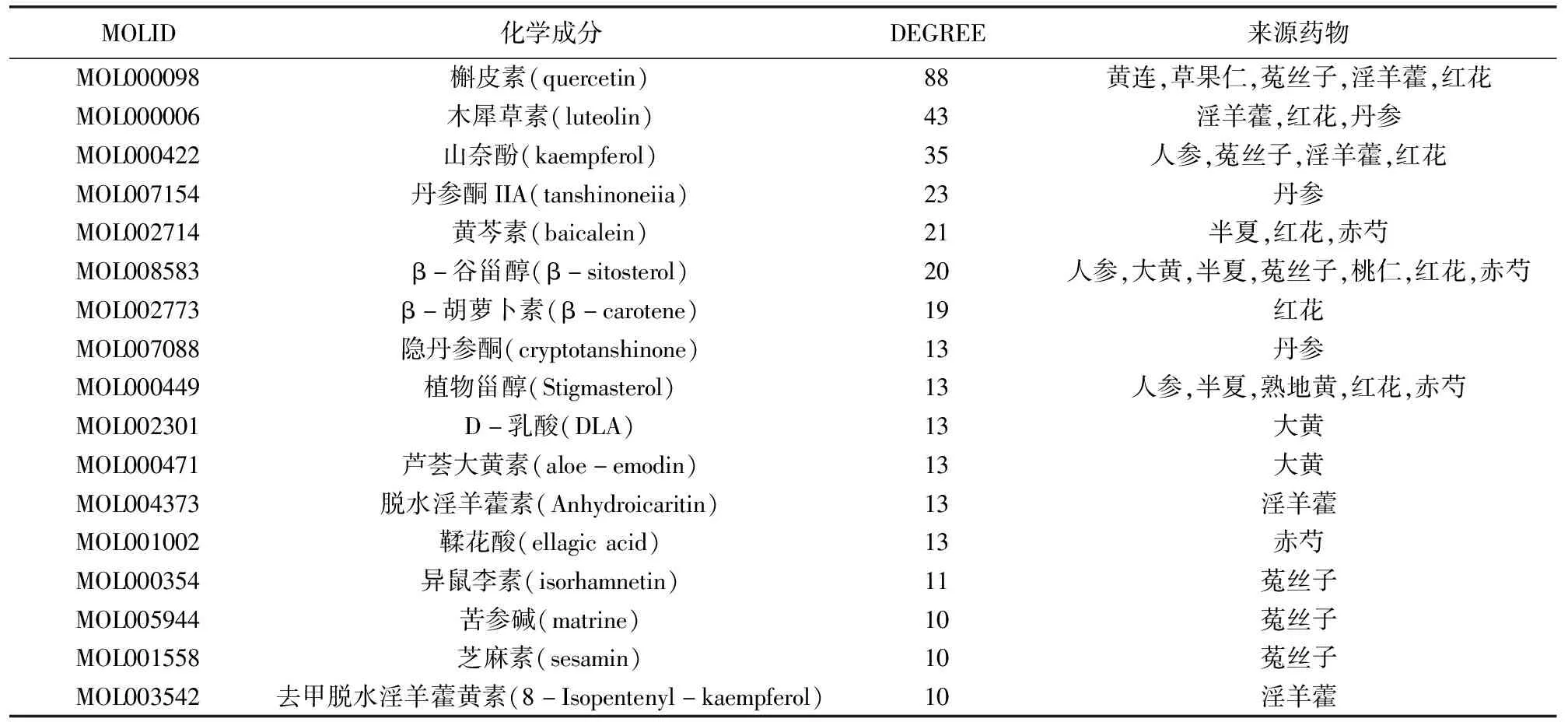
表2 主要成分-药物关系表
在网络中,如槲皮素来源于黄连、草果仁、菟丝子、淫羊藿、红花,可作用于ADRB2、AKT1、ALOX5、BAX、BCL2、BCL2L1、BIRC5、CASP3等靶点上。而人参、菟丝子、淫羊藿、红花中的活性成分木犀草素,半夏,红花,赤芍中的活性成分黄芩素亦可以作用于AKT1靶点上,上述一种成分与多个靶点作用,多种成分又可共同作用于同一个靶点的现象体现了参地补肾胶囊多成分、多靶点的综合调控特点。
2.5 基因本体(GO)与京都基因与基因组百科全书(KEGG)通路富集分析 应用Metascape数据平台对参地补肾胶囊抗RIF的相关靶点进行GO和KEGG富集分析,借助Origin Lab 2019对结果进行可视化,得到筛选靠前的20条通路;其中Y轴为通路名称,X轴分别代表富集在此通路的数量(Count)及富集显著性(q-Value)。BP分析结果显示,这些靶点主要涉及对脂多糖的反应,细胞因子介导的信号通路,对无机物的反应,凋亡信号通路,活性氧代谢过程等生物过程。见图4。
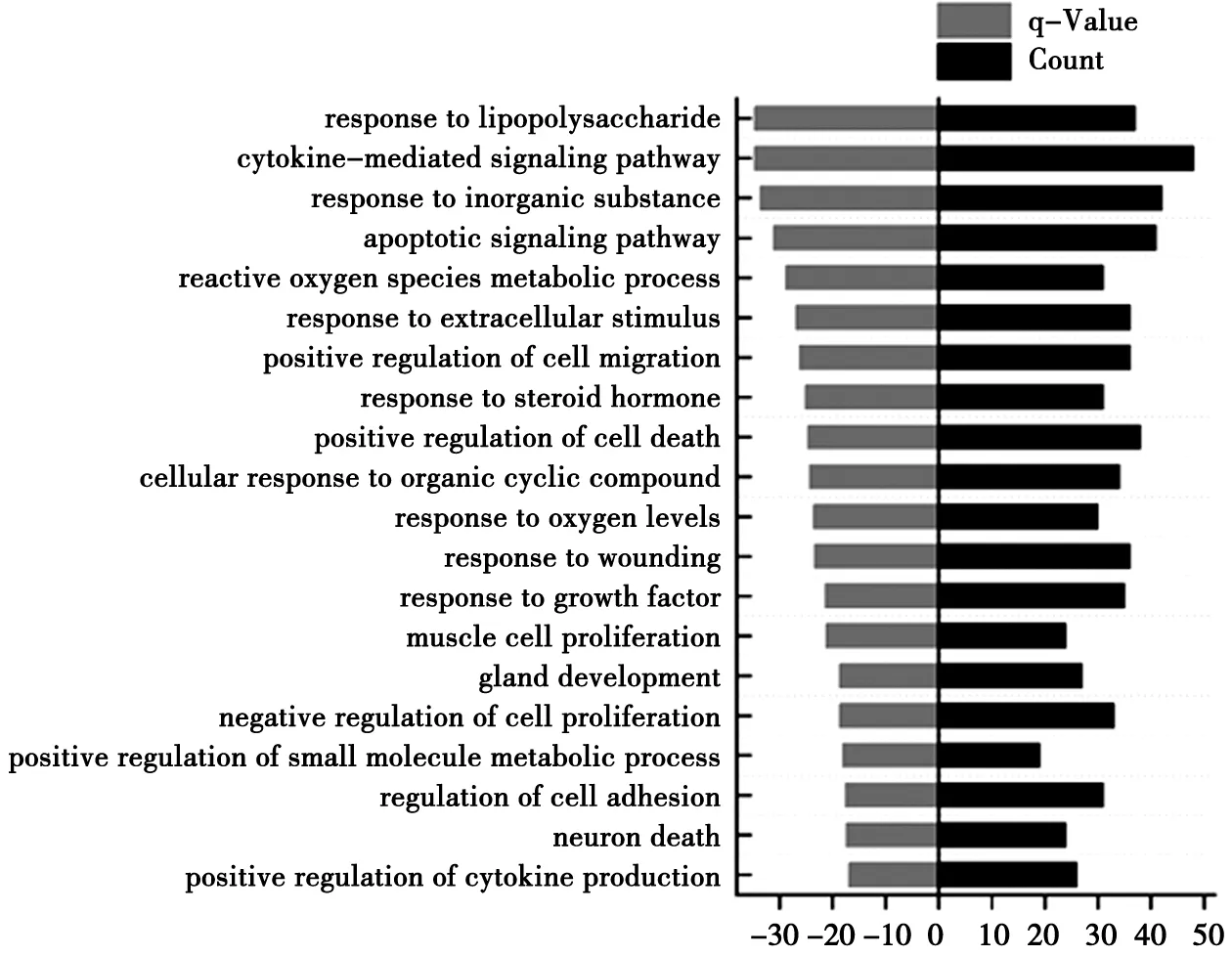
图4 BP分析结果
CC分析结果显示,可以看出这些靶点主要涉及细胞内的膜筏,膜微区,膜区,小窝,质膜筏等。见图5。
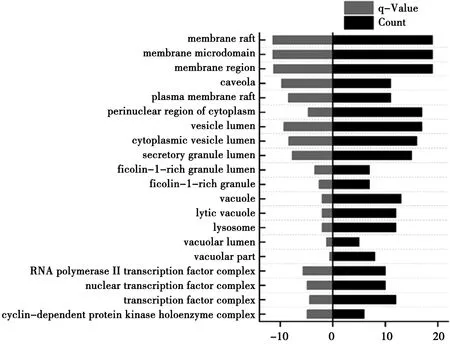
图5 CC分析结果
MF分析显示靶点主要涉及在激酶结合,细胞因子受体结合,蛋白质结构域特异性结合,转录因子结合,蛋白质均二聚活性等。见图6。
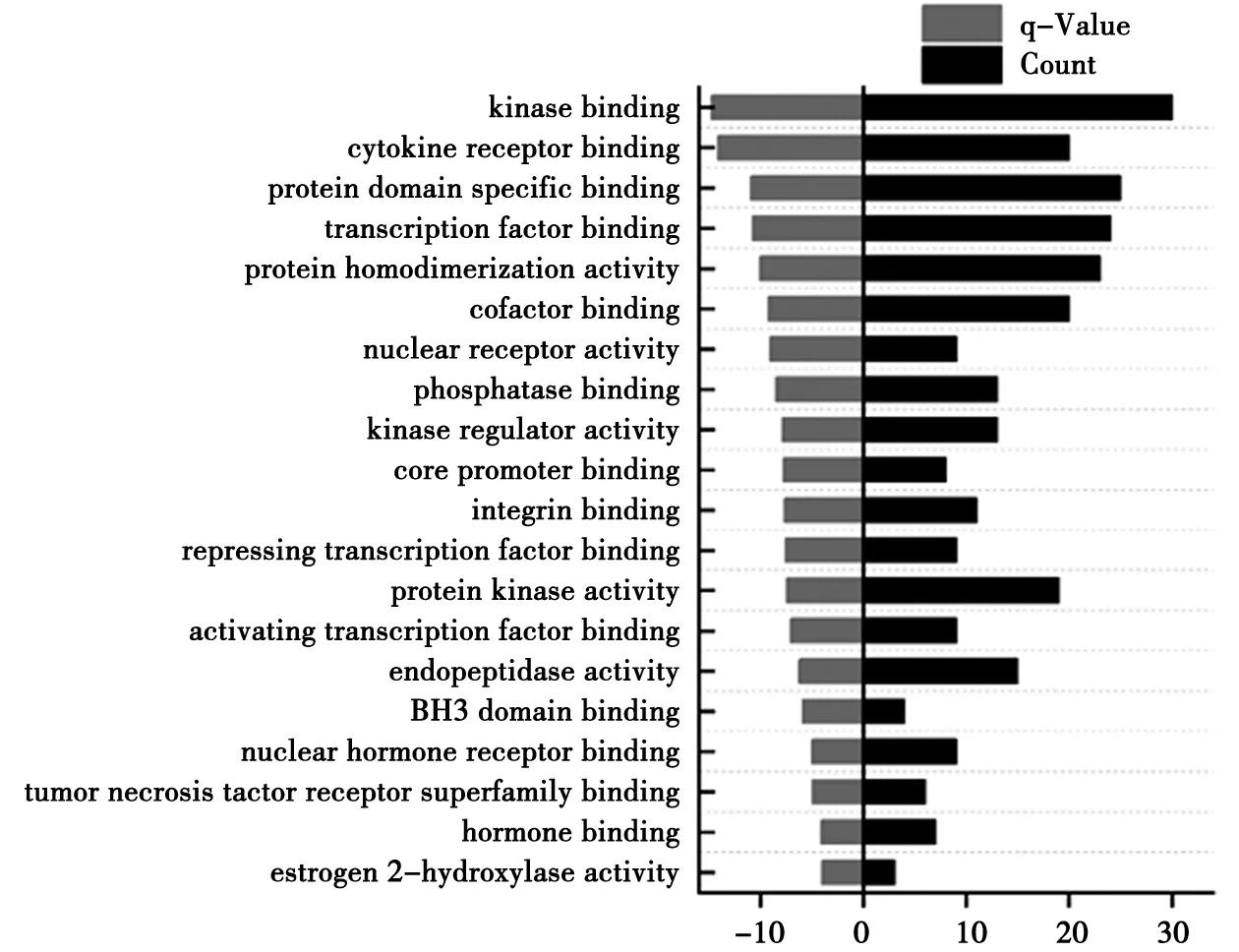
图6 MF分析结果
KEGG通路富集分析显示主要是是流体剪切应力与动脉粥样硬化,癌症的途径,乙型肝炎,HIF-1信号通路,TNF信号通路等。见图7。
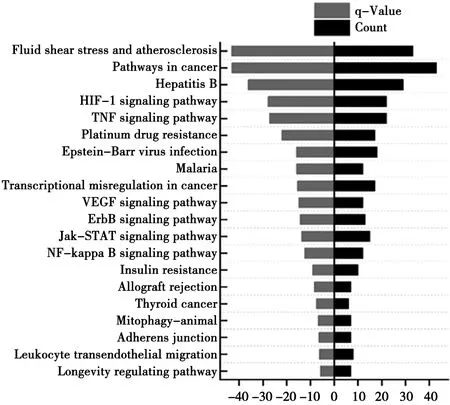
图7 KEGG分析结果
3 讨论
CRF是各种原因等导致的肾脏功能不可逆地丧失,临床出现以代谢产物潴留,水、电解质、酸碱平衡失调,全身各系统受累尤其是心脑血管为主的综合征。近些年糖尿病、高血压等基础疾病已成为导致CRF的主要原因[5]。目前研究表明,虽然RIF和肾小球硬化都可以导致慢性肾脏病(CKD)发展为CRF,但对于肾功能的减退程度而言,RIF扮演着更为重要的角色[6]。RIF机制与细胞外基质(ECM)沉积、细胞因子释放增加,炎性细胞浸润,上皮到间充质转化(EMT)和成纤维细胞活化等有关,最终导致纤维化的组织替代失去功能的肾单位[7]。
参地补肾胶囊是国医大师张琪教授根据多年治疗CRF的经验,铆定CRF脾肾两虚、湿浊内蕴的病机特点而拟定,广泛在临床上使用且疗效颇佳。参地补肾胶囊药物组成为人参、白术、茯苓、熟地黄、菟丝子、淫羊藿、大黄、黄连、半夏、草果仁、竹茹、桃仁、红花、丹参、赤芍。全方药味主要从补虚、泻实与活血方面着手。人参、白术、茯苓相伍为补气健脾;菟丝子补肾益精;淫羊藿与熟地黄二药合用则阴阳并补;大黄、黄连、草果仁、竹茹、半夏专为CRF主要的病理产物湿、瘀、毒而设;桃仁、红花、丹参和赤芍 4味药物活血化瘀,温凉相配,相须为用。纵观全方,攻补兼施,温凉并用,标本兼顾。多药协同起到补肾健脾、化湿浊、解毒活血之功用。
本研究通过网络药理学方法初步筛选参地补肾胶囊治疗抗RIF的活性成分。排名前5的是槲皮素、木犀草素、山奈酚、丹参酮IIA、黄芩素;此类化合物广泛存在于自然界,已有许多学者对其进行系统研究。研究表明槲皮素可通过降低TGF-β1水平抑制高糖诱导的肾小球系膜细胞增殖,并通过抑制Smad2磷酸化影响TGF-β1/Smads信号通路的激活,起到抗RIF的作用[8]。张翠等[9]研究表明木犀草素对肾脏保护的机制可能与其抗氧化作用及降低肾组织TGF-β1、PAI-1的蛋白表达有关。段斌等[10]研究发现山奈酚对高糖条件下人肾小球内皮细胞氧化应激及凋亡具有抑制作用。丹参酮IIA磺酸钠干预阿霉素肾病大鼠肾损伤的研究发现,丹参酮IIA磺酸钠能降低24h尿蛋白定量、改善病理组织损伤、可能与抑制肾组织TGF-β1、PAI-1的表达有关[11]。研究显示β-谷甾醇可通过抑制TNF-α、NF-κB和TβR1-Smad2/3等信号通路达到抗小鼠肝纤维化[12]。黄芩素可抑制糖尿病肾病患者外周血NF-κB活化及降低VEGF、TGF-β1水平,减少尿白蛋白排泄延缓糖尿病肾病进展,对早期糖尿病肾病进展延缓明显[13]。鞣花酸可通过抗氧化、减少炎症反应和抑制肾小管上皮细胞凋亡起到抗RIF的作用[14]。异鼠李素预处理对大鼠IR损伤导致的急性肾损伤(AKI)有保护作用,且呈剂量依赖性,其作用机制可能是抑制了NF-κB信号转导系统的过度活化及氧化应激[15]。
本研究分析获得参地补肾胶囊与RIF有关的靶点共有121个,对靶点构建PPI网络图分析发现度值≥20的有15个,分别为STAT3、TP53、JUN、AKT1、TNF、SRC、MAPK1、MAPK8、IL-6、MAPK14、RELA、VEGFA、EGFR、FOS、ESR1。STAT3是信号转导和转录激活因子(STAT)家族的成员,并在其中充当转录激活因子,该蛋白通过响应各种细胞因子和生长因子,包括IFN、EGFR、IL6等磷酸化而被激活,可刺激转化生长因子-β(TGF-β)和ECM的分泌,导致ECM在肾间质大量沉积促进RIF。JAK/STAT信号转导通路的激活可上调FOS、JUN的表达,形成的转录因子活化蛋白-1(AP-l)可引起TGF-β的表达增多,启动RIF的进程[16]。TP53、AKT1常见于肾肿瘤中异常表达。EGFR也称ErbB-1,是表皮生长因子受体HER家族成员之一,EGFR是上皮生长因子(EGF)细胞增殖和信号传导的受体。其突变或过表达一般会引发肿瘤。有研究显示其过度表达可能导致RIF[17]。肿瘤坏死因子(TNF)作为一种重要的细胞因子,可诱导NF-κB通路和MAPK通路引起基质金属蛋白酶(MMPs)表达异常,导致ECM降解紊乱引起RIF;其中RELA作为NF-κB的一种蛋白质亚基参与调节NF-κB的活性和功能[18]。SRC是酪氨酸蛋白激酶家族的重要成员,缺氧条件下其磷酸化后可调节多种与RIF相关的膜受体信号通路,如:TGF-β/Smad、STAT3等通路。
本研究发现参地补肾胶囊抗RIF涉及7条关键信号通路:流体剪切应力与动脉粥样硬化、HIF-1信号通路、TNF信号通路、VEGF信号通路血管内皮、ErbB信号通路、Jak-STAT信号通路、NF-κB信号通路。KEGG结果显示流体剪切应力和动脉粥样硬化通路为显著性最高的通路,已有研究证实该通路中相关的Toll样受体、NF-κB、MAPK信号通路等密切参与了RIF的过程[19];而心血管疾病(CVD)中尤其是那些涉及全身性炎症过程的疾病,例如动脉粥样硬化,是慢性肾脏病(CKD)患者发病和死亡的主要原因;心肌和血管的重塑会导致多种心血管并发症,例如心肌病,动脉粥样硬化进而导致缺血性心脏病,心力衰竭,脑血管和心血管死亡以及CRF的进展[20]。缺氧诱导因子-1(HIF-1)作为一种转录因子,可以通过与这些基因的启动子区域中的缺氧反应元件结合,直接调节纤维化因子的表达,激活基因转录,从而激活成纤维细胞和ECM沉积导致RIF[21];HIF-1除了直接激活纤维化因子的转录外,HIF还可以与多种促纤维化信号通路(包括TGF-β、Notch、NF-κB和PI3K/Akt通路)发生串扰,调控肾纤维化的过程[22]。而TGF-β信号转导途径是公认的RIF的一个重要途径,它通过刺激MMPs的产生,减少ECM降解的蛋白酶的产生和上调蛋白酶抑制剂的产生来诱导ECM[23-24]。HIF又是VEGF通路的主要调节因子,现在有许多证据表明,VEGFR-2是内皮细胞中VEGF驱动反应的主要介体,并且被认为是生理和病理性血管生成中的关键信号转导者;VEGF与VEGFR-2的结合可导致内皮细胞增殖基因上调。在肾脏中,VEGF-1主要在肾小球足细胞和肾小管上皮细胞中表达,其正常表达对于维持完整的肾小球和肾小管毛细血管内皮十分重要[25-26];研究表明VEGF-1的过表达导致肾小球增大和肾小球膜扩张,以及引起RIF[27]。TNF通路中TNF-α可诱导许多基因的激活,其中涉及NF-κB通路和MAPK通路。NF-κB信号通路是炎症相关的经典通路,而炎症反应被认为是肾纤维化发展的驱动力,因为它开始了纤维化阶段。研究表明尿蛋白可激活肾小管上皮细胞中NF-κB信号通路,引起炎症反应,引起肾单位损伤[28]。Fuihara CK等[29]在大鼠5/6肾消融模型中,使用PDTC进行治疗,可在不降低肾小球血压的情况下大大减轻肾脏损害和炎症,这表明观察到的直接决定因素是直接抑制或通过抗氧化活性抑制NF-κB系统。TNF通路还可调控MMPs从而干预ECM的生成过多和(或)降解受抑,而ECM是导致在肾间质的过度沉积是引起RIF的主要原因之一[30]。JAK/STAT通路是多种细胞因子和生长因子的主要信号传导机制。细胞因子与其同源受体结合后,STATs被酪氨酸激酶的JAK家族成员激活。一旦激活,它们就会二聚化并转运至细胞核,并调节靶基因的表达。Peter Y.Chuang等[31]研究证实血管紧张素II介导的肾小球系膜细胞中,JAK/STAT途径的激活可增强TGF-β,胶原IV和纤连蛋白的产生引起ECM过度沉积引起RIF。ErbB信号通路上的受体在被EGF,TGF-α等配体激活后,可通过许多途径发出信号,包括Akt和MAPK途径,导致细胞异常增殖,分化,凋亡参与RIF的进展。其中ErbB-1即EGFR,许多临床前研究表明EGFR可能是肾脏疾病的潜在治疗靶标,正常表达于肾小球和肾小管间质区。EGFR其信号通路的激活与几种细胞反应的调节有关,包括细胞增殖,炎症过程和细胞外基质调节,所有这些都参与肾脏损害的发生和发展。实验研究表明,阻断EGFR可能是通过调节炎症、细胞增殖达到抗RIF的作用。ErbB家族其他成员(ErbB2,ErbB3和ErbB4)又可与EGFR发生串扰,并将其信号广布[32-33]。可见ErbB信号通路在RIF的研究前景未来可期。
综上所述,本研究发现RIF涉及多条通路、多个靶点;而在这些通路中尤其需要关注HIF-1信号通路、TNF通路、JAK/STAT通路和ErbB信号通路,这几个通路中的蛋白和下游蛋白表达常常是其他通路参与RIF的启动因子或其他通路中的关键因子。参地补肾胶囊的多种成分协同作用于多条通路,多个靶点,综合调控干预可能是参地补肾胶囊抗RIF,治疗CRF的途径。
