超声引导导丝定位术对乳腺不可触及肿块的精准切除*
2021-04-28刘晶焰彭玉兰苟泽辉骆洪浩赵海娜张琼马步云卢强吕青阎锋于波洋田野陈爽凌文武
刘晶焰 彭玉兰 苟泽辉 骆洪浩 赵海娜 张琼 马步云 卢强 吕青 阎锋 于波洋 田野 陈爽 凌文武
(四川大学华西医院 1.超声医学科;2.乳腺外科;3.临床超声影像药物研究室,四川 成都 610041)
随着人们健康意识的提升和乳腺影像技术的发展,通过乳腺超声、乳腺X线、胸部计算机断层扫描(Computer Tomography, CT)和磁共振成像(Magnetic Resonance Imaging, MRI)检查发现的不可触及的乳腺肿块迅速增加[1-2]。对不可触及的乳腺肿块的微创精准切除已成为乳腺外科医师的难题[3]。导丝定位术是国际认可的术前定位乳腺不可触及肿块的有效方法[4],但我国尚未普及使用。我院2004年较早开展超声引导导丝定位术,迄今导丝定位已经超过1000例,该技术为外科开展不可触及乳腺肿块微创精准切除提供了支持,符合现代外科微创、精准、有效的理念,可最大程度兼顾肿块精准切除和女性对乳房美观的追求[5]。本研究总结我院全部的超声引导导丝定位术的乳腺患者此技术的操作流程、经验和教训,旨在通过学术交流,促进临床应用,形成同行可借鉴的操作流程,通过微创技术促进更多女性手术获益。
1 材料与方法
1.1 纳入与排除标准 纳入标准:选取我院2004年1月1日~2018年9月19日行超声引导导丝定位术的乳腺不可触及肿块的患者,收集患者的超声资料和相关临床资料。排除标准:①肿块位于乳腺假体(植入物)浅面。②超声图文数据不完整。③导丝定位术中囊液流出,导致肿块消失的单纯性囊肿(无需手术切除,及时与患者和外科医师沟通,获得患者理解)。
1.2 超声仪器 多款中高档彩色多普勒超声诊断仪器,包括Philips IU22,Philips 5000,SuperSonic和HI VISION Avius,乳腺超声导丝定位时使用超声仪器标准配置的高频线阵探头(浅表器官探头),中心频率≥7.5 MHz。
1.3 定位导丝 GHITAS®单倒钩乳腺定位针,目录号47720,规格尺寸和针长20 G*7 cm,由Bard Peripheral Vascular,Inc.(美国,亚利桑那州,坦佩)制造,见图1。该型号的导丝是单钩,定位针上有间距1 cm的深度标识,导丝前端距离倒钩1、2、3 cm处分别有3处可触及串珠(提供可视、可触摸、可快速找到病灶的参考点,辅助外科医师手术时判断肿块的深度),导丝体部有一处串珠,串珠到达针向辨识处可知导丝已在体内展开(辅助超声医师放置导丝时知道倒钩的深度信息)。

图1 GHITAS®单倒钩乳腺定位针
1.4 导丝定位术的临床路径 ①时间和地点:超声引导导丝定位术在超声医学科介入手术室进行,时间是外科手术的当日。如果是外科手术第一台,则在手术前一日完成。②医嘱:外科医师的医嘱需要注明手术日期和需要导丝定位的肿块部位及数量。患者由中央运输陪同前来超声医学科。③患者在导丝定位术前,在超声医学科签署书面的知情同意书,进行医患沟通。④超声医师实施超声引导导丝定位术。
1.5 超声引导导丝定位术的操作流程 ①导丝定位前,介入医师再次与患者核对和确认导丝定位的肿块部位和数量。②患者体位:仰卧位,双上肢外展,双手自然上举置于头部两侧,充分暴露定位侧的乳腺和腋窝。如果肿块位于乳房外侧,则侧卧位,充分暴露外侧肿块。在患者背部放置三角形垫枕,使患者更加舒适,也方便医师介入操作。③常规消毒和铺设无菌洞巾,探头使用无菌套保护,2%利多卡因局部麻醉。操作过程遵守无菌原则。④进针前进行超声检查,明确肿块位置、大小、回声类型、深度、血流,并采用十字交叉的体表定位法标记导丝定位的肿块,十字交叉点深面对应肿块所在位置(图2,适用于初学者)。⑤采用一步法操作,即导丝和定位针同步操作。进针前取出定位导丝,将倒钩放置到引导针鞘内,导丝尾端的可触摸串珠是标记,操作时可触摸串珠在引导针鞘的尾端外面提示导丝的倒钩正好到达针尖但不出针体。⑥导丝定位遵循垂直进针的最短路径的理念,采用非平面内进针法(短轴法)和平面内进针法(长轴法)[6]。非平面内进针,进针点在肿块的体表投影的十字交叉点(图3A),探头斜切扫查,只能看到针体的横断面(图3B),需要提插针鞘,观察和判断针尖位置。平面内进针法,操作时进针点在肿块边缘1~10 mm(图3C),进针过程全程可通过超声图像看到针尖和针体的实时进程(图3D)。实际操作过程,通常采取非平面内进针和平面内进针联合,即在肿块边缘1~10 mm的体表进针(非平面内进针),图像监控针尖到达肿块前缘的深度时偏转穿刺针,使穿刺针与体表皮肤有一定角度(图3C),此时采用平面内进针法观察针尖和针体的实时进程,穿刺深度是针尖到达肿块深面,对于10 mm内的小结节,针尖应穿出肿块深面2~5 mm,退出针鞘后倒勾正好从深面勾住肿块,否则导丝容易滑脱。肿块位置较深,容易伤及胸膜,可通过偏转穿刺针角度避免针尖穿刺损伤胸肌筋膜和胸大肌,否则会产生剧烈疼痛。确认导丝定位准确后,退出针鞘。退出针鞘的过程轻,一只手的拇指和食指捏住导丝,轻加推力,确保导丝不被针鞘带出。另一只手缓慢退出针鞘,退出针鞘后,超声图像再次确认定位准确。⑦导丝尾端的处理:采用我院独创的打圈方法,使裸露在体表外的导丝尾端形成环状(简称尾圈)(图4),将尾圈夹在无菌纱布的两层之间,使用医用胶布固定于体表,患者的日常生活基本不受影响。

图2 乳腺肿块的体表标记

图3 乳腺肿块行超声引导导丝定位术的进针方法及超声图像

图4 导丝尾圈法用于定位导丝尾端
1.6 辅助外科精准切除肿块 在随后的手术切除过程中,外科医生可沿着导丝,通过导丝前端的三处可触摸串珠了解肿块的深度和位置,从而实现精准切除。手术中,外科医师确认手术切除标本已经有肿块。
1.7 随访病理诊断结果和患者术后复查的影像资料 随访切除肿块的全部病理结果并录入超声工作站,我院乳腺病理的诊断采用世界卫生组织(WHO)乳腺肿瘤分类标准[7],术后3~6个月常规乳腺超声检查进行随访。
1.8 统计学分析 数据采用SPSS 18.0软件进行统计分析,采用t检验比较良性和恶性组的肿块大小。采用卡方检验比较肿块位置的差异性。P<0.05为差异有统计学意义。
2 结果
2.1 患者一般资料 纳入患者全部为女性,年龄16~77岁,中位年龄为45岁。
2.2 超声引导导丝定位术数量 共实施超声引导导丝定位术985例,共1166个乳腺不可触及肿块,每年度实施数见图5。实施超声引导导丝定位术的超声医师共计11位,介入超声医师的介入工作年限1~20年。
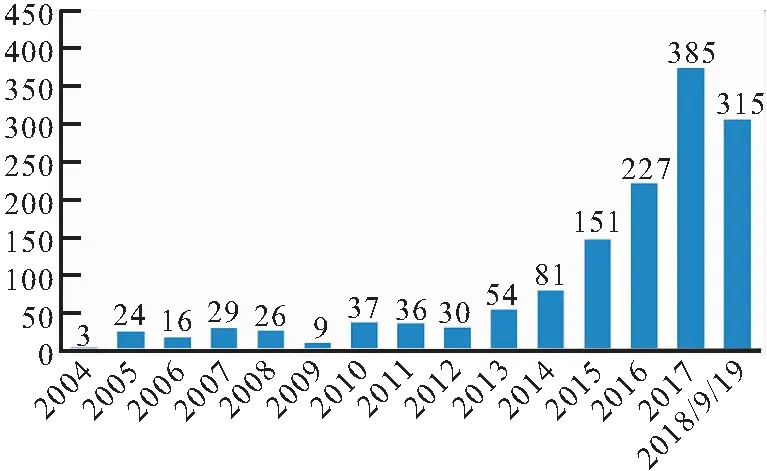
图5 2004年1月1日~2018年9月19日在我院实施的超声引导导丝定位术数量
2.3 不可触及的乳腺肿块的大小 根据超声报告记录的肿块大小,以最大径进行统计分析,肿块中位大小为10(2,41)mm。不可触及的乳腺肿块的大小,见表1。恶性肿块的中位值为10(4,36)mm,良性肿块的中位值为9(2,41)mm,良性和恶性肿块的大小有统计学差异(P=0.019)。

表1 不可触及的乳腺肿块的大小
2.4 不可触及的乳腺肿块的位置 1166个乳腺肿块的位置分布见表2。肿块数量在不同象限的分布有统计学差异(P<0.05)。在不同象限中,良性和恶性肿块的数量无统计学差异(2=2.586,P=0.736)。
2.5 不可触及的乳腺肿块的病理类型及病理结果 恶性肿块102个(8.75%),良性肿块1064个(91.25%)。在良性肿块内,非典型导管增生、非典型小叶增生、导管内乳头状瘤和非典型增生伴其它良性共计170个(170/1064,15.98%)。胸壁肌肉内肿块病理结果为1例淋巴结反应性增生,1例为炎细胞。在恶性肿块中,33个导管原位癌,2个小叶原位癌;66个浸润性癌,见表3。

表2 不可触及的乳腺肿块的位置

表3 不可触及的乳腺肿块的病理类型
2.6 不可触及的乳腺肿块的随访结果 在102例乳腺癌患者中,全部为单发肿块,保乳手术48例(47.06%),单纯乳房切除术28例(27.45%),改良根治性乳房切除术26例(25.49%)。术后乳腺超声随访,肿块完全切除率为100%,无1例出现血肿、感染、导丝迁移、气胸等明显的并发症,超声引导导丝定位术的初期有1例在穿刺过程突发局部疼痛,于当日手术取出导丝后疼痛缓解。
3 讨论
对于不可触及的乳腺肿块手术切除,传统方法是根据影像学报告的定位描述进行手术切除[8]。针对外科医师精准切除不可触及肿块的难题,逐渐发展出各种术前定位方法[9-11]、术中定位辅助切除[12]和影像引导下乳腺微创旋切[13]等。基于术前准确定位开展的乳腺微创切除可降低患者二次手术的风险[14-17]。在没有开展导丝定位术之前,针对不可触及的乳腺肿块,通常在术前超声检查时进行体表标记定位,或超声引导下染料法(亚甲蓝)定位。但体表定位法不够精准,通常需要切除相对多的乳腺组织以保证肿块被切除;染料示踪法(亚甲蓝)[18]需要术前30 min内进行,而且需要专业的介入超声医师实施。染料法容易导致染料扩散污染手术区域影响肿块判断,扩大的染色范围可能扩大切除的影响并延长手术时间,进一步增加出血和感染的风险[6]。Shin等[19]认为,导丝定位术通过增加手术成功率和减少需要再次手术的阳性切缘率以改善手术效果。同时,文献报道了导丝定位术的缺点,包括导丝的迁移或移位,工作时间表的灵活性受到限制以及手术室效率的降低等[19-21]。我院超声引导导丝定位术开展后,对不可触及的乳腺肿块的外科切除提供非常大的帮助,但限于介入医师的短缺和超声医学科常规医疗任务繁重,难以保证临床需求,故较长时期此项技术进展缓慢。随着介入超声医师的增多和介入超声成为每日常规医疗后,超声引导导丝定位术的开展才逐渐能够满足临床需求。目前,超声引导导丝定位术已经成为不可触及乳腺肿块外科切除术前不可或缺的医疗需求。由于介入超声的推动,相信更多的医院有针对不可触及肿块的切除难题,故特推荐乳腺外科医师越来越接受的导丝定位技术。
本研究切除肿块中最大径小于20 mm的乳腺肿块占比95.37%(1112/1166)。有2例肿块较大,其中1例病理诊断是囊性乳腺增生,术前最大径41 mm,术前不可触及,另1例病理诊断是导管原位癌,最大径36 mm,因为临床医师触诊不满意,要求对肿瘤进行定位。乳腺肿块以外上象限中更为常见(45.89%),肿块在不同象限的分布有统计学差异(P<0.05),但在不同象限中,良性和恶性肿块的分布没有统计学差异(P>0.05)。本组良性肿块1064个(91.25%),恶性肿块102个(8.75%),保乳手术48例(47.06%),保乳手术率高于我院乳腺癌的平均保乳手术率(约23%)。本研究结果表明,超声引导导丝定位术可促进乳腺癌早期发现,提高保乳手术率,使患者获益[22-23]。
本研究1166个乳腺不可触及肿块通过超声引导导丝定位术成功进行手术切除,漏切除率为0。临床实践证明超声引导导丝定位术可精准切除不可触及肿块,缩短了手术时间,并减少术后感染、出血和其他并发症,与研究文献相符[24-26]。临床反馈不良事件有6例(0.4%),4例导丝位置太浅,2例胸壁肿块,定位后疼痛明显。定位不当发生率低于Alamdaran等[27]6.4%和Franco等[28]6.0%的报告。核实4个导丝位置太浅的患者,肿块大小在5~10 mm,定位导丝都准确无误地进入肿块,倒钩的尖端都位于肿块内,并达到肿块的深面,病理结果均为腺病。有研究表明,当目标肿块位于近胸大肌处时,在女性致密腺体组织中进行乳腺X线引导的导丝定位术具有挑战性,对于较深的目标肿块,超声引导导丝定位比X线引导导丝定位更实用[29]。我院超声介入组达成一致的改进意见,对小于10 mm的小肿块,定位导丝放置的深度以超过肿块后缘2~5 mm,倒钩从肿块深面钩住肿块,减少脱钩的几率。如果乳腺肿块深面临近胸壁肌层,则导丝进入肿块后将引导针尾端向胸壁方向倾斜,定位导丝的倒钩到达肿块的侧后方,既满足深度的需求,又减小对胸壁的损伤,增加安全性。胸壁疼痛的患者,考虑是胸壁肿块,损伤胸壁神经所致,手术切除肿块后疼痛即刻缓解。对于微小钙化灶的定位常用乳腺X线引导导丝定位[30],但也有研究表明,超声引导导丝也可以精确定位微钙化[31]。针对乳腺不可触及肿块的术前定位,目前还有放射性粒子定位[32],SAVI SCOUT定位[33],射频识别定位[34]、磁性粒子定位[35]等多种新技术报道,期待未来能够发展出更经济实用的定位技术。
4 结论
超声引导下导丝定位符合微创外科的临床需求,满足现代女性的治疗和对乳腺形状的美观需求,可在临床推广应用。
