负载β-环糊精的矿物和生物炭对甲基橙的吸附性能
2021-04-25郭吉丽郑盛阳黄满红
郭吉丽,郑盛阳,2,黄满红
(1. 东华大学 环境科学与工程学院,上海 201620;2. 扬州大学 环境科学与工程学院,江苏 扬州 225008)
吸附法作为废水处理中最常用的方法之一,具有成本低廉、操作简单等优点[2]。沸石和蛭石是良好的吸附材料[3]。沸石具有特殊的层状网络结构,孔隙率高,比表面积大[4]。蛭石的层间有一个实质性的内表面,可容纳大量的阳离子。此外,同晶替代产生的负电荷也能增强吸附阳离子的能力[5]。生物炭具有多孔性的表面且表面基团含量较高[6],具有很强的吸附性能和再生性能。β-环糊精(β-CD)是一类由亲水的外部和疏水的内腔组成的绿色、可生物降解的环状低聚糖大分子[7-8],可用于对废水中有机污染物的富集和定量分析[9],但β-CD吸附污染物后不易从废水中分离出来。将β-CD负载到非水溶性材料上作为吸附剂,既可以有效吸附废水中污染物,还利于吸附剂的回收再利用。
本研究将β-CD负载到矿物(沸石和蛭石)和生物炭(棕榈生物炭和秸秆生物炭)上制备了新型吸附材料,表征了其结构特征,考察了新型吸附材料对水体中甲基橙的吸附性能。
1 实验部分
1.1 材料、试剂和仪器
沸石(F0)和蛭石(ZH0)(均为60目)分别购自康泰矿产品加工厂和天江矿业有限公司;棕榈生物炭(Z0)和秸秆生物炭(J0)均购自永邦科技股份有限公司;其他试剂均为分析纯。
Hitachi S-4800型场发射扫描电子显微镜:日本日立公司;Nicolet 6700型红外光谱仪:美国Varian公司;Vario EL cube型元素分析仪:德国Elementar公司;Pyris 1型热重分析仪:美国PerkinElmer公司。
1.2 新型吸附材料的制备
分别将15.00 g F0、ZH0、Z0和J0加入到1 mol/L的HCl溶液(150 mL)中,浸泡12 h后弃去上清液,用去离子水洗涤至中性,置于110 ℃烘箱中烘干至恒重。活化后的沸石、蛭石、棕榈生物炭和秸秆生物炭分别记作F1、ZH1、Z1和J1。
称取10.00 g β-CD和作为交联剂的环氧氯丙烷(EPI)(摩尔比为4∶1),加入到0.875 mol/L的NaOH溶液(100 mL)中,在室温下以120 r/min的转速搅拌6 h,配制成修饰溶液。
分别称取3.00 g F1、ZH1、Z1和J1,各加入100 mL修饰溶液,室温下搅拌5 h(120 r/min)后用去离子水洗涤,抽滤至滤液呈中性。在75 ℃烘箱中烘干至恒重,得到负载了β-CD的沸石、蛭石、棕榈生物炭和秸秆生物炭,分别记作F2、ZH2、Z2和J2。
1.3 阳离子交换容量(CEC)的测定
采用改良的乙酸铵替换法测定CEC。依次使用20 mL去离子水、乙酸钠溶液(pH=7,1 mol/L)、乙醇(质量分数95%)和乙酸铵溶液(pH=7,1 mol/L)冲洗0.500 g样品,收集滤液,使用6400A型火焰光度计(上海精其仪器有限公司)测定其Na+浓度。
1.4 吸附实验
分别将1.000 gβ-CD负载前后的吸附材料加入到50 mL不同质量浓度(20,50,100,200,500 mg/L)的甲基橙溶液中,置于恒温水浴振荡器中,在25 ℃、120 Hz下振荡120 min后,用混合滤膜过滤。测定溶液中的甲基橙质量浓度。再在甲基橙溶液质量浓度为200 mg/L时,分别以10,30,60,120,180 min的振荡吸附时间进行上述实验。
1.5 数据处理
采用式(1)计算溶液中甲基橙的平衡吸附量(qe,mg/g):

式中:ρ0为甲基橙的初始质量浓度,mg/L;ρe为吸附平衡时的甲基橙质量浓度,mg/L;m为吸附剂加入量,g;V为甲基橙溶液的体积,L。
采用准一阶动力学方程(式(2))和准二阶动力学方程(式(3))研究其吸附动力学[10]。

式中:qt为t时刻的甲基橙吸附量,mg/g;k1为准一级速率常数,min-1;k2为准二级速率常数,g/(mg·min)。
采用Langmuir模型(式(4))和Freundlich模型(式(5))研究其吸附等温线[11]。

式中:qmax为最大吸附量,mg/g;KL为Langmuir常数,L/mg;n(无量纲)和KF(mg/g)为Freundlich吸附常数。
1.6 分析表征
采用75系列紫外-可见分光光度计(上海光谱仪器有限公司)测定溶液中的甲基橙质量浓度;分别采用FTIR、SEM、TG等技术表征吸附材料的微观结构。
2 结果与讨论
2.1 吸附材料的表征结果
2.1.1 FTIR
负载β-CD前后4种材料的FTIR谱图见图1。由图1a可见,相对于F0,F2在3 650 cm-1处出现了新的伸缩振动峰[12],在2 926 cm-1处和1 450 cm-1处出现了β-CD分子所具有的2个分别代表—CH2—和—OH的新峰[13]。由图1b可见,相比于J0,J2在2 900 cm-1处和1 167 cm-1处出现了分别代表—CH2—和C—O—C的新峰,且在3 377 cm-1处和1 610 cm-1处的—OH和酯羰基伸缩振动峰明显增强,在1 010 cm-1处的Si—O伸缩振动峰有一定幅度的偏移。由图1c可见,相比于ZH0,ZH2在2 900 cm-1处和1 420 cm-1处也出现了代表—CH2—和—OH的新峰,且在1 630 cm-1处和1 020 cm-1处的酯羰基和Si—O伸缩振动峰明显增强。由图1d可见,相比于Z0,Z2在1 400 cm-1处出现了—OH的新峰,且在3 377 cm-1处和1 042 cm-1处的2个—OH伸缩振荡峰明显增强。可见,β-CD成功负载到了沸石、蛭石、秸秆生物炭和棕榈生物炭的表面。
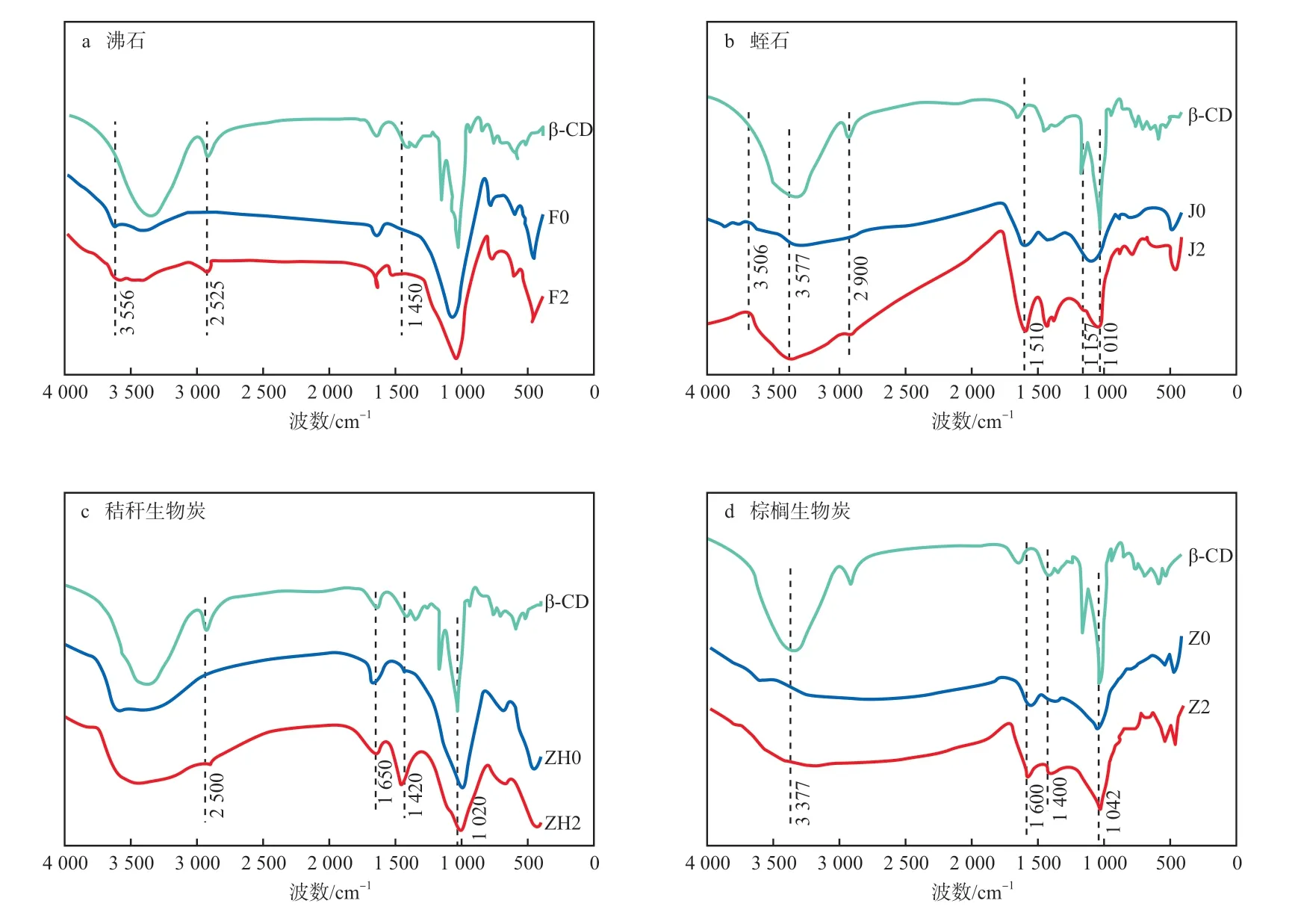
图1 负载β-CD前后4种材料的FTIR谱图
2.1.2 元素分析
负载β-CD前后4种材料表面的元素含量见表1。由表1可见,F2、ZH2、J2和Z2的C原子含量分别比F0、ZH0、J0和Z0提高了1.38百分点、2.19百分点、0.36百分点和3.60百分点;H原子含量分别提高了0.14百分点、0.47百分点、0.90百分点和0.34百分点。β-CD主要成分为C和H,元素分析结果进一步证实β-CD已成功负载到沸石、蛭石、秸秆生物炭和棕榈生物炭上。
2.1.3 SEM
负载β-CD前后4种材料的SEM照片见图2。由图2可见:F0和ZH0表面较光滑,且杂质较少;而F2和ZH2表面十分粗糙且覆盖了许多白色颗粒物。由此推测,β-CD成功地接枝到了沸石和蛭石表面。
从图2还可见,J0和Z0具有许多细小的孔隙,表面较平整;而J2和Z2的孔隙变大,表面粗糙且孔隙中被白色颗粒物填充。由此推测,β-CD成功地接枝到了秸秆生物炭和棕榈生物炭表面。

表1 负载β-CD前后4种材料表面的元素含量 w,%

图2 负载β-CD前后4种材料的SEM照片
2.1.4 TG
F0、ZH0、F2和ZH2的TG曲线见图3。由图3a可见:F0在0~100 ℃失重1.9%,这主要是矿物表面吸附水的脱失[14];100~400 ℃矿物的层间水脱失和200~600 ℃有机物的分解共失重4.3%;F2在0~100 ℃和100~600 ℃分别失重5.3%和8.8%。由此得到,在100~600 ℃,F2比F0多失重了4.5%,这归因于所吸附的有机物。由图3b可见:ZH0在0~100 ℃、100~600 ℃和600~800 ℃之间分别失重5.5%、5.5%和0.6%;ZH2在0~100 ℃、100~600 ℃和600~800 ℃之间分别失重5.5%、8.3%和0.3%,ZH2总失重比ZH0多2.8%。

图3 F0、F2、ZH0和ZH2的TG曲线
TG结果表明,负载到F0和ZH0上的β-CD和EPI的量分别为矿物本身质量的4.5%和2.8%。这一方面证实了β-CD附着在矿物表面以及单位质量沸石所负载的β-CD量要高于蛭石。因为沸石表面具有许多孔洞,可允许一定大小的分子进入内部[5];而蛭石属于层状结构,有机分子难以进入内部晶层,只能负载于外表面,所以负载到蛭石上的β-CD相对较少。
由于棕榈生物炭和秸秆生物炭自身含有较复杂的有机物[15],难以根据TG损失的有机物质量估算出负载β-CD的量。
2.2 甲基橙初始质量浓度对平衡吸附量的影响
在溶液pH为6.8、吸附时间为120 min、溶液温度为25℃的条件下,甲基橙初始质量浓度对4种材料平衡吸附量的影响见图4。由图4可见:各种吸附剂的平衡吸附量均随溶液中甲基橙初始质量浓度的增加而升高,负载β-CD后材料的平衡吸附量增加尤其显著;F2、ZH2和J2均在甲基橙初始质量浓度为300 mg/L时达到平衡吸附量;Z2在甲基橙初始质量浓度为200 mg/L时基本达到平衡吸附量。综合考虑,本实验选择甲基橙初始质量浓度为200 mg/L。

图4 甲基橙初始质量浓度对4种材料平衡吸附量的影响
CEC反映了材料表面基团交换可电离质子/阳离子的能力。CEC越高,材料对溶液中质子/阳离子的吸收能力越强。负载β-CD前后4种材料的CEC见表2。由表2可见,负载β-CD后4种材料的CEC均明显提高,说明F2、ZH2、J2和Z2对甲基橙吸附量的提升是因为β-CD改变了材料表面的基团,赋予了材料更好的交换可电离质子/阳离子的能力。
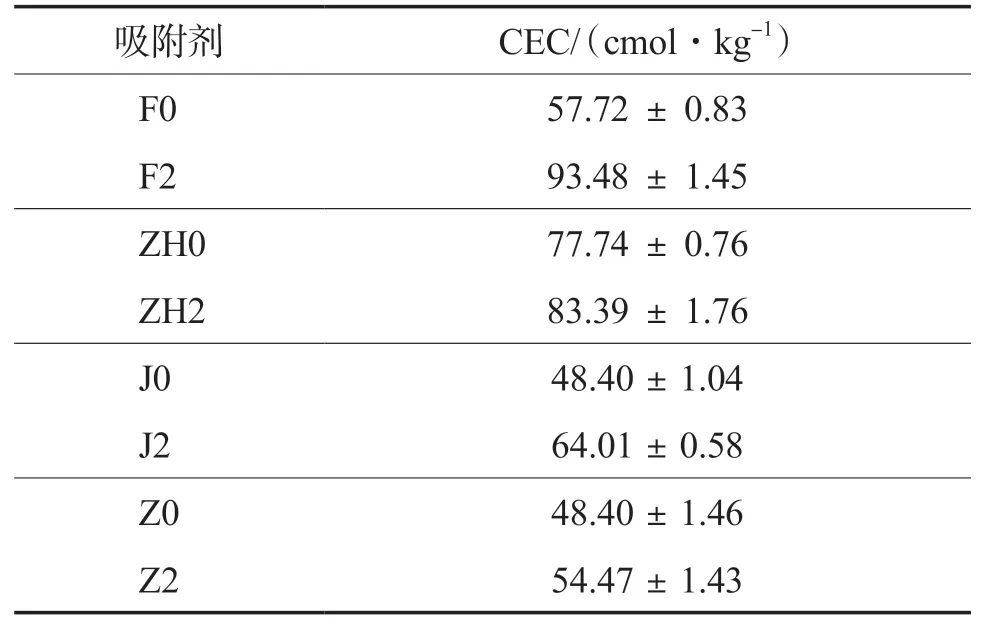
表2 负载β-CD前后4种材料的CEC
2.3 吸附时间对甲基橙吸附量的影响
在溶液pH为6.8、溶液温度为25℃、甲基橙初始质量浓度为200 mg/L的条件下,吸附时间对负载β-CD后4种材料的甲基橙吸附量的影响见图5。
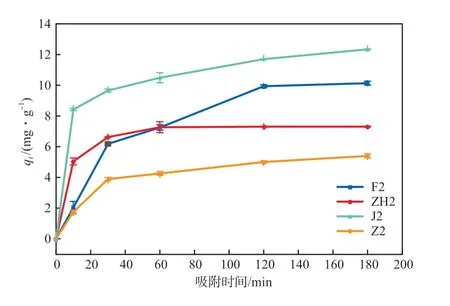
图5 吸附时间对甲基橙吸附量的影响
由图5可见:F2在吸附时间为0~120 min时吸附量增加显著,在吸附时间为120 min时趋于吸附平衡,平衡吸附量为9.94 mg/g;ZH2在吸附时间为0~30 min时吸附量增加显著,在吸附时间为60 min时趋于吸附平衡,平衡吸附量为7.27 mg/g;J2在吸附时间为0~10 min时吸附量增加显著,在吸附时间为10~180 min时吸附量缓慢增加,在吸附时间为180 min时趋于吸附平衡,平衡吸附量为12.35 mg/g;Z2在吸附时间为0~30 min时吸附量增加显著,在吸附时间为180 min时趋于吸附平衡,平衡吸附量为5.40 mg/g。4种材料的平衡吸附量大小顺序为:J2> F2> ZH2> Z2。综合考虑,本实验选择吸附时间为180 min。
2.4 溶液pH对甲基橙平衡吸附量的影响
在溶液温度为25℃、吸附时间为180 min、甲基橙溶液初始质量浓度为200 mg/L的条件下,溶液pH对负载β-CD后4种材料的甲基橙平衡吸附量的影响见图6。由图6可见,随着溶液pH的升高,4种材料的甲基橙平衡吸附量均呈上升趋势。因为F2、ZH2、J2和Z2在酸性条件下表面均带正电荷,而甲基橙是一种带正电荷的阳性染料,因静电排斥作用导致对甲基橙的吸附量较低。在碱性条件下吸附效果更佳,综合考虑,本实验选择溶液pH为9。
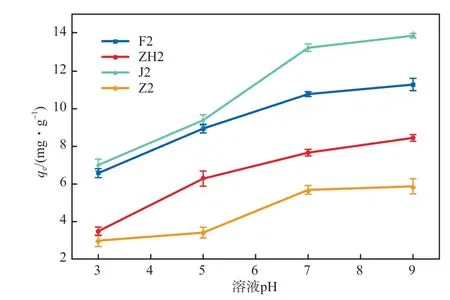
图6 溶液pH对甲基橙平衡吸附量的影响
2.5 溶液温度对甲基橙平衡吸附量的影响
在甲基橙溶液初始质量浓度为200 mg/L、溶液pH为9、吸附时间为180 min的条件下,溶液温度对甲基橙平衡吸附量的影响见图7。由图7可见,溶液温度为45 ℃时F2、ZH2、J2和Z2的甲基橙平衡吸附量均高于溶液温度为25 ℃,说明提高溶液温度有利于对甲基橙的吸附。

图7 溶液温度对甲基橙平衡吸附量的影响
2.6 吸附动力学和等温吸附模型
负载β-CD后4种材料吸附甲基橙的动力学模型和等温吸附模型的相关系数见表3。由表3可见,用准一级动力学模型拟合负载β-CD后4种材料对甲基橙的吸附行为,相关系数均大于0.962;准二级动力学模型的拟合效果较差。可见负载β-CD后4种材料吸附甲基橙过程中物理吸附对吸附速率起着主导作用。4种材料的Langmuir模型相关系数均大于Freundlich模型,说明负载β-CD后4种材料对甲基橙的吸附更符合Langmuir型吸附等温线模型,趋向于单分子层吸附。
2.7 吸附材料的重复使用性能
将吸附饱和的吸附材料分别用盐酸溶液(0.1mol)和去离子水洗涤3次,然后于65 ℃真空干燥箱中干燥24 h后进行重复使用。吸附材料重复使用3次的吸附量变化见图8。由图8可见,4种材料重复使用3次后的吸附量均为原始吸附量的70%以上,说明它们具有良好的重复使用性能。
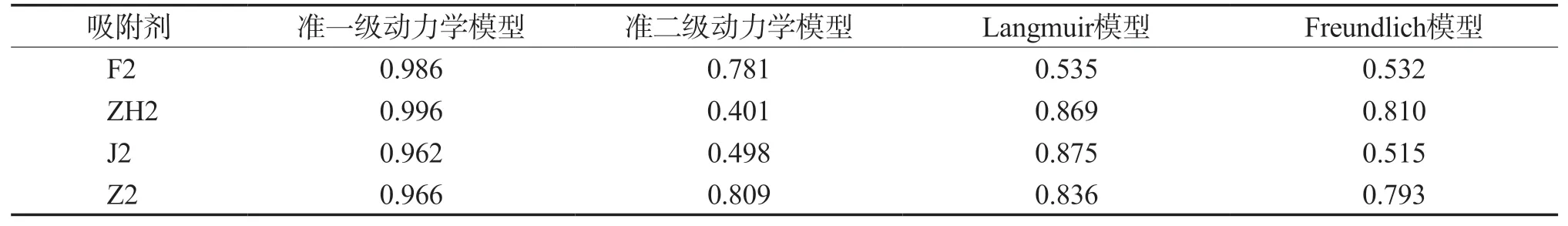
表3 负载β-CD后4种材料吸附甲基橙的动力学模型和等温吸附模型的相关系数

图8 吸附材料重复使用3次的吸附量变化
3 结论
a)采用HCl溶液对沸石、蛭石、秸秆生物炭和棕榈生物炭进行活化预处理,以EPI为交联剂,将β-CD负载到原始材料上,制备了4种新型吸附材料F2、ZH2、J2和Z2。FTIR、元素分析、SEM和TG表征结果显示,β-CD被成功地负载到沸石、蛭石、秸秆生物炭和棕榈生物炭上。
b)负载β-CD后的4种材料对甲基橙的平衡吸附量大小顺序为:J2> F2> ZH2> Z2。
c)溶液pH和吸附温度的提高可有效提升4种材料对甲基橙的吸附能力。
d)吸附动力学和热力学研究表明,4种材料对甲基橙的吸附过程中物理吸附起着主导作用,且更趋向于单分子层吸附。
e)4种材料均具有良好的重复使用性能。
