微生态制剂辅助复方甘草酸苷片对非酒精性脂肪肝患者脂肪肝指数及免疫炎症介质的影响①
2021-04-23许日新邓雅丽林俊芳梁丽娟
许日新,邓雅丽,林俊芳,梁丽娟
(莆田市第一医院感染性疾病科,福建莆田351100)
非酒精性脂肪肝(Non-alcoholic fatty liver disease,NAFLD)是消化内科常见病,可诱发肝纤维化和肝硬化,且有癌变风险,近年来随着居民生活方式与饮食结构改变,NAFLD发病率呈上升趋势[1-2]。药物是临床治疗NAFLD的主要手段,复方甘草酸苷片可改善肝功能异常,通过抗炎、抗氧化、抑制肝细胞损伤等机制发挥保肝作用,可用于NAFLD的治疗[3]。研究发现,肠道微生物群生态失调与NAFLD密切相关,黏膜免疫功能受损及炎症反应在NAFLD发生、发展中的作用越来越受临床重视,肠道菌群调节已成为NAFLD的重要治疗靶点[4-5]。微生态制剂是一种能够促进正常微生物繁殖生长,抑制致病菌繁殖生长的制剂,可快速构建肠道微生态平衡,调节肠道功能[6]。本研究分析微生态制剂辅助复方甘草酸苷片在NAFLD治疗中的应用价值,以期为NAFLD患者寻求一种安全、有效的治疗方案,现报道如下。
1 资料与方法
1.1 一般资料 选取2018年9月-2020年3月莆田市第一医院感染性疾病科收治的168例NAFLD患者,其中男性103例,女性65例,年龄27~65岁,平均(43.74±7.68)岁;病程1~6年,平均病程(3.21±1.01)年。合并症:糖尿病45例,高脂血症84例,高血压63例,冠心病48例。按照随机数字表法分为观察组与对照组,每组84例。2组性别、年龄、病程、合并症等基线资料比较差异无统计学意义(P>0.05),本研究经莆田市第一医院伦理委员会审核批准,见表1。
1.2 纳入与排除标准[7]纳入标准:(1)符合《非酒精性脂肪性肝病诊断标准》中NAFLD诊断标准;(2)未合并严重心脑血管病变;(3)认知与沟通正常,无视听障碍;(4)近4周内无微生态制剂或保肝药物使用史;(5)自愿签署研究知情同意书。排除标准:(1)患有酒精性肝炎、药物性肝炎或病毒性肝炎;(2)合并恶性肿瘤疾病;(3)合并甲状腺功能亢进或减退等内分泌系统疾病;(4)合并自身免疫性疾病;(5)妊娠期或哺乳期女性;(6)不配合研究者。
表1 2组患者一般资料比较(±s)

表1 2组患者一般资料比较(±s)
组别观察组对照组t、χ2值P值n 84 84男/女51/33 52/32 0.025 0.874年龄/岁44.28±7.56 43.19±8.02 0.906 0.366病程/年3.17±1.02 3.24±0.98 0.454 0.651合并症[n(%)]糖尿病24(28.57)21(25.00)0.273 0.601高脂血症43(51.19)41(48.81)0.095 0.758高血压30(35.71)33(39.29)0.229 0.633冠心病26(30.95)22(26.19)0.467 0.495
1.3 治疗方法 2组患者均给予调脂、降糖常规治疗,纠正不良生活习惯,制定合理的能量摄入方案,调整饮食结构,进行中等量有氧运动。在上述基础上对照组患者给予复方甘草酸苷片(乐普药业股份有限公司国药准字H20073723)治疗:2片/次,每片含甘草酸苷25 mg、蛋氨酸25 mg、甘氨酸25 mg,饭后口服,3次/d。观察组患者给予微生态制剂+复方甘草酸苷片治疗:采用双歧杆菌三联活菌胶囊(上海上药信谊药厂有限公司,国药准字S10970104),420 mg/次,口服,3次/d,复方甘草酸苷片用法用量同对照组。2组患者连续治疗8周。
1.4观察指标(1)脂肪肝指数(FLI):对比2组患者治疗前后FLI变化,计算公式为FLI=[e0.953×ln(TG)+0.139×BMI+0.718×ln(GCT)+0.053×WC-15.745]/[1+e0.953×ln(TG)+0.139×BMI+0.718×ln(GCT)+0.053×WC-15.745]×100,其中e为自然对数底数,ln代表取自然对数,BMI为体质量指数,WC为腰围,TG为三酰甘油,GCT为γ-谷氨酰转肽酶。(2)肝功能:抽取患者空腹状态下外周静脉血3 mL,离心分离血清送检,采用美国贝克曼库尔特AU5800型全自动生化分析仪检测天冬氨酸氨基转移酶(AST)、丙氨酸氨基转移酶(ALT)及γ-谷氨酰转肽酶(γ-GT)水平。(3)免疫炎症介质:抽取患者空腹状态下外周静脉血3 mL,离心分离血清,采用酶联免疫吸附法检测白细胞介素-6(IL-6)、白细胞介素-10(IL-10)、肿瘤坏死因子-α(TNF-α)水平。(4)安全性:治疗期间监测患者血常规、尿常规、心电图,记录不良反应发生情况以及处理方案、缓解时间,客观评价治疗安全性。
1.5 疗效评定标准 症状、体征基本消失,肝功能恢复正常为显效;症状、体征明显减轻,或大部分消失,肝功能指标改善50%以上,且低于2倍正常值上限为有效;症状、体征未缓解,肝功能无变化,或病情呈恶化趋势为无效;总有效率=显效率+有效率[8]。
1.6 统计学处理 采用SPSS22.0统计学软件对数据进行统计分析,计量资料以均数±标准差(±s)表示,采用t检验,计数资料以例(%)表示,采用χ2检验,以P<0.05表示差异有统计学意义。
2 结果
2.1 2组患者临床疗效比较 与对照组(84.52%)比较,观察组临床总有效率(94.05%)升高,差异有统计学意义(P<0.05),见表2。
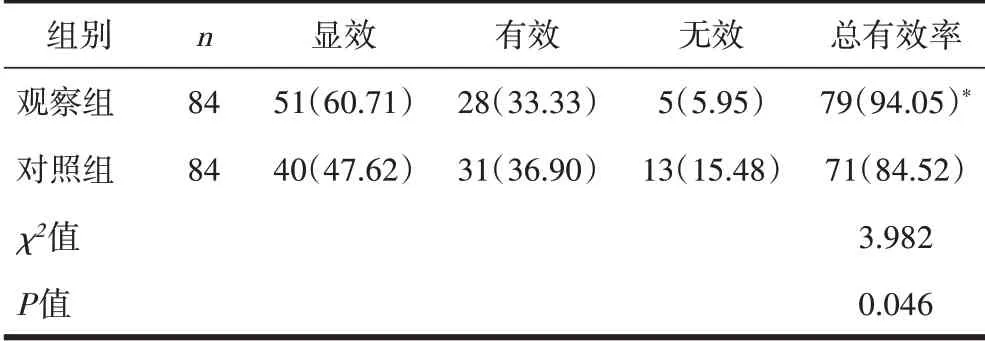
表2 2组临床总有效率比较[n(%)]
2.2 2组患者治疗前后FLI比较 与本组治疗前比较,治疗后4、8周后FLI均降低,差异有统计学意义(P<0.05)。与对照组比较,观察组患者治疗4、8周后FLI均降低,差异有统计学意义(P<0.05),见表3。
表3 2组患者治疗前后FLI比较(±s)

表3 2组患者治疗前后FLI比较(±s)
注:与本组治疗前比较,*P<0.05;与对照组比较,#P<0.05。
组别观察组对照组χ2值P值n 84 84治疗前46.87±4.63 48.02±5.05 1.538 0.126治疗4周后38.62±4.21*#41.33±5.02*3.791 0.000治疗8周后32.24±3.52*#36.78±4.04*7.765 0.000
2.3 2组患者治疗前后肝功能指标比较 与本组治疗前比较,2组患者治疗8周后血清ALT、AST、γ-GT水平均降低,差异有统计学意义(P>0.05)。与对照组治疗比较,观察组治疗8周后血清ALT、AST、γ-GT水平均降低,差异有统计学意义(P>0.05),见表4。
表4 2组患者治疗前后肝功能指标比较(±s,U/L)

表4 2组患者治疗前后肝功能指标比较(±s,U/L)
注:与本组治疗前比较,*P<0.05;与对照组比较,#P<0.05。
组别观察组对照组t值P值n 84 84 AST治疗前82.34±12.56 81.65±11.48 0.372 0.711治疗8周后35.62±6.41*#39.46±7.82*3.481 0.001 ALT治疗前79.53±10.36 78.46±9.58 0.695 0.488治疗8周后38.49±8.42*#43.67±9.03*3.845 0.000 γ-GT治疗前86.59±15.24 88.06±14.82 0.634 0.527治疗8周后56.37±10.17*#64.73±12.34*4.792 0.000
2.4 2组患者治疗前后血清免疫炎症介质水平比较与本组治疗前比较,2组患者治疗8周后血清IL-6、TNF-α水平均降低,IL-10水平升高,差异有统计学意义(P>0.05)。与对照组比较,观察组患者治疗8周后血清IL-6、TNF-α水平均降低,IL-10水平升高,差异有统计学意义(P>0.05),见表5。
2.5 2组患者治疗前后安全性比较 治疗期间2组患者血常规、尿常规、心电图检查未见异常,未见消化系统、神经系统等不良反应,2组安全性均有保障,未对治疗产生影响。
表5 2组患者治疗前后血清免疫炎症介质水平比较(±s,pg/mL)

表5 2组患者治疗前后血清免疫炎症介质水平比较(±s,pg/mL)
注:与本组治疗前比较,*P<0.05;与对照组比较,#P<0.05。
组别观察组对照组t值P值n 84 84 IL-6治疗前163.58±16.84 165.25±17.03 0.639 0.524治疗8周后81.02±10.33*#92.26±13.25*6.132 0.000 IL-10治疗前3.95±0.82 4.01±0.78 0.486 0.628治疗8周后8.65±1.52*#7.15±1.13*7.259 0.000 TNF-α治疗前10.84±2.02 11.05±1.94 0.687 0.493治疗8周后6.03±1.21*#7.84±1.63*8.172 0.000
3 讨论
NAFLD是临床常见肝病,与糖尿病、肥胖、高血压及血脂异常密切相关,调查显示,随工业化、城市化发展及饮食结构、生活方式改变,近年NAFLD发病率有明显升高趋势,在全世界内广泛流行,且在我国已取代乙型肝炎成为第一大慢性肝病,严重威胁国民身心健康[9-10]。目前,临床尚无特效药治疗NAFLD,治疗策略主要以延缓病情进展,预防肝纤维化与肝硬化,改善患者生存质量为主[11]。甘草酸制剂是现阶段肝病领域用于抗炎保肝治疗的一线药物,且随研究深入,医学界对甘草酸制剂在NAFLD、药物性肝损伤等各类肝病中的临床应用已积累较多循证医学证据[12]。复方甘草酸苷片适应证为各类肝病,本品为甘草酸苷、蛋氨酸、甘氨酸复方制剂,具有包括抗过敏、阻碍花生四烯酸代谢酶在内的抗炎症作用,以及免疫调节、抑制实验性肝细胞损伤、抑制病毒增殖及病毒灭活等多重作用,进而发挥多机制保肝作用,促进疾病改善。张建集[13]研究显示,采用复方甘草酸苷片治疗脂肪肝,可有效控制肝纤维化,且有利于改善T淋巴细胞亚群水平,调节细胞因子水平,进而提高患者肝功能。复方甘草酸苷片治疗NAFLD虽可取得一定成效,但尚未取得最为理想的疗效,仍有部分患者获益不佳,进而影响预后及生存质量改善。目前,临床已认识到肠道菌群与慢性肝病密切相关,正常情况下,肠道菌群处于动态平衡状态,维持着肠道正常功能,但肠道生态在失衡状态下,可通过对宿主能量代谢、免疫系统及炎症反应的影响,决定NAFLD等代谢综合征的发生、进展[14-15]。随之,微生态制剂经肠道菌群调节机制为NAFLD的治疗开辟了新的方向,逐渐引起临床关注。本研究试在复方甘草酸苷片基础上联合微生态制剂(双歧杆菌三联活菌胶囊)治疗NAFLD,结果显示,经治疗观察组临床疗效、FLI、肝功能指标均优于对照组(P<0.05),且2组均未发生不良反应,提示上述联合用药方案治疗NAFLD安全、有效,有利于降低肝脏脂肪含量,改善患者肝功能,有望成为NAFLD新的治疗方案。双歧杆菌三联活菌胶囊是临床应用较为广泛的一种微生态制剂,本品可直接补充有益菌群,抑制有害菌群繁殖、生长,同时可在肠道黏膜表面形成保护屏障,维持肠道正常生理功能,进一步阻止有害菌群侵袭,减少内毒素产生对肝脏的刺激[16]。此外,研究表明,肠道细菌过度生长可影响脂质代谢,导致肝脏脂肪沉积加重,双歧杆菌三联活菌等微生态制剂通过维持肠道菌群平衡,促进脂质代谢,进而减少脂肪沉积,有利于缓解脂肪肝病情[17]。
本研究结果还显示,治疗后观察组血清IL-6、IL-10、TNF-α水平优于对照组(P<0.05),提示微生态制剂辅助复方甘草酸苷片对NAFLD患者血清免疫炎症介质表达具有显著调节作用。近年,随临床对肠道菌群与NAFLD关系的研究进展,肠黏膜免疫功能受损及炎症反应在NAFLD发生、进展中参与作用越来越受临床重视[18]。研究显示,肠道菌群失调可导致肠道屏障完整性被破坏,致使免疫功能受损,并诱发肠道炎症,随后肠道细菌及免疫炎症介质易位可造成肝脏损伤,成为NAFLD重要发病机制之一[19-20]。微生态制剂通过调节肠道菌群动态平衡、维持肠道屏障完整性,可有效抑制细菌易位及对肝脏的侵袭,并可诱导抗菌肽产生,减轻炎症反应,增强机体免疫功能,调节血清IL-6、IL-10、TNF-α等免疫炎症介质表达,进而促使疾病康复[21]。因此,微生态制剂辅助复方甘草酸苷片治疗NAFLD可通过多作用机制发挥协同保肝作用。综上,微生态制剂辅助复方甘草酸苷片治疗NAFLD安全、有效,可有效缓解脂肪肝症状,改善患者肝功能,调节血清炎症免疫介质表达。
