一步水热法合成钼箔支撑的MoS2纳米片用于高效电催化产氢反应
2021-04-20黄剑锋冯亮亮曹丽云
黄剑锋, 肖 婷, 冯亮亮, 曹丽云, 徐 瑞
(陕西科技大学 材料科学与工程学院 陕西省无机材料绿色制备与功能化重点实验室, 陕西 西安 710021)
0 引言
全球经济的发展推动着能源快速消耗,化石燃料作为不可再生的能源,过度开发和使用已经造成了严重的能源枯竭和环境污染[1].氢能作为一种清洁、高效、可持续的能源,是未来最具潜能的可替代能源,采用环保且高效的制氢技术显得尤为重要,其中电催化分解水制氢技术表现突出[2].阳极析氧反应(OER)和阴极析氢反应(HER)是电解水的两个重要反应,阴极析氢反应(HER)是一种简单、直接且有效的制氢方法,然而该反应的动力学缓慢,通常需要一定的过电位,才能实现一个理想的电解水电流密度[3,4],探索一种在低过电位下具有高效电解水析氢性能的催化剂具有重要意义.目前,贵金属Pt基催化剂表现出了最高效的产氢性能,但其昂贵的价格和稀缺的储量很大程度上限制了它的应用和生产[5].因此,开发储量丰富、低成本、高效且稳定的非贵金属电催化剂是目前的研究热点.
近年来,研究者已经设计合成了许多优异的非贵金属电催化剂,例如磷化物[6,7]、硫化物[8,9]、碳化物[10,11]、氮化物[12,13]等非贵金属电催化剂,其中过渡金属硫化物在OER和HER方面都具有很高的电催化活性,这是由于它们具备调节电子态的能力,从而在电解水过程引入更多催化位点[14].过渡金属Mo元素地球储量丰富,且已经广泛应用于人类活动的各个领域,是析氢电催化剂潜在替代者之一.而MoS2这一层状过渡金属硫化物已经广泛用于生物传感器、晶体管、电极材料、光(电)水分解等行业,表现出广阔的发展前景[15].相关研究发现,MoS2的电催化活性主要来源于其各项异性生长的二维片层边缘位置,边缘的不饱和硫原子数量是影响其催化性能的重要因素[16].然而2H相的MoS2在导电性和各向异性方面表现较差,八面体的1T相MoS2具有优良的电子传输能力及更多的催化活性位点[17],所以合成1T相的MoS2是研究重点.除此之外,电催化剂载体的选择也需要坚持廉价且高效的原则,钼箔作为经济、实惠且高导电的基体,与MoS2直接接触有利于电子传输.
在本工作中,通过一步水热法在钼箔上成功合成了1T/2H-MoS2纳米片,此电极命名为MoS2/MF.电催化测试表明,最优化的MoS2/MF电极在酸性条件下100 mA/cm2时的过电势为269 mV,甚至能比得上20% Pt/C/MF,且能稳定工作65 h.本研究证实了一步水热合成的MoS2/MF材料可作为一种高效且稳定的酸性产氢电催化剂.
1 实验部分
1.1 原材料
钼箔(MF,面积为1×6 cm2);六水合钼酸铵 ((NH4)6·Mo7O24·4H2O);硫代乙酰胺(C2H5NS);氨水(NH3·H2O);铂碳电极(20 wt% Pt/C);硫酸(H2SO4);异丙醇((CH3)2CHOH);丙酮(C3H2O);无水乙醇(CH3CH2OH).
1.2 样品的制备
MoS2/MF:称取0.112 5 g四水合钼酸铵((NH4)6·Mo7O24·4H2O)和0.81 g硫代乙酰胺(C2H5NS),放入装有30 mL去离子水(DI)和3 mL氨水(NH3·H2O)的混合溶液中,将混合溶液转移到45 mL水热釜中,磁力搅拌20分钟使溶液混合均匀且澄清.然后取一片干净的大小为1×6 cm2钼箔(MF)放入该溶液.随后,密封水热釜并于烘箱中180 ℃反应24 h,然后自然冷却至室温取出水.最后,从冷却的高压釜中取出钼箔,用水和乙醇交替冲洗3次,于真空干燥箱60 ℃干燥6 h,得到MoS2/MF.
不同氨水量MoS2/MF的合成:与MoS2/MF合成步骤相同,氨水加入量分别为1 mL、2 mL、3 mL、4 mL,得到样品分别记为MoS2/MF-1、MoS2/MF-2、MoS2/MF-3、MoS2/MF-4.
1.3 样品的表征
样品的物相组成与晶体结构由X射线衍射仪(Rigaku,D/max-2200 pc)和显微共焦拉曼光谱仪(Renishaw,Renishaw-invia)进行测定及分析.
样品的形貌和微观结构利用场发射扫描电子显微镜(FESEM,Hitachi,S4800)及透射电镜(TEM,JEM-3010)进行表征及分析.
样品的元素组成和表面化学状态用X射线光电子能谱仪(XPS,AXIS Supra)来检测及分析.
1.4 电化学测试
采用典型的三电极系统,在CHI 660E B17060电化学工作站(中国上海CH仪器公司)上进行电催化析氢测试.在三电极系统中,MoS2/MF电极可直接用作工作电极(面积为~0.1 cm2,负载量为~3 mg/cm2),对电极为碳棒,参比电极为饱和甘汞电极(SCE).线性扫描伏安曲线(LSV)扫描速率为5 mV/s.所有制备的样品均在酸性(0.5 M H2SO4)环境中进行电催化析氢性能测试.
为了进行比较,当用粉末电催化剂(20 wt% Pt/C)作为工作电极时,其制备过程如下:(1)称取10 mg催化剂于装有200μL异丙醇溶液的离心管中,超声10 min使其形成均匀混合物;(2)移液枪取4μL上述溶液滴于工作面积为0.06 cm2的MF上;(3)于空气中自然干燥负载催化剂的MF,为防止催化剂在电催化测试过程中掉落,再取3μL的1% Nafion异丙醇滴加在MF上并自然晾干.
2 结果与讨论
2.1 样品的XRD与Raman分析
采用XRD、拉曼光谱进一步分析了MoS2/MF纳米薄片中的1T相和2H相.图1(a)中XRD图谱证实,与MoS2标准卡片(PDF#75-1539)对比可知,MoS2主峰(002)比原来位置往低角度偏移,表明MoS2层间距增加,而氨水加入量的改变并未明显造成MoS2物相的变化.图1(b)为不同氨水加入量样品的拉曼光谱图,144 cm-1处的特征峰为Mo-Mo伸缩振动,280 cm-1、376 cm-1、401 cm-1和450 cm-1处的特征峰,是由于E1g、E、A1g和纵向声子模的振动[18].此外,氨水加入量为3 mL时,MoS2/MF-3样品在230 cm-1和332 cm-1处出现了新的特征峰,证明此样品存在大量的1T相.
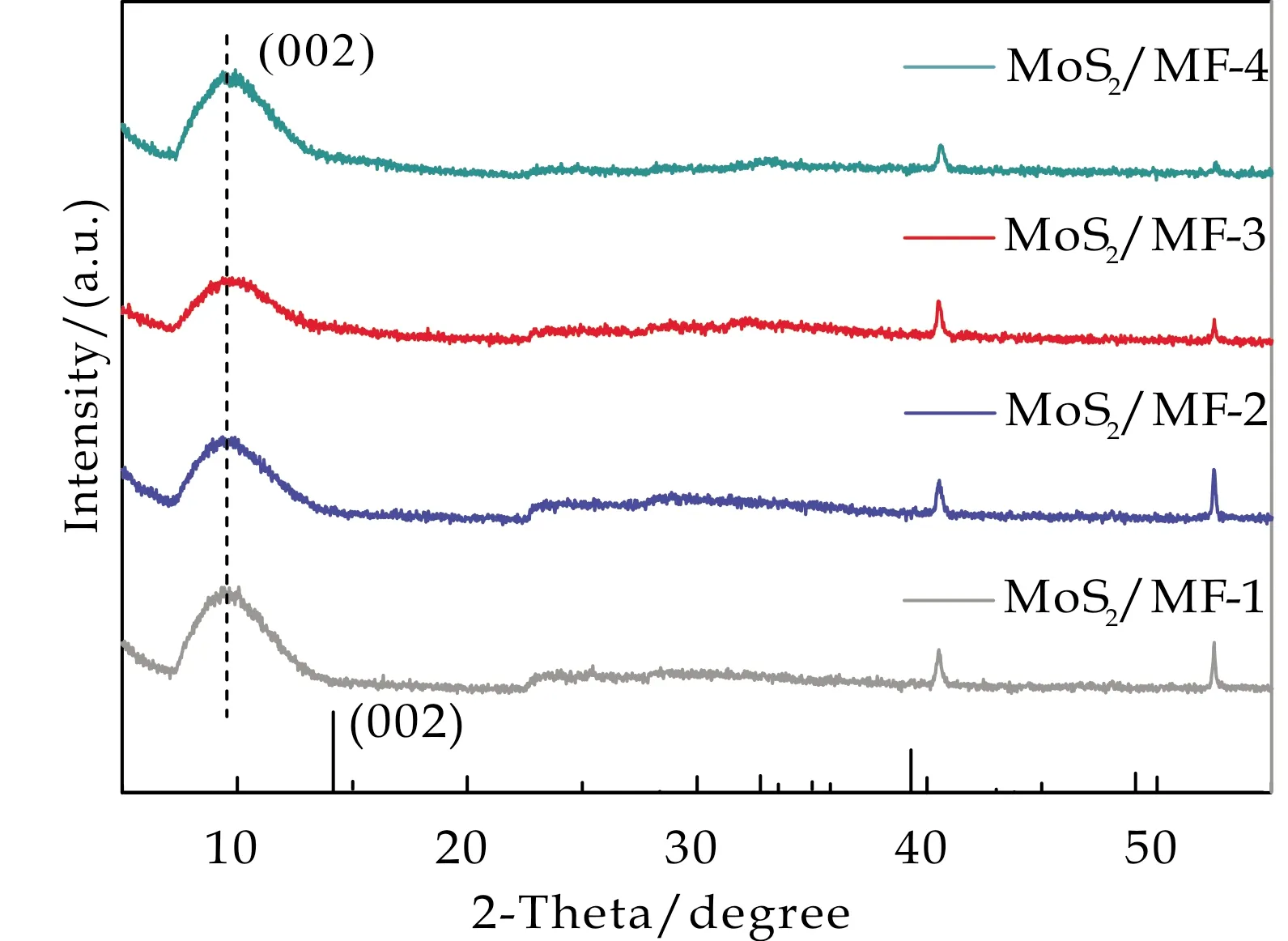
(a)XRD图谱

(b)Raman图谱图1 MoS2/MF的XRD图谱和Raman图谱
2.2 样品的形貌及微观结构分析
图2(a)、(b)是MoS2/MF样品的SEM图.由图可以看出,MoS2/MF材料为规整的纳米片结构,且MF表面完全被MoS2纳米片覆盖.通过透射(TEM)来进一步观察MoS2/MF材料的微观结构,图2(c)为低倍放大透射电镜下观察到MoS2为纳米薄片结构.图2(d)的HRTEM图像显示MoS2/MF为单层或多层结构,测量MoS2/MF的四层晶格条纹间距为1.95 nm,则Mo-Mo间距为0.65 nm.且图2(d)的HRTEM图像中明显地观察到硫空位、晶格扭曲和钼边缘位点存在于MoS2的基底平面样品中,这些缺陷和边缘能生成更多的活性位点从而提高催化性能.
此外,在HRTEM图2(e)中能清楚地观察到,2H相为常见的蜂窝状,2H-MoS2基体中形成的1T-MoS2相为三角晶格,证明了1T相和2H相同时存在于MoS2/MF中.相关研究表明,1T-MoS2导电性(2.1 S cm-1)比2H-MoS2(1.3×10-5S cm-1)导电性高5个数量级.因此,1T相MoS2的存在不仅能显著提高MoS2导电性,还能提高其电催化活性.图2(f)为MoS2/MF的元素分布图,可以观察到,在MoS2/MF纳米片中Mo、S元素的存在且分布均匀.

(a)、(b)SEM

(e)HRTEM

(f)elemental mapping图2 MoS2/MF的形貌及微观结构图
因此,可以得出结论,与2H相的MoS2相比,1T相MoS2的形成能够显著提高MoS2的催化活性,且存在于MoS2的基底平面的硫空位、晶格扭曲和钼边缘能够提供更多的析氢活性位点.
为了研究氨水加入量的不同对MoS2/MF形貌结合及催化活性的影响,分别制备了氨水加入量为1 mL、2 mL、3 mL、4 mL的四个样品.首先通过SEM对各样品的形貌进行了表征,如图3所示.图(a)、(b)是氨水加入量为1 mL时MoS2/MF (MoS2/MF-1)的形貌,此加入量下没有完整地形成纳米片,且纳米片形貌不规整.如图(c)、(d)所示,增加氨水加入量为2 mL(MoS2/MF-2)时开始得到形貌清晰且均匀覆盖在钼箔表面的纳米片.当增加氨水加入量为3 mL(MoS2/MF-3)时,如图(e)、(f)所示,形成了更加规整的纳米片,纳米片尺寸较小.进一步增加氨水加入量到4 mL (MoS2/MF-4)时,如图(g)、(h)所示,纳米片逐渐变厚且相互黏结在一起,这不利于电催化析氢.实验结果表明,当氨水加入量为3 mL时,能够得到最规整且尺寸最小的MoS2纳米片.

(a)、(b)1 mL

(c)、(d)2 mL

(e)、(f)3 mL

(g)、(h)4 mL图3 不同氨水加入量下得到 的样品的扫描图
2.3 各样品的电化学性能测试
图4是对不同氨水加入量的样品在酸性(0.5 M H2SO4)条件下进行的电化学性能测试图.在电流密度为100 mA cm-2下,MoS2/MF-3所需要最小过电势为269 mV,相同的电流密度下,其他不同氨水加入量的样品需要更高的过电位,分别为MoS2/MF-1=364 mV,MoS2/MF-2=285 mV,MoS2/MF-4=294 mV,表明存在一个最优的氨水加入量.MoS2/MF-3样品甚至在大电流密度下表现出赶超20% Pt/C/MF的趋势.实验结果表明,MoS2/MF-3样品的形貌及电催化活性皆为最优,因此,下面将对氨水加入量为3 mL时的样品(记为MoS2/MF)展开详细讨论.

图4 各样品的线性伏安曲线(LSV)
2.4 MoS2/MF的XPS分析
利用X射线光电子能谱(XPS)对MoS2/MF样品的表面化学成分和状态进了行表征.图5的XPS图谱证明了MoS2/MF样品中存在Mo、S和O元素,使用C 1s 峰的结合能284.6 eV校准了MoS2/MF所有拟合峰的结合能.
图5(a)为Mo 3d XPS图谱,228.8 eV和231.7 eV处峰值对应MoS2/MF样品中1T-MoS2的Mo4+的3d5/2和3d3/2的结合能,而2H-MoS2的Mo4+的3d峰值分别为229.3 eV和232.5 eV,与1T-MoS2相比,Mo 3d中的峰值向1 eV以上的结合能偏移.且在较高结合能处出现两个峰,对应Mo6+的结合能,表明部分Mo4+暴露在空气中被氧化形成了MoO3[19].
图5(b)为S 2p 的XPS图谱,161.7 eV和162.8 eV处的峰值分别对应1T-MoS2中S 2p3/2和2p1/2的结合能,同样比2H-MoS2中S的结合能低.此外,在166~169 eV之间出现的宽峰,可能为水热反应过程中硫被氧化生成的硫酸盐的特征峰[20].
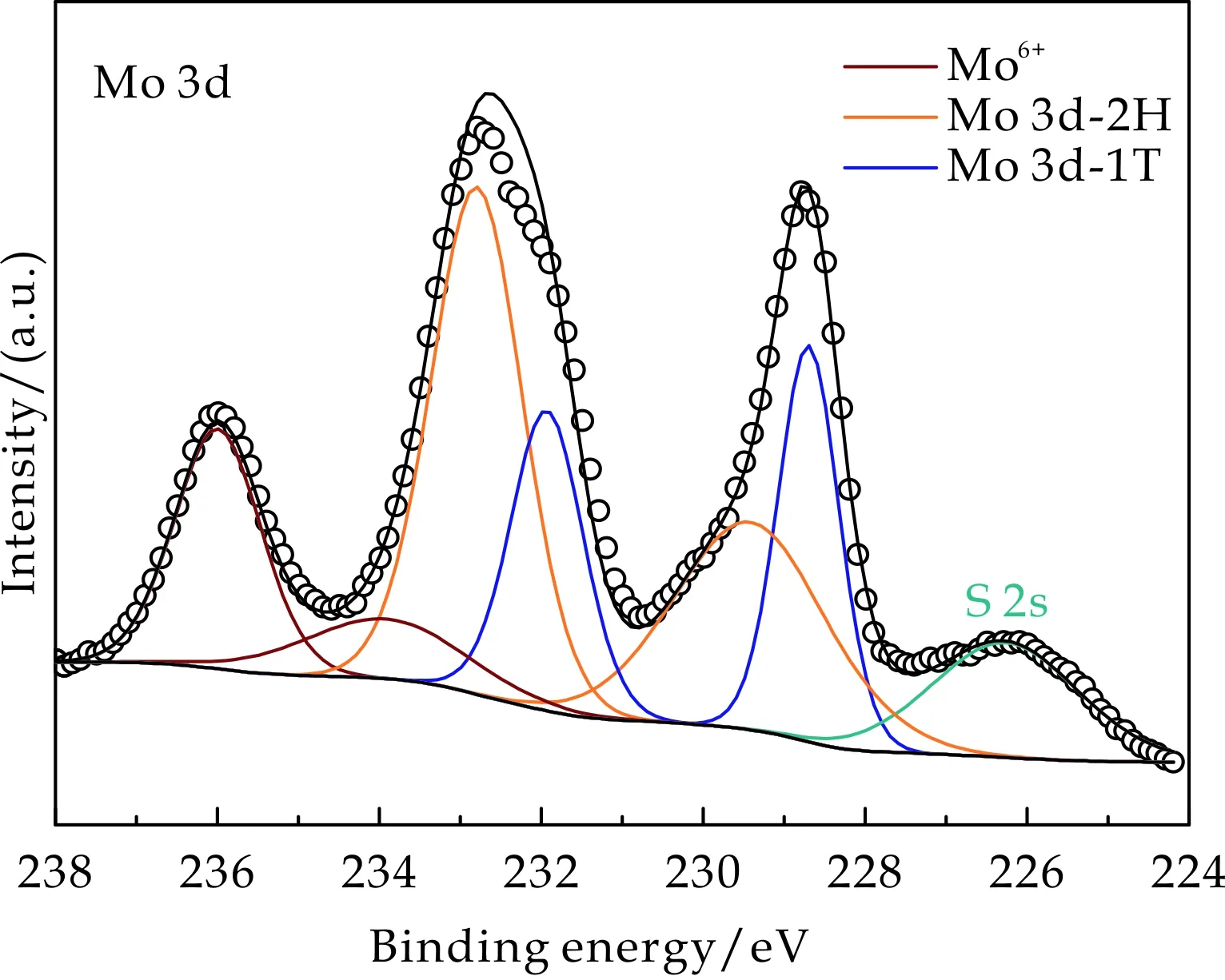
(a)Mo 3d XPS图谱
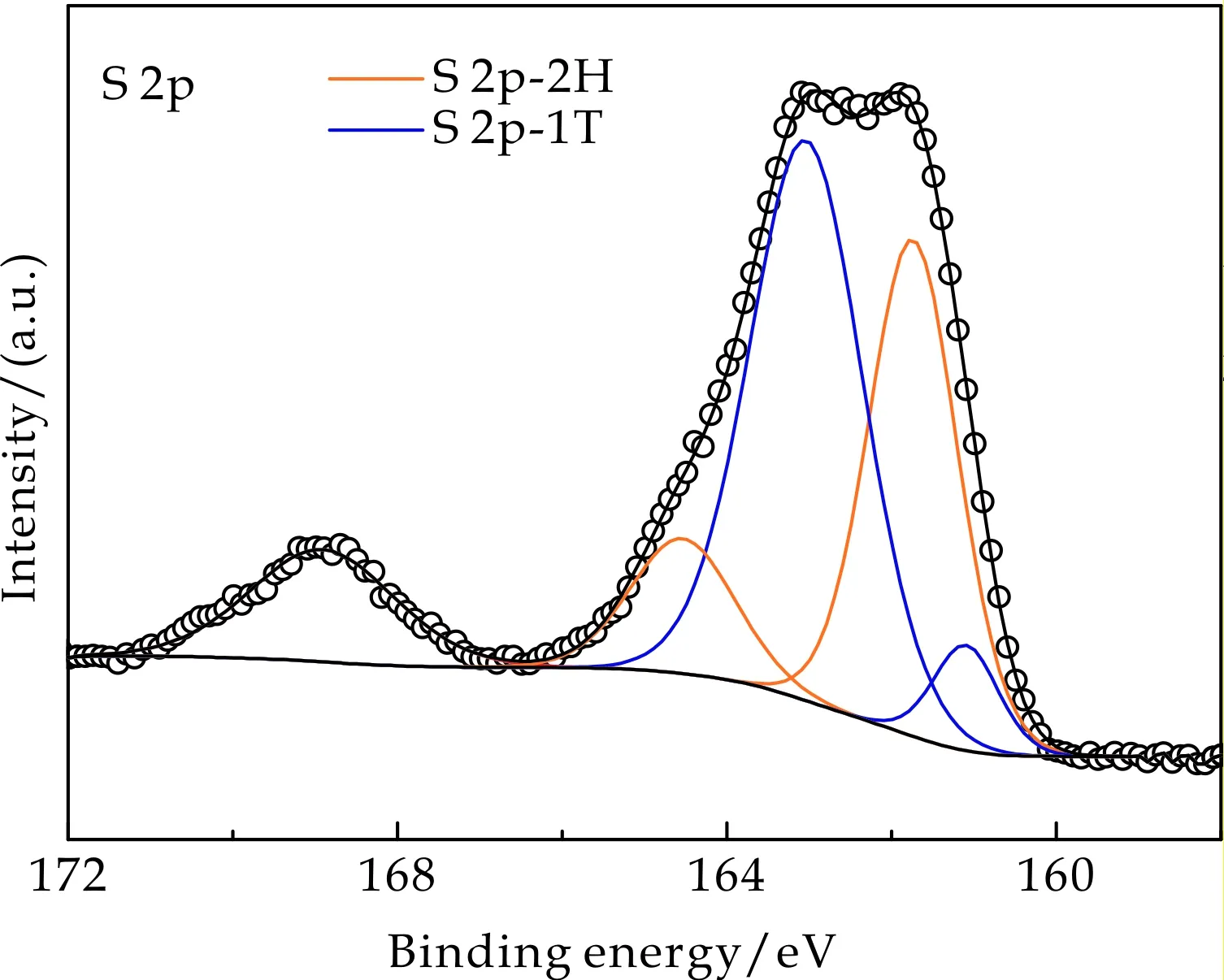
(b)S 2p XPS图谱图5 MoS2/MF的XPS图谱
2.5 MoS2/MF的析氢动力学分析
将图4中的LSV曲线转化计算得到各样品的塔菲尔斜率,如图6(a)所示.可以看出,MoS2/MF-3 Tafel斜率为53 mV dec-1,低于其他样品,但略高于20% Pt/C/MF,说明MoS2/MF-3样品表明的电催化析氢反应更容易发生,Volmer步是决速步骤.
利用电化学阻抗谱(EIS)对催化剂的导电性进行了分析如图6(b)所示.0.5 M H2SO4溶液中,在过电位为269 mV时,MoS2/MF-3样品的电荷转移阻力(Rct)值相较其他样品是最低的,表明在电催化析氢反应过程中,MoS2/MF-3样品的电荷传输能力最强.
图6(c)为样品电化学活性面积测试.可以看出,MoS2/MF-3样品的双层电容值(Cdl)最大,为80 mF cm-2,其他样品分别为2 mF cm-2、65 mF cm-2、47 mF cm-2,双层电容与电化学活性表面积(ECSA)成正比,则MoS2/MF-3样品的ECSA值最大,说明其电催化反应活性位点数量最多,ECSA较其他样品增加的原因可能是存在丰富的缺陷结构,这决定了MoS2/MF-3样品的催化动力学,并解释了其优异电催化析氢活性的原因.因此,氨水加入量为30 mL时,MoS2/MF-3样品拥有最佳的HER活性.
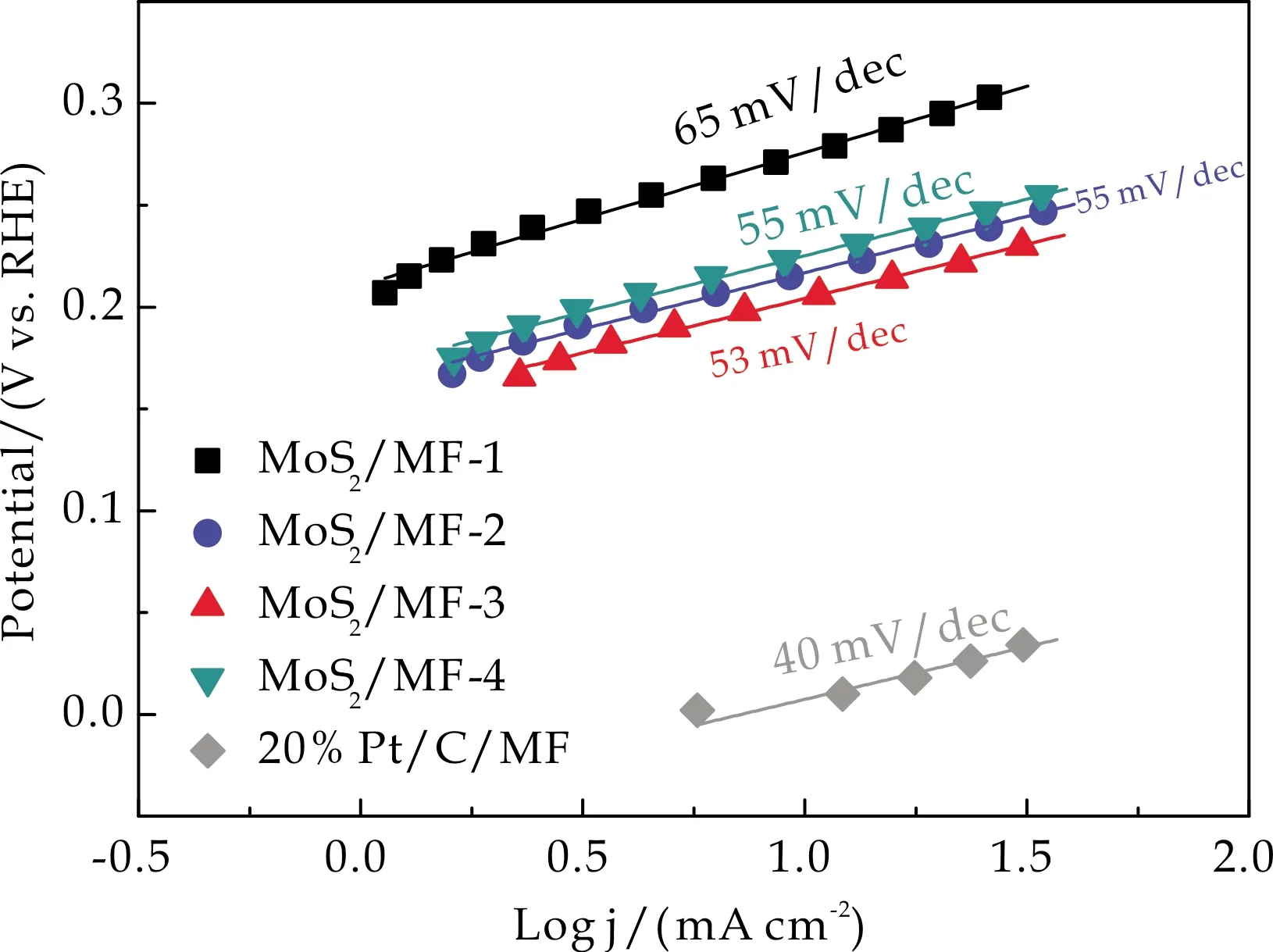
(a)Tafel曲线
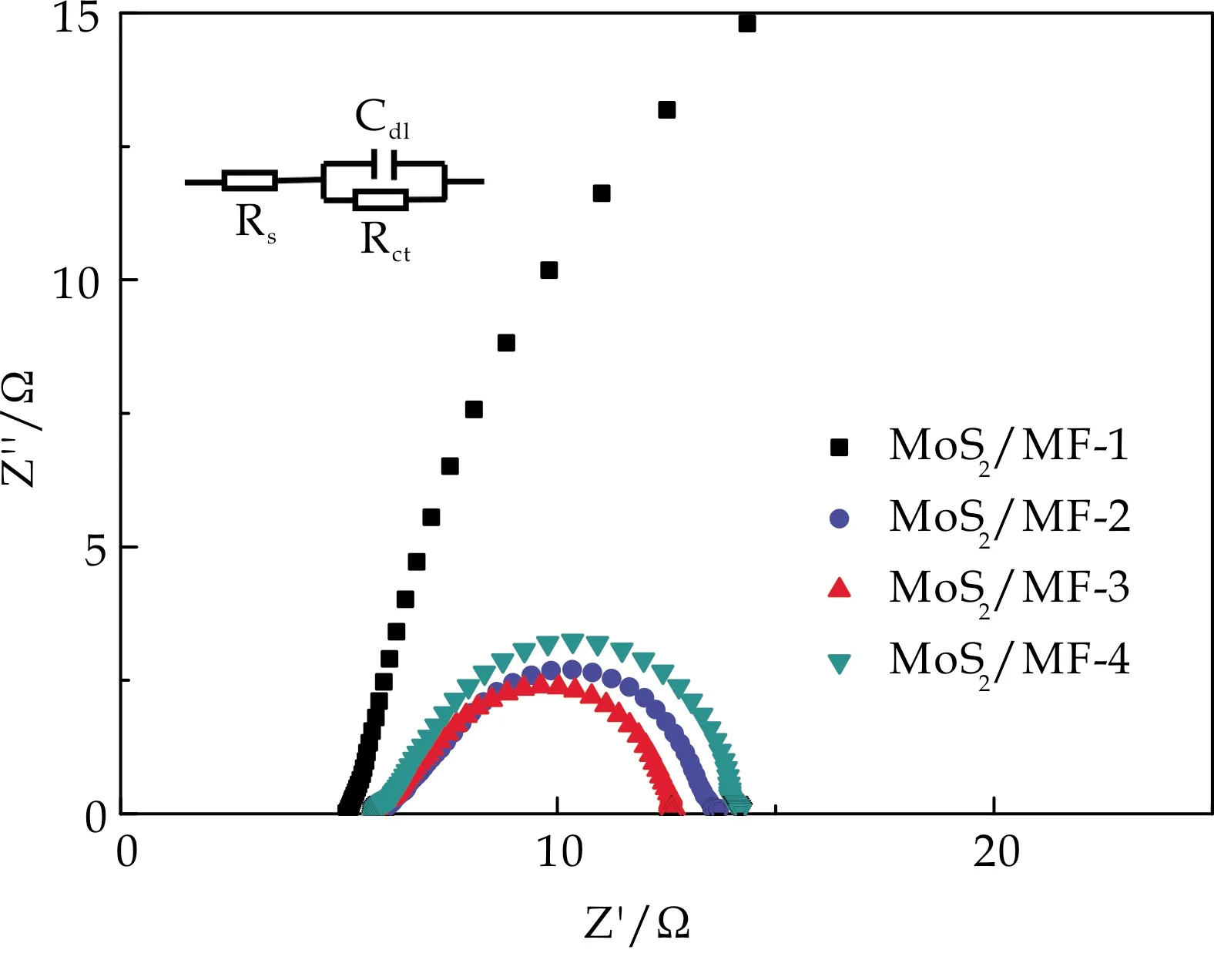
(b)阻抗图

(c)电化学活性面积图6 在0.5 M H2SO4溶液中各样 品产氢性能测试
2.6 MoS2/MF的电化学稳定性测试
图7(a)为电催化剂的稳定性测试,是评价电化学能的重要指标之一.在电流密度j=10 mA cm-1下,在0.5 M H2SO4溶液中对MoS2/MF样品进行了65 h的稳定工作,MoS2/MF电催化剂的电流密度表现出良好的耐久性,并且在不同的过电势下均表现出稳定的电流密度(如图7(b)所示),说明MoS2/MF在酸性条件中具有优异的电催化析氢稳定性.综上所述,可以认为MoS2/MF是一种优异且高度稳定的析氢电催化剂.

(a)i-t曲线

(b)多步计时电流曲线图7 MoS2/MF的稳定性测试
2.7 非贵金属MoS2基电催化析氢性能比较
本文总结了一部分与MoS2相关的非贵金属析氢电催化剂进行对比,如表1所示.MoS2/MF样品的电催化析氢性能不论是在电流密度为10 mA cm-1或100 mA cm-1时都是比较优异的.

表1 非贵金属MoS2基析氢电催化剂的对比
3 结论
(1)本工作使用简单的一步水热法,通过调节水热反应过程中的氨水加入量,控制样品形貌以及活性位点数,成功制备出具有最佳电催化析氢活性的MoS2/MF材料.MoS2/MF作为一种高效的析氢电催化剂,在0.5 M H2SO4溶液中,电流密度为100 mA/cm2时仅需过电势为269 mV,且至少可以稳定工作65 h.
(2)形貌和结构表征表明,氨水能使MoS2牢牢地生长在钼箔上,纳米片较为规整排列的结构使得催化剂与电解液之间充分接触拥有更多的活性位点.此外,该体系具有显著提高的电催化性能归因于1T-MoS2的掺入有效地减小了MoS2催化剂的带隙,提高了本征电导率,以及MoS2的基底平面中产生的许多缺陷和边缘,能够通过降低表面能促进生成更多的活性位点从而提高电催化性能.
