时空编码核磁共振方法及其应用
2021-04-17蔡淑惠蔡聪波
蔡淑惠,蔡聪波,陈 忠
(厦门大学电子科学与技术学院,福建省等离子体与磁共振研究重点实验室,福建 厦门 361005)
自发现核磁共振(nuclear magnetic resonance,NMR)现象以来的70多年里,NMR在物理、化学、生物及医学领域已获得了6次诺贝尔奖,新技术新方法不断涌现,在物理、化学、生物、医药、石油勘探等领域获得了广泛的应用.
二维及多维NMR波谱广泛应用于化学和生物学分析,而磁共振成像(magnetic resonance imaging,MRI)广泛应用于医学诊断和生命科学研究.然而,传统的二维及多维NMR谱的间接维信息采用时间增量方式获取,而MRI通常采用梯度面积增量方式进行成像以获取物质的空间分布信息,因此它们的采样时间都比较长.提高采样效率、缩短采样时间一直是NMR研究的一个重要方向.
2002年Frydman课题组受回波平面成像(echo planar imaging,EPI)原理的启发,提出了时空编码(spatiotemporal encoding,SPEN)技术,该技术首先应用于单扫描获取二维NMR谱[1-2],随后又应用于单扫描二维MRI[3].单扫描SPEN技术使二维谱/像扫描时间降低到毫秒级,实现了超快速采样.
SPEN技术一经提出,立即引起了广泛的兴趣.本课题组也围绕其展开研究,设计出一系列快速SPEN NMR波谱和成像脉冲序列,并提出相应的快速高质量重建方法,得到了国际同行的重视和认可.本文将简要介绍SPEN原理,对本课题组十几年来在SPEN NMR领域的研究进行系统的阐述.
1 SPEN NMR波谱和成像原理
SPEN NMR技术采用编码脉冲在梯度场的辅助下不同时刻作用于不同位置上的核自旋,使得编码脉冲结束后核自旋相位随空间位置变化;采样期在梯度场的作用下解码这些相位信息即得到编码维的谱信息或核自旋空间位置分布信息[4].编码脉冲通常为线性扫频(chirp)脉冲[5].chirp脉冲的激发频率与时间成线性关系,相位是时间的二次项[2].
1.1 SPEN NMR波谱原理
在NMR波谱测量中,样品有一定的长度,因此沿着样品长度方向(假设为z方向)可以实施SPEN及解码.图1示意了使用两个180° chirp脉冲的SPEN序列对含有两个化学位移(δ1和δ2)的样品的时空编解码原理.首先序列中的第一个射频(radio frequency,RF)脉冲将样品所有z空间位置自旋磁化矢量都翻转到x-y平面,此时所有位置上的横向磁化矢量相位是一致的,如图1(a)所示.第一个180° chirp脉冲在SPEN梯度GE作用下不同时刻翻转不同z位置上的自旋[2,6],在该脉冲结束后自旋的相位是位置z的二次项函数(抛物线函数,如图1(b)所示;对于不同化学位移,抛物线函数的驻点位置不同).由于采样期通常使用矩形梯度,只能对线性相位进行解缠绕,所以需要使用第二个180° chirp脉冲在-GE梯度下将二次项相位转变为线性相位[2,6].第二个180°chirp脉冲后得到如图1(c)所示的横向磁化矢量相位.不同化学位移的磁化矢量相位随位置的线性变化程度不同,即得到SPEN相位φE=Cδ·z,其中C为受实验条件控制的SPEN常数.在解码梯度GD下进行采样,对于不同的化学位移,φE在不同时刻被解缠绕,磁化矢量得到重聚,这个时刻可以得到该磁化矢量的回波峰,如图1(c)所示.如果将采样梯度进行反转继续采样,即在-GD下采样,第一个GD采样结束后缠绕的相位将再一次发生重聚和散相,在-GD的不同时刻亦可得到不同化学位移的回波峰.重复在GD和-GD下采样,可以得到一系列不同化学位移的回波,这些回波组成与EPI中的相位编码维(无相位编码梯度)类似的一个维度,称为直接维.由于该维度化学位移的演化不受梯度作用,随时间自由演化,所以沿着直接维进行傅里叶变换(FT)可以得到化学位移信息.这就是超快速SPEN NMR波谱原理.单次扫描后只需对直接维进行FT便得到二维谱.
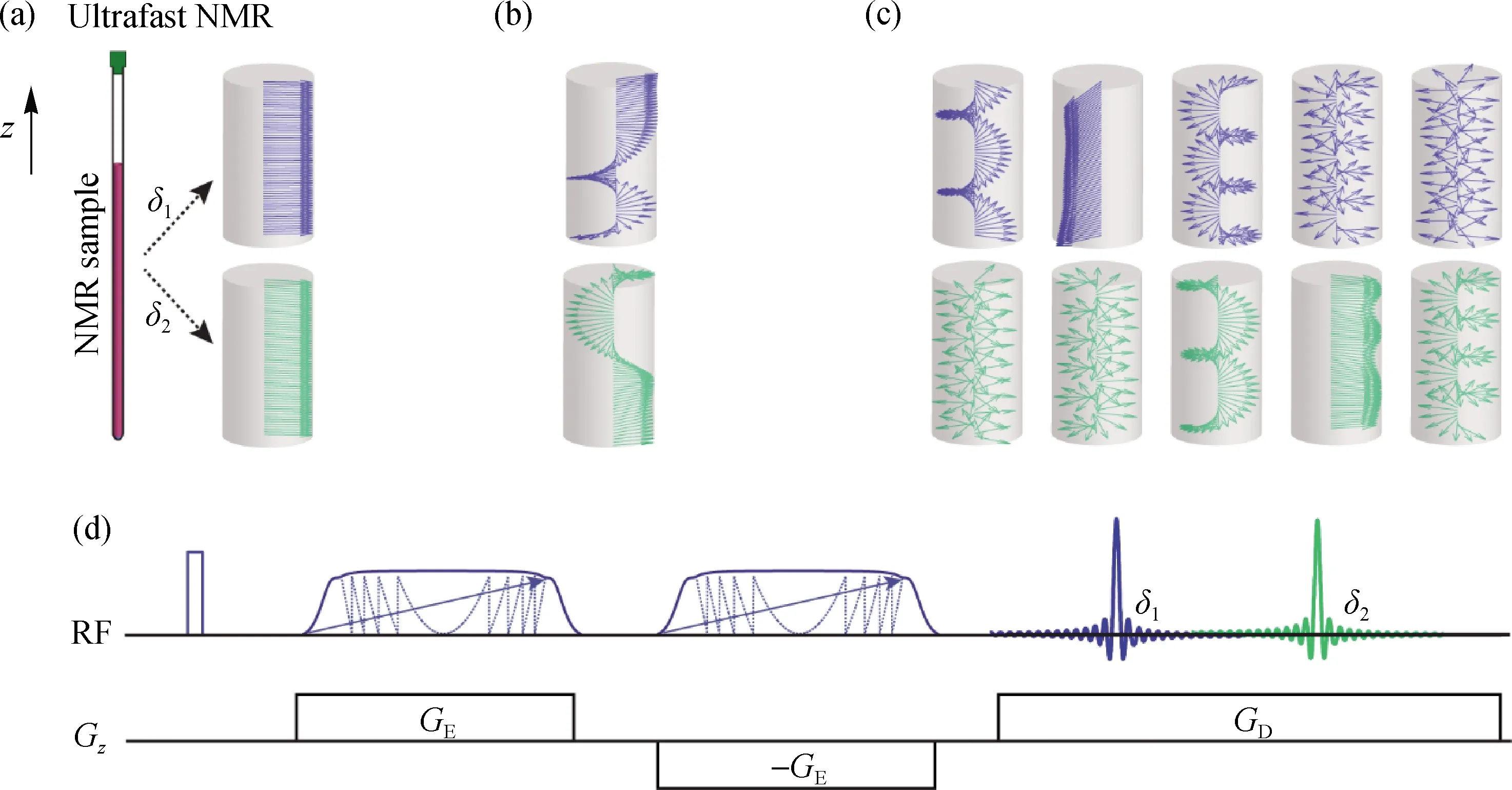
(a)~(c)包含两个不同化学位移的样品在脉冲序列作用下不同时刻x-y平面上的磁化矢量分布示意图;(d)包含两个180° chirp脉冲的SPEN脉冲序列.
1.2 SPEN MRI原理
本文用一维水模来说明SPEN MRI原理.水模沿着z方向的包络如图2(a)所示.脉冲序列的第一个脉冲将水模的所有自旋磁化矢量都翻转到x-y平面,此时沿着z方向所有的x-y磁化矢量都是同相位的.同SPEN NMR原理,180°chirp脉冲在SPEN梯度GE不同时刻翻转不同z位置上的自旋.在该脉冲结束后,得到相位φE沿着z方向成二次项函数分布的磁化矢量,如图2(b)所示,此时φE=a·(z-z0)2,其中a为受实验条件控制的SPEN常数,z0为由chirp脉冲决定的位置常数.当a足够大时,φE只在z0附近变化缓慢,而远离z0时则快速变化.因为线圈检测信号是对空间所有位置信号的累积,此时远离z0的信号由于其相位的快速变化被平均后对检测信号的贡献微乎其微,所以检测信号主要来源于z0附近小范围的信号,z0被称为稳定相位点,其附近的有用信号范围反映了SPEN的空间分辨率.改变z方向的SPEN梯度作用可以改变SPEN的稳定相位点.为了从水模的边缘开始进行信号检测,首先使用移位梯度(purge)将稳定相位点移至成像视野的边缘处,然后在采样梯度GD下进行信号检测,稳定相位点区域(黄色区域)将随着采样时间从成像视野的一端移动至另一端,如图2(c)所示.随着稳定相位点的变化,检测得到水模内不同体素的信号,从而无需FT即直接得到水模的包络,如图2(d)中GD上方的虚线包络所示.由于稳定相位点附近的有用信号区域大小直接反映观测信号的空间分辨率,所以可以通过调节SPEN脉冲序列参数得到较高分辨率的包络.因为在编码参数(如编码脉冲长度、编码梯度大小等)已知的情况下,整个样品区间的φE可通过计算得出,所以在SPEN空间分辨率较低的情况下,可以通过超分辨率重建算法得到高空间分辨率的水模包络[7].将EPI中的相位编码维取代为上述的SPEN维而保留读出梯度维,可以得到二维SPEN MRI序列,该序列得到的信号只需对读出梯度维进行FT即可得到二维图像.SPEN MRI可以得到与EPI类似的分辨率和信噪比,而且抗不均匀磁场和化学位移伪影的能力增强.
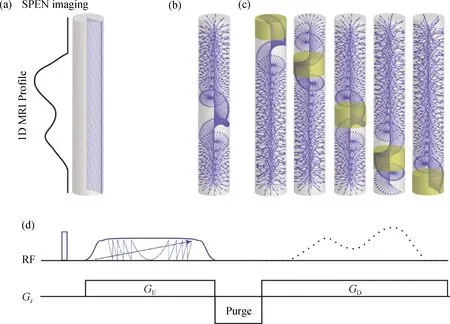
(a)~(c)一维水模沿着z方向在脉冲序列作用下不同时刻x-y平面上磁化矢量分布示意图,黄色区域表示采样期稳定相位点附近区域;(d)包含180° chirp脉冲的SPEN脉冲序列.
2 超快速SPEN NMR波谱方法及其应用
SPEN二维NMR波谱和常规二维NMR波谱采样方式不同.在常规二维NMR实验中,核自旋受激发后在x-y平面演化,演化时间通常用t1表示;在混合期,所需要的相干阶被转换成可观测的信号;最后在采样期t2收集可观测信号.为了得到一张二维NMR谱,需要重复N1次采样,每次t1增加Δt1,每一个t1值对应一次单独的一维NMR采样,如图3(a)所示.连续两次一维采样之间还需要一个等待时间使自旋系统弛豫恢复到平衡状态.因此传统二维及多维NMR最大的缺点就是实验时间长,这限制了其在实时监测化学反应过程等对时间分辨率要求高的场景中的应用.SPEN NMR方法用SPEN代替传统的t1时间编码,即将样品按空间分成N1份,每份经历不同的演化时间来代替,检测期用回波平面谱成像(echo planar spectroscopic imaging,EPSI)方式进行采样,如图3(b)所示,因此单次扫描即可获得一张二维谱,大大缩短了实验时间.不仅如此,SPEN NMR的采样方式使其在抗磁场不均匀不稳定性影响方面具有独特优势.本节将分别介绍均匀磁场下、不均匀磁场下、不稳定磁场下SPEN NMR方法,并简要介绍其应用.

图3 常规二维NMR波谱(a)和SPEN二维NMR波谱(b)原理图
2.1 均匀磁场下超快速SPEN NMR波谱方法
Frydman课题组[8]最早提出的SPEN方法是离散SPEN方法,这种方法在实验过程中需要快速进行磁场梯度切换,实验难度较高,而且离散快速采样还会导致间接维出现干扰的“鬼峰”.为了克服此缺点,Pelupessy[5]应用绝热脉冲代替离散的射频脉冲,避免了编码期间频繁的磁场梯度切换,有效消除了间接维的“鬼峰”.在绝热脉冲应用于SPEN单扫描快速采样后,Shrot等[9]提出在使用正负梯度场的同时,使用相同的90° chirp脉冲进行激发,这种方法被定义为连续调制SPEN.由于这种方法属于幅度调制,不能应用于需要通过相位调制的相关谱(correlated spectroscopy,COSY)实验.对该SPEN单扫描快速采样序列进行改进,可以设计出连续相位调制SPEN单扫描快速采样序列,调制方式分为实时相位调制和恒时相位调制.相位调制编码使超快速获得COSY成为可能.Tal等[10]提出了一种由90°-180° chirp脉冲组成的实时相位调制编码脉冲序列,可以在大约100 ms的时间内获得一张二维COSY谱,然而该方法在实验中需要仔细调节参数,实现起来比较困难.为了克服上述问题,本课题组提出了基于恒时相位调制SPEN的梯度选择相关谱(gradient-selective COSY, g-COSY)和双量子滤波梯度选择相关谱(double-quantum-filtered gradient-selective COSY, gDQF-COSY)序列来快速获得二维COSY谱,新序列的编码部分由180°-180°chirp脉冲组成[6].此外,本课题组提出了基于SPEN和相干转移技术的两个超快速采样脉冲序列UFSECSY(ultrafast spin-echo correlated spectroscopy)和UFSETOCSY(ultrafast spin-echo total correlated spectroscopy),以单扫描获得二维同核COSY和全相关谱(total correlation spectroscopy, TOCSY)[11].
SPEN单扫描超快速采样方法降低了NMR谱的采样时间,极大地提高了采样速度.此方法一经提出,就先后应用于二维COSY[6,10,12]、J分解谱[10,13]、TOCSY[1,5,10,14]、扩散排序谱(diffusion ordered spectroscopy,DOSY)[15]、异核多量子相干谱(heteronuclear multiple quantum coherence,HMQC)[16]、异核单量子相干谱(heteronuclear single quantum coherence,HSQC)[5,14]以及异核多键相关谱(heteronuclear multiple-bond correlation,HMBC)[17]等.在多维谱方面,Frydman课题组[18]在2003年进行了单扫描SPEN超快速采样的原理论证,随后利用二维SPEN与二维时间编码结合得到生物大分子的三维1H-15N-13CO相关谱(1H-15N-13CO correlation,HNCO)[19].Giraudeau等[20]提出了三维超快速J-COSY方法(ultrafastJ-COSY, UFJCOSY)同时获取J分解谱和COSY,该方法中的一维仍采用传统采样方式,采样时间在分钟量级.
虽然SPEN单扫描超快速采样方法极大地提高了二维和多维谱的采样速率,但与此同时,由于超快速SPEN实验中谱宽和分辨率之间的矛盾关系,谱图的灵敏度和分辨率较常规谱而言受到了限制.为了解决这个矛盾,Shrot等[21]提出了一种空间/频谱编码方法,但其受选择脉冲不准以及谱图灵敏度损失等限制,应用范围有限.Giraudeau等[12]提出了梯度控制折叠(gradient-controlled folding)方法,通过在混合期前后施加合适的脉冲场梯度,获得折叠样谱,在减少谱宽的同时恢复所有自旋共振信息.该方法不采用选择性脉冲,避免了选择性脉冲相关问题,然而,从折叠谱中重建非折叠谱比较困难,而且脉冲梯度场的参数设置需要先验信息.本课题组[23]提出了反转采样方法:分两个阶段分别对谱的不同频率范围进行检测,提高了整体观测频谱谱宽;反转采样可以在宽谱宽和窄谱宽的系统中使用,并可与梯度控制折叠等技术组合实现更大的谱宽.为了消除时间编码谱经协方差方法处理后产生的伪峰,本课题组设计了基于模式识别的伪峰校正算法.对三维NMR谱,本课题组[23]提出了离散解码方法,通过提供合适的采样速度来解决不同维度谱宽的平衡问题.离散解码有助于将NMR研究限定在某些选定的化学位点上以产生一个子谱,使谱图更易解析.
2.2 不均匀磁场下超快速SPEN高分辨NMR波谱方法
要获取高分辨率的NMR谱需要有高度均匀的磁场,但由于磁场本身均匀度较差或者样品本身磁化率不均匀等原因,在许多情况下无法得到高度均匀的磁场.SPEN采样方法在不均匀磁场中也展现出独特的应用价值.Frydman课题组[24]利用SPEN NMR的特点,结合外加磁场梯度和频率选择性脉冲获得了不均匀磁场下高分辨NMR谱.这种方法最大的缺点是需要提前绘制不均匀磁场,当磁场的不均匀性复杂时难以找到补偿方法.
SPEN谱的间接维信息经过编码后可直接由磁场梯度读出,因而编码方向的一阶磁场不均匀只是移动回波位置,并不引起谱线增宽.在此基础上,间接维做自旋回波演化,再经过谱图变换,可在不均匀磁场下获得高分辨的COSY,但这种方法对磁场不均匀的抵抗能力仅停留在编码方向的一阶磁场不均匀,且间接维自旋回波演化引入了更多的横向弛豫衰减,降低了灵敏度.本课题组[25]提出了非对称编解码方法,避免了自旋回波演化,提高了序列的灵敏度;同时,借助3轴同时施行编解码的方式,将超快速方法对磁场的抵抗能力拓展为3个正交方向的一阶磁场不均匀.本课题组[11]提出的UFSECSY和UFSETOCSY方法也能在线性不均匀磁场下单扫描获得高分辨自旋回波相关谱(spin-echo correlated spectroscopy,SECSY)和自旋回波TOCSY(spin-echo TOCSY,SETOCSY).该方法在采样期前将不同空间位置上不均匀磁场的影响通过自旋回波的方式消除,而在采样期将线性不均匀磁场导致的回波位置线性倾斜通过后期数据处理进行校正.因为该方法的间接维为化学位移差信息,且关于零频中心对称,所以通过只采样间接维谱宽的一半可降低SPEN的谱宽要求,同时可以提高谱间接维的分辨率,得到半自旋回波相关谱(half-SECSY)和半自旋回波全相关谱(half-SETOCSY)的谱图,这些谱图通过数据重建可以转换为常规的COSY和TOCSY图.图4给出了不均匀磁场下采用该方法获得的γ-氨基丁酸和谷氨酰胺混合物的COSY,采样时间120 ms.作为对比,图4也给出了均匀磁场下和同一个不均匀磁场下该混合物的常规COSY,每个谱的采样时间是27 min.可以看出,SPEN方法不仅极大地缩短了采样时间,而且可以消除磁场不均匀的影响,得到高分辨谱图.
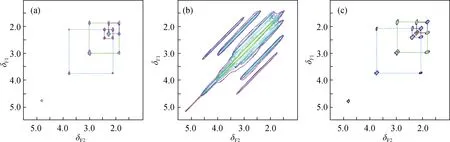
(a)均匀磁场下常规COSY谱;(b)不均匀磁场下常规COSY谱;(c)不均匀磁场下SPEN half-SECSY重建的COSY谱.
如何实现任意不均匀磁场下超快速SPEN高分辨谱是需要解决的一个问题.Pelupessy及其合作者[26]提出了通过追踪J偶合连接的自旋进动频率差并进行SPEN,在未知不均匀磁场下实现高分辨二维谱的获取,然而该谱图的直接维为化学位移差信息,无法直接得到化学位移信息,且孤立自旋不能被检测到.借鉴Pelupessy等获得高分辨谱的思路,本课题组[27]提出了超快速获得不均匀磁场下高分辨HSQC、HMBC和异核J分解谱的方法,不过只有异核J分解谱方法适用于任意不均匀磁场,HSQC和HMBC方法仍只适用于一维线性不均匀磁场.本课题组[28]还提出了一种基于反k空间的校正方法,该方法不需要改变原有的脉冲序列设计,只需要在新的数据空间即反k空间进行相位和幅度校正,就可以改善谱图的分辨率、信噪比及线型.反k空间校正方法适用于大部分超快速SPEN方法,不需要预先获得场图就能消除不均匀磁场对超快速谱的影响.
分子间多量子相干(intermolecular multiple-quantum coherence, iMQC)源于分子间的偶极相互作用,被广泛应用于在不均匀磁场下获取高分辨谱[29].然而,iMQC方法只能在间接维获取高分辨信息,因而要在不均匀磁场下获取高分辨一维谱,需要进行二维谱实验,为了获取高分辨二维谱,需要进行三维谱实验,以此类推,这导致实验时间成数量级增长.将SPEN技术与iMQC技术结合可以快速获得不均匀磁场下高分辨谱.本课题组提出了一种基于恒时相位调制SPEN的超快速分子间零量子相干(intermolecular zero-quantum coherence, iZQC)方法,该方法能够单次扫描获得二维iZQC谱.由于iZQC信号固有的对不均匀磁场不敏感,在演化期使用恒时相位调制,可以直接获得不受非均匀线宽增宽影响的一维去偶质子谱.通过在编码期编码iZQC信号,检测期施加J偶合检测模块,建立了iZQC相干转移结合SPEN的不均匀磁场下超快速高分辨二维J分解谱方法[30].与Pelupessy等[26]提出的方法相比,本课题组的方法能直接保留化学位移和J偶合裂分信息,且可检测孤立自旋.然而,该方法获得不均匀磁场下高分辨谱需要2次扫描.为此,本课题组进一步提出了一种不均匀磁场中单扫描高分辨J分解谱方法(single-scan high-resolutionJ-resolved spectroscopy,SSHRJRES)[31].相对于需要2次扫描的iZQCJ分解谱方法[30],SSHRJRES方法的采样效率得到了提升,同时,该方法将分子间双量子相干(intermolecular double-quantum coherence, iDQC)信号作为测量信号,信号强度更强.由于iZQC信号灵敏度低,为改善SPEN iMQC高分辨谱的信噪比,本课题组[32]还设计了基于分子间单量子相干(intermolecular single-quantum coherence, iSQC)的SPEN脉冲序列,用于快速获得高分辨一维NMR谱和二维COSY.以上方法均基于同核iMQC,溶剂和溶质之间的化学位移差会影响溶剂自旋的选择性激发,从而限制克服不均匀磁场获得高分辨谱的能力[29].为此,本课题组[33]提出了一种基于异核iZQC和SPEN技术的方法,既避免了同核iMQC方法激发溶剂时对溶质自旋的干扰,又可以省去溶剂峰信号压制模块,可以在未知磁场空间分布情况下超快速获取同核二维J分解谱.
在三维谱方面,本课题组[34]提出了利用iMQC和SPEN在未知空间分布的磁场下获取高分辨三维谱的方法,其中二维为高分辨异核相关信息,另外一维为J偶合信息.本课题组在高分辨同核二维J分解谱[30]和三维J分解相关谱[20]的基础上,设计了iZQC序列来快速得到高分辨同核三维JCOSY和JTOCSY,前者能同时得到高分辨COSY和J分解谱,后者能同时得到高分辨TOCSY和J分解谱[35].
2.3 不稳定磁场下超快速SPEN高分辨NMR波谱方法
NMR实验通常要求静磁场强度的短时稳定性达到1×10-9量级,并且长时间内无磁场漂移.只有在这种磁场环境下,化学位移和J偶合信息才能得以区分,从而获取分子结构信息.然而,在阻抗和阻抗-超导混合磁体下,难以实现均匀稳定的磁场,因而难以获得传统的高分辨NMR谱.Shapira等[36]利用SPEN在美国强磁场中心25 T Keck阻抗磁体内获取了一维和二维谱图,Pelupessy等[26]基于J偶合自旋相干转移的SPEN脉冲序列可在不均匀度1×10-3T/cm和漂移慢于2 Hz的磁场下获取高分辨NMR谱,然而这些方法对于短时不稳定磁场却无能为力.本课题组提出了将iZQC信号进行SPEN,同时使用J偶合检测模块进行空间解码的超快速方法,在不均匀不稳定磁场下获得了高分辨一维NMR谱[37].该方法不仅适用于长时漂移场也适用于短时漂移场.
2.4 SPEN NMR波谱方法应用
SPEN NMR已经在很多实验时间要求严格的研究中得以运用,例如蛋白质折叠[38]、实时监测化学反应和动力学过程[39-41]、生物组织成分定域谱分析[42]、实时液相色谱分离产物鉴定[43]等.本课题组还将结合了iMQC的SPEN技术应用于存在场不均匀性的鱼类及其副产品[44]以及酸奶、番茄酱等黏稠液体食品的成分检测[45],这样检测时不会对样品造成侵害性损害,也无需进行均匀磁场和样品预处理,节约时间.
3 超快速SPEN MRI方法及其应用
2005年,Frydman课题组[3]提出SPEN MRI方法.SPEN MRI是在EPI的基础上提出的一种超快速成像方法.SPEN MRI和EPI均采用快速切换的梯度场进行连续采样,因此二者的采样时间相当.与EPI不同的是,SPEN MRI采用chirp脉冲进行激励,从而产生一个特殊的二次相位调制.该二次相位调制使得SPEN MRI具备了一系列新的特性,例如对不均匀磁场和化学位移伪影良好的抵抗性、灵活小视野(reduced field-of-view, rFOV)成像采样等.根据稳定相位近似定理,直接对SPEN MRI信号求模即可获得MRI图像.然而,由此得到的SPEN MRI图像的空间分辨率低于相同情况下得到的EPI图像,因此需要进行超分辨率(super-resolved, SR)重建.本节将介绍SPEN MRI方法,包括SPEN图像的SR重建、rFOV成像、不均匀磁场下高分辨成像、非笛卡尔采样、三维SPEN MRI,并介绍相关典型应用.
3.1 SPEN MRI图像重建方法
为了提高SPEN MRI的空间分辨率,2010年Frydman课题组[7]提出了SR重建的概念.SR重建利用SPEN相邻采样点之间的冗余信息,不增加采样点数即可得到与传统FT方法相比拟的空间分辨率.早期SR重建采用共轭梯度法(conjugate gradient, CG)[7],通过求解一个线性方程组来获得SR图像.该方法虽然能够有效提高SPEN MRI图像的空间分辨率,但由于系数矩阵条件数不稳定,重建图像易受噪声或伪影的影响.本课题组针对SPEN采样信号的特点提出了部分FT(partial FT,PFT)重建算法[46]和去卷积算法(deconvolution algorithm)[47],这两种算法无需求解线性方程组,不受条件数的影响,具有良好的鲁棒性,而且这两种算法无需迭代即可重建出SR图像,大大提高了重建速度.然而,当沿着SPEN维的采样率不满足奈奎斯特采样定理时,上述方法都会在重建图像中引入混叠伪影.为此,本课题组进一步提出了一种结合随机采样、奇异值分解(singular value decomposition,SVD)和压缩感知(compressed sensing, CS)的方法来减轻这种混叠伪影,提高图像质量[48].通过对SPEN MRI在欠采样情况下的点扩散函数(point spread function)的分析,本课题组发现,SPEN MRI在SR重建之后产生的每个混叠伪影都有一个与二次相位有关的额外相位.利用这个额外的相位,可以在不损失空间分辨率的情况下移除混叠伪影.此外,通过预先提取边缘伪影的信息制作加权矩阵,结合CS重建可以有效去除边缘伪影.本课题组将这种重建算法命名为SEED(super-resolved enhancing and edge deghosting)[49],该算法可以恢复出理论上最优的空间分辨率.图5给出了采用不同MRI序列和重建方法获得的活体鼠脑的轴向面和矢状面实验结果,以多扫描梯度回波序列结果(Multi-scan)为参考.从图中可以看到,EPI图像受不均匀磁场影响发生明显畸变(如箭头所指),而SPEN MRI可以有效减轻不均匀磁场引起的畸变.从放大区域可以看到,SEED算法重建结果的分辨率优于EPI和基于CS混合(Hybrid)重建方法[48]获得的结果.
3.2 rFOV SPEN MRI方法
SPEN MRI中chirp脉冲的边带选择特性赋予了其rFOV成像的能力[46,50].Frydman课题组[51]提出了一种rFOV成像方法,采用多维激发脉冲实现感兴趣区域(region of interest, ROI)的选择成像.本课题组提出沿SPEN方向进行rFOV成像,提高了图像的分辨率和抑制不均匀磁场的能力[46].然而,当成像视野变小时,所用的编码和解码梯度变大,这将导致高噪声和低信噪比.此外,该方法一次激发只能对单一的ROI进行rFOV成像.因而,本课题组进一步提出了一种灵活的rFOV成像方法[52],与上述固定的rFOV成像方法相比,该方法不仅可以获得更好的成像效果,而且单次激发即能获取视野内多个分立ROI的rFOV图像,可应用于一些磁化非均匀性较强的组织和器官的成像,亦可应用于分立器官和肢体的成像,提高成像效率.将该方法的90° chirp脉冲换为幅值调制的chirp脉冲,可选择激发ROI内的核自旋,从而获得重点关注区域的rFOV图像,不仅继承原方法的优点,而且可以减小特异吸收率(specific absorption rate, SAR)[53].
3.3 不均匀磁场下SPEN MRI方法
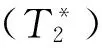
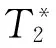
最近,Zhang等[58]提出了利用交叉SPEN(cross-term SPEN,xSPEN)的单扫描超快速方法,该方法可以单次扫描获取抗拒不均匀磁场影响的无扭曲和伪影的图像.xSPEN技术不同于以往为了获取某一个维度的图像,通过在该维度使用梯度读出k空间或者位置空间信息,而是在编码期通过添加一个辅助维与成像维组成xSPEN,在采样期仅仅在辅助维的作用下获取成像维的信息.
3.4 非笛卡尔采样SPEN MRI方法
常规的SPEN MRI都在笛卡尔采样下进行.由于欠采样和快速梯度切换,SPEN MRI图像容易受到混叠伪影的影响[48].与笛卡尔采样相比,非笛卡尔采样能够有效抵抗混叠伪影,而且采样效率高,对硬件要求低[59].Frydman课题组[54]证实了SPEN MRI非笛卡尔采样的可行性.他们采用一个90°硬脉冲结合两个180° chirp脉冲对自旋信号进行编码,在采样阶段采用等密度螺旋采样对信号进行解码.然而,由于没有进行SR重建,其图像空间分辨率很低.Layton等[60]证实了增加ROI的采样密度可以提高图像的空间分辨率.STEREO(steering resonance over the object)[61]采用多维SPEN策略,在激励阶段激发一个螺旋的区域,在采样阶段采用相同的螺旋轨迹对信号进行重聚.由于每一个采样信号都是全重聚的,因此该方法对不均匀磁场具有非常好的抵抗性.Wang等[62]证实非线性相位编码结合非笛卡尔采样可以增强图像的质量.本课题组提出了非笛卡尔变密度采样策略,其解码梯度通过最优化算法自动生成[63].通过调整采样轨迹,使采样点集中在ROI中,由此获得具有更高空间分辨率和信噪比的图像.相应地,本课题组建立了有效的SR重建算法,提高了非笛卡尔采样下SPEN MRI的图像质量.
3.5 三维SPEN MRI方法
单扫描SPEN MRI既具有EPI良好的时间分辨率,又可以有效抑制由于磁场不均匀及化学位移伪影造成的图像畸变.然而,SPEN方法使用的chirp脉冲SAR较大,进行单层扫描没有太大影响,但是对多层成像,过大的SAR将限制其临床应用[55,64].为了减少SAR,Frydman课题组[55]提出了一种多层SPEN MRI方法.该方法通过一个90°硬脉冲结合一个180° chirp脉冲实现全局激发、整体SPEN,然后将编码信息存储,最后分层解码采样.因为整个序列仅使用一个180° chirp脉冲,有效降低了SAR.然而这种扫描方式带来另一个问题,即由于纵向弛豫效应导致的SPEN信号衰减.信号的衰减随着成像层数的增加越来越严重,这限制了该方法的扫描层数.为了同时解决传统SPEN多次扫描带来的高SAR问题,以及上述多层MRI方法的信号衰减问题,本课题组提出了分段SPEN(segmented SPEN, SeSPEN)多层MRI方法[65].该方法通过分段激发、分段编码的方式,有效降低了SAR,缓解了由纵向弛豫效应造成的信号衰减.SeSPEN MRI可以通过成像系统的“array”功能排列每一段的频率偏置,从而选择不同段的位置以及设置不同段的激发顺序.与此同时,还可以根据实际情况,灵活设置每一段的厚度以及段内的成像层数.在此基础上,本课题组提出了多回波同时重聚SeSPEN(multi-echo SeSPEN,ME-SeSPEN)多层MRI方法[66].ME-SeSPEN方法利用两个90°层选射频脉冲激励多个不同层的信号,该信号由不同的散相梯度调制,在同一读出梯度的不同时刻重聚.当采集相同层数时,ME-SeSPEN比SeSPEN需要进行梯度切换的次数少,因此扫描时间缩短;此外还将螺旋采样引入SeSPEN MRI,并针对该采样方法建立了去卷积SR重建算法.螺旋采样在采样阶段使用连续振荡的梯度,与笛卡尔采样方法相比,梯度切换的难度降低,图像信噪比更高,涡流效应对图像的影响减弱.
3.6 SPEN MRI方法应用
超快速MRI方法在一些需要高时间分辨率的应用中发挥着重要的作用,例如功能MRI、自由呼吸成像和扩散张量成像.SPEN MRI由于其超快速和良好的抗磁场不均匀性能,自提出以来,已经在许多方面得到应用,例如小鼠胎盘发育研究[67]、人体乳腺[68]以及妊娠小鼠发育[69]的扩散成像、横向弛豫时间T2定量成像[70]、水脂分离和谱成像[71-75]、化学交换饱和转移(chemical exchange saturation transfer, CEST)成像[76-77]、功能MRI[78-79]等.本课题组在水脂分离成像和CEST成像[77]方面开展了相关应用研究.
MRI通常检测的是氢质子所产生的信号,而许多分子内都含有氢质子,如水和脂肪.大部分情况下,人们感兴趣的是来自水中氢质子所产生的信号,但是由于脂肪的纵向弛豫时间较短,它在许多成像结果中显示为高信号.强脂肪信号的存在会影响医生对水信号的判断,从而影响临床诊断,因而有必要对水、脂信号进行分离.已有的水脂分离技术大多是基于多扫描成像序列,采样时间比较长,不利于临床应用.本课题组将SPEN MRI应用于水脂分离成像,并提出一种结合了化学位移先验信息的水脂分离SR重建方法来得到高质量的水脂分离图像[74].本课题组还针对基于SPEN MRI的单回波水脂分离技术提出一种新的求解算法,有效提高图像的清晰度、信噪比及对比度噪声比,并使水脂分离的结果更加可靠[75].
CEST能够用于定量表征代谢物质子和水质子之间的化学交换,已经成功应用于许多MRI中,如体内成像、标记细胞成像和代谢物水平测定.然而,CEST MRI需要采集多个不同饱和频率点下的饱和图像以绘制出Z谱,从而计算出CEST对比图像,因此CEST成像采样时间长,限制了其活体应用.本课题组探索了基于单扫描SPEN MRI的快速CEST成像,并成功应用于肿瘤鼠脑NOE成像[76].本课题组还将SeSPEN MRI应用于CEST成像,实现了单扫描多层CEST成像,极大缩短了采样时间[77].
4 总结与展望
NMR波谱和成像技术在化学、材料、医学、生命科学等领域都具有重要的应用价值.提高采样效率、缩短采样时间一直是NMR发展的重要挑战.SPEN技术不仅可用于快速获取NMR谱信息,也可用于快速获取MRI信息,甚至谱成像信息.近年来SPEN技术获得了长足的发展,为NMR更广泛的应用提供了更多更强的技术保障.SPEN技术有其独特的优越性,也有其局限性.对SPEN NMR而言,其超快速采样是以牺牲信噪比为代价的,因此必须在加速采样与信噪比之间进行权衡.对于低浓度样品,SPEN NMR需要借助超极化等技术增强信号强度[17,80];对SPEN MRI而言,其抗不均匀磁场和化学位移伪影能力与信噪比是矛盾的,因此SPEN MRI的应用需要在不均匀磁场和化学位移伪影抵抗性与图像质量之间做一个较好的权衡.对于腹部等具有较低信噪比的成像区域,SPEN MRI的应用仍然面临极大的挑战.随着超极化、并行成像等信号增强技术和深度学习等谱图和图像后处理技术的应用和发展,相信SPEN低信噪比问题将有望得到克服,SPEN技术必将在其优势领域发挥作用.
