累及椎体中1/3的急性骨质疏松性骨折经皮椎体成形术后骨水泥分布与疗效的关系
2021-04-13白露露郝定均王文涛都金鹏李恒张子龙王宇航
白露露 郝定均 王文涛 都金鹏 李恒 张子龙 王宇航
随着世界人口老龄化的来临,每年大约发生1 400 多万例骨质疏松性椎体压缩骨折(osteoporotic vertebral compression fracture,OVCF)[1]。OVCF 常导致胸背部持续疼痛、活动障碍,严重降低病人的生活质量。其中大部分病人可通过卧床休息、口服止疼药物、佩戴支具局部制动等方法保守治疗,但也有部分病人通过保守治疗无法得到有效缓解,疼痛和功能障碍持续存在[2]。经皮椎体成形术(percutaneous vertebroplasty,PVP)是一种经皮穿刺将聚甲基丙烯酸甲酯(PMMA)骨水泥注入到骨折椎体内的微创手术方法,常用于经保守治疗后症状未缓解的急性OVCF,可快速减轻病人疼痛等症状,改善功能障碍[3]。
PVP治疗OVCF 的主要机制之一是骨水泥凝固后提高脊柱的稳定性,降低骨折端微动,从而加速骨折愈合[4]。目前,大部分研究集中在骨水泥注入量、注入方式及PVP 术后并发症等方面,对于骨水泥分布与疗效的相关研究较少。有研究发现骨水泥分布可能是预测OVCF单侧经皮球囊扩张椎体后凸成形术(percutaneous kyphoplasty,PKP)重建效果的潜在指标[5],还有研究表明PKP 术后双侧骨水泥融合分布的病人较分离分布的病人获得更快的疼痛缓解等效果[6]。然而,针对急性OVCF 且骨折线位于椎体中1/3的病人接受PVP 术后骨水泥的差异分布与临床结果的关系仍有待阐明。本研究聚焦于这一问题,旨在探讨骨水泥的分布差异与疗效的关系及近期疗效的影响因素,为其治疗提供依据。
资料与方法
一、纳入标准与排除标准
纳入标准:①符合急性OVCF 的诊断标准且经保守治疗2~4 周症状无明显缓解的病人;②术前经双能X线吸收测定法测量骨密度,并确诊为“骨质疏松症”(腰椎平均骨密度T值<-2.5 SD);③MRI提示骨折为急性期(<6 周)OVCF 且骨折线位于椎体中1/3的单一胸腰椎骨折;④术前完善检查且骨质疏松性胸腰椎骨折严重程度评分(osteoporotic throcacolumbar injury classification and severity score,OTLICS)≥5分,接受PVP手术治疗;⑤随访资料完整。
排除标准:①非骨质疏松性骨折,如病理性骨折等;②陈旧性骨折,如Kümmell 病等;③继发性骨质疏松;④合并强直性脊柱炎、椎管狭窄等疾病:⑤资料不完整或失访者。
二、一般资料
回顾性收集西安交通大学附属红会医院2016年1月1日至2016年12月31日急性OVCF且骨折线位于椎体中1/3而接受PVP 手术的病人资料。根据纳入标准及排除标准,本研究共纳入92 例,均为胸腰段单一椎体骨折,其中T108例,T1112例,T1225例,L129例,L218例。所有病人术前均有剧烈的腰背部疼痛且均不伴有神经功能损伤。
根据术前及术后影像资料判断骨折线位置并评估骨水泥与骨折线的差异分布,将研究对象分为两组。骨水泥与骨折线相对位置良好的43 例纳入A组,其中男14例,女29例,年龄为(65.4±5.7)岁,身体质量指数(body mass index,BMI)为(23.8±3.1)kg/m2,病程为(14.6±10.0)d,骨密度T值为(-3.5±0.5)SD,骨水泥注入量为(4.3±0.5)mL。骨水泥与骨折线相对位置较差的49例纳入B组,其中男15例,女34例,年龄为(66.1±5.2)岁,BMI 为(24.7±2.6)kg/m2,病程为(16.4±9.5)d,骨密度T 值为(-3.6±0.6)SD,骨水泥注入量为(4.1±0.6)mL。两组间年龄、性别、BMI、骨密度、骨水泥注入量等指标比较,差异均无统计学意义(P均>0.05)。
三、手术方法
所有手术均由我院经验丰富的副主任医师完成。病人取俯卧位,局部麻醉,所有病人均采取单侧经皮穿刺。穿刺点位于骨折椎体椎弓根投影外侧缘9 点或3 点钟,经椎弓根穿刺进针到达椎体前缘,拔出针芯,置入导丝,循导丝置入工作通道至椎体后缘,取出导丝,用环钻钻孔达椎体前方。然后混匀骨水泥,待骨水泥“拉丝期”时,首先将少量骨水泥(约0.5 mL)缓慢注入椎体前方,然后将通道后退约0.3~0.5 cm,再缓慢注射骨水泥(约0.5 mL),以此类推,每次将通道后退0.5 cm 后再注入0.5 mL 骨水泥,待通道后退至椎体后1/3 时,骨水泥应缓慢注入且每次注入骨水泥量不超过0.5 mL,全程透视监测。骨水泥注射完毕后,旋转但不拔出工作管道,待骨水泥固化后拔出工作管道,无菌敷料包扎伤口,记录骨水泥使用量。
病人术后2 h 内平卧,2 h 后允许佩戴胸腰部支具适当下床活动。术后24 h内以卧床休息为主。所有病人术后均予以抗骨质疏松药物(依降钙素注射液,20 U/次,每周1 次;骨化三醇,0.25 μg/次,每天2次;阿仑磷酸钠10 mg/d,每天1次)治疗。
四、骨折线及骨水泥分布情况的评价方法
以椎体后缘高度画出椎体三等分线,根据术前X 线片、CT、MRI 检查确定骨折线累及位置(图1)。根据术后正侧位X 线和CT 检查判断骨水泥的差异分布,将骨水泥集中分布在椎体中1/3(正侧位X 线片及CT检查示骨水泥填充范围超过50%)定义为骨水泥分布与骨折线相对位置良好,反之,则定义为骨水泥分布与骨折线相对位置较差。
五、功能评价
所有评估均由同一研究助理独立完成,记录术前、术后1 d及末次随访时的疼痛视觉模拟量表(visual analogue scale,VAS)评分、Oswestry 功能障碍指数(Oswestry disability index,ODI)、健康调查简表(the MOS item short from health survey,SF-36)评分;测量术前、术后1 d及末次随访时的椎体前缘高度及Cobb角,并记录术后相关并发症发生情况。
六、统计学方法
采用SPSS 18.0统计软件(IBM公司,美国)进行分析。正态分布的计量资料以均数±标准差(±s)表示,多组间比较采用方差分析,两组间比较采用独立样本t检验;计数资料以率表示,采用χ2检验。采用多元线性回归分析术后1 d时的症状改善(术后VAS评分-术前VAS评分)的影响因素。以P<0.05为差异有统计学意义。
结 果
一、功能评分的比较
A组和B组的随访时间分别为(41.4±3.6)个月、(40.8±3.2)个月,组间比较,差异无统计学意义(P>0.05)。所有病人术后1 d 及末次随访时的VAS 评分、ODI、SF-36 评分均较术前得到明显改善(P 均<0.05);但在术后1 d 时,A 组的VAS 评分明显低于B组,两组比较,差异有统计学意义(P<0.05)。末次随访时,两组病人的VAS评分、ODI、SF-36评分较术后1 d时有改善,但差异无统计学意义(P均>0.05),且组间比较,差异无统计学意义(P均>0.05)。见表1。
二、影像学比较
所有病人术后1 d 及末次随访时椎体前缘高度均较术前显著提高,Cobb 角均较术前显著降低,与术前比较,差异均有统计学意义(P均<0.05)。但组间比较,差异均无统计学意义(P均>0.05)。见表2。
术后两组病人均无伤口感染、肺部栓塞等严重手术并发症。A 组出现5 例(11.6%)骨水泥渗漏,B组出现2 例(4.1%)骨水泥渗漏;其中渗漏到椎旁6例、椎间隙1例,所有病人均无症状。末次随访时A组出现1例邻椎骨折,B组出现6例邻椎骨折。典型病例影像学资料见图2、3。
三、症状改善程度的多元线性回归分析
骨水泥与骨折线相对位置、病程与术后1 d时症状改善(术后VAS-术前VAS)程度密切相关(P<0.05)。共线性诊断结果表明2个变量之间无多重共线性。见表3。
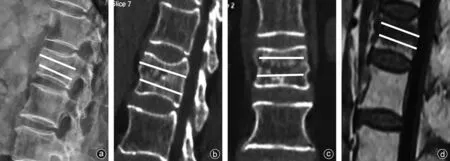
图1 a~d:术前X线片、CT、MRI均显示骨折线位于椎体中1/3
表1 两组病人术前术后的VAS评分、ODI、SF-36评分比较(±s)

表1 两组病人术前术后的VAS评分、ODI、SF-36评分比较(±s)
注:与同组术前比较,*P<0.05
组别A组B组t值P值例数43 49 VAS(分)ODI(%)SF-36(分)末次随访32.2±1.6*31.8±1.5*1.479 0.143--术前8.1±0.9 7.8±0.8 1.199 0.234术后1 d 2.2±0.1*2.8±0.9*-2.566 0.012末次随访2.3±0.1*2.7±0.9*-1.571 0.120术前40.1±3.4 39.1±3.1 1.362 0.177术后1 d 8.1±0.9*7.9±0.9*1.161 0.249末次随访7.9±1.2*7.7±1.1*0.538 0.592术前23.3±2.8 24.1±2.6-1.404 0.164术后1 d 32.3±1.8*31.7±1.5*1.836 0.070

图2 病人,女,65岁,无明显诱因致腰背部疼痛2 d,术前病史、体格检查及影像学检查提示急性OVCF,行PVP治疗,术后症状明显缓解 a~e:术前正侧位X线片、CT、MRI示骨折线累及椎体中1/3的急性OVCF;f~j:术后1 d的X线片、CT示骨水泥分布与骨折线相对位置良好;k、l:末次随访正侧位X线片示无明显塌陷
表2 两组病人术前术后的椎体前缘高度、Cobb角比较(±s)

表2 两组病人术前术后的椎体前缘高度、Cobb角比较(±s)
注:与同组术前比较,*P<0.05
组别A组B组t值P值例数43 49椎体前缘高度(mm)Cobb角(°)末次随访9.4±1.2*9.8±1.2*-1.552 0.124--术前16.6±1.4 16.1±1.5 1.493 0.139术后1 d 20.7±1.6*20.4±1.5*0.764 0.447末次随访20.5±1.6*20.4±1.4*0.647 0.519术前18.6±2.7 19.2±2.8-1.007 0.316术后1 d 9.3±1.3*9.7±1.2*-1.786 0.077

图3 病人,女,73 岁,无明显诱因致腰背部疼痛15 d,术前病史、体格检查及影像检查提示急性OVCF。完善相关检查,排除手术禁忌证,行PVP治疗,术后症状明显缓解 a~e:术前正侧位X线片、CT、MRI示骨折线累及椎体中1/3的急性OVCF;f~j:术后1 d的X线片、CT示骨水泥分布与骨折线相对位置较差;k、l:末次随访正侧位X线片未见明显椎体高度降低
讨 论
椎体成形术是一种针对急性OVCF病人的安全有效的微创手术治疗方法,具有快速缓解疼痛和临床疗效满意等优点[7],最早于1987年由法国医生应用于椎体骨折的治疗[8],通过术中在透视状态下向骨折椎体内灌注骨水泥,使骨折得以稳定,达到治疗效果。但既往有研究发现OVCF病人经PVP手术治疗后,病人在疼痛缓解等方面较对照组并未获得更大的获益[9],产生上述结果的可能原因是研究者将具有轻微临床症状的病人及一部分由陈旧性椎体压缩性骨折导致顽固性疼痛的病人纳入并采取手术治疗,这与我们临床工作中的手术指征有较大差异。此外,对照组中对骨折椎体使用的局麻药物对比治疗也可能是疼痛改善的原因之一。本研究中,我们分析了PVP 对急性OVCF 病人的疗效,结果表明:PVP 可明显缓解急性OVCF 病人的症状,改善活动能力,重建椎体稳定性,减轻脊柱后凸畸形及椎体的压缩程度,提高病人生活质量。
进一步分析发现所有研究对象在术后1 d 和末次随访时VAS 评分、ODI、SF-36评分及Cobb 角均较术前得到明显好转,但A 组病人在术后1 d 时VAS评分较B 组病人改善明显,差异有统计学意义(P<0.05),说明骨折线位于椎体中1/3时,骨水泥差异分布可能是影响PVP 术后短期疗效的影响因素。其原因可能有以下几点:首先,骨水泥分布良好时,可以充分弥散充填黏合断裂的骨小梁,增加骨折椎体的即时稳定性,承担部分轴向应力,减少断裂骨小梁对神经末梢的刺激,从而使得疼痛缓解[10]。其次,骨水泥分布与骨折线相对位置较差时,骨折椎体内仍有部分断裂骨小梁存在,骨折椎体骨折线位置仍存在相对位移,持续刺激神经末梢而产生术后持续的胸腰背部疼痛。最后,骨水泥与骨折线相对位置较差时,可能会造成椎体的负载偏向转移,降低骨折椎体的稳定性导致椎体内骨小梁的微动,也可能是引发术后持续背部疼痛的原因之一[11]。我们还发现在末次随访中,B组VAS评分高于A组,可能原因为部分病人术后发生不明原因的残余疼痛并持续存在,且本研究样本量较小,可能对结果产生偏倚;但两组病人比较,差异并无统计学意义(P>0.05),我们认为在末次随访时两组病人骨折均获得良好的愈合。此外,多元线性回归分析显示骨水泥与骨折线的相对位置、病程与病人术后1 d时症状迅速改善密切相关,可能与骨折急性期椎体内部骨小梁破坏,骨折线周围的血肿形成与吸收影响骨水泥在骨折线附近的弥散相关。骨水泥在骨折椎体分布的影响因素有很多,如骨质疏松程度、压缩程度、骨水泥注射压力与速度、穿刺角度等均可能影响骨水泥分布。在临床工作中,我们发现在某些情况下,即使工作套管精确穿刺到达椎体骨折线然后不断增加注射骨水泥量,骨水泥与骨折线的位置仍然较差,其原因可能是急性(<6 周)OVCF 的病人处于骨折愈合过程中的血肿机化期(2~3周)和血痂形成期(4~6周),随着发病时间的延长,骨折线周围的血肿机化和血痂形成可能会影响骨水泥的弥散,使骨水泥在骨折线上分布不良,短期临床结果较差。骨水泥的合理分布对急性OVCF 病人的临床效果至关重要。He 等[12]发现骨水泥分布在预测病人疼痛缓解方面优于骨水泥体积。Lin等[5]采用双侧注射骨水泥,根据术后X线片将骨水泥分布形态分为骨水泥双侧融合型和双侧分离型,最终得出骨水泥双侧融合型病人术后疼痛缓解效果更好。邵珂等[13]发现术前骨折水肿信号的面积大小可能影响骨水泥的分布从而导致早期症状缓解程度的不同,因此要尽量使骨水泥均匀弥散。

表3 影响症状改善的多元线性回归分析结果
除此之外,在本研究中我们还发现末次随访时A 组出现1 例邻椎骨折,B 组出现6 例邻椎骨折。PVP术后邻近椎体再骨折是评价PVP疗效的一项重要依据,但邻椎骨折的发生可能受到多种因素影响,如病人的性别、年龄、BMI、邻近椎体的骨密度、术后活动能力,全身健康状况及骨水泥分布模式等。Tanigawa等[14]认为尽管PVP术后的骨水泥分布与近期的临床效果没有显著关系,但骨水泥呈团块状分布组较海绵状分布组再骨折的发生率更高,尤其是相邻椎体的骨折。Liebschner 等[15]通过试验得出,当骨水泥注入过多但不均匀分布时,虽然椎体的强度和硬度提高,但造成骨折椎体内应力传导不平衡,降低骨折椎体的稳定性,从而影响骨折的愈合,造成术后椎体的再塌陷。Lin 等[16]也分析了PVP 术后发生再骨折的影响因素,得出骨折椎体前缘高度恢复较好的病人,尽管术后临床结果更佳,但是也更容易发生再骨折。可能原因是PVP 术后,椎体的应力传导转移,使得骨水泥分布不均匀而未被填充的部分骨质应力骤增,从而增加椎体再骨折的风险。
本研究存在以下几个局限性。首先,本研究为回顾性研究,但我们术前、术后1 d 的VAS 评分、ODI、SF-36评分及影像资料均在病人住院期间由同一科研助理评估并记录,且术后病人获得长期的随访。其次,我们的样本量是从单一中心获取且数量相对较少,可能对结论产生偏倚,因此需要进行大数据的多中心研究以进一步支持我们的发现。另外,骨水泥分布与骨折线的相对位置的定义可能存在多种方法且本研究结论缺乏相关生物力学、生物材料学方面的结果支持,后期仍需对骨水泥分布与骨折线的相对位置的定义方法进一步深入研究并进行相应的基础实验研究观察与论证。最后,虽然我们通过研究发现两组OVCF病人的症状和功能得到巨大的改善,但如何使骨水泥更充分地分布在骨折线内仍然是我们面临的挑战。