侧前方入路椎体次全切除固定融合术治疗陈旧性骨质疏松椎体压缩性骨折继发胸腰椎后凸畸形
2021-04-08郭昭庆李危石陈仲强孙垂国钟沃权孙卓然
姜 宇 郭昭庆 李危石 陈仲强 齐 强 曾 岩 孙垂国 钟沃权 孙卓然
(北京大学第三医院骨科 脊柱疾病研究北京市重点实验室,北京 100191)
随着年龄的增长,骨质疏松症使人体骨组织结构退化、骨量降低、骨脆性增加。骨质疏松椎体压缩性骨折(osteoporotic vertebral compression fracture,OVCF)好发于胸腰椎,是骨质疏松症最严重的临床表现之一[1]。OVCF在保守治疗过程中可以发生椎体骨折不愈合(Kummell病)或畸形愈合,进而导致骨折椎体高度降低,继发形成胸腰椎局部后凸畸形,引起明显的腰背部疼痛[2]。反复出现的腰背部疼痛使躯干前倾以降低疼痛,造成胸腰椎后凸畸形进展加重,甚至局部后凸畸形直接牵拉或压迫脊髓导致出现神经损害,使生活质量严重下降。椎体成形术(percutaneous vertebroplasty,PVP)、椎体后凸成形术(percutaneous kyphoplasty,PKP)在治疗新鲜OVCF和预防脊柱局部后凸畸形方面获得较好的临床疗效,具有操作时间短,术中出血少等特点,但是陈旧性OVCF,尤其是骨折椎体后壁破裂塌陷或椎体已压缩愈合成扁薄楔状,前者可以导致骨水泥渗漏至椎管内造成脊髓受压损伤,后者可继发形成僵硬的局部后凸畸形,PVP与PKP难以有效撑开椎体矫正后凸[3,4]。后路截骨矫形手术可以获得较高的畸形矫正率,但是陈旧性OVCF继发胸腰椎后凸畸形患者大多高龄且合并骨质疏松症,后路手术需多节段固定分担椎弓根螺钉应力或者采用骨水泥强化螺钉,手术时间延长,出血量较多,并发症增多[5, 6]。对于部分骨折椎体直接压迫脊髓造成神经损害的病例,术中需要从侧后方进行非直视下神经减压操作,增加术中神经损伤的风险[7]。基于对以上不同术式特点的考虑,我院2004年5月~2016年6月采用侧前方入路手术治疗22例单节段陈旧性OVCF继发胸腰椎后凸畸形,现将手术特点与随访结果报道如下。
1 临床资料与方法
1.1 一般资料
本组22例,男9例,女13例。年龄54~76岁,(62.0±8.5)岁。5例无明确外伤史,17例有明确的外伤史,均为低能量损伤(滑倒、弯腰、搬重物、打喷嚏)。20例主诉腰背部疼痛,疼痛视觉模拟评分(Visual Analogue Score,VAS)为(5.7±2.3)分;2例表现为尿潴留。术前日本骨科学会 (Japanese Orthopedic Association,JOA)29分法(JOA-29)[8]为(14.1±5.2)分,Oswestry功能障碍指数 (Oswestry Disability Index,ODI)[9]为(47.0±18.7)%。发现骨折距离手术治疗的病程中位数9个月(6~36个月)。均为单节段椎体骨折,术前X线片与CT显示局部后凸顶点位于骨折椎体水平,其中T12椎体骨折10例,L1椎体骨折5例,L2椎体骨折5例,L3椎体骨折2例。术前后凸角(Cobb角)、腰椎前凸角(lumbar lordosis,LL)分别为29.4°±3.2°和31.0°±4.1°。11例合并神经功能损害,按照改良Frankel分级系统[9],5例D1级,5例D2级,1例D3级。骨密度(0.73±0.10)g/cm2,T=-3.1±1.0,符合骨质疏松症诊断。5例合并原发性高血压。既往史无特殊。
病例选择标准:①双能X线吸收测定法测量,T≤-2.5,诊断骨质疏松症;②轻微外伤或无外伤史致胸腰椎骨折;③CT显示为单节段椎体陈旧骨折或骨折不愈合;④MRI T2抑脂相除外新鲜椎体压缩性骨折;⑤规律服用抗骨质疏松药物超过半年,参加门诊末次随访;⑥胸腰椎局部后凸角度≥20°或椎体后壁破裂压迫脊髓或者神经根出现神经损害;⑦经过3个月保守治疗无效的顽固性腰痛。排除标准:①合并脊柱感染或脊柱肿瘤;②2个或以上节段出现骨折;③MRI T2加权相和抑脂像证实为新鲜骨折;④有脊柱手术史;⑤随访资料缺失。
1.2 方法
全麻后右侧卧位。透视确认骨折椎体节段和邻近的椎体,皮肤上标记受累椎体的前后边界和上下终板的位置。沿肋骨走行方向切口约8 cm。切开皮肤、皮下组织、背阔肌深层与前锯肌,显露并切除部分肋骨,注意保护肋间神经和肋间动脉。插入肋骨撑开器后沿胸膜后、腹膜外暴露至胸膜反折处,钝性分离软组织,显露责任椎体,插入克氏针并通过透视证实。L1以下节段通常需要分离膈肌,一般做半圆形切开而非沿直径切开,以避免膈疝或膈肌麻痹。钳夹或电凝椎体骨折侧方节段血管,显露并保护好椎体前方大血管,切除骨折椎体与相邻椎间盘,注意切除骨折椎体时松质骨出血情况。植入装有自体骨的钛网或人工椎体,选用侧方钛棒固定至相邻椎体,透视证实内固定位置满意后,逐层缝合切口。术中需注意陈旧椎体骨折部位与周围软组织是否有粘连,在分离椎体侧方节段血管时需使用纱布剥离子钝性分离钳夹或电凝止血,以防止进行椎体次全切除时突然大量出血。骨折椎体后壁因后凸压迫脊髓腹侧,直视分离椎体后壁时注意保护神经,向远离脊髓方向进行操作,避免神经损伤。术中如果发现壁层胸膜撕裂,用2-0抗菌薇乔缝线连续缝合修补胸膜,如果胸膜裂口较大,无法通过缝合修补,需在关闭手术切口时在同侧胸腔放置胸腔闭式引流管,降低术后出现血气胸的机率。
术中常规应用神经电生理监测,包括体感诱发电位(somatosensory evoked potentials,SEPs)和运动诱发电位(motor evoked potentials, MEPs),保护脊髓安全。麻醉中保持血压不低于90/60 mm Hg(1 mm Hg=0.133 kPa)。本组大多高龄患者,术中及术后需监测血红蛋白,及时输血及补液维持血压平稳,提供良好的脊髓血液灌注,防止脊髓缺血性损伤出现。术后常规预防应用抗生素24~48 h。术后第1天开始佩戴腰围进行床旁活动。切口引流量<50 ml/24 h可拔除切口引流管。术后均佩戴胸腰部支具至少3个月,口服抗骨质疏松症药物(碳酸钙片+骨化三醇+阿仑膦酸钠)至少6个月。按照术后3、12个月及末次随访门诊复查,复查手术部位及全脊柱正侧位X线片、CT和MRI。
1.3 观察指标
影像学观察指标:术前胸腰椎与全脊柱正侧位X线平片、CT(平扫+重建)、MRI(平扫+重建)和骨密度检查。应用影像归档和通信系统(Picture Archiving and Communication Systems,PACS)测量Cobb角(伤椎头端未受累椎体上终板延长线与尾端未受累椎体下终板延长线的夹角)、LL(第1腰椎上终板与第1骶骨上终板的夹角),CT观察手术节段植骨融合和内固定是否松动,MRI观察椎管内脊髓受压迫情况。
手术观察指标:手术时间(切皮开始至切口缝合结束)、术中出血量(手术记录单出血量)、围术期并发症(包括术中神经根损伤、硬脊膜撕裂、胸膜撕裂、血气胸、术后血肿、切口感染、脑脊液漏、神经症状加重、本次住院出现内科疾病如肺炎、低白蛋白血症等)。
功能评价指标:JOA-29、疼痛VAS评分、ODI、改良Frankel分级系统评估神经功能改善情况。
1.4 统计学处理
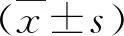
2 结果
22例术中神经电生理监测满意,均顺利完成手术,术后未出现神经功能受损加重。术中进行椎体次全切除,前柱使用钛网装入自体骨或人工椎体进行支撑。手术时间(199.1±50.4)min,术中出血量(793.2±479.4)ml。2例出现围术期并发症:1例在术中显露责任椎体时出现壁层胸膜撕裂,裂口长约2 cm,立即用2-0抗菌微乔缝线进行连续缝合修补壁层胸膜并覆盖肌肉软组织,术后未出现血气胸;1例术后第2天出现胸闷憋气症状,X线片示右侧胸腔出现少量胸腔积液,因积液量少,B超无法定位且未达到放置胸腔闭式引流标准,遂保守治疗,同时鼓励患者积极锻进行胸式呼吸锻炼呼吸肌,早期进行床旁活动,复查胸片患者胸腔积液已吸收,患者保守治疗满意后出院。术后住院时间(5.4±1.0) d。
术后即刻Cobb角与LL分别为19.5°±2.3°和30.4°±3.0°,Cobb角术后即刻较术前明显改善(P=0.000),见表1,手术平均矫正9.9°,后凸矫形率33.7%[后凸矫形率=术前Cobb角-术后Cobb角)/术前Cobb角];末次随访Cobb角和LL分别为25.8°±2.5°和30.5°±3.7°,Cobb角有丢失,较术前局部后凸改善不明显(P=0.056),LL较术前改善不明显(P>0.05)。末次随访CT未见内固定松动,通过CT矢状位重建可见植骨区骨性融合满意,见图1。3例末次随访CT上可见钛网或人工椎体较术后CT下沉,未诉腰背部疼痛。
22例术后平均随访96.3月(39~133个月),截至末次随访,均未发生远期并发症而进行二次手术治疗。末次随访腰背部疼痛VAS评分、JOA-29评分和ODI较术前明显改善(P=0.000),见表1。术前11例神经损害,改良Frankel分级为5例D1级、5例D2级、1例D3级,末次随访仅存在1例D2级、6例D3级,其中9例神经功能改良Frankel分级在术后至少提高1级(表2)。2例末次随访诉症状较术前有改善,但仍有腰背部疼痛。

图1 男,64岁,摔伤伴腰背部疼痛7个月,逐渐加重,无法久坐久站,腰背痛VAS 评分7分,平卧可缓解 A.术前腰椎侧位X线示T12椎体压缩骨折;B.术前MRI T2加权相示T12骨折椎体为低信号;C.术前MRI T1加权相示T12骨折椎体为等信号和低信号;D.术前MRI T2抑脂像示略高信号;E.术前CT矢状位重建示陈旧T12椎体骨折未愈合;F,G.术后即刻腰椎正侧位X线示内固定位置满意,已矫正局部后凸畸形;H~J.末次随访CT矢状位重建(H)与全脊柱正侧位X线(I、J)示内固定位置良好,植骨融合满意,钛网无下沉

表1 22例术前后影像学及症状评分比较
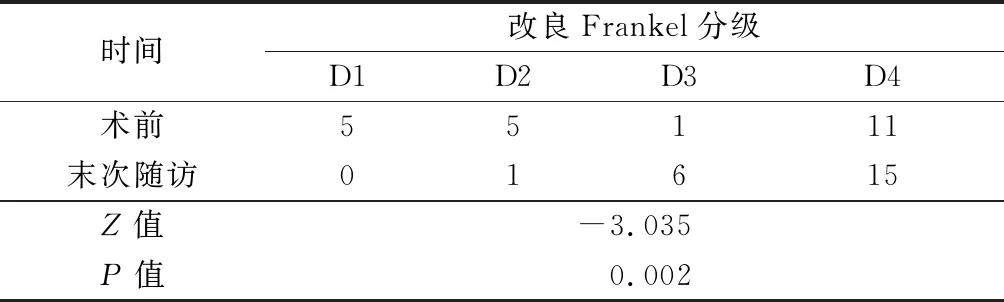
表2 22例术前后改良Frankel分级比较(n=22)
3 讨论
OVCF好发于胸腰椎,患者多高龄、椎体骨质疏松或合并内科疾病,保守治疗无效或不恰当的手术是形成陈旧性OVCF不愈合或继发局部后凸畸形的主要原因[3,5,7]。骨折椎体继发形成局部后凸畸形可直接压迫脊髓造成神经损害,部分患者出现腰椎代偿前凸或无法代偿进一步出现脊柱矢状位失平衡,以上特点为治疗陈旧性OVCF继发胸腰椎后凸畸形带来诸多挑战[4,5]。陈旧性OVCF继发胸腰椎后凸畸形通常需要手术治疗,手术指征包括:①腰背部疼痛保守治疗无效;②脊髓或神经根损伤;③胸腰椎后凸畸形进展;④骨折椎体不愈合形成假关节或骨不连[4~6,10]。
文献已报道多种治疗陈旧性OVCF继发胸腰椎后凸畸形的术式,包括PVP、PKP、PVP与PKP联合后路内固定手术、后路截骨矫形手术、侧前方入路手术、前后路联合手术等[11~14]。PVP和PKP作为微创术式治疗新鲜OVCF引起的腰背部疼痛、强化骨折椎体、预防和矫正局部后凸畸形等方面获得很好的临床疗效[11]。王大林等[2]选择PVP和PKP治疗陈旧性OVCF骨折不愈合情况如Kummell病,将骨水泥填充至存在裂隙的骨折不愈合椎体内,达到稳定椎体的目的,一定程度缓解骨折椎体内不稳定所致腰背痛并矫正局部后凸畸形。但是PVP能够矫正局部后凸畸形效果有限,郝晨等[3]比较PVP与骨水泥强化椎弓根螺钉联合PVP治疗60例无神经症状的Ⅲ期Kummell病,平均随访超过1年,短期临床疗效较好,2组术前平均后凸角度均未超过14°,末次随访显示2种术式矫正局部后凸Cobb角度有限。PVP联合后路固定术可以减少后凸矫形丢失,吴兆艺等[15]采用短节段椎弓根螺钉固定联合PVP治疗63例OVCF,63例均分为3组进行比较,末次随访短节段固定联合PVP组VAS评分优于单纯PKP组和单纯短节段固定组,且椎体高度和后凸角度丢失明显少于后2组,但手术时间与出血量明显增加。本组术前后凸Cobb角29.4°±3.2°,术后即刻后凸Cobb角为19.5°±2.3°,单节段前路手术实现平均约9.9°的矫正,末次随访VAS、JOA-29评分和ODI较术前均有明显改善,手术治疗效果明显。
对于陈旧性OVCF椎体后壁破裂继发椎管狭窄、骨折椎体呈楔形愈合形成局部后凸压迫或者牵张脊髓造成神经损害、胸腰椎局部后凸继发脊柱矢状位失平衡或导致腰椎代偿性过度前凸、椎体后滑移使关节突关节发生应力损伤而出现下腰痛等情况,PVP与PKP很难同时实现解除神经压迫、稳定椎体、矫正后凸畸形和重建脊柱序列等目的,开放手术可以同时满足以上几点考虑[4,10,13,16]。对于单节段继发胸腰椎后凸畸形,可以考虑侧前方入路减压固定融合手术治疗。Kanayama等[12]报道31例前路手术治疗合并神经损害的OVCF,80%单纯前路手术即可实现神经减压和前柱重建,术后即刻矫正后凸Cobb角18°,末次随访时丢失8°,建议多节段前路椎体次全切除和重度骨质疏松症患者需同时行后路固定增加稳定性。本组术前11例合并神经损害,末次随访9例改良Frankel分级至少1级的提高,神经功能明显改善。2例术前腰背痛,末次随访诉腰背痛较术前明显缓解,但仍存在腰背痛,考虑可能与术前胸腰段后凸导致腰椎过度代偿前凸、上腰椎后滑移、关节突关节剪切应力集中导致的疼痛有关。部分高龄患者胸腰椎后凸畸形多合并腰背肌长时间牵拉无力所致的炎症性疼痛,也可能是术后远期腰痛的原因之一。
赵同生等[7]认为>20°的后凸畸形应当进行校正,陈伯华[14]和陈仲强等[16]认为局部或整体矢状面后凸角≥30°,且全身麻醉下体位复位不佳时,建议行后路截骨矫形手术。对于陈旧性OVCF,由于椎弓根骨皮质变薄、椎体骨质疏松,骨质对螺钉的把持力降低,为减少术后螺钉松动及切割的发生率,后凸畸形应尽量矫正[4,7,16]。后路截骨矫形手术如经椎弓根截骨或经椎弓根椎间隙截骨可以有效矫正脊柱后凸畸形,但陈旧性OVCF继发胸腰椎后凸畸形患者大多高龄,合并骨质疏松症,内科合并症较多,耐受开放手术能力较差[7]。我们曾报道单纯后路截骨矫形手术治疗陈旧性OVCF继发胸腰椎后凸畸形,术前平均后凸Cobb角45.9°,术后凸矫形率76.7%,患者神经功能及生活质量较术前明显提高,但是手术时间平均4.6 h,术中出血量平均1942 ml,手术创伤较大,且围术期及远期均出现手术相关并发症[4]。本组均为单节段陈旧性OVCF继发胸腰椎后凸畸形,采用侧前方入路减压固定融合手术,手术平均矫正9.9°,后凸矫形率33.7%,相比后路截骨矫形手术,矫形效率较低,且末次随访后凸矫形部分丢失。但是单纯侧前方入路手术可以保留后方肌肉韧带复合体的完整性,对于高龄患者减少对后方软组组的破坏。前路手术可以在充分视野下显露病灶,有效切除责任骨折椎体,解除脊髓前方致压物,还可以进行前柱植骨融合并置入内固定器械完成有效的前柱支撑[6]。本组手术时间(199.1±50.4)min,术中出血量(793.2±479.4)ml,在进行椎体次全切除操作时,椎体松质骨面出血较多,可使用骨蜡封堵骨面出血。对于单节段陈旧性OVCF继发胸腰椎后凸畸形,侧前方入路手术是实现脊髓减压和有限矫正后凸的一个方法。
侧前方入路手术广泛应用于胸腰段脊柱肿瘤或结核的前路手术中,在显露病灶过程时,可能干扰胸腹部脏器和大血管,术前需严格评估患者内科状况[4,17,18]。大多数脊柱外科医生更熟悉后路手术解剖结构与路径,侧前方手术入路与解剖需要一定的学习曲线。本组2例发生围术期并发症,1例在显露过程发生,造成壁层胸膜撕裂,术中立即严密缝合胸膜裂口,避免更严重并发症如血气胸的发生;1例术后出现手术侧少量胸腔积液,不排除此并发症为手术操作时壁层胸膜受损伤所致,术后严格给予内科治疗,复查胸部X线片胸腔积液完全吸收后出院。
侧前方入路术中需掌握操作细节,在充分显露骨折椎体后,预先结扎或电凝椎体侧方的节段血管。骨质疏松椎体内骨小梁变少,松质骨内静脉窦增多,对椎体进行次全切除时面临较高的出血风险,需及时增加静脉补液,确保手术操作过程中血压平稳。前柱使用钛网或人工椎体支撑,可植入肋骨、髂骨取出的自体骨或咬碎的骨折椎体骨质。在放置钛网前,尽可能用骨膜剥离器刮除相邻椎体的软骨终板,增加自体骨与植骨面接触面积,提高植骨融合率,本组末次随访CT矢状位重建全部可见植骨融合。由于骨质疏松症造成椎体骨皮质变薄,术中应避免使用骨膜剥离器过度刮除骨性终板,导致内固定松动或脱出。末次随访CT见3例出现术区钛网下沉,考虑可能原因有两点:一是骨质疏松症患者椎体骨皮质变薄、骨小梁稀疏,术中过度打磨骨性终板使其承载能力降低;一是术中过度撑开椎体间高度,植入较高钛网或人工椎体,使前柱应力集中在内固定物与骨界面,内固定物破坏脆弱的骨性终板,造成钛网下沉。考虑患者高龄合并骨质疏松症,植入钛网或人工椎体需选择较大直径内固定器械,增加内固定器械、植入的自体骨与椎体终板骨面的接触面积。侧方应用钛板螺钉固定系统或者钉棒固定系统时,采用双皮质螺钉固定,增加内固定器械把持力,减少内固定松动的机率。
本组患者骨密度(0.7±0.1)g/cm2,T=-3.1±1.0,术后嘱咐患者严格佩戴胸腰部支具至少3个月,规律服用抗骨质疏松药物治疗骨质疏松症。 22例末次随访腰背痛VAS、JOA-29评分和ODI较术前明显改善(P=0.000),日常生活功能较手术前明显提高。可见,采用侧前方入路手术治疗陈旧性OVCF继发胸腰椎后凸畸形可以获得较好的临床疗效。本研究为回顾性研究,存在一定局限性,病例数较少,尚需进一步积累病例与后路手术比较疗效差异,如何实现微创或小切口侧前方入路减压固定术也是我们努力的方向。
综上所述,对于单节段陈旧性OVCF继发胸腰椎后凸畸形,侧前方入路手术可以有效解除神经压迫,重建脊柱前柱稳定性并保留脊柱后方肌肉韧带复合体,同时一定程度矫正局部后凸畸形。术中需关注内固定与植骨面的处理,预防内固定松动与失败。治疗成功的关键还需要关注患者高龄合并骨质疏松症的特点,围术期规律服用抗骨质疏松药物,以期取得满意的临床疗效。
