成人髓母细胞瘤诊断和治疗研究进展☆
2021-04-06刘裕肖爵贤桂诗凯程天祥程祖珏
刘裕 肖爵贤 桂诗凯 程天祥 程祖珏
髓母细胞瘤(medulloblastoma,MB)是一种恶性原发性中枢神经系统肿瘤,好发于儿童,成人较为少见,成人MB每年发病率仅有6/1000万[1]。临床医生常将其忽视,误诊为室管膜瘤、血管母细胞瘤和胶质瘤等其他疾病。成人MB的治疗包括手术切除肿瘤,术后辅以全脑全脊髓放疗(craniospinal irradiation,CSI)联合后颅窝加强放疗,同时予以化疗,5年生存率为70%~80%[2]。目前对于成人MB放疗、化疗方案尚无统一的标准,预后影响因素也存在争议。本文针对成人MB的诊断、治疗以及预后影响因素的最新进展作一综述。
1 分型与分期
1.1 MB分型2021年WHO第五版中枢神经系统肿瘤分类(WHO CNS5)更新了MB的组织学分型和分子分型,对MB的诊断提供了新的指导。MB的组织学类型分为:经典型(classi,CL)、促结缔组织增生/结节型髓母细胞瘤(desmoplastic/nodular,DN)、广泛的结节型髓母细胞瘤(medulloblastoma with extensive nodularity,MBEN)和大细胞/间变型髓母细胞瘤(large cell/anaplastic,LC/A)[3]。WHO CNS5将2016年版中的group3和group4归为一组,将SHH活化型分裂为TP53野生型以及TP53突变型两组。WHO CNS5更新的MB分子分型为:髓母细胞瘤,WNT活化型(medulloblastoma,WNT-activated);髓母细胞瘤,SHH活化和TP53野生型(medulloblastoma,SHH-activated and TP53-wildtype);髓母细胞瘤,SHH活化和TP53突变型(medulloblastoma,SHH-activated and TP53-mutant);髓母细胞瘤,非WNT/非SHH活化型(medulloblastoma,non-WNT and non-SHH)[3]。
1.2 MB分期1969年CHANG等根据肿瘤大小和转移情况制订MB的TM分期,并被广泛的应用[4]。CHANG氏分期系统主要借鉴于其他肿瘤的TMN分期,其中T分期描述肿瘤侵犯情况,M分期描述肿瘤的播散转移、脑脊液浸润和远处转移情况,见表1。目前主要依据CHANG TM分期将MB分为标危组和高危组,其中标危组为T1~T3aM0,高危组为T3bM1~M4、T4M1~M4。
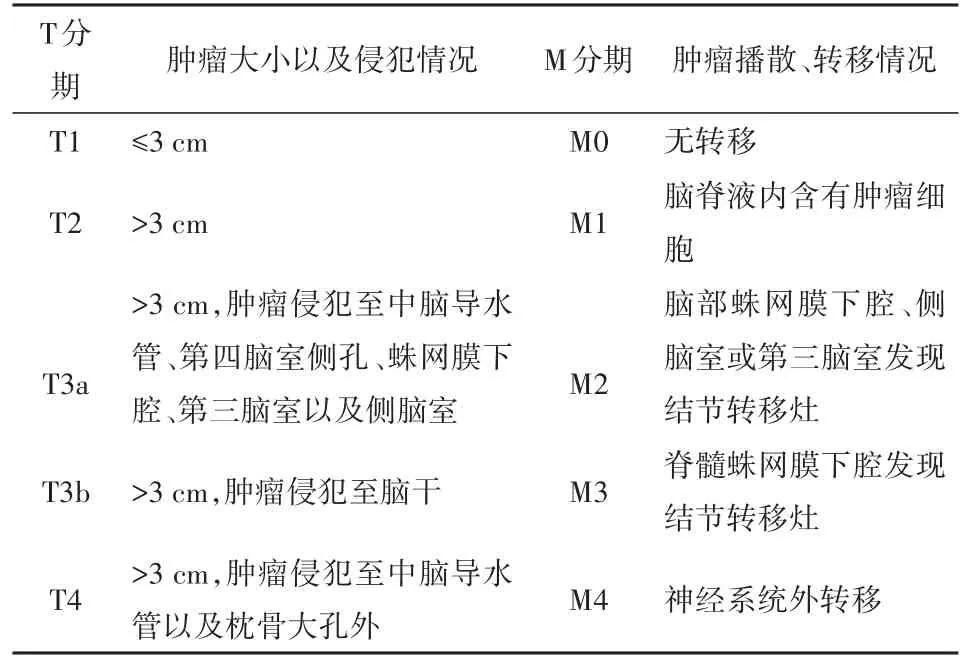
表1 CHANG氏分期
2 诊断
2.1 基因筛查MB发病与某些遗传性癌症易感基因存在着密切联系。WASZAK等[5]发现APC、BRCA2、PALB2、PTCH1、SUFU和TP53等基因在MB发生发展中起重要作用,尤其在WNT活化型及SHH活化型表现更为明显。相关研究表明TP53、PTCH1和SUFU基因突变患者更容易发生SHH活化型髓母细胞瘤[6]。
2.2 临床症状成人MB好发于后颅窝,潜伏期1~18个月(平均7个月),常表现为小脑功能障碍、脑积水相应表现及颅高压症状[7]。小脑功能障碍的临床症状及体征可能因病变位置而不同[8]。中线区小脑MB多为串联步态受损和闭目难立征阳性;小脑半球MB则多表现快速轮替运动障碍、指鼻试验以及跟膝胫试验阳性体征[8]。由于成人颅缝已经闭合,成人MB起病更加危急,颅高压症状更加明显。因此,大多数成人患者由于头痛、恶心呕吐或意识障碍等颅高压相关症状而就诊。脑神经受累的临床症状也常出现,如外展神经受损导致复视,这可能是由于脑神经直接受累或者颅内压升高所导致[8]。MB也可以通过蛛网膜下腔播散转移,多数转移至椎管内以及大脑表面,极少数转移至淋巴结、骨、肺和肝脏,从而导致相应临床症状[2,8-9]。
2.3 影像学表现颅脑CT和MRI是诊断MB常用影像学方法。成人MB多起源于小脑半球以及桥小脑角区,其颅脑CT多表现为小脑半球或桥小脑角区的高密度或混杂密度影,周围环绕着低密度水肿带,增强扫描肿瘤呈均匀强化[10]。颅脑MRI常表现为小脑半球处边缘清晰的类圆形占位病变,多伴有囊性成分,T1加权像中肿瘤组织表现为等信号或低信号,T2加权像中肿瘤组织表现为等信号或者高信号,弥散加权成像(diffusion weighted imaging,DWI)中,肿瘤组织多提示弥散受限[10-11]。一项成人MB放疗的多中心研究(NOA-07试验)发现,肿瘤出血以及脑室内转移多提示WNT活化型髓母细胞瘤[12]。PERREAUT等[13]发现MB分子亚型与肿瘤位置密切相关,WNT活化型多位于桥小脑角区,SHH活化型多位于小脑半球,非WNT/非SHH活化型多位于小脑蚓部或第四脑室。MORA等[14]发现,磁共振波谱成像(magnetic resonance spectrum,MRS)有利于区别MB与其他类型肿瘤:高胆碱提示MB,高肌醇提示室管膜瘤,高脂提示转移瘤或血管母细胞瘤。罗楚涵等[15]在儿童MB鉴别诊断中应用动态对比增强磁共振(dynamic contrast-enhanced perfusion MRI,DCE-MRI)准确地显示病变血流动力学变化,从而通过容量转移常数(Ktrans)、速率常数(Kep)、血管外/细胞外间隙容积分数(Ve)、血浆容积分数(Vp)值等多种参数准确地对髓母细胞瘤与其他后颅窝肿瘤进行鉴别诊断,这也为成人MB与其他肿瘤的鉴别提供了一种新思路。
3 治疗
3.1 外科治疗成人MB首选手术切除。不同部位肿瘤可采取相应的手术入路。中线区MB可经膜髓帆入路或者蚓部入路,脑室内肿瘤可能还需要切除下蚓部进行肿瘤的暴露[6]。经膜髓帆入路更有利于切除延伸至外侧隐窝的肿瘤[6]。成人MB常选择俯卧位或侧俯卧位,在神经导航下行旁正中入路幕下病变切除术。临床医生可根据肿瘤部位而选择不同的手术体位,但是与体位相对应的并发症需重视,比如坐位可能导致空气栓塞以及气颅等风险[16-17]。术中持续电生理监测(包括体感诱发电位及运动诱发电位的持续监测)在幕下病变切除术中起着重要的警示作用[18]。部分患者由于肿瘤压迫导致脑脊液循环通路受阻,从而发展为梗阻性脑积水。对于此类患者优先选择第三脑室造瘘术,需慎重选择脑室-腹腔分流术,以防止增加腹膜转移的风险[11,19]。
3.2 放疗成人MB术后辅以CSI联合后颅窝加强放疗为标准治疗。放疗能够控制局部肿瘤的生长以及延长患者的无进展生存期,然而对于成人MB放疗的剂量选择尚无统一标准[20]。成人MB患者放疗剂量的选择大多参考儿童患者临床数据,其存在一些局限性。成人对放疗的中枢神经系统毒性作用耐受强于儿童,然而骨髓以及其他器官对放疗的耐受却更差[6,21]。目前成人MB的标危组患者通常予以CSI(23.4 Gy)联合后颅窝加强放疗(54 Gy),辅以前期化疗,或者CSI(36 Gy)联合后颅窝加强放疗(54.8 Gy);对于高危组患者予以CSI(36 Gy)联合后颅窝加强放疗(54 Gy),辅以前期化疗[22]。ABACIOGLU等[23]发现,成人患者术后3周内、3~6周和6周后予以放疗的5年无病生存率分别为0、85%和75%(P=0.002)。放疗时机的选择与成人MB的预后密切相关。西班牙医学肿瘤学会(SEMO)关于成人MB的指南建议放疗时机应在术后3~6周开始[7]。质子放疗是一种新的放疗方式,射线粒子的能量可直接进入肿瘤细胞内释放,对正常组织以及脏器的毒害作用较小,效果优于普通的X射线以及电子线[22]。然而质子放疗设备昂贵,限制了其在临床的广泛应用。
3.3 化疗化疗在儿童MB患者中取得较好效果。对于成人MB术后行放疗的同时也予以化疗。KOCAKAYA等[24]对227篇成人MB论文进行meta分析,表明一线化疗患者的生存时间明显长于单纯放疗患者或肿瘤复发时接受化疗的患者。在一项根据儿科HIT-2000方案治疗成人非转移性MB的前瞻性多中心研究中,49例接受联合放化疗的非转移性疾病成人患者的4年无病生存率为74%,总体生存率为94%[25]。目前SEMO以及EANO-EURACAN两项关于成人MB的指南均建议,成人患者在接受手术切除以及放疗的同时需行化疗[6-7]。然而成人MB的化疗方案无统一标准,大多借鉴儿童MB患者的方案。Packer方案是最为常见的一种化疗方案,其包括放疗期间予以长春新碱(1.5 mg/m2,不超过2 mg),随后予以8个疗程洛莫司汀(75 mg/m²),顺铂(70mg/m²)和长春新碱(1.5 mg/m2,不超过2 mg)治疗[6-7]。成人MB患者对Packer化疗方案的耐受性似乎比儿童患者更差,然而没有其他对成人毒副作用小的药物能够替代顺铂、洛莫司汀或长春新碱等化疗药物,对于成人患者化疗药物的选择待进一步研究[22]。
3.4 其他治疗自体干细胞移植联合高剂量化疗在治疗复发的成人MB是一种可行方案[22]。GILL等[26]一项关于复发的成人MB研究中,将自体干细胞移植联合高剂量化疗与接受常规化疗的成人患者进行了比较,自体干细胞移植联合高剂量化疗组患者中位生存期高于常规化疗组,表明接受自体干细胞移植联合高剂量化疗的复发成人MB患者具有更好预后。
随着对MB分子亚型的认知加深,个体化靶向治疗也成为了一种新的治疗方案,SHH活化型是成人MB最为多见的分子亚型,其特征是Sonic-Hedgehog途径的异常激活[27]。SMO抑制剂治疗SHH亚型MB的早期临床试验结果欠佳。但是ROBINSON等[27]研究发现:SMO抑制剂对于成人患者效果较好,对于而儿童患者效果较差,原因是成人患者多为SHH通路的上游突变,而儿童患者多为下游突变,比如GLI基因的扩增以及SUFU基因的突变,这导致了对SMO抑制剂的耐药性。Vismodegib(GDC-49)和sonidegib是两种典型SMO抑制剂,通过与SMO结合,抑制SHH旁路并诱导肿瘤的退化,该药物在MB的小样本研究以及个案中具有良好疗效[27-28]。关于Vismodegib(GDC-49)和sonidegib治疗MB的一项meta分析也表明该药物患者耐受性好、副作用小,并显示了良好的抗肿瘤活性[29]。
4 预后影响因素
4.1 年龄与性别年龄是影响儿童MB预后的一个重要因素,然而是否影响成人MB的预后却存在着争议[30-32]。LAI等[31]通过分析454名成人MB的临床数据,发现18~20岁的患者预后最好,21~40岁或40岁以上的患者预后最差。其他研究则认为年龄对于成人MB预后无意义。有研究表明女性MB患者比男性MB患者预后更好,然而更多研究则认为性别与成人患者的预后无相关性[32]。
4.2 组织学分型LC/A已被证明是儿童患者预后不良的因素,DN被认为儿童患者预后良好的因素[30]。成人患者中LC/A虽较为少见,但也提示预后不良[22]。张娜等[32]关于成人MB研究发现:DN 5年无进展生存期及总体生存率最好,CL和MBEN次之,LC/A预后最差。LAI等[31]一项关于成人MB的研究结果表明:LC/A及DN均预后较差。
4.3 分子分型WNT活化型约占成人MB的15%,对应的组织学类型多为经典型,预后最好,5年生存率约为90%,常与6号染色体、CTTNB1癌基因突变相关[33]。SHH活化型发病率表现为年龄的双波峰分布,第一个峰值为出现在婴儿组(0~3岁),第二个峰值在16岁以上青少年和成人,3~16岁患者少见[34]。SHH活化型约占成人MB 60%,WHO CNS5依据TP53基因有无突变分为TP53野生型以及TP53突变型,TP53突变型患者预后较差[3,33]。WHO CNS5将group3和group4合并为非WNT/非SHH活化型,其约占成人MB 25%,组织学类型多为经典型,5年生存率约为50%,常与MYCN和CDK6等基因的突变相关[23]。
4.4 转移以及肿瘤切除程度诊断时出现肿瘤转移已证实是成人MB预后不良的重要因素[2]。BRANDES等[34]一项评估成人MB预后的前瞻性研究结果表明:无转移MB患者的预后明显好于存在转移MB患者,5年无进展生存期分别为75%和45%(P=0.01)。目前肿瘤全切除是儿童MB患者预后良好的重要因素,术后肿瘤残留>1.5 cm2的儿童患者预后往往较差,然而肿瘤切除程度对于成人MB患者预后影响却并不明确[29]。LAI等[31]多因素回归分析表明肿瘤全切除是成人MB有利的预后因素。然而也有研究认为肿瘤切除程度并不是成人MB患者的预后影响因素[35]。虽然肿瘤切除程度对于成人MB的预后尚有争议,但最大限度地安全切除肿瘤仍然是成人MB的手术目标。
5 总结与展望
从目前已有研究上看,成人MB发病率低,颅脑MRI是其首选的诊断方法,MRS以及DCE-MRI的应用可减少MB的误诊率。手术切除肿瘤是成人MB的首选治疗方式,术后辅以放、化疗能够明显改善患者的预后。分子分型为SHH活化和TP53突变型的成人MB预后差,个体化的靶向治疗有望改善其预后。
