分子生物学技术在感染性疾病诊断中的应用进展
2021-04-01吕晶南余方友
吕晶南,余方友
(1. 苏州大学第二附属医院检验科,江苏苏州215004;2. 同济大学附属上海市肺科医院检验科,上海 200082)
2019新型冠状病毒(2019-nCoV)的暴发,使分子生物学技术在临床感染性疾病诊断、治疗、疗效评价及预防等方面得到前所未有的重视和飞速发展。本文就近年来基于核酸检测技术鉴定病原体进行系统化讨论,同时也对这些方法在临床实验室应用时可能遇到的挑战和机遇进行阐述。
1 呼吸道感染
1.1病毒 呼吸道病毒的感染对全球流行病公共卫生可引起严重的威胁,如1918年甲型流感大流行,2003年严重急性呼吸系统综合征(SARS)冠状病毒暴发,2009年甲型H1N1流感引起的大流行,2012年阿拉伯半岛出现由冠状病毒引起的中东呼吸综合征(MERS),2019年2019-nCoV的暴发。值得注意的是,仅基于体征和症状区分病毒来源较困难,同时不同病毒感染采取的治疗方案不同,因此,呼吸道病毒对人类健康构成严重威胁[1]。目前,食品药品监督管理局(Food and Drug Administration,FDA)批准的多重呼吸道病毒组合能够检测多达20种不同的病毒靶标[2]。
Luminex xMAP检测是一种基于多重RT-PCR的检测方法,采用多色荧光标记的微球(珠)杂交,可同时检测和鉴定12种呼吸道病毒和亚型[2]:首先通过多重RT-PCR扩增病毒的保守区域,然后通过含有生物素的脱氧核苷酸延伸反应,扩增产物被生物素标记,与颜色编码微球上的病毒特异性探针进行杂交,检测荧光信号。
Verigene系统(Nanosphere公司)通过PCR扩增结合纳米金颗粒标记的探针,与排列在载玻片上的捕获寡核苷酸靶序列进行杂交。探针捕获目标片段后,信号随即放大。FDA已批准Verigene系统用于检测甲型流感病毒、甲型流感病毒H3亚型、甲型流感病毒2009 H1N1亚型、乙型流感病毒和呼吸道合胞病毒(RSV)A和B亚型[3]。该系统已开发出用于检测13种病毒和3种细菌靶标的多重呼吸道检测组合(部分见表1)。
FilmArray用于同时检测和鉴定17种病毒和3种细菌呼吸道病原体(部分见表1):使用多重两步RT-PCR,对靶扩增子进行高分辨率熔解曲线分析,以检测每种组合中的分析物[4]。该系统完全封闭,因此不会出现交叉污染。
eSensor系统采用基于电化学检测的DNA微阵列技术,基于夹心测定原理,可检测14种不同类型和亚型的呼吸道病毒(部分见表1)[5]。由于该检测需要对样品进行PCR后处理,因此必须注意避免由扩增子交叉污染引起的假阳性。
1.2百日咳鲍特菌(Bordetellapertussis) 鲍特菌属中有4种可引起人类呼吸系统疾病:百日咳鲍特菌、副百日咳鲍特菌、支气管败血鲍特菌、霍氏鲍特菌。百日咳是由百日咳鲍特菌引起的高度传染性呼吸道疾病。高达20%的副百日咳鲍特菌感染可能引起百日咳样疾病,更常见于幼儿[6]。支气管败血鲍特菌常发生在免疫受损的个体中,常有牲畜接触史[7]。霍氏鲍特菌是最近发现的与人类百日咳样疾病相关的病原微生物[8]。鲍特菌属4个种都在人类呼吸道疾病中发挥重要作用[9]。
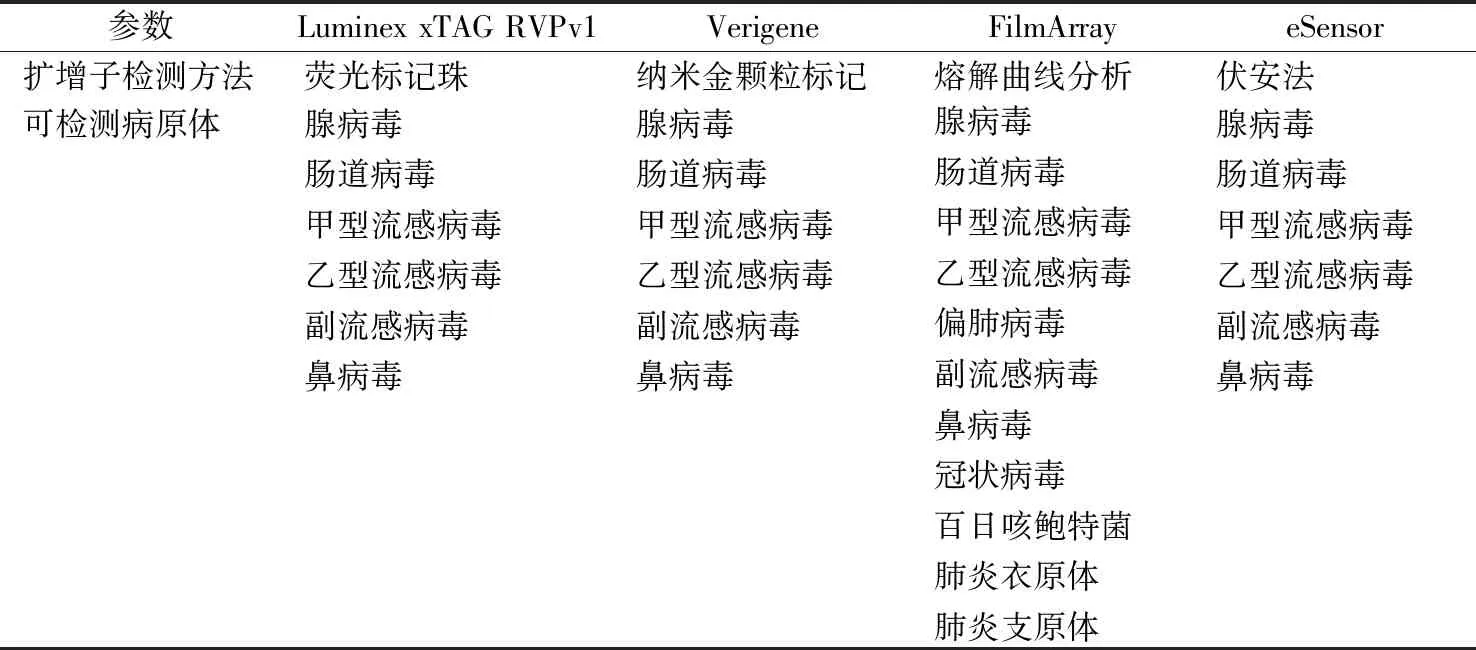
表1 FDA批准的检测呼吸道病毒组合参数
分子检测(nucleic acid amplification tests,NAATs)可有效用于鲍特菌属间的鉴别[9]。通过检测多拷贝插入序列(insertion sequence,IS)来提高特异性。IS481是百日咳鲍特菌最有效的多拷贝靶点,也可见于霍姆鲍特菌及支气管脓毒鲍特菌。因此,以IS481作为唯一的靶位来检测百日咳鲍特菌存在一定的局限性,特别是在暴发流行中,会出现假阳性。IS1002见于百日咳鲍特菌和副百日咳鲍特菌,而霍姆鲍特菌或支气管脓毒鲍特菌中不存在IS1002。IS1001见于副百日咳鲍特菌以及支气管脓毒鲍特菌。针对上述3种ISs多拷贝靶点的组合可鉴别感染相关的鲍特菌属。百日咳毒素启动子区域(pertussis toxin operon, PT)常用于检测百日咳鲍特菌。该靶点同时见于副百日咳鲍特菌和支气管脓毒鲍特菌中,但在这2种菌中由于启动子区域存在突变,导致该蛋白质不表达。总之,通过增加特异性扩增靶点(如采用双重或三重PCR方法)可提高NAATs检测百日咳鲍特菌的检出率[9]。
1.3结核分枝杆菌(Mycobacteriumtuberculosis) 目前,FDA批准2种NAATs可用于直接检测临床标本中的结核分枝杆菌,分别是结核分枝杆菌扩增直接检测试剂(MTD检测,Hologic/Gen-Probe)和Xpert MTB/RIF试剂(Cepheid公司)。MTD检测基于转录介导的核糖体RNA扩增,可用于检测抗酸杆菌涂片阳性和涂片阴性呼吸道标本。Xpert MTB/RIF使用半巢式实时定量PCR检测痰标本中结核分枝杆菌的DNA以及与利福平耐药性相关的突变基因rpoB。该检测系统使用一次性检测盒,GeneXpert仪器可自动进行核酸提取、扩增及检测,敏感性为95%,特异性为99%[10]。
2 中枢神经系统感染
1型和2型单纯疱疹病毒(herpes simplex virus, HSV)可引起各种临床综合征,包括皮肤黏膜、眼睛、中枢神经系统以及生殖系统的感染。其中引起的脑炎临床症状与其他病毒引起的脑炎,如西尼罗河病毒、圣路易斯脑炎病毒和东部马脑炎病毒引起的脑炎,临床症状比较相似,不易区分。细胞培养或活检是诊断HSV脑炎的金标准。脑脊液(CSF)培养对成人HSV脑炎的诊断敏感性低于10%。检测CSF中HSV抗原或抗体的敏感性和特异性分别为75%~85%和60%~90%[11]。由于传统方法的局限性,高敏感性检测脑炎患者脑脊液中HSV DNA的方法得到广泛关注,其中也包括二代测序技术(next-generation sequencing,NGS)[12]。
FDA已经批准了几种用于检测生殖道标本中HSV DNA的商品化试剂,但对于脑脊液样本FDA仅批准了1种,即Simplexa HSV 1和2 Direct Kit(Focus Diagnostics公司)。该试剂提供作为分析物特异性试剂(analyte-specific reagents,ASRs)的引物和探针,使用实验室自建检测方法(laboratory developed tests, LDT)检测系统进行检测。检测HSV DNA的靶点包括:编码聚合酶,糖蛋白B,糖蛋白D或胸苷激酶的基因。这些靶点应具有特异性,即引物不能扩增与神经系统疾病相关的其他疱疹病毒的DNA,如巨细胞病毒、水痘带状疱疹病毒、6型人疱疹病毒和爱泼斯坦-巴尔病毒。宏基因组二代测序(metagenome next-generation sequencing,mNGS)能够用较少的样本量,通过其高通量、深度测序的特点快速、准确地检测感染相关的病原体。2020年Osterman等[13]应用 mNGS对1例48岁疑似病毒性脑炎患者的脑脊液进行了检测,结果发现该重症患者感染1型人类疱疹病毒(HHV-1)。mNGS不仅可以快速准确地检测出常见的病原体, 同时也可对病原体进行定量研究。Liu等[12]应用mNGS诊断出1例患有HSV脑炎的1岁患儿,经阿昔洛韦治疗后,症状消失,同时检测患儿脑脊液中HSV1 DNA定量从4 290下降至0。研究表明,脑脊液 mNGS对常见的疱疹病毒感染的脑炎确诊以及治疗效果的评估具有重要的临床价值。
3 血流感染
目前已有多种基于核酸扩增的方法,可有效缩短鉴定血培养中病原菌所需的时间。其中FDA批准的检测方法包括肽核酸荧光原位杂交(peptide nucleic acid-fluorescence in situ hybridization,PNA FISH)、RT-PCR以及基于巢式PCR的血培养鉴定板[14]。
PNA FISH探针是一种DNA探针,其中带负电荷的糖磷酸骨架被带中性电荷的肽骨架取代。这种中性电荷结构使探针与靶核酸结合时不存在静电排斥作用,因此杂交更加紧密、快速[15]。该技术可用于快速鉴定金黄色葡萄球菌、凝固酶阴性葡萄球菌、肠球菌、大肠埃希菌、肺炎克雷伯菌、铜绿假单胞菌及念珠菌(包括白念珠菌、近平滑念珠菌、热带假丝酵母、光滑念珠菌和克柔念珠菌),操作简便,30 min后通过荧光显微镜观察结果。
对疑似金黄色葡萄球菌感染的菌血症患者,万古霉素是标准治疗方案。因为在大多数临床微生物实验室,50%或更多分离的菌株为耐甲氧西林金黄色葡萄球菌(methicillin-resistantStaphylococcusaureus,MRSA);然而,万古霉素对甲氧西林敏感的金黄色葡萄球菌(methicillin sensitiveStaphylococcusaureus,MSSA)的效果不及甲氧西林。因此,在血流感染中快速鉴别MRSA和MSSA十分重要。Xpert MRSA/SA BC(Cepheid公司)和GeneOhm StaphSR (BD Diagnostics公司)是FDA批准的2种real-time PCR试剂盒,可直接用于鉴别阳性血培养中的MRSA和MSSA[16-17]。
Verigene革兰阳性和革兰阴性细菌鉴定板(Nanosphere公司)以及FilmArray血培养鉴定(BCID)系统(BioFire Diagnostics公司)可直接检测血培养中病原微生物[18-20]。
FilmArray BCID可同时在一块板上联合检测包括革兰阳性细菌、革兰阴性细菌以及多种酵母菌在内的24种病原菌和3种抗菌药物耐药基因。该鉴定板可以鉴定出阳性血培养中80%~90%病原微生物,并检测对甲氧西林耐药的葡萄球菌,对万古霉素耐药的肠球菌以及产碳青霉烯酶的革兰阴性肠杆菌科细菌[20]。
Verigene BCID系统采用纳米金基因芯片法可直接从阳性培养瓶中鉴定病原微生物,不需要进行核酸扩增[18]。当血培养瓶出现阳性报警时,根据革兰染色结果选择不同的血培养鉴定板。Verigene革兰阳性菌血培养鉴定板已被批准测定12个属或种的细菌以及3种耐药基因。Verigene革兰阴性菌血培养鉴定板可以在2.5 h内检测8个属或种和9个耐药基因。革兰阳性菌血培养鉴定板可以检测mecA、vanA和vanB基因,革兰阴性菌血培养鉴定板可以检测6种不同的β-内酰胺酶基因。检测真菌的Verigene鉴定板正在开发中,该鉴定板可以检测白念珠菌、杜氏假丝酵母、光滑念珠菌、克鲁斯念珠菌、近平滑念珠菌、热带假丝酵母、隐球菌和新型隐球菌[21-22]。
基质辅助激光解吸电离飞行时间质谱(matrix-assisted laser desorption/ionization time of flight mass spectrometry, MALDI-TOF MS)通过使用蛋白质组学对病原体进行鉴定。阳性的血培养瓶中的病原体可直接应用该方法进行鉴定[23]。
二代测序可在血液中检测出大量非致病微生物序列,同时现有研究尚未给出单纯基于测序结果判断污染菌或致病菌的标准,因此对测序结果的判读常需结合临床综合判断。
4 胃肠道感染
肠道病毒(Enterovirus,EV)是一组属于微核糖核酸科的单链RNA病毒。目前,人类肠道病毒被分为7个种类。EV感染的诊断通常基于临床表现和NAATs。
目前,有2种脑脊液EV检测试剂盒通过了FDA的认证,分别是:NucliSENS EasyQ(bioMérieux公司)和Xpert EV(Cepheid公司)[24]。但是,NucliSENS Easy Q EV试剂盒不能通过商业渠道获得。Xpert EV的敏感性为97%,特异性达100%[25-26],且操作简单,经过自动化的核酸提取、扩增和检测,2.5 h内即可出检测结果。
艰难梭菌(Clostridiumdifficile)是一种革兰阳性产芽胞厌氧杆菌,定植后可引起腹泻等症状。抗菌药物的使用导致肠道菌群紊乱,有助于该菌在肠道中定植。目前,已有15种不同的检测平台获得了FDA批准,包括实时PCR、环介导扩增、解旋酶依赖性扩增和基因芯片技术等多种不同方法。通过检测多种靶基因,包括tcdA、tcdB、tcdA和tcdC,其中后两者可以用于鉴定核糖体型027菌株[27-28]。
传染性胃肠炎(infectious gastroenteritis, IGE)是全球发病率和死亡率的主要原因。在美国,每年大约发生1.788亿例IGE,其中有474 000例患者接受住院治疗以及5 000例患者死亡[11,29]。常见的检测方法,包括抗原检测、培养、虫卵和寄生虫的显微镜检查,以及单靶位点的NAATs,都用来检测与IGE有关的病原体或毒素。此外,诊断方法的选择需要根据患者的年龄、疾病严重程度、免疫功能低下状态、腹泻的持续时间和类型、旅行史和患病季节时间来决定[30]。通常来说,由于临床医生对每种诊断方法的适用范围不够了解,因此可能会漏检[31]。 FDA已经批准了5个用于检测肠道病原体组的试剂盒。
Prodesse ProGrastro SSCS(Hologic/Gen-Probe)使用实时荧光定量PCR技术检测鉴定沙门菌属、志贺菌属和弯曲杆菌属,同时可以在不同大肠埃希菌的混合物中鉴别产志贺毒素1(stx1)和志贺毒素2(stx2)2种大肠埃希菌[32]。
BD MAX EBP使用单个实时荧光定量PCR来检测病原体和毒素,包括:志贺菌属、肠道侵袭性大肠埃希菌、弯曲杆菌属以及毒素stx1/stx2。与Prodesse ProGrastro SSCS分析不同的是,BD MAX可以自动完成从样品制备到靶基因扩增和检测的所有步骤[32-33]。
Luminex xTAG GPP通过多重PCR技术和液珠阵列检测包括弯曲杆菌属、艰难梭菌、大肠埃希菌O157、产肠毒素大肠埃希菌、沙门菌属、志贺菌属、霍乱弧菌、腺病毒40/41、诺如病毒GⅠ/GⅡ、轮状病毒A、隐孢子虫属、溶组织内阿米巴和贾第鞭毛虫[34]。虽然该系统检测通量高,但仍需手工进行核酸提取,这样增加交叉污染,引起假阳性。另外,该系统耗时较长。
多重PCR技术和金纳米颗粒微阵列可用于检测5种细菌、2种毒素和2种病毒,包括Verigene弯曲杆菌属、沙门菌属、志贺菌属、弧菌属、小肠结肠炎耶尔森菌、stx1、stx2、诺如病毒和轮状病毒[35]。这是一个简单易用的一体化的检测系统,但因为一次只能运行一个样本,所以其输入输出量有限。
Film Array通过多重PCR技术和熔解曲线可同时检测12种细菌、5种病毒和4种原虫,包括弯曲杆菌属、艰难梭菌毒素A/B、类志贺邻单胞菌属、沙门菌属、弧菌属、霍乱弧菌、小肠结肠炎耶尔森菌、肠道聚集大肠埃希菌、肠致病性大肠埃希菌、产肠毒素大肠埃希菌、产志贺样毒素大肠埃希菌、大肠埃希菌O157、腺病毒F 40/41、星状病毒、诺如病毒GⅠ/GⅡ、轮状病毒A、沙波病毒、隐孢子虫属、环孢子虫、溶组织内阿米巴和蓝氏贾第鞭毛虫[36]。这是目前检测病原体较全面的方法。与所有Film Array产品类似,使用简单,可在约1 h内提供检测结果,主要的缺点是输出量低和高成本。
5 结语
每种检测方法都有不同的优缺点,只有多种分子生物学方法联合应用,并与传统培养鉴定相结合,才有助于感染性疾病的诊断。
