脑胶质瘤的MRI检查及影像学分析
2021-03-30陈欢,王红
陈 欢,王 红
(新疆医科大学第二附属医院医学影像科 新疆 乌鲁木齐 830011)
脑胶质瘤(Brain glioma)是神经外科较常见的原发性颅脑恶性肿瘤,约占颅内肿瘤的35.2%~61.0%[1]。脑胶质瘤是一种常见的原发性颅脑肿瘤,因大脑和脊髓胶质细胞癌变所引起,每年的发病人数约为3~8人/10万人口,胶质瘤也和其他肿瘤(疾病)一样,因环境的挚爱因素和先天性的遗传因素导致,目前临床已经明确了一部分因素,如神经纤维瘤病(I型)以及结核性硬化疾病等,病理认为胶质瘤是的形成可能是外部环境和内部遗传因素发生相互作用而产生的结果,而在表观遗传物质和细胞的遗传物质水平,均发生了一定的突变,这种突变足以致癌[2]。由成胶质细胞衍化而来,有着较高发病率、复发率及死亡率。当前,其发病机制尚不明确,可能与病毒感染、化学、电磁辐射、生活环境相关,不同类型的脑干胶质瘤有着不同的生物学特点,鉴于有着较差的预后,应提高其诊断率[3]。胶质瘤的诊断西药进行综合判断,包括患者病史、症状、体征、辅助检查以及术后病理[4],患者出现明显的临床症状之后,依靠相关影像学诊断方法,近年来,随着影像学技术的发展,MRI在脑胶质瘤中得到广泛应用。本文现将脑胶质瘤的MRI检查及影像学报告如下。
1 资料与方法
1.1 一般资料
选取本院2018年1月—2020年10月就诊的85例脑胶质瘤患者作为研究对象,其中男性52例,女性33例;年龄5~58岁,平均年龄(27.78±5.34)岁;头晕18例,走路不稳22例,恶心呕吐10例,饮水呛咳8例,病程0.5~3年,平均(2.14±0.23)年。
纳入标准:(1)所有患者均经术后病理证实为脑胶质瘤;(2)经过病理或影像学判断脑胶质瘤患者分化、分级清楚,未发生转移等现象;(3)患者的相关资料可以被搜集;(4)患者读本研究悉数知情,且本研究也是在符合伦理道德的前提下进行的。排除标准:(1)合并妊娠、哺乳女性,或无法进行影像学检查者;(2)凝血功能异常者、免疫系统疾病者;(3)发生了其他部位的恶性疾病者,并且对本文研究疾病具有明显影响,或者中间变量者;(3)不配合临床治疗者,拒绝参加、不依从者;(4)精神疾病者以及意识障碍者,无法有效配合研究者。
1.2 研究方法
采用飞利浦Gyroscan NT 3.0T磁共导仪。行MRI平扫、增强扫查,行轴位SE序列T1WI、T2WI及水抑制成像序列、失状位及冠状位T1WI扫描。T1WI:TR/TE:400 ms/14ms;T2WI:TR/TE:5000 ms/128 ms。水抑制像TR/TE:9000 ms/110 ms,层厚8 mm,矩阵198×256.FOV:184×210 mm。增强对比剂Gd-DTPA,静脉注射量0.1 mmol/kg,进行SE序列三个断面的T1WI扫描。由2名高年资影像诊断医师共同阅片。
1.3 病理类型及分组
类型:胶质母细胞瘤、星形细胞瘤、少突胶质细胞瘤、间变性星形细胞瘤。
脑胶质瘤分级[5]:世界卫生组织(world health organization, WHO)制定的分级系统:脑胶质瘤分为1级(恶性程度最低、预后最好)到4级(恶性程度最高、预后最差),其中,传统细胞病理学所谓的间变胶质瘤与WHO的3级相对应,胶质母细胞瘤与WHO的4级相对应,按肿瘤细胞的恶性程度划分:低级别胶质瘤(WHO 1~2级),为分化良好的胶质瘤;高级别胶质瘤(WHO 3~4级),为低分化胶质瘤。
1.4 统计学方法
采用SPSS 17.0统计软件处理,计数资料以[n(%)]表示,行χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 脑胶质瘤的发病部位及类型
85例脑胶质瘤患者发病部位:脑桥30例(35.3%),延髓30例(35.3%),中脑25例(29.4%)。类型:34例局灶内生型(40.0%),30例外生型(35.3%),21例顶盖型(24.7%)。
2.2 脑胶质瘤的影像学特征
脑胶质瘤在T1WI的信号呈现低信号,在T2WI上呈均匀高信号,部分呈现混杂信号。所有胶质瘤患者行手术治疗,根据具体情况进行放疗、化疗治疗。
2.3 脑胶质瘤病理级别与MRI表现的关系
高级别患者的肿瘤大小、跨中线生长、坏死、囊变、基底动脉包绕与低级别相比,均有统计学意义(P<0.05)。其具体数据如表1所示。
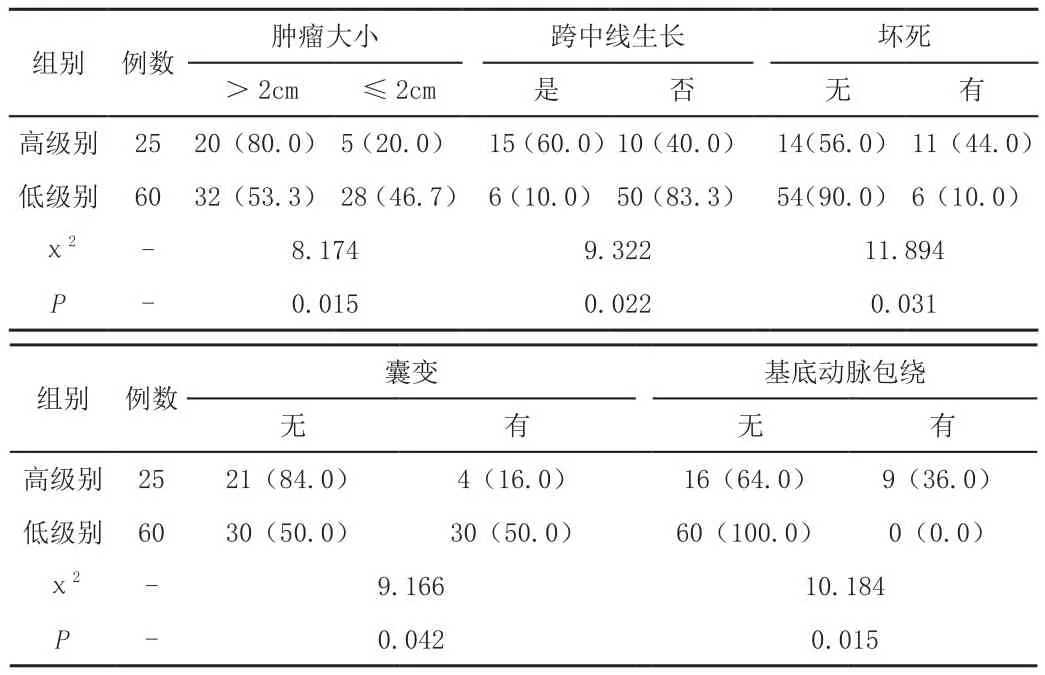
表1 脑胶质瘤病理级别与MRI表现的关系
3 讨论
脑胶质瘤作为神经外科常见恶性肿瘤,若不及时给予诊断及治疗,直接威胁患者生命安全。其疾病包括室管膜下巨细胞性星形细胞瘤、多型性黄色星形细胞瘤、星形细胞瘤、毛细胞型星形细胞瘤,其中以星形胶质细胞所形成的肿瘤即为星形细胞瘤,多发生于男性。多型性黄色星形细胞瘤是脑膜及脑间叶组织肿瘤,部分因为许多瘤细胞产生基底膜。室管膜下巨细胞性星形细胞瘤多发生于青少年及部分未成年儿童,且男性发生于女性,并以不同程度神经系统缺失为临床特征[6]。毛细胞型星形细胞瘤具有较为清晰的边界,且其生长的速度缓慢,在儿童和年轻人的囊性星形细胞瘤中较为常见,且不存在明显的差异。脑胶质瘤多发生于脑桥,其发生的原因可能是弥散型高级别胶质瘤,弥散型高级别胶质瘤在脑桥胶质瘤中较常见,有着较差的预后性。延髓体积具有相对较小的体积,因骨性结构包围,外加延髓被盖部纤维束相对基底椎体束稀少,导致延髓胶质瘤容易形成外形生长,最终向脑干背侧突出,也就是腹外侧、腹侧多的原因。因此,临床应明确肿瘤部位、病理级别。
随着临床影像学的发展,MRI在脑胶质瘤的诊断中得到应用。肿瘤的主体存在于脑干中,且城乡弥漫性增粗或者为局限性膨胀。T1WI肿瘤多呈现的信号形式为低和略低,T2WI及水抑制系列呈现的信号作为高或者较高,对患者进行造影剂的注射之后,强化的片状、结节状、环状在实质部分出现,在其囊变区则未出现。混杂强化则出现在分化较低的肿瘤中。肿瘤包裹基底动脉使其迁移,多数瘤周轻度-中度水肿。MR血管造影大脑后动脉及小脑上动脉向外向上移位,基底动脉前移位贴近枕骨斜坡,基底静脉抬高。肿瘤大无脑积水是脑胶质瘤的主要特征之一[7]。根据脑胶质瘤的分类,可将其分为内生型、外生型、顶盖型。此次研究中30例局灶内生型,30例外生型,21例顶盖型,类型无显著差异(P>0.05)。判断脑胶质瘤良性恶性程度的依据之一即为局灶内生型肿瘤是否过跨脑干中线生长,主要是因为许多位于脑干中的纤维束沿着脑干中线,交叉到了对侧,并一直上行、下行或者横行,而密集的上下行纤维束使得脑干中线部位具有较其他不问更加密集的组织。在本次的研究结果中:囊变多鉴于低级别胶质瘤,其坏死灶出现多预示肿瘤性质偏恶性,较差有。低级别胶质瘤尤其是毛细胞型胶质瘤多鉴于囊变。此次数据还观察到脑桥胶质瘤在脑干内浸润,向前、后或者外侧方呈现不对称生长,进而引起脑干不对称增大膨突。
综上所述,脑胶质瘤诊断中采用脑胶质瘤检查,可在一定程度上判断脑胶质瘤的恶性程度,为临床治疗提供参考依据,具有临床推广应用的价值。
