急性缺血性卒中患者脑小血管病影像总负担的危险因素分析
2021-03-28刘若凡张根明马丽芳
刘若凡 张根明 马丽芳▲
1.北京中医药大学第一临床医学院,北京 100029;2.北京中医药大学东直门医院脑病二科,北京 100700
脑小血管病(cerebral small vessel diseases,CSVD)是各种病因致脑内小血管受累的一系列临床、影像、病理综合征,标志性影像改变有腔隙性梗死(lacunar infarction,LI)、脑白质高信号(white matter hyperintensity,WMH)、血管周围间隙扩大(perivascular space,PVS)、脑微出血(cerebral microbleeds,CMB)、新发小的皮质下梗死等,起病隐匿进展缓慢,部分可急性发作[1],临床表现缺乏特异性且易被忽视。CSVD 与急性缺血性卒中(acute ischemic stroke,AIS)密切相关,约半数AIS 患者存在CSVD,严重的CSVD 对AIS 患者静脉溶栓的预后及随访期死亡率产生不利影响[2-3],因此及时识别此类患者有助于后续治疗方案的选择。目前已知CSVD 危险因素包括年龄、高血压病、糖尿病等,而AIS 患者中是否有其他危险因素与CSVD 严重程度相关尚不明确。Staals 等[4]提出CSVD 影像总负担及评分方法,将标志性影像特征LI、WMH、CMB、PVS组合为测量指标以评估CSVD 整体情况和严重程度[5]。本研究拟采用上述评分方法探索AIS 患者的危险因素及其与CSVD 影像总负担之间的相关性,为临床上存在严重CSVD 的AIS 患者的预防和早期识别提供参考。
1 资料与方法
1.1 一般资料
选取2019 年1 月—2020 年1 月就诊于北京中医药大学东直门医院发病24 h 内的AIS 患者62 例,均于入院48 h 内完成核磁共振(MRI)常规序列+磁敏感加权成像(SWI)检查。本研究为回顾性研究,仅采集患者临床资料,未对研究对象的治疗方案进行任何干预,不会对患者生理带来风险。
纳入标准:①依据《中国急性缺血性卒中诊治指南2018》[6]诊断标准确诊为AIS;②入院48 h 内完成颅脑MRI 检查。排除标准:①存在中毒性脑病、脱髓鞘疾病等其他原因引起的脑白质病变;②服用B 族维生素等影响同型半胱氨酸(Hcy)代谢的药物。
1.2 方法
1.2.1 一般资料收集 收集患者一般资料包括性别,年龄,入院时美国国立卫生研究院卒中量表(NIHSS)[7],入院时血压,TOAST 分型,病灶部位,梗死面积,既往病史(卒中、高血压病、高脂血症、糖尿病、冠心病、心房颤动、心力衰竭),吸烟史及饮酒史。其中梗死面积以弥散加权成像(DWI)序列上梗死灶最大层面的最大直径计算,多发梗死患者以最大梗死灶直径计算,分为小面积(<1.5 cm2)、中等面积(1.5~3.0 cm2并累及小血管分支闭塞)、大面积(>3.0 cm2并累及2 个以上主干血管供血区)[8]。高血压病、高脂血症、糖尿病的诊断根据《中国高血压防治指南(2018 年修订版)》[9]、《中国成人血脂异常防治指南(2016 年修订版)》[10]、《中国2 型糖尿病防治指南(2017 年版)》[11]诊断标准执行,既往卒中史、冠心病、心房颤动、心力衰竭均为本次发病前已明确诊断并进行药物治疗。吸烟史指连续吸烟≥6 个月且平均超过1 支/d[12],饮酒史指饮酒时间≥6 个月,平均摄入酒精量超过30 g/d[13]。
收集患者血清学指标包括总胆固醇(TC)、三酰甘油(TG)、高密度脂蛋白(HDL)、低密度脂蛋白(LDL)、Hcy、血糖等。
1.2.2 CSVD 影像总负担评分及分组 对纳入患者进行CSVD 影像总负担评分,标准如下[4]:①腔隙灶≥1 个记1 分;②不规则脑室周围白质病变延伸到深部白质(Fazekas 3 级)和/或早期融合的深部脑白质病变(Fazekas 2~3 级)时记1 分;③基底节区中-重度血管周围间隙(半定量量表2~4 级)记1 分;④CMB≥1 个记1 分;总分4 分。患者根据上述评分标准分为两组,0~1 分为0~1 组,2~4 分为2~4 组。
1.2.3 影响AIS 患者CSVD 影像总负担亚组分析 将62 例AIS 患者根据影像检查中有无LI、WMH、PVS、CMB 各分为两组,对影响CSVD 总负担严重程度的危险因素进行亚组分析。
1.3 统计学方法
采用SPSS 22.0 对所得数据进行统计学分析,符合正态分布的计量资料采用均数±标准差()表示,组间比较采用t 检验;不符合正态分布的计量资料以中位数(M),四分位数(P25,P75)表示,组间比较采用秩和检验。计数资料采用百分率表示,组间比较采用χ2检验。将CSVD 评分单因素分析中P <0.1 的变量作为自变量,CSVD 评分分组作为因变量,进行logistic 多因素回归分析。以P <0.05 为差异有统计学意义。
2 结果
2.1 两组基线资料比较
62 例AIS 患者中0~1 组36 例,2~4 组26 例。2~4 组年龄高于0~1 组,差异有统计学意义(P <0.05);两组男性占比、吸烟史、饮酒史、入院NIHSS 评分,既往卒中、高血压病、高脂血症、糖尿病、冠心病、心房颤动、心力衰竭病史比较,差异均无统计学意义(均P >0.05)。见表1。
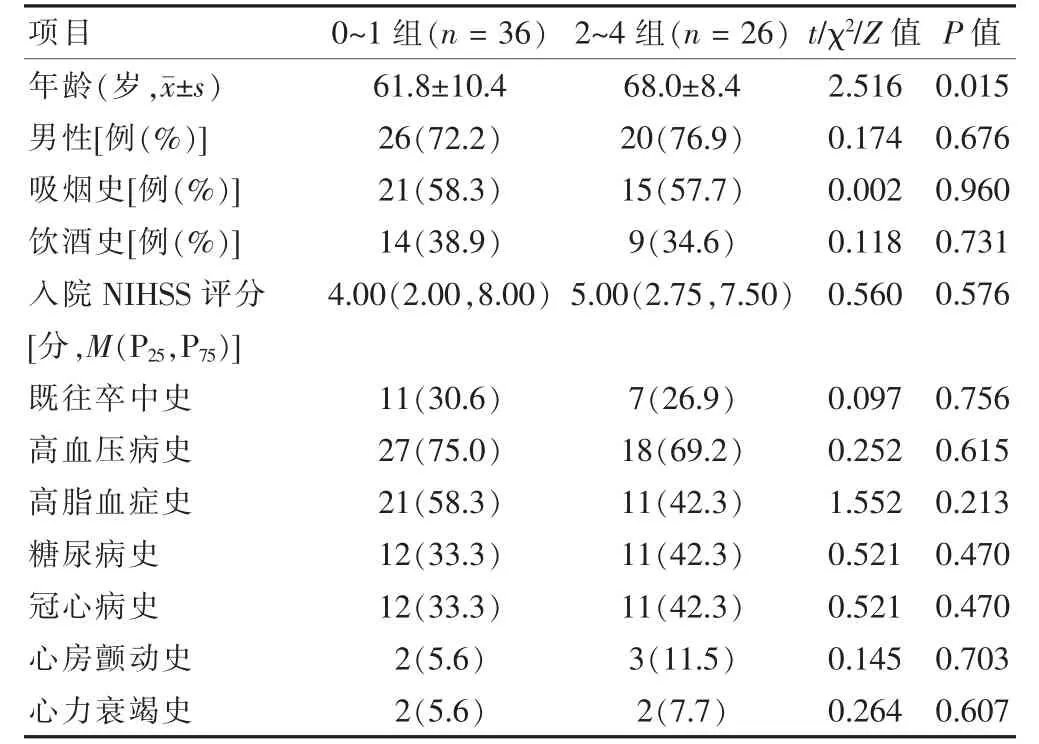
表1 两组基线资料比较
2.2 两组梗死面积、梗死部位和TOAST 分型比较
两组梗死面积、梗死部位、TOSAT 分型比较,差异无统计学意义(P >0.05)。见表2。

表2 两组梗死面积、梗死部位和TOAST 分型比较[例(%)]
2.3 两组血清学指标、血压比较
2~4 组Hcy 水平高于0~1 组,差异有统计学意义(P <0.05);两组TG、TC、HDL、LDL、血糖、入院收缩压和入院舒张压比较,差异无统计学意义(P >0.05)。见表3。
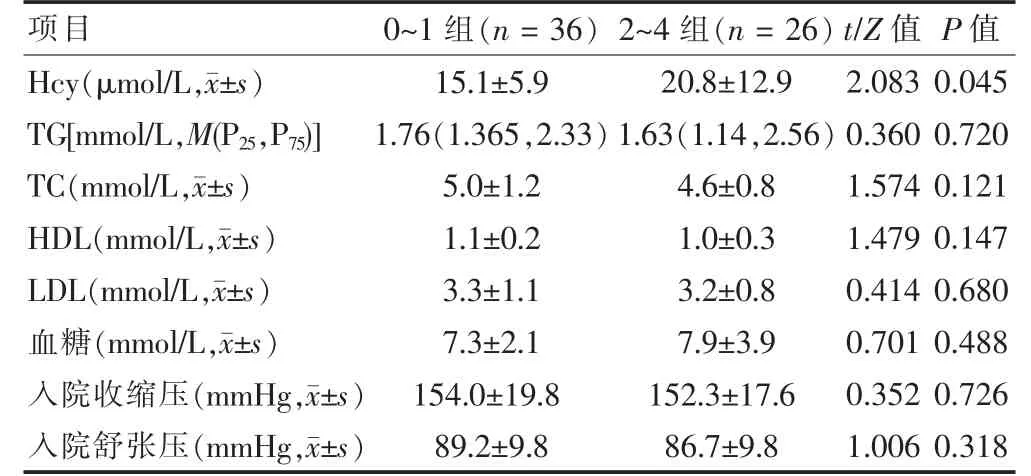
表3 两组血清学指标、血压比较
2.5 AIS 患者CSVD 影像总负担多因素logistic 回归分析
年龄和Hcy 是AIS 患者CSVD 总负担严重程度的独立危险因素(OR >1,P <0.05)。见表4。

表4 AIS 患者CSVD 影像总负担多因素logistic 回归分析
2.6 影响AIS 患者CSVD 影像总负担亚组分析
WMH 组Hcy 水平和年龄均高于无WMH 组,差异均有统计学意义(均P <0.05);其余亚组组间Hcy水平和年龄比较,差异无统计学意义(均P >0.05)。见表5。
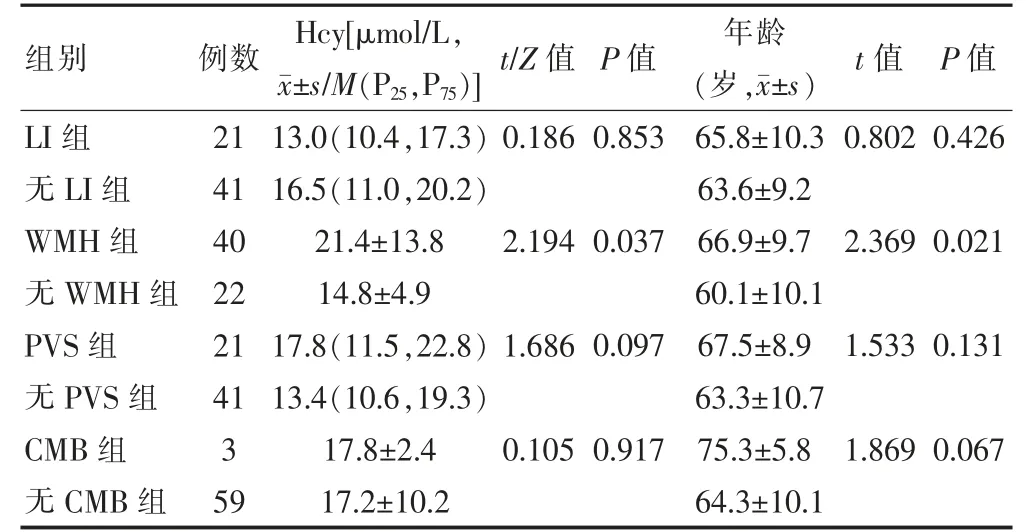
表5 AIS 患者CSVD 影像总负担亚组分析
3 讨论
CSVD 涉及多种病因致脑内小动脉、微动脉、小静脉、微静脉、毛细血管病变,神经影像学是早期诊断的重要工具[14],AIS 患者中CSVD 影像总负担评分2~4 分者出现溶栓后出血转化、卒中复发等不良预后的风险较高[15-17]。本研究发现Hcy 水平与年龄在AIS患者CSVD 影像总负担评分2~4 分者中显著增高(P <0.05),且是AIS 患者CSVD 影像总负担的独立危险因素,提示高Hcy、高龄AIS 患者的CSVD 影像总负担更重。
亚组分析结果显示,WMH 组年龄和Hcy 水平高于无WMH 组(P <0.05)。提示动脉粥样硬化患者其CSVD 影像总负担更严重,其MWH 与CMB 严重程度也更高[18]。研究显示[19-21],高同型半胱氨酸血症是动脉粥样硬化疾病的独立危险因素,本研究发现Hcy 水平是AIS 患者CSVD 影像总负担较重的独立危险因素之一,提示AIS 患者CSVD 中部分亚型可能与高Hcy水平导致穿支动脉硬化、血管内皮细胞损伤有关。一项纳入5088 例患者的荟萃分析显示CSVD 中脑白质病变患者Hcy 水平更高,其次为无症状缺血性脑卒中和LI[22],也有研究证实Hcy 水平是LI 和严重WMH的危险因素[23],本研究仅提示存在WMH 的AIS 患者血Hcy 水平更高,可能与样本量较小有关。
目前发现CSVD 患病率随年龄增长而增加,其中WMH 与年龄增加密切相关[24],LDL 是CSVD 诱发短暂性脑缺血发作的主要危险因素[25]。本研究发现年龄是AIS 患者CSVD 影像总负担评分增加的独立危险因素,存在WMH 的患者年龄相对更高,与之前研究结果一致,而CSVD 影像总负担严重程度不同的患者,其高血压病史、入院血压、TG、TC、HDL、LDL、血糖等指标比较,差异无统计学意义(均P >0.05),原因可能与样本量较小有关。
本研究结果提示,在AIS 患者中,较高的Hcy 水平和高龄是加重CSVD 影像总负担的独立危险因素。因此AIS 患者且合并高龄或血Hcy 水平较高时,有必要筛查其CSVD 整体情况,为确定下一步静脉溶栓等治疗方案及评估患者的预后提供参考。本研究为回顾性研究且纳入患者数量较少,尚需扩大样本量进行多中心研究进一步探索证实。
